Der Aufbau der Materie bei isotropen Krften Inhalt

Der Aufbau der Materie bei isotropen Kräften

Inhalt • Kräfte zwischen den Bausteinen • Modell-Potentiale für isotrope Wechselwirkung

Kräfte zwischen den Bausteinen der Materie • Massen* – immer anziehend: Gravitationsgesetz • Ladungen* – anziehend oder abstoßend: Coulombgesetz • *Es gibt keine Ladung ohne Masse • *Es gibt Massen ohne Ladung
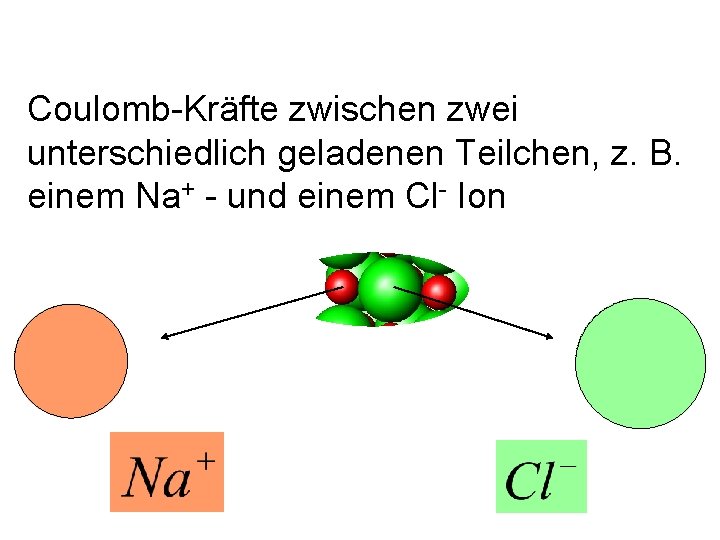
Coulomb-Kräfte zwischen zwei unterschiedlich geladenen Teilchen, z. B. einem Na+ - und einem Cl- Ion
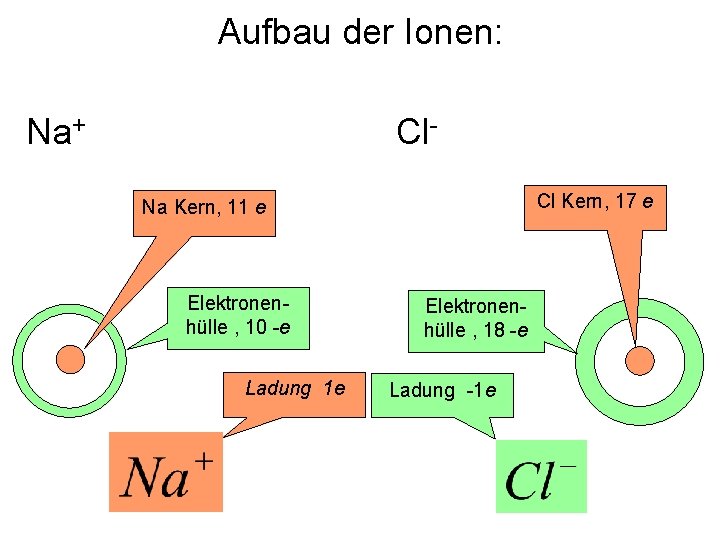
Aufbau der Ionen: Na+ Cl. Cl Kern, 17 e Na Kern, 11 e Elektronenhülle , 10 -e Ladung 1 e Elektronenhülle , 18 -e Ladung -1 e
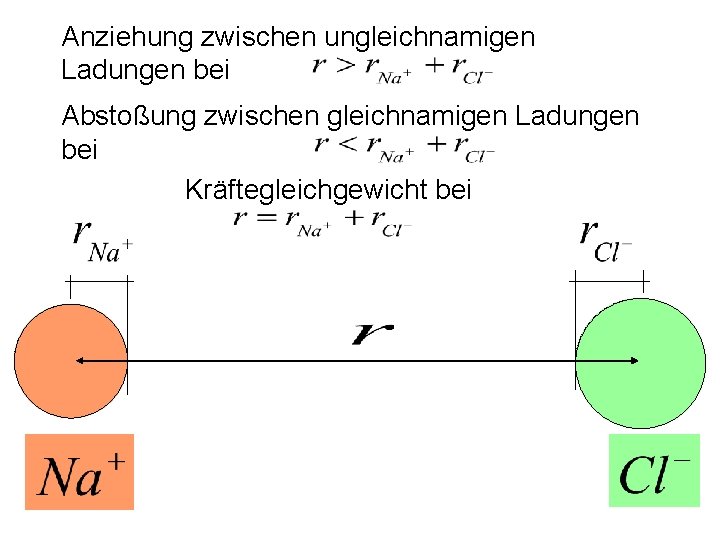
Anziehung zwischen ungleichnamigen Ladungen bei Abstoßung zwischen gleichnamigen Ladungen bei Kräftegleichgewicht bei
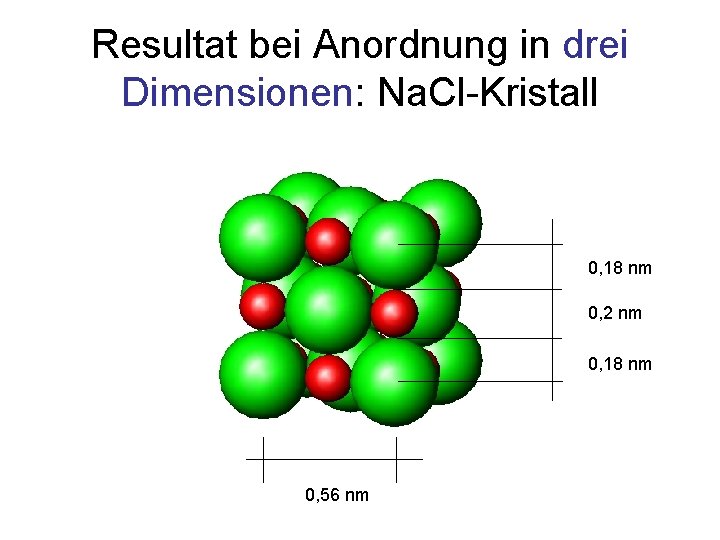
Resultat bei Anordnung in drei Dimensionen: Na. Cl-Kristall 0, 18 nm 0, 2 nm 0, 18 nm 0, 56 nm

Zum Aufbau der Materie: ISS • Die Materie besteht aus Massen und Ladungen, die im dreidimensionalen Raum auf vielfältige Weise kombiniert werden können – Coulomb- und Trägheitskräfte steuern die Struktur auf atomarer Skala (z. B. Struktur der Moleküle), – Gravitations- und Trägheitskräfte wirken in großen Dimensionen (z. B. Satellitenbahnen, Planetenbewegung) • Kräfte werden durch Felder übermittelt • Die Energie bleibt bei allen Vorgängen erhalten

Coulomb Potential 1 J Coulomb-Potential zwischen elektrischen Ladungen Im Abstand
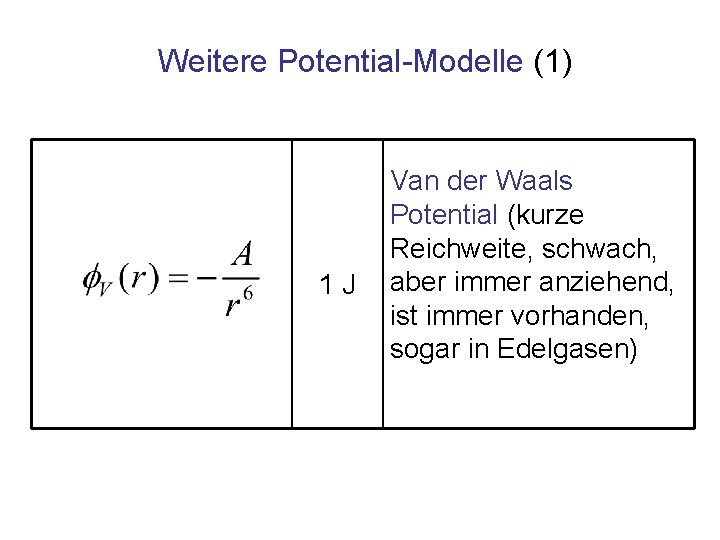
Weitere Potential-Modelle (1) 1 J Van der Waals Potential (kurze Reichweite, schwach, aber immer anziehend, ist immer vorhanden, sogar in Edelgasen)

Potential-Modelle (2) 1 J Lenard Jones Potential: Van der Waals Potential mit abstoßendem Anteil

Potential-Modelle (3) 1 J Buckingham-Potential: Ähnlich dem Lennard Jones Potential, aber anderer Formulierung des abstoßenden Anteils

Potential-Modelle (4) 1 J Summe aus Lenard Jones- und Coulomb Potential: Modellpotential für numerische Simulation bei isotroper Bindung mit stark ionischem Anteil
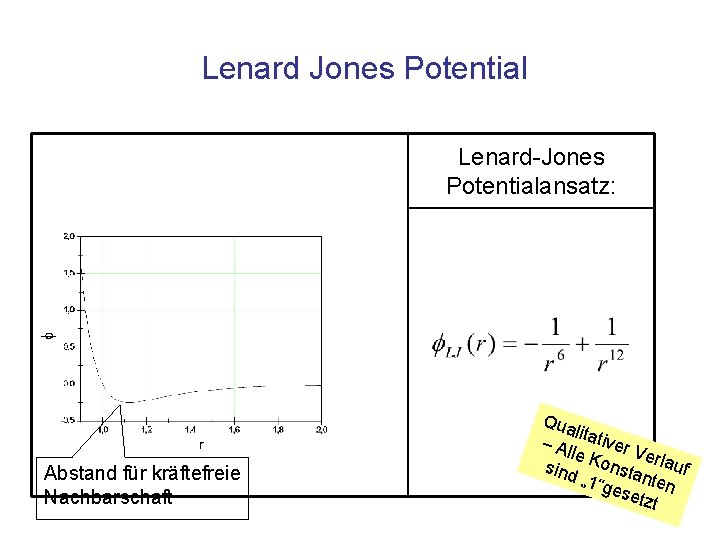
Lenard Jones Potential Lenard-Jones Potentialansatz: Abstand für kräftefreie Nachbarschaft Qua li – Al tativer V le K e sind onsta rlauf nt „ 1“g ese en tzt

Isotrope Materialien • Reine Ionenbindungen • Reine Van der Waals-Bindung • Reine Metallbindung
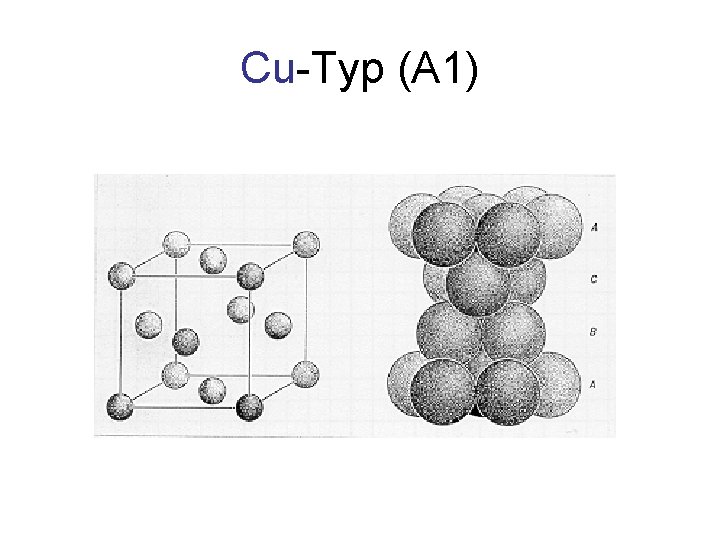
Cu-Typ (A 1)
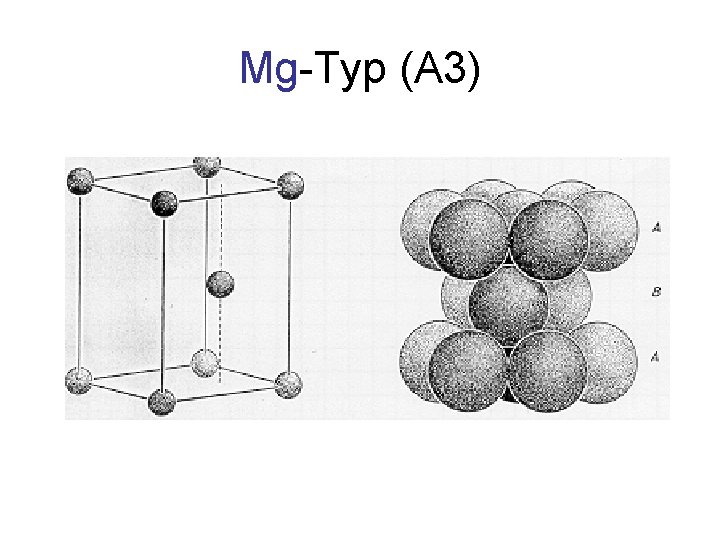
Mg-Typ (A 3)
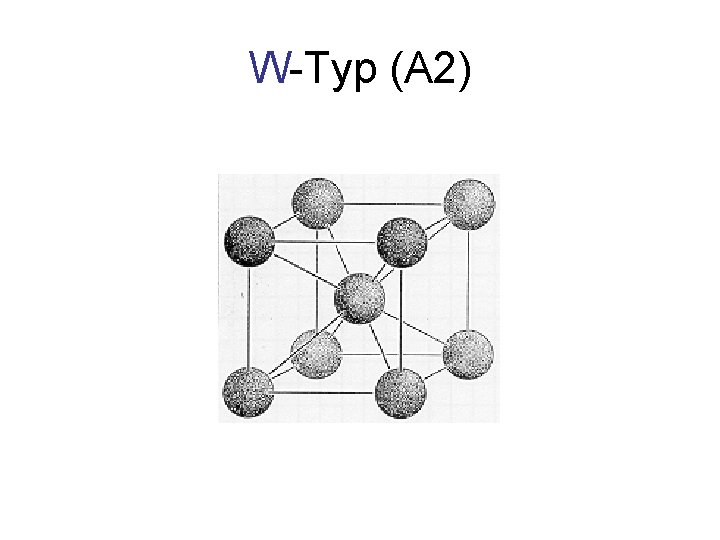
W-Typ (A 2)

Zusammenfassung Isotrope Wechselwirkung in – Ionenkristallen – Metallen • Klassische isotrope Potentialansätze : – Coulomb Potential für Ionenkristalle – Van der Waals Potential, sehr schwach, anziehend, immer vorhanden – Lenard-Jones zur Modellierung des Gleichgewicht. Abstands – Buckingham Potentiale zur Modellierung des effektiven Potentials mit Coulomb-Anteil • Die meisten Bindungen zeigen Mischungen von van der Waals, ionischen und kovalenten Anteilen
Finis
- Slides: 20