Deney 3 ASTBAZ TTRASYONU PROF DR GLFEM BAKAN

Deney 3 ASİT-BAZ TİTRASYONU PROF. DR. GÜLFEM BAKAN Samsun/2019

DENEYİN AMACI Asit ve bazda mevcut olan H+ ve OH- iyonlarının tayin edilmesi ve tayin yöntemlerinin öğrenilmesi

Teori Standart Çözelti: Birim hacimde bilinen miktarda çözünen madde ihtiva eden çözeltidir. Normal Çözelti: Bir litre başına bir eşdeğer gram madde ihtiva eden çözeltidir. Eşdeğer (Ekivalent) Ağırlık: Bir atom-gram (1. 0089) yer değiştirebilir hidrojen ihtiva eden veya onun eşdeğerine karşılık gelen molekül ağırlığının bir kısmı veya tamamıdır. Kısaca bir element veya birleşiğin, dolaylı veya dolaysız olarak, hidrojenle veya oksijenle birleşen veya yer değiştirebilen ağırlıkça miktarıdır.

TİTRASYON Asit-baz titrasyonu, asidik olduğu bilinen bir çözeltiye belirli miktarlarda baz (damlatılarak) eklemek ya da bunun tam tersi bazik olduğu bilinen bir çözeltiye belirli miktarlarda asit ekleme işlemidir. Titrasyon işleminde büret kullanılır. Temel amaç asit veya bazın derişimini tespit etmektir. Buradan da çözeltinin p. H değerini kolayca hesaplayabiliriz. Çözeltinin dengelendiği zamanı hassas olarak yakalamak için derişimi bilinmeyen çözeltinin içine indikatör konur. İndikatör renk değiştirdiği anda titrasyon işlemi durdurulur. İndikatör seçimi asit veya bazın tipine göre değişiklik gösterir çünkü indikatörlerin renk değişikliği göstereceği p. H aralıkları farklıdır. Titrasyon için kullanılabilcek birçok indikatör vardır. İndikatör seçimi yaparken şu maddeleri göz önünde bulundurmalıyız. 1. Kuvvetli asit ile kuvvetli bazın tepkimesi nötrleşme tepkimesi olacağından p. H değeri 7 olur. 2. Kuvvetli asit ile zayıf bazın tepkimesi sonucu p. H değeri 7’den küçük olur. 3. Kuvvetli baz ile zayıf asitin tepkimesi sonucu p. H değeri 7’den büyük olur.

Titrasyon işleminde birbiri ile etkileşen asit ve baz çözeltilerinin eşdeğer noktasında hacimleri ile normaliteleri arasında söyle bir ilişki vardır: Na. Va=Nb. Vb hacim ve normalitelerin çarpımı eşdeğer gram sayısını verir. Kullanılan indikatörün (dönüm noktasında) renginin değişmesinde iki çözeltinin eşdeğer gram sayıları birbirine eşit olur. Bu ana «Titrasyon Sonu» veya «Nötralizasyon Noktası» denir.

Asitler ve Bazlar Asit ve bazların tanımı önemlidir. Gerçekte hemen bütün kimyasal tepkimeler, asit-baz tepkimeleri olarak sınıflandırılabilir. Asit ve bazlar için yapılan tanımların çoğu, sulu çözeltilerde gözlenen özelliklerine dayanır. Sulu çözeltileri turnusol kağıdını kırmızıya dönüştüren ve ekşimsi bir tadı olan maddelere «asit» , maviye dönüştüren maddelere ise «baz» denir. Bazların sulu çözeltileri kaygan olup acımsı bir tat verirler.

Arrhenius Asit-Baz Teorisi Arrhenius’a göre asit, suda hidrojen iyonu (H+); baz hidroksit iyonu (OH-) oluşturarak çözünen maddedir. Arrhenius’un asitbaz tanımı, maddelerin yalnız sulu çözeltileri için geçerlidir. HCI(g) H+ (suda) + CI- (suda) (Asit) HNO 3 (S) H+ (suda) + NO 3 – (suda) (Asit) Na. OH (k) Na+(suda) + OH-(suda) (Baz) Ba(OH)2 (k) Ba+2 +2 OH- (suda) (Baz)

Bronsted-Lowry Asit-Baz Teorisi İngiliz kimyacısı Lowry ve Danimarkalı kimyacı Bronsted’e göre, bir tepkimede proton (H+ iyonu) verici madde asit; proton alıcı madde ise bazdır. Örneğin; HCI suda çözündüğünde suya H+ iyonu vererek onu hidronyum veya hidroksonyum iyonuna (H 3 O+) dönüştürür. HCI(g) + H 2 O(S) H 3 O+(suda) + CI- (suda) Bu tepkimede, HCI proton verici olduğundan asit, H 2 O proton alıcı olduğundan bazdır. Bu tepkimenin tersi düşünüldüğünde; H 3 O+(suda) + CI- (suda) HCI(g) + H 2 O(S) H 3 O+ iyonu CI- iyonuna proton verdiği için asit; CI- iyonu proton aldığı için bazdır. Bronsted-Lowry asit-baz teorisinde aralarında H+ iyonu kadar fark olan asit-baz çiftine «eşlenik (konjuge) asit-baz çifti» denir. Yukarıdaki tepkimede HCI/ CI- ve H 3 O+/H 2 O eşlenik asit-baz çiftleridir.

Lewis Asit- Baz Teorisi Amerikalı kimyacı Newton Lewis da bir asit-baz teorisi geliştirdi. Lewis’e göre baz, elektron çifti verebilen asit; elektron çifti alabilen maddedir. Bir maddenin elektron nokta (Lewis) yapısına bakarak maddenin asit mi, yoksa baz mı olduğuna karar verilebilir. Bu nedenle Lewis teorisi diğer teorilerden daha geneldir.

Asitlerin ve Bazların Genel Özellikleri Asitlerin ortak özellikleri şunlardır. 1. Tatları ekşidir. Limonun ekşiliği içindeki sitrik asitten, sirkenin ekşiliği içindeki asetik asitten ileri gelir. 2. Boya maddelerine etki ederler. Örneğin; turnusol boyasının rengini kırmızıya dönüştürürken, fenolftalein boyasını renksizleştirirler. 3. Karbonat ve bikarbonatlarla tepkimeye girerek CO 2 gazı oluştururlar. 4. Bazlarla birleşerek tuz ve su oluştururlar.

Bazların Özellikleri 1. Suda iyon oluşturarak çözünürler. Çözeltileri elektrik akımını iletir. 2. Tatları acıdır. Sabun köpüğünün acılığı yapısındaki sodyum hidroksitten, karabiberin acılığı yapısındaki piperidin bazından ileri gelir. 3. Boya maddelerine etki ederler. Kırmızı turnusolu mavi, renksiz fenolftaleini pempe yaparlar. 4. Elle tutulduklarında kayganlık hissi verirler. Sabunun, yumurta akının ve deniz suyunun kayganlıkları yapılarındaki bazlardan kaynaklanır. 5. Asitleri nötrleştirirler. Yani asitlerle veya asit oksitlerle tuzları oluştururlar.

Aletler ve Maddeler Analitik tartı Büret Erlen Reaktifler a) Na. OH (analitik reaktif derecesinde) b) H 2 SO 4 çözeltisi c) Fenol ftalein indikatörü

Yöntem A-1) Yaklaşık 0, 01 N Baz Çözeltisinin Hazırlanması Terazi ile, temiz bir saat camı veya beherde yaklaşık 0, 25 gram Na. OH tartılır. Na. OH fazla bekletilmeden önceden temizlenmiş 500 ml’lik balon jojeye aktarılır. Üzerine biraz saf su konarak tamamen çözününceye kadar çalkalanır. Sonra jojenin boynundaki işaret çizgisine kadar saf su ilave edilir. Kapağı kapatılarak birkaç kez ters yüz edilir. Temiz ve üzerinde isim ve konsantrasyonu yazılı şişe içerisine aktarılır ve bir kenara bırakılır.

A-2) Standart H 2 SO 4 Çözeltisine Karşı Na. OH Çözeltisinin Ayarlanması: Temiz bir büret içerisine bir miktar standart H 2 SO 4 çözeltisi konarak çalkalanır. Sonra büret ayarlı H 2 SO 4 çözeltisi ile doldurulur. 25 ml önceden hazırladığımız Na. OH’dan alınarak erlen içerisine konulur ve üzerine 3 damla fenolftalein çözeltisi damlatılır. Pembe renk oluşacaktır. Oluşan pembe renk kayboluncaya kadar erlen çalkalanarak H 2 SO 4 damlatılır. Elde edilen verilerden bazın normalitesi hesaplanır. B-) Derişimi Bilinmeyen Asidin Normalitesinin Tayini Derişimi bilinmeyen bir asit çözeltisinden 25 ml alınır. 3 damla fenolftalein damlatılır. Pembe renk oluşuncaya kadar normalitesi bilinen Na. OH çözeltisi ile titre edilir. Bu veriler yardımı ile de asit çözeltisinin konsantrasyonu hesaplanır.

VERİ ANALİZİ VERİLER Kullanılan H 2 SO 4’ün Normalitesi: NAsit Titrasyonda sarfedilen H 2 SO 4 miktarı: VAsit Deneyde kullanılan Na. OH miktarı: VBaz VERİ ANALİZİ VE HESAPLAMALAR Aşağıdaki formülü kullanarak Na. OH baz çözeltisinin normalitesini hesaplanır. NAVA=NBVB
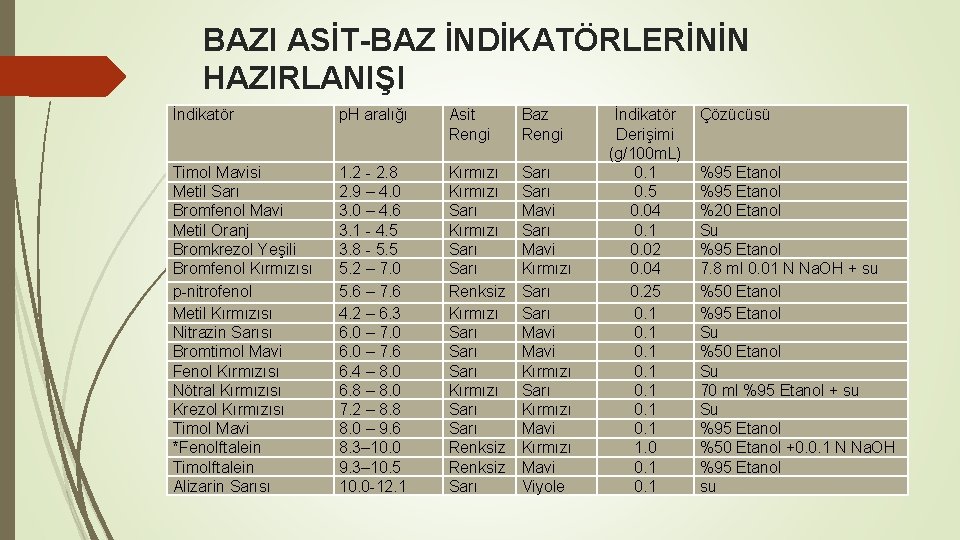
BAZI ASİT-BAZ İNDİKATÖRLERİNİN HAZIRLANIŞI İndikatör p. H aralığı Asit Rengi Baz Rengi Timol Mavisi Metil Sarı Bromfenol Mavi Metil Oranj Bromkrezol Yeşili Bromfenol Kırmızısı p-nitrofenol Metil Kırmızısı Nitrazin Sarısı Bromtimol Mavi Fenol Kırmızısı Nötral Kırmızısı Krezol Kırmızısı Timol Mavi *Fenolftalein Timolftalein Alizarin Sarısı 1. 2 - 2. 8 2. 9 – 4. 0 3. 0 – 4. 6 3. 1 - 4. 5 3. 8 - 5. 5 5. 2 – 7. 0 5. 6 – 7. 6 4. 2 – 6. 3 6. 0 – 7. 0 6. 0 – 7. 6 6. 4 – 8. 0 6. 8 – 8. 0 7. 2 – 8. 8 8. 0 – 9. 6 8. 3– 10. 0 9. 3– 10. 5 10. 0 -12. 1 Kırmızı Sarı Renksiz Kırmızı Sarı Kırmızı Sarı Renksiz Sarı Mavi Kırmızı Sarı Kırmızı Mavi Viyole İndikatör Derişimi (g/100 m. L) 0. 1 0. 5 0. 04 0. 1 0. 02 0. 04 0. 25 0. 1 0. 1 1. 0 0. 1 Çözücüsü %95 Etanol %20 Etanol Su %95 Etanol 7. 8 ml 0. 01 N Na. OH + su %50 Etanol %95 Etanol Su %50 Etanol Su 70 ml %95 Etanol + su Su %95 Etanol %50 Etanol +0. 0. 1 N Na. OH %95 Etanol su

KAYNAKLAR Prof. Dr. İsmail TORÖZ, Çevre Mühendisliği ve Bilimi için Kimya, 2013, Nobel Yayınevi, istanbul. Prof. Dr. Ahmet SAMSUNLU , ÇEVRE Mühendisliği Kimyası, 2008, Birsen Yayınevi, İstanbul. URL-1: http: //akademik. maltepe. edu. tr/~ilkunorbak/END%20104%20 End%C 3%BCstri%20 M%C 3%BChendisli%C 4%9 Fi%20 Laboratuvar%C 4%B 1/Deney%204%20%20 Asit%20 -%20 Baz%20 Titrasyonlar%C 4%B 1. pdf Erişim Tarihi: 19. 10. 2015 URL-2: http: //www. nkfu. com/asit-ve-bazlarin-genel-ozellikleri-asit-bazlar-konu-anlatimi/Erişim Tarihi: 19. 10. 2015
- Slides: 17