Demoseiten aus den Programmen Atombau Chemische Bindung www

Demoseiten aus den Programmen Atombau Chemische Bindung www. didactec. de © 2009 weiter durch Mausklick ►
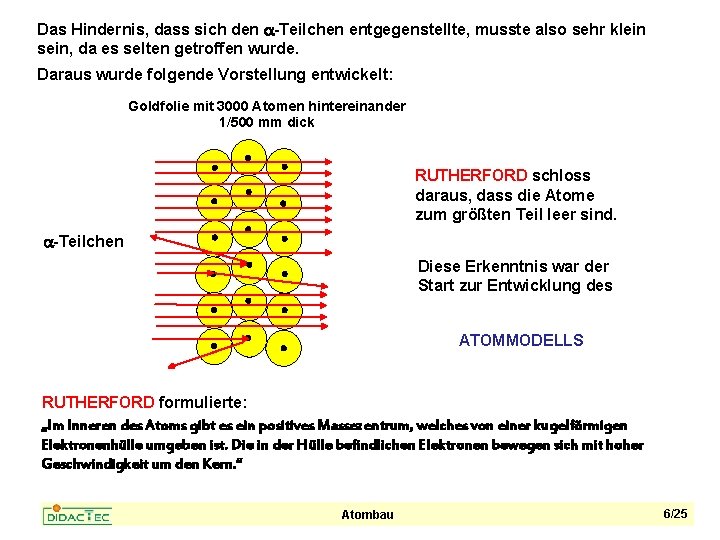
Das Hindernis, dass sich den -Teilchen entgegenstellte, musste also sehr klein sein, da es selten getroffen wurde. Daraus wurde folgende Vorstellung entwickelt: Goldfolie mit 3000 Atomen hintereinander 1/500 mm dick RUTHERFORD schloss daraus, dass die Atome zum größten Teil leer sind. -Teilchen Diese Erkenntnis war der Start zur Entwicklung des ATOMMODELLS RUTHERFORD formulierte: „Im Inneren des Atoms gibt es ein positives Massezentrum, welches von einer kugelförmigen Elektronenhülle umgeben ist. Die in der Hülle befindlichen Elektronen bewegen sich mit hoher Geschwindigkeit um den Kern. “ Atombau 6/25
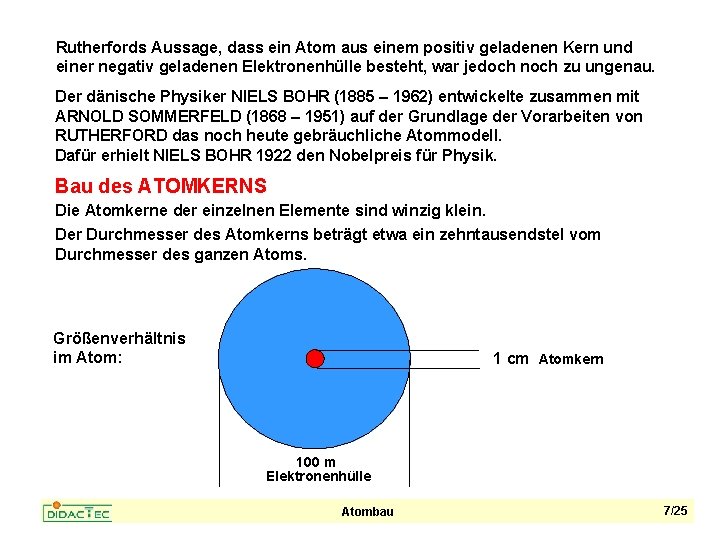
Rutherfords Aussage, dass ein Atom aus einem positiv geladenen Kern und einer negativ geladenen Elektronenhülle besteht, war jedoch noch zu ungenau. Der dänische Physiker NIELS BOHR (1885 – 1962) entwickelte zusammen mit ARNOLD SOMMERFELD (1868 – 1951) auf der Grundlage der Vorarbeiten von RUTHERFORD das noch heute gebräuchliche Atommodell. Dafür erhielt NIELS BOHR 1922 den Nobelpreis für Physik. Bau des ATOMKERNS Die Atomkerne der einzelnen Elemente sind winzig klein. Der Durchmesser des Atomkerns beträgt etwa ein zehntausendstel vom Durchmesser des ganzen Atoms. Größenverhältnis im Atom: 1 cm Atomkern 100 m Elektronenhülle Atombau 7/25
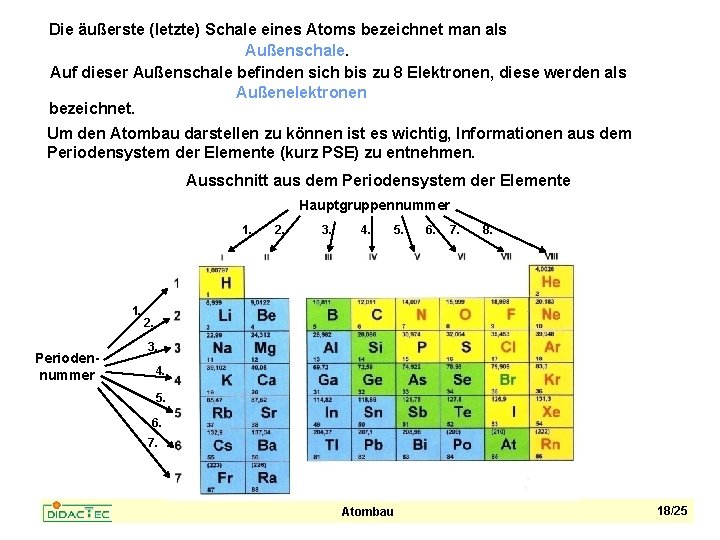
Die äußerste (letzte) Schale eines Atoms bezeichnet man als Außenschale. Auf dieser Außenschale befinden sich bis zu 8 Elektronen, diese werden als Außenelektronen bezeichnet. Um den Atombau darstellen zu können ist es wichtig, Informationen aus dem Periodensystem der Elemente (kurz PSE) zu entnehmen. Ausschnitt aus dem Periodensystem der Elemente Hauptgruppennummer 1. Periodennummer 2. 3. 4. 5. 6. 7. 8. 2. 3. 4. 5. 6. 7. Atombau 18/25
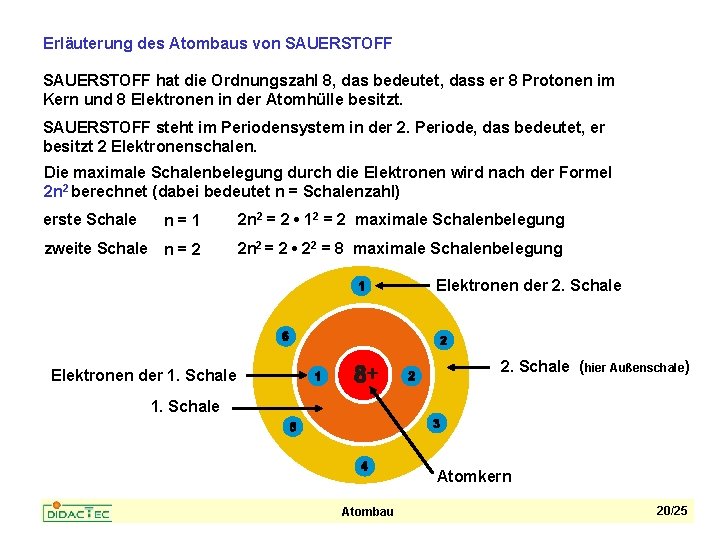
Erläuterung des Atombaus von SAUERSTOFF hat die Ordnungszahl 8, das bedeutet, dass er 8 Protonen im Kern und 8 Elektronen in der Atomhülle besitzt. SAUERSTOFF steht im Periodensystem in der 2. Periode, das bedeutet, er besitzt 2 Elektronenschalen. Die maximale Schalenbelegung durch die Elektronen wird nach der Formel 2 n 2 berechnet (dabei bedeutet n = Schalenzahl) n=1 2 n 2 = 2 • 12 = 2 maximale Schalenbelegung zweite Schale n = 2 2 n 2 = 2 • 22 = 8 maximale Schalenbelegung erste Schale Elektronen der 2. Schale (hier Außenschale) Elektronen der 1. Schale Atomkern Atombau 20/25

Atome können maximal 8 Elektronen auf der Außenschale besitzen. Ist diese Anzahl von Elektronen auf der Außenschale erreicht, spricht man von der „Achterschale“ oder dem Edelgaszustand. Die Edelgase sind die Elemente, die auf der Außenschale 8 Elektronen besitzen (Ausnahme ist Helium mit nur 2 Außenelektronen). Alle Edelgase (Helium He, Neon Ne, Argon Ar, Krypton Kr, Xenon Xe und Radon Rn) sind daher sehr stabil und können auf Grund der 8 Außenelektronen keine chemische Verbindung eingehen. Alle anderen Elemente haben als Atom auf der Außenschale weniger Elektronen. Um so stabil wie die Edelgase zu werden, ist jedes Atom deshalb bestrebt, auf die Außenschale 8 Elektronen zu bekommen, um so auch den „Edelgaszustand“ zu erreichen. Dies gelingt entweder durch Aufnahme von Elektronen durch Abgabe von Elektronen oder durch gemeinsame Nutzung von Elektronen, wenn Elemente miteinander eine chemische Verbindung eingehen. Nur so ist es möglich, dass die Atome den Edelgaszustand erreichen, d. h. den Zustand, bei dem 8 Elektronen auf der Außenschale vorhanden sind. Chemische Bindungen 5/25
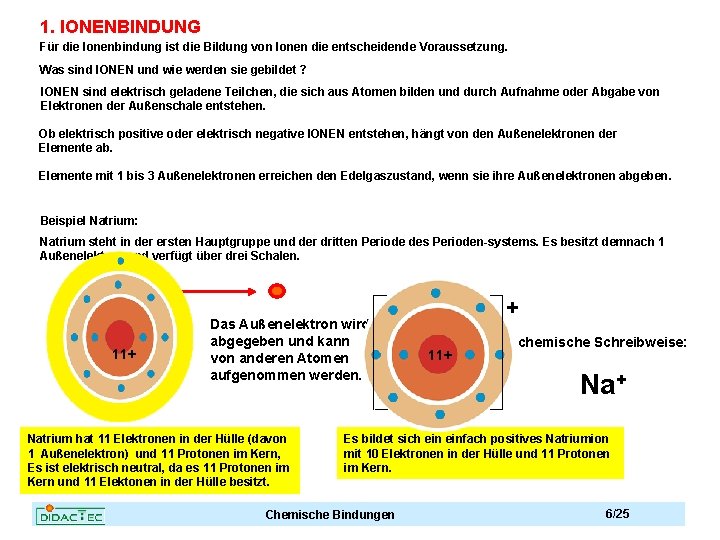
1. IONENBINDUNG Für die Ionenbindung ist die Bildung von Ionen die entscheidende Voraussetzung. Was sind IONEN und wie werden sie gebildet ? IONEN sind elektrisch geladene Teilchen, die sich aus Atomen bilden und durch Aufnahme oder Abgabe von Elektronen der Außenschale entstehen. Ob elektrisch positive oder elektrisch negative IONEN entstehen, hängt von den Außenelektronen der Elemente ab. Elemente mit 1 bis 3 Außenelektronen erreichen den Edelgaszustand, wenn sie ihre Außenelektronen abgeben. Beispiel Natrium: Natrium steht in der ersten Hauptgruppe und der dritten Periode des Perioden-systems. Es besitzt demnach 1 Außenelektron und verfügt über drei Schalen. 11+ Das Außenelektron wird abgegeben und kann von anderen Atomen aufgenommen werden. Natrium hat 11 Elektronen in der Hülle (davon 1 Außenelektron) und 11 Protonen im Kern, Es ist elektrisch neutral, da es 11 Protonen im Kern und 11 Elektonen in der Hülle besitzt. + 11+ chemische Schreibweise: Na+ Es bildet sich einfach positives Natriumion mit 10 Elektronen in der Hülle und 11 Protonen im Kern. Chemische Bindungen 6/25
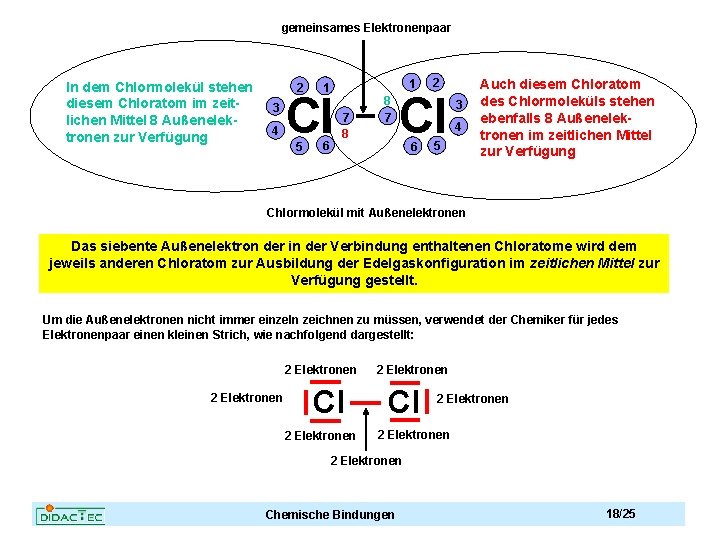
gemeinsames Elektronenpaar In dem Chlormolekül stehen diesem Chloratom im zeitlichen Mittel 8 Außenelektronen zur Verfügung 2 3 4 Cl 5 1 1 6 7 8 8 7 2 Cl 6 3 4 5 Auch diesem Chloratom des Chlormoleküls stehen ebenfalls 8 Außenelektronen im zeitlichen Mittel zur Verfügung Chlormolekül mit Außenelektronen Das siebente Außenelektron der in der Verbindung enthaltenen Chloratome wird dem jeweils anderen Chloratom zur Ausbildung der Edelgaskonfiguration im zeitlichen Mittel zur Verfügung gestellt. Um die Außenelektronen nicht immer einzeln zeichnen zu müssen, verwendet der Chemiker für jedes Elektronenpaar einen kleinen Strich, wie nachfolgend dargestellt: 2 Elektronen Cl 2 Elektronen Chemische Bindungen 18/25

Demoseiten aus den Programmen Atombau Art. -Nr. : 30000 und Chemische Bindungen Art. -Nr. : 30010 Naturwissenschaftliche Lehrmittel Biologie ∙ Chemie ∙ Physik Tel. : 02226 - 809 807 ∙ Fax: 02226 - 169 190 Email: info@didactec. de Internet: www. didactec. de ∙ Webshop: www. didactec. biz © DIDACTEC e. K. - Rheinbach - 2009 - Alle Rechte vorbehalten Kontakt Weitere Präsentationen in Vorbereitung DIDACTEC e. K Technische Lehrmittel Telemannstraße 1 D-53359 Rheinbach
- Slides: 9