Degradacin aerbica de tolueno el plsmido TOL Representative

Degradación aeróbica de tolueno: el plásmido TOL
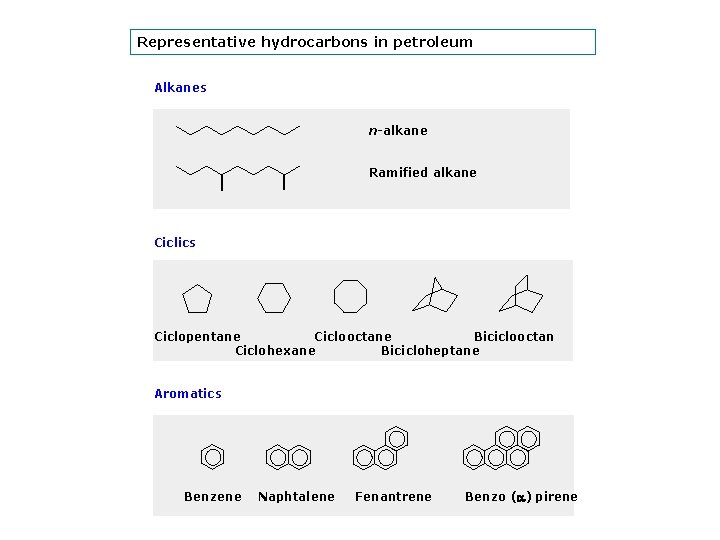
Representative hydrocarbons in petroleum Alkanes n-alkane Ramified alkane Ciclics Ciclopentane Ciclooctane Biciclooctan Ciclohexane Bicicloheptane Aromatics Benzene Naphtalene Fenantrene Benzo ( ) pirene

Hidrocarburos aromático: Representativos de contaminación (petróleo e industria) Estructuras muy estables Contaminantes antropogénicos Estructuras diseñadas para ser muy estables (Diseñadas para ser tóxicas) DIFÍCILES DE DEGRADAR

COMPUESTOS CONTAMINANTES DE ORIGEN INDUSTRIAL Orgánicos Pesticidas (concentraciones traza pero MUY tóxicos) Compuestos aromáticos policíclicos Hidrocarburos policlorados, solventes orgánicos y carburantes (BTEX) Solventes orgánicos NO clorados Tintes, detergentes, . . . Inorgánicos Fosfatos y nitratos (agricultura intensiva) Metales tóxicos (Zn, Cd, Ni, Cu, Pb, Cr, Hg, Mo, As, Se)

ORGANISMOS IMPLICADOS EN LA RECUPERACIÓN DE SUELOS CONTAMINADOS MICROORGANISMOS Bacterias Muy versátiles Buen nivel de conocimiento Fáciles de manipular Hongos Versátiles Bajo nivel de conocimiento de cepas silvestres Difíciles de manipular PLANTAS Gran tamaño (visibles) Manipulables INVERTEBRADOS Como reactores (futuro? )

Manipulación requiere CONOCIMIENTO PREVIO • Organismos y sus posibilidades • Rutas disponibles • Regulación de la rutas • Mecanismos disponibles para su manipulación ¿Qué conocimiento tenemos? ¿Cómo llegamos esta información?
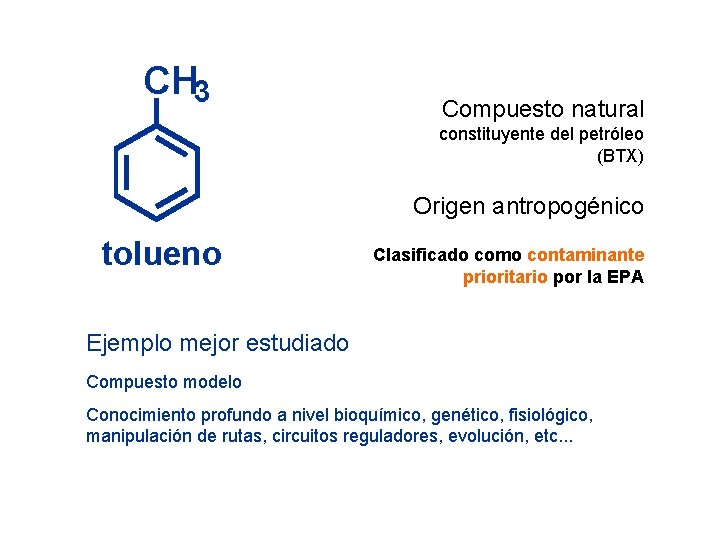
CH 3 Compuesto natural constituyente del petróleo (BTX) Origen antropogénico tolueno Clasificado como contaminante prioritario por la EPA Ejemplo mejor estudiado Compuesto modelo Conocimiento profundo a nivel bioquímico, genético, fisiológico, manipulación de rutas, circuitos reguladores, evolución, etc. . .
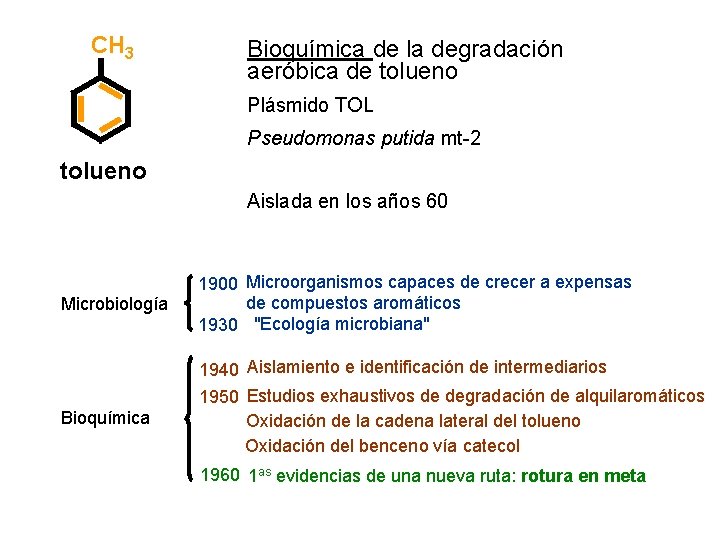
CH 3 Bioquímica de la degradación aeróbica de tolueno Plásmido TOL Pseudomonas putida mt-2 tolueno Aislada en los años 60 Microbiología Bioquímica 1900 Microorganismos capaces de crecer a expensas de compuestos aromáticos 1930 "Ecología microbiana" 1940 Aislamiento e identificación de intermediarios 1950 Estudios exhaustivos de degradación de alquilaromáticos Oxidación de la cadena lateral del tolueno Oxidación del benceno vía catecol 1960 1 as evidencias de una nueva ruta: rotura en meta

Pseudomonas putida mt-2 COOH Dos rutas diferentes para la degradación de benzoato: Rotura en orto (puede degradar BENZOATO) Rotura en meta (puede degradar METIL-BENZOATOS) Aparecen mutantes espontáneos que parecen cambiar su metabolismo de tipo meta a tipo orto. ben+, m-ben. Han perdido TODAS las enzimas de la ruta meta. Son MUY estables (no hay revertientes). Mismo fenotipo se obtiene curando con Mitomicina C El carácter el TRANSMISIBLE Los genes de la ruta meta presentes en un plásmido: TOL (p. WW 0) COOH CH 3

Métodos para el estudio de rutas • Detección e identificación de compuestos intermediarios (resting cells) • Estudios isotópicos • Estudios de adaptación simultánea • Obtención y análisis de mutantes
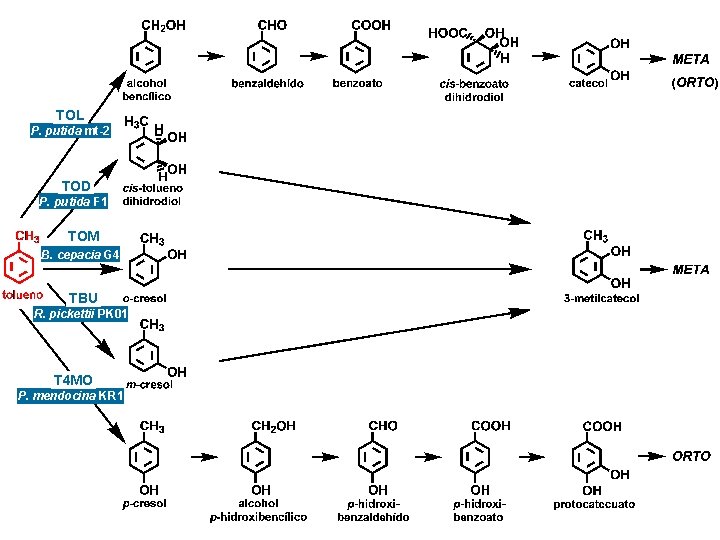
TOL P. putida mt-2 TOD P. putida F 1 TOM B. cepacia G 4 TBU R. pickettii PK 01 T 4 MO P. mendocina KR 1
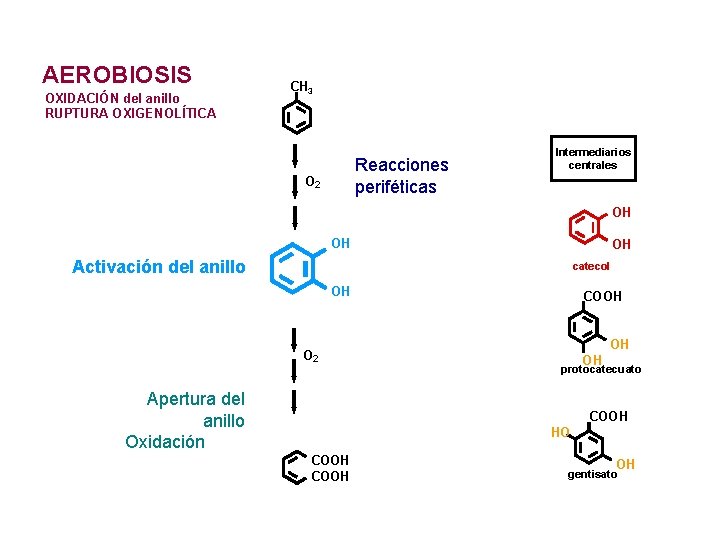
AEROBIOSIS OXIDACIÓN del anillo RUPTURA OXIGENOLÍTICA CH 3 Reacciones periféticas O 2 Intermediarios centrales OH OH OH Activación del anillo catecol OH O 2 Apertura del anillo Oxidación COOH OH OH protocatecuato COOH HO COOH OH gentisato
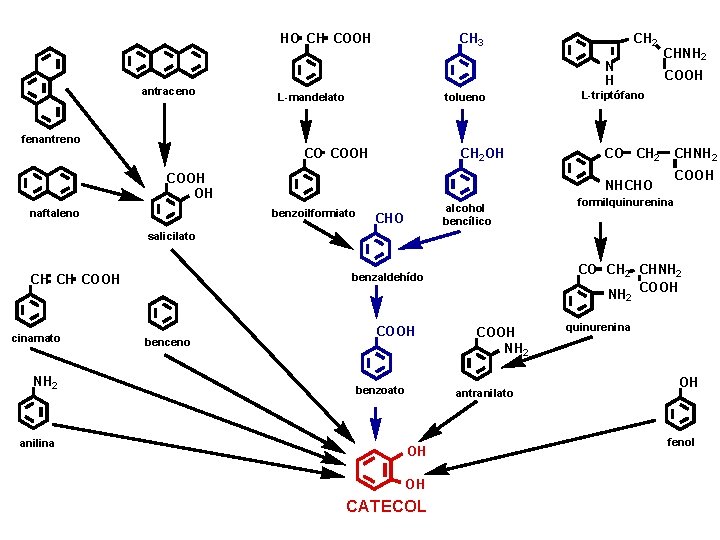
HO CH COOH antraceno CH 3 CH 2 N H L-mandelato tolueno CHNH 2 COOH L-triptófano fenantreno CO COOH CH 2 OH COOH OH naftaleno CO CH 2 CHNH 2 COOH NHCHO benzoilformiato alcohol bencílico CHO formilquinurenina salicilato CO CH 2 CHNH 2 NH COOH benzaldehído CH CH COOH 2 cinamato NH 2 anilina benceno COOH benzoato COOH NH 2 antranilato OH OH CATECOL quinurenina OH fenol
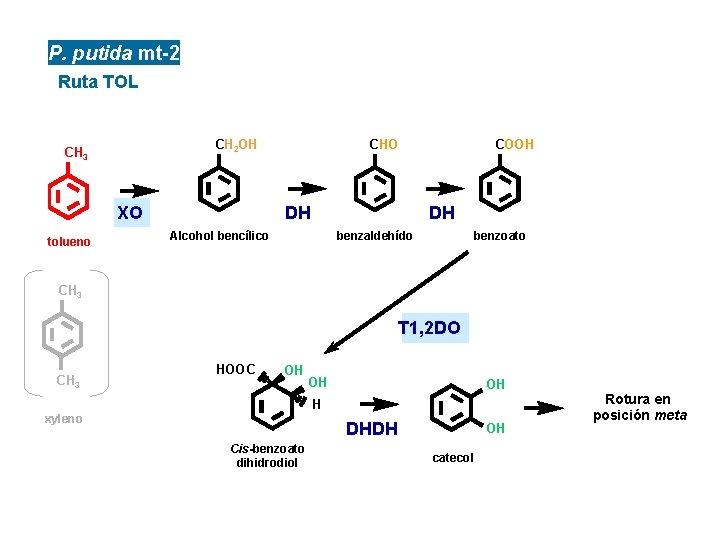
P. putida mt-2 Ruta TOL CH 2 OH CH 3 XO tolueno CHO COOH DH DH Alcohol bencílico benzaldehído benzoato CH 3 T 1, 2 DO CH 3 HOOC OH OH OH H xyleno DHDH Cis-benzoato dihidrodiol OH catecol Rotura en posición meta
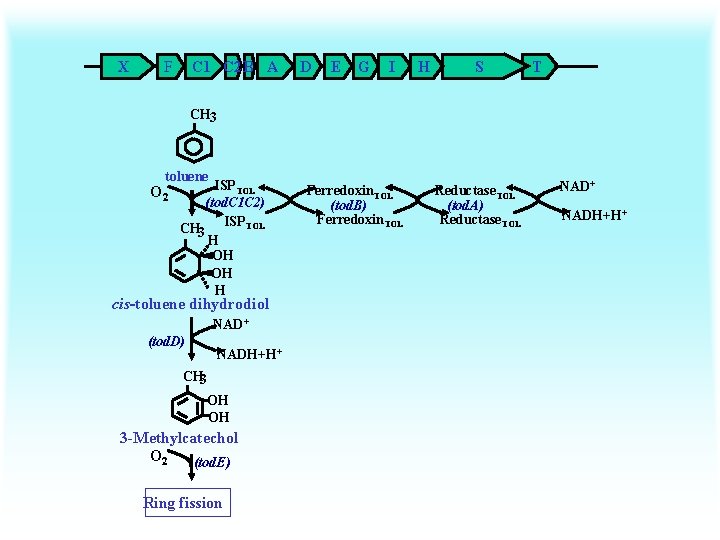
X F C 1 C 2 B A D E G I H S T CH 3 toluene O 2 ISPTOL (tod. C 1 C 2) ISPTOL CH 3 H OH OH H cis-toluene dihydrodiol NAD+ (tod. D) NADH+H+ CH 3 OH OH 3 -Methylcatechol O 2 (tod. E) Ring fission Ferredoxin. TOL (tod. B) Ferredoxin. TOL Reductase. TOL (tod. A) Reductase. TOL NAD+ NADH+H+
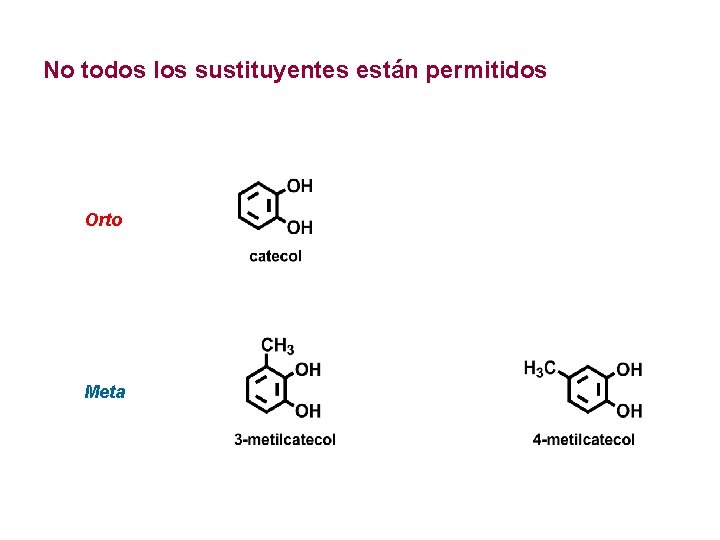
No todos los sustituyentes están permitidos Orto Meta
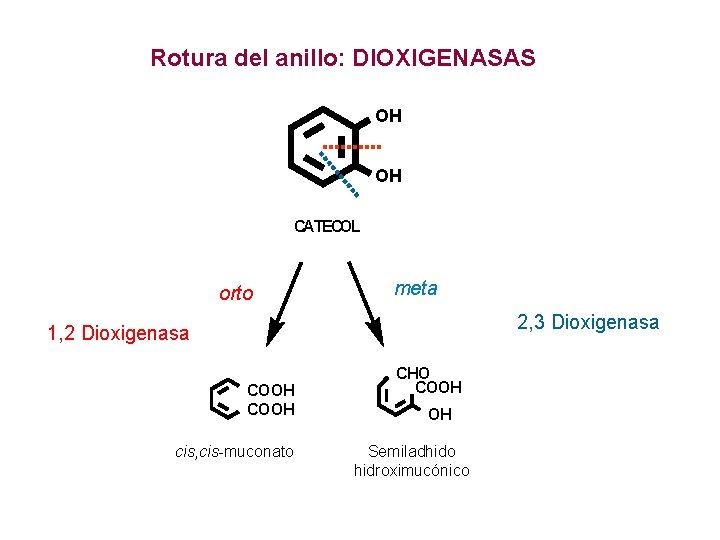
Rotura del anillo: DIOXIGENASAS OH OH CATECOL orto meta 2, 3 Dioxigenasa 1, 2 Dioxigenasa COOH cis, cis-muconato CHO COOH OH Semiladhido hidroximucónico
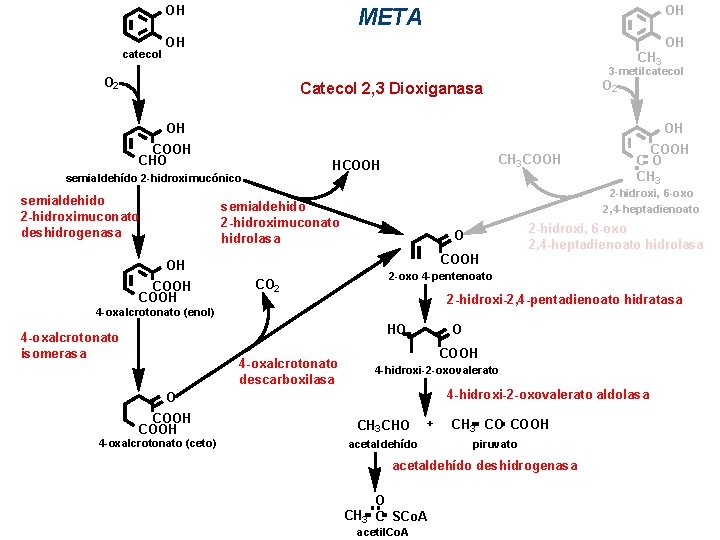
OH catecol OH META OH OH CH 3 3 -metilcatecol O 2 Catecol 2, 3 Dioxiganasa OH OH COOH CHO HCOOH semialdehído 2 -hidroximucónico semialdehido 2 -hidroximuconato deshidrogenasa CH 3 COOH 2 -hidroxi, 6 -oxo 2, 4 -heptadienoato semialdehido 2 -hidroximuconato hidrolasa CO 2 2 -oxo 4 -pentenoato 2 -hidroxi-2, 4 -pentadienoato hidratasa 4 -oxalcrotonato (enol) O HO 4 -oxalcrotonato isomerasa 4 -oxalcrotonato descarboxilasa COOH 4 -hidroxi-2 -oxovalerato aldolasa O COOH 4 -oxalcrotonato (ceto) 2 -hidroxi, 6 -oxo 2, 4 -heptadienoato hidrolasa O COOH OH COOH C O CH 3 CHO + acetaldehído CH 3 CO COOH piruvato acetaldehído deshidrogenasa O CH 3 C SCo. A acetil. Co. A
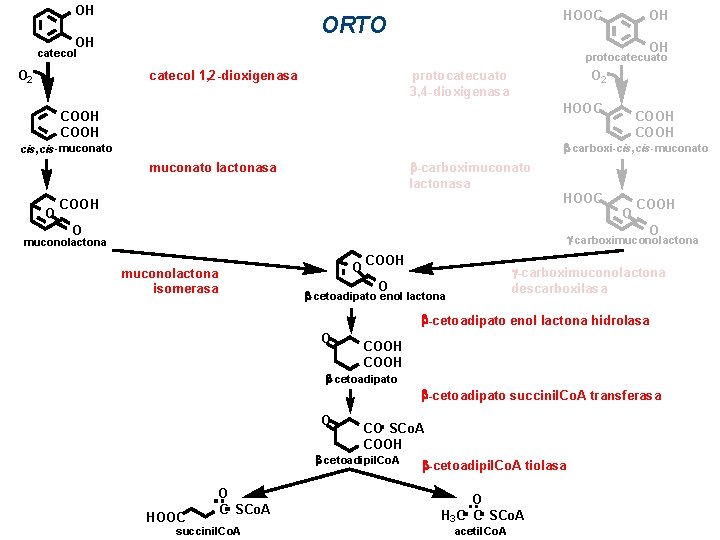
OH HOOC ORTO OH OH catecol protocatecuato catecol 1, 2 -dioxigenasa O 2 protocatecuato 3, 4 -dioxigenasa O 2 HOOC COOH -carboxi-cis, cis-muconato -carboximuconato lactonasa O OH COOH HOOC O O COOH O g-carboximuconolactona O muconolactona isomerasa COOH g-carboximuconolactona descarboxilasa O -cetoadipato enol lactona hidrolasa O COOH -cetoadipato succinil. Co. A transferasa O CO SCo. A COOH -cetoadipil. Co. A HOOC O C SCo. A succinil. Co. A -cetoadipil. Co. A tiolasa O H 3 C C SCo. A acetil. Co. A
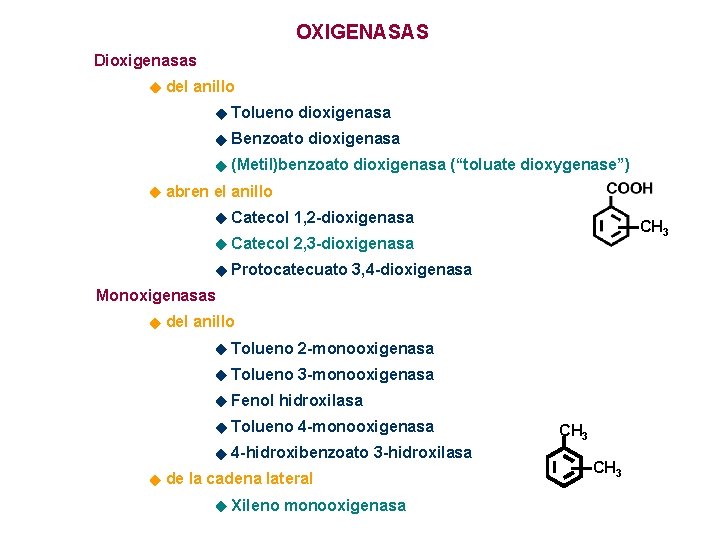
OXIGENASAS Dioxigenasas del anillo Tolueno dioxigenasa Benzoato dioxigenasa (Metil)benzoato dioxigenasa (“toluate dioxygenase”) abren el anillo Catecol 1, 2 -dioxigenasa Catecol 2, 3 -dioxigenasa Protocatecuato 3, 4 -dioxigenasa CH 3 Monoxigenasas del anillo Tolueno 2 -monooxigenasa Tolueno 3 -monooxigenasa Fenol hidroxilasa Tolueno 4 -monooxigenasa 4 -hidroxibenzoato 3 -hidroxilasa de la cadena lateral Xileno monooxigenasa CH 3
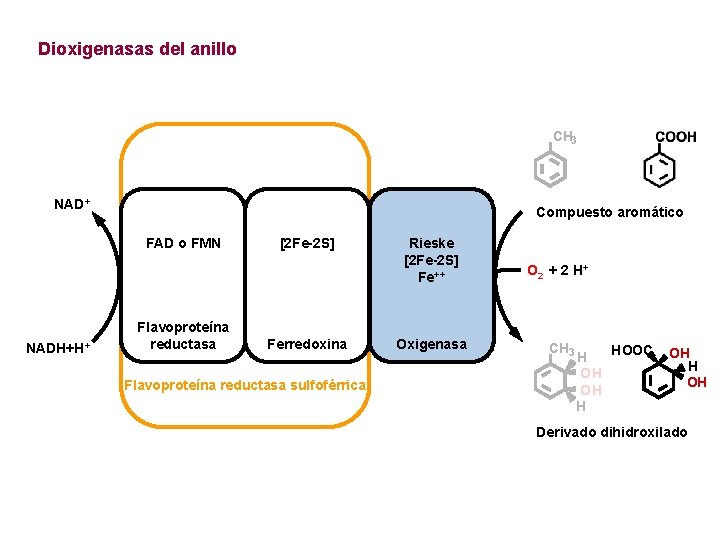
Dioxigenasas del anillo CH 3 NAD+ Compuesto aromático FAD o FMN NADH+H+ Flavoproteína reductasa [2 Fe-2 S] Ferredoxina Flavoproteína reductasa sulfoférrica Rieske [2 Fe-2 S] Fe++ Oxigenasa O 2 + 2 H + CH 3 H OH OH H HOOC OH H OH Derivado dihidroxilado
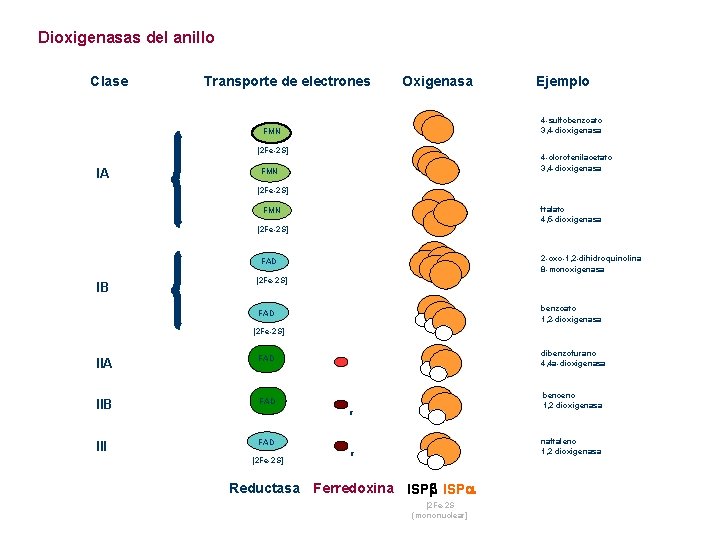
Dioxigenasas del anillo Clase Transporte de electrones Oxigenasa 4 -sulfobenzoato 3, 4 -dioxigenasa FMN [2 Fe-2 S] IA Ejemplo 4 -clorofenilacetato 3, 4 -dioxigenasa FMN [2 Fe-2 S] ftalato 4, 5 -dioxigenasa FMN [2 Fe-2 S] 2 -oxo-1, 2 -dihidroquinolina 8 -monoxigenasa FAD IB [2 Fe-2 S] benzoato 1, 2 -dioxigenasa FAD [2 Fe-2 S] IIA FAD dibenzofurano 4, 4 a-dioxigenasa IIB FAD benceno 1, 2 dioxigenasa III FAD R [2 Fe-2 S] naftaleno 1, 2 dioxigenasa R Reductasa Ferredoxina ISP [2 Fe-2 S (mononuclear]

A resaltar: Generalmente varias subunidades Cadena más o menos compleja de transporte de electrones. La reacción que llevan a cabo es similar. Especificidad de sustrato Sustratos metabolizados por la ruta TOL: tolueno, m-xyleno, p-xyleno, 3 -etiltolueno, 1, 2, 4 trimetilbenzeno, . . . Es una limitación, pero es manipulable. “Rasgos” que identifican una ruta: Modo de activación del anillo Modo de rotura del anillo
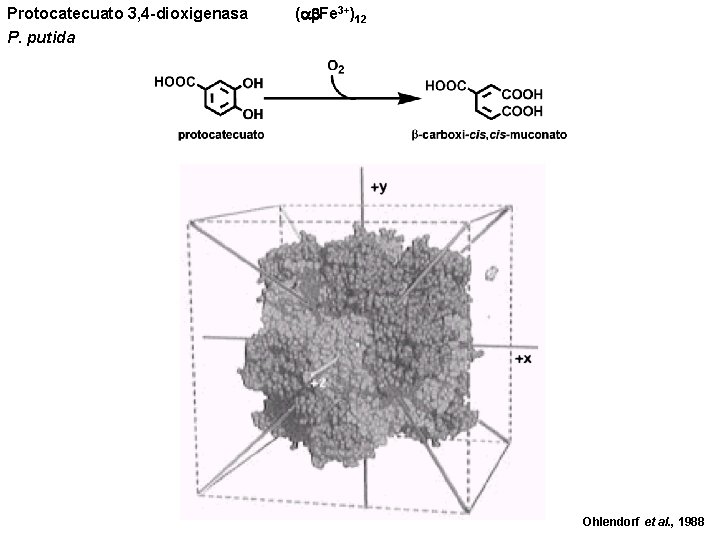
Protocatecuato 3, 4 -dioxigenasa P. putida ( Fe 3+)12 Ohlendorf et al. , 1988
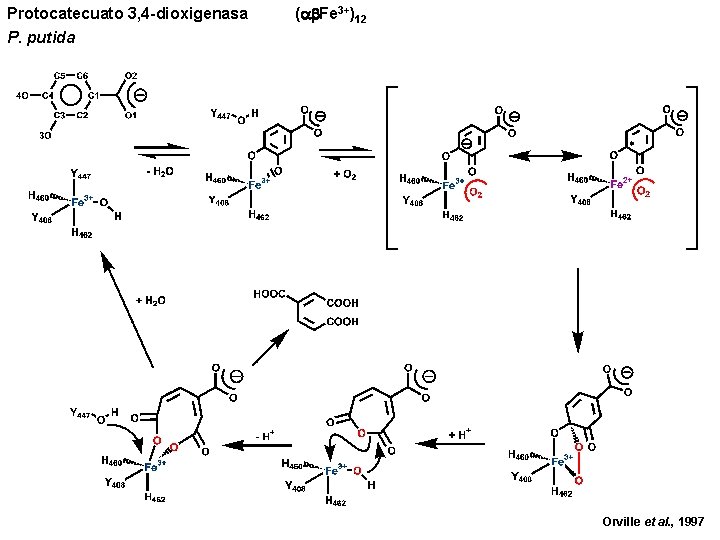
Protocatecuato 3, 4 -dioxigenasa P. putida ( Fe 3+)12 Orville et al. , 1997
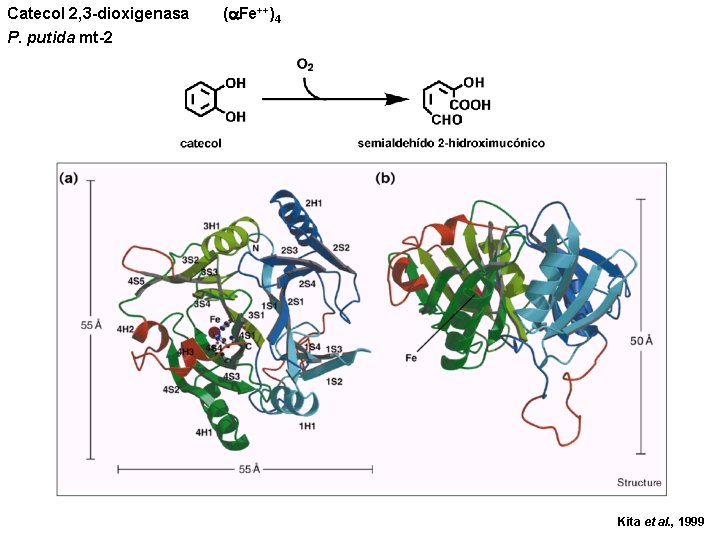
Catecol 2, 3 -dioxigenasa P. putida mt-2 ( Fe++)4 Kita et al. , 1999
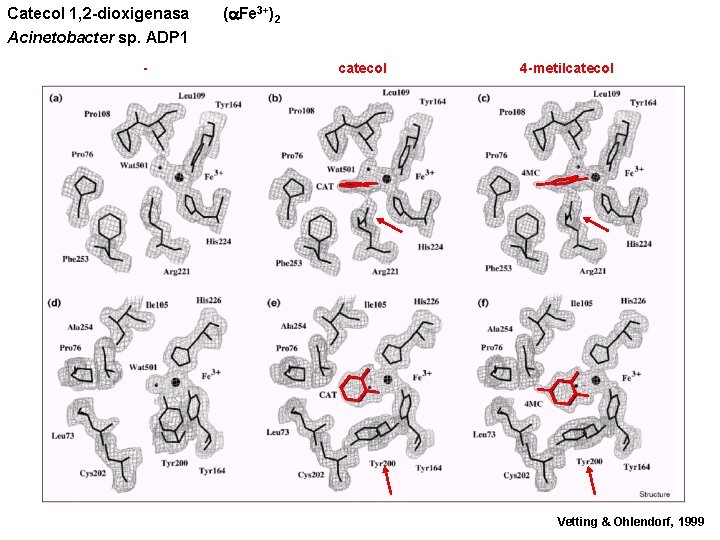
Catecol 1, 2 -dioxigenasa Acinetobacter sp. ADP 1 - ( Fe 3+)2 catecol 4 -metilcatecol Vetting & Ohlendorf, 1999

Degradación anaeróbica de tolueno

Introducción Catabolismo de hidrocarburos aromáticos se consideraba EXTRICTAMENTE dependiente de O 2. En las rutas descritas, el ataque inicial del anillo requiere SIEMPRE O 2 molecular (Mono- y Dioxigenasas). Últimos 10 años: algunos organismos TAMBIÉN puede degradar Hidrocarburos en ANAEROBIOSIS. Procesos anaerobios están empezando a mostrar un gran POTENCIAL para la solución de problemas de contaminación ambiental.

Historia Observación: aromáticos NO se acumulan en la naturaleza en zonas anaerobias. 1985 -86 El tolueno es degradado en sedimentos contaminados con hidrocarburos. 1990 Se consiguen los primeros cultivos puros. Tanto de zonas contaminadas como pristinas Están taxonómicamente relacionados

Aerobio vs anaerobio Aerobios: Oxígeno cumple dos funciones: - Aceptor de electrones (RESPIRACIÓN) - Sustrato de las dioxigenasas Anaerobios: - Oxígeno puede sustituirse por OTROS ACEPTORES - La reactividad del O 2 en Oxigenasas es INSUSTITUIBLE Estos organismos deben de haber desarrollado rutas diferentes, novedosas, independientes del oxígeno.

Reacciones estequiométricas de oxidación anaeróbica de tolueno acopladas a la reducción de diferentes aceptores de electrones. • Bacterias desnitrificantes : C 7 H 8 + 7. 2 NO 3 - + 0. 2 H+ 7 HCO 3 - + 3. 6 N 2 + 0. 6 H 2 O Gº’ = - 3554 k. J (mol tolueno)-1 • Bacterias reductoras de hierro (III) : C 7 H 8 + 94 Fe(OH)3 7 Fe. CO 3 + 29 Fe 3 O 4 + 145 H 2 O Gº’ = -3398 k. J (mol tolueno)-1 • Bacterias sulfatoreductoras : C 7 H 8 + 4. 5 SO 4= + 3 H 2 O 7 HCO-3 + 2. 5 H+ +4. 5 HS Gº’ = -205 k. J (mol tolueno)-1

Cepas bacterianas disponibles en cultivo puro e identificadas Bacterias desnitrificantes (subclase de proteobacterias) • • • Thauera aromatica K 172 Thauera aromatica T 1 Azoarcus sp. Cepa T. Azoarcus tolulyticus Tol 4 Azoarcus tolulyticus Td 15 Bacterias reductoras de hierro (subclase de proteobacterias) • Geobacter metallireducens GS 15 Bacterias sulfatoreductoras (subclase de proteobacterias) • • Desulfobacula toluolica Tol 2 Desulfobacterium cetonicum

Elucidación de la ruta La activación del sustrato (tolueno) y la rotura en ausencia de O 2 es similar en todas las cepas anerobias, independientemente del aceptor de electrones que utilice. ¿Cómo se activa el anillo? ¿Cómo es la apertura del anillo? Microbiología/ecología de anaerobios.
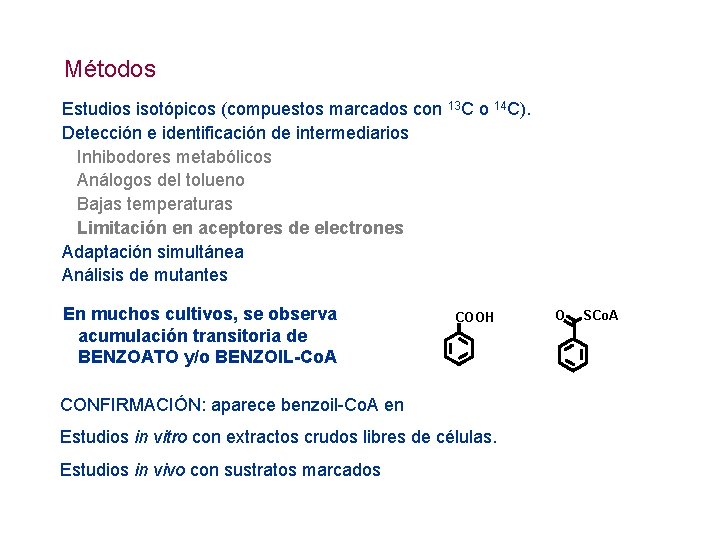
Métodos Estudios isotópicos (compuestos marcados con 13 C o 14 C). Detección e identificación de intermediarios Inhibodores metabólicos Análogos del tolueno Bajas temperaturas Limitación en aceptores de electrones Adaptación simultánea Análisis de mutantes En muchos cultivos, se observa acumulación transitoria de BENZOATO y/o BENZOIL-Co. A COOH CONFIRMACIÓN: aparece benzoil-Co. A en Estudios in vitro con extractos crudos libres de células. Estudios in vivo con sustratos marcados O SCo. A
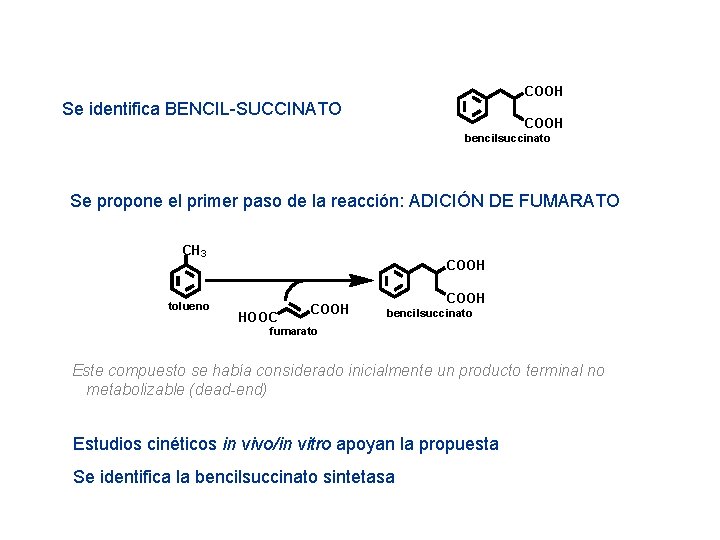
COOH Se identifica BENCIL-SUCCINATO COOH bencilsuccinato Se propone el primer paso de la reacción: ADICIÓN DE FUMARATO CH 3 tolueno COOH HOOC COOH bencilsuccinato fumarato Este compuesto se había considerado inicialmente un producto terminal no metabolizable (dead-end) Estudios cinéticos in vivo/in vitro apoyan la propuesta Se identifica la bencilsuccinato sintetasa
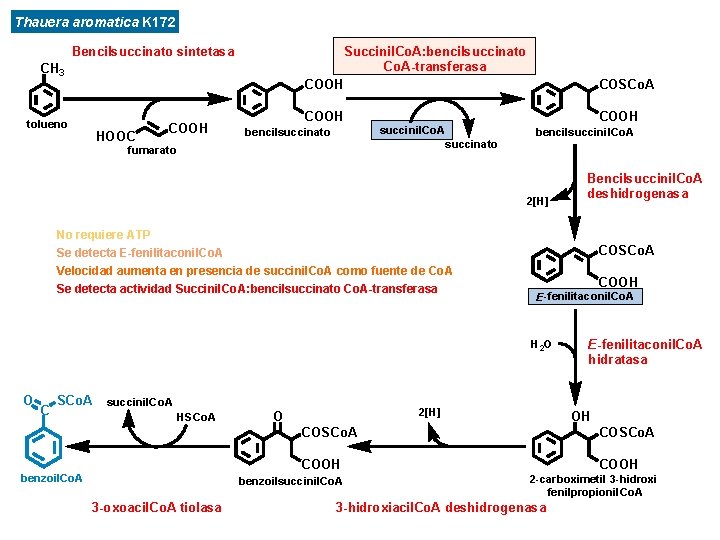
Thauera aromatica K 172 Bencilsuccinato sintetasa Succinil. Co. A: bencilsuccinato Co. A-transferasa COOH CH 3 tolueno HOOC COOH COSCo. A COOH succinil. Co. A bencilsuccinato bencilsuccinil. Co. A succinato fumarato 2[H] No requiere ATP Se detecta E-fenilitaconil. Co. A Velocidad aumenta en presencia de succinil. Co. A como fuente de Co. A Se detecta actividad Succinil. Co. A: bencilsuccinato Co. A-transferasa COSCo. A COOH E-fenilitaconil. Co. A H 2 O O C SCo. A succinil. Co. A HSCo. A 2[H] O COSCo. A COOH benzoilsuccinil. Co. A 3 -oxoacil. Co. A tiolasa E-fenilitaconil. Co. A hidratasa OH COSCo. A benzoil. Co. A Bencilsuccinil. Co. A deshidrogenasa COOH 2 -carboximetil 3 -hidroxi fenilpropionil. Co. A 3 -hidroxiacil. Co. A deshidrogenasa

No se han detectado ni todos los intermediarios ni todas las reacciones. Pero cada vez hay más datos que apoyan esta ruta. Comprobado en detalle en Thauera y Azoarcus (desnitrificantes) Algunas de las reacciones se han identificados en bacterias sulforreductoras (muy distintas filogenéticamente). Mecanismo común a todas las cepas (? ) Anillo activado (benzoil. Co. A) Rotura: en todos los casos, reacción hidrolítica. Es necesaria una reducción previa del anillo: Benzoil. Co. A Reductasa (requiere ATP; es MUY específica) Sigue -oxidación Las reacciones hasta la rotura del anillo están DEMOSTRADAS en Thauera y en Rhodopseudomonas
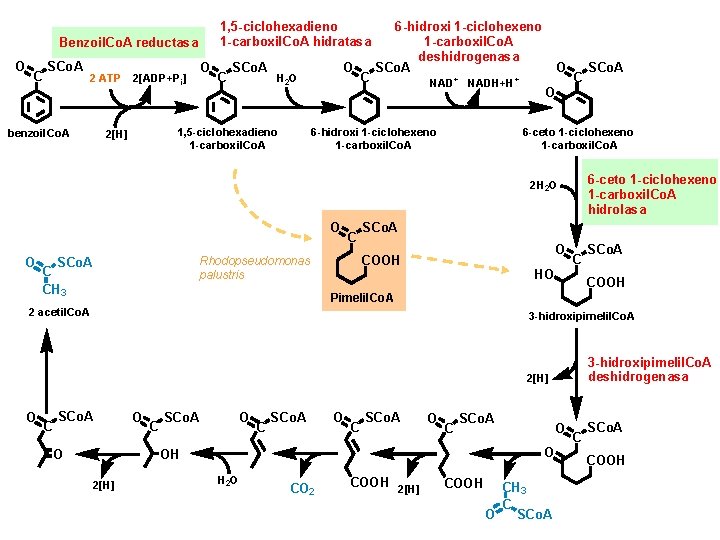
1, 5 -ciclohexadieno 1 -carboxil. Co. A hidratasa Benzoil. Co. A reductasa O C SCo. A 2 ATP benzoil. Co. A O 2[ADP+Pi] C SCo. A 1, 5 -ciclohexadieno 1 -carboxil. Co. A 2[H] O H 2 O C 6 -hidroxi 1 -ciclohexeno 1 -carboxil. Co. A deshidrogenasa SCo. A NAD + NADH+H 6 -hidroxi 1 -ciclohexeno 1 -carboxil. Co. A O + C O 6 -ceto 1 -ciclohexeno 1 -carboxil. Co. A hidrolasa 2 H 2 O O O C C CH 3 SCo. A O COOH Rhodopseudomonas palustris SCo. A C HO COOH 3 -hidroxipimelil. Co. A deshidrogenasa 2[H] C SCo. A Pimelil. Co. A 2 acetil. Co. A O SCo. A O O C SCo. A O OH 2[H] O H 2 O CO 2 COOH 2[H] COOH CH 3 C O SCo. A COOH
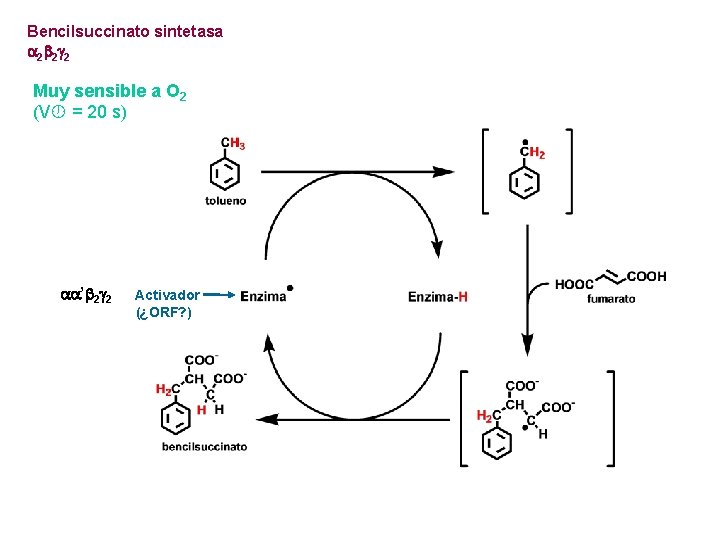
Bencilsuccinato sintetasa 2 2 g 2 Muy sensible a O 2 (V = 20 s) ’ 2 g 2 Activador (¿ORF? )
![Benzoil. Co. A reductasa Especificida de sustrato 2[4 Fe-4 S] Donador de electrones? Ferredoxina Benzoil. Co. A reductasa Especificida de sustrato 2[4 Fe-4 S] Donador de electrones? Ferredoxina](http://slidetodoc.com/presentation_image/d68e262d90ae3e9d49ea79b4be6f13f5/image-41.jpg)
Benzoil. Co. A reductasa Especificida de sustrato 2[4 Fe-4 S] Donador de electrones? Ferredoxina Fe/S FAD Benzoil Co. A reductasa g
![Co-sustratos anaerobios: 2 [H], CO 2, ATP, Co. A, H 2 O O 2 Co-sustratos anaerobios: 2 [H], CO 2, ATP, Co. A, H 2 O O 2](http://slidetodoc.com/presentation_image/d68e262d90ae3e9d49ea79b4be6f13f5/image-42.jpg)
Co-sustratos anaerobios: 2 [H], CO 2, ATP, Co. A, H 2 O O 2 [H] 2 ATP ANAEROBIOSIS O CO SCo. A benzoil-Co. A H 2 O Intermedios centrales (anaerobios) OH SCo. A OH resorcinol REDUCCIÓN del anillo RUPTURA HIDROLÍTICA OH Co. ASH COOH HO OH fluoroglucinol OH O 2 OH catecol OXIDACIÓN del anillo RUPTURA OXIGENOLÍTICA OH COOH OH AEROBIOSIS OH O 2 OH protocatecuato COOH Co-sustratos aerobios: O 2, H 2 O COOH HO OH gentisato Intermedios centrales (aerobios)
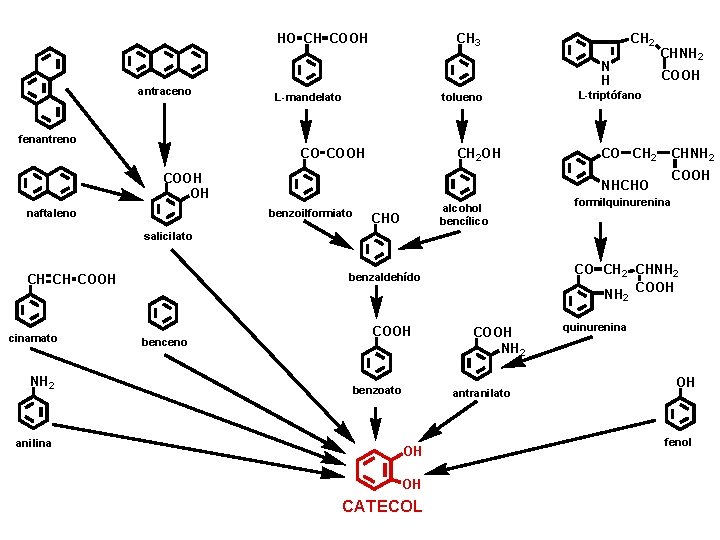
HO CH COOH antraceno CH 3 CH 2 N H L-mandelato tolueno CHNH 2 COOH L-triptófano fenantreno CO COOH CH 2 OH COOH OH naftaleno CO CH 2 CHNH 2 COOH NHCHO benzoilformiato alcohol bencílico CHO formilquinurenina salicilato CO CH 2 CHNH 2 NH COOH benzaldehído CH CH COOH 2 cinamato NH 2 anilina benceno COOH benzoato COOH NH 2 antranilato OH OH CATECOL quinurenina OH fenol
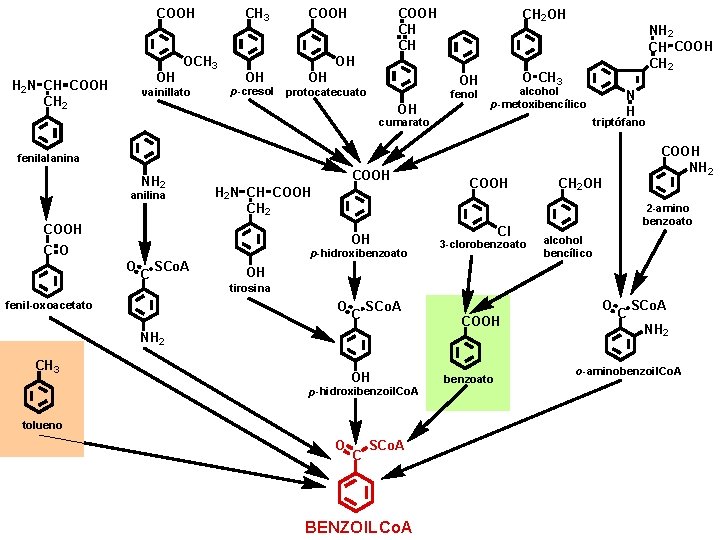
CH 3 COOH OH H 2 N CH COOH CH 2 OCH 3 vainillato COOH CH CH COOH CH 2 OH NH 2 CH COOH CH 2 OH OH p-cresol OH OH protocatecuato fenol OH O CH 3 alcohol p-metoxibencílico N H triptófano cumarato COOH NH 2 fenilalanina NH 2 anilina COOH H 2 N CH COOH CH 2 COOH OH C O O C SCo. A p-hidroxibenzoato COOH Cl 3 -clorobenzoato CH 2 OH 2 -amino benzoato alcohol bencílico OH tirosina O fenil-oxoacetato C O SCo. A COOH NH 2 CH 3 OH p-hidroxibenzoil. Co. A tolueno O C SCo. A BENZOILCo. A benzoato C SCo. A NH 2 o-aminobenzoil. Co. A

Características generales de cepas anaerobias que degradan tolueno Tanto estrictas como facultativas. Espectro de hidrocarburos aromáticos que son capaces de degradar es MUY REDUCIDO. tg generalmente mayor que en aerobios. (desnitrificantes son las que tienen velocidad de crecimiento mayor) Muchas formas de respiración.

Identificación de GENES Mutagénesis al azar - química - transposones SELECCIÓN de clones inactivos secuenciación (cromosoma) Genoteca - Complementación - Búsqueda de actividades Confirmación - producto génico - Comparación con proteína conocida Análisis de secuencia

Aplicaciones Gran potencial para la solución de problemas de contaminación medioambiental. Zonas contaminadas con frecuencia son ANAEROBIAS. OXIGENACIÓN $$ TRANSPORTE no es considerable en áreas grandes. Considerar recuperación in situ basada en organismos ANAEROBIOS. Adición de otros aceptores de electrones, más solubles (fácil y barato). Degradación lenta Aplicable cuando la contaminación sólo afecta al suelo (no hay acuífero amenazado).

Estimaciones energéticas potenciales Oxígeno disuelto en agua saturada: Esto permitiría oxidar 2, 8 mg tolueno/l 8, 6 mg/l Concentración saturante de sulfato en agua: Esto permitiría oxidar (anaeróbicamente) 2 g/l 300 mg tolueno/l Pero Procesos aerobios son mucho más RÁPIDOS. Organismos aerobios son más versátiles.
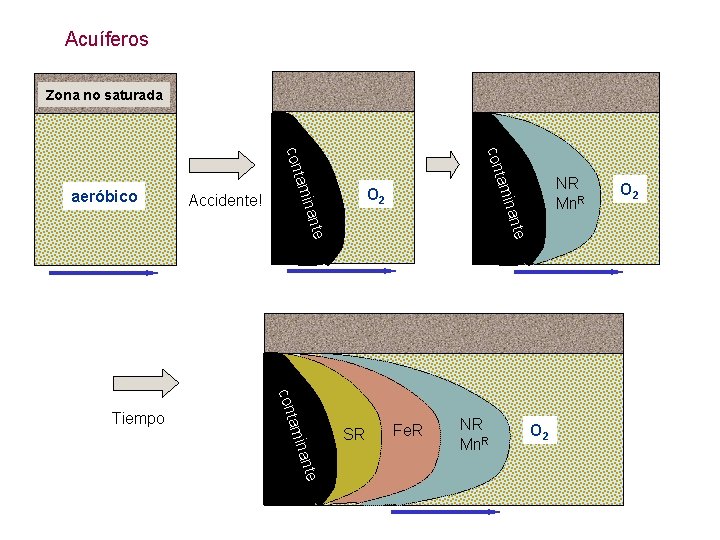
Acuíferos Zona no saturada O 2 ante nte mina a cont Tiempo NR Mn. R amin Accidente! cont aeróbico SR Fe. R NR Mn. R O 2
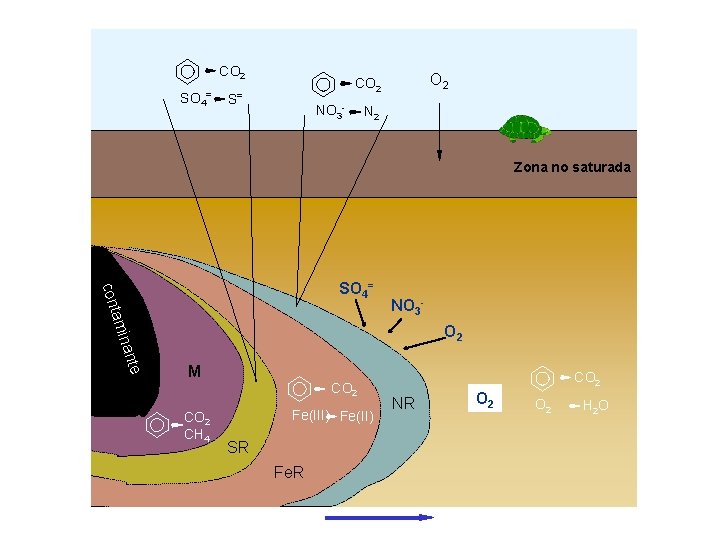
CO 2 SO 4= O 2 CO 2 S= NO 3 - N 2 Zona no saturada NO 3 - nte mina a cont SO 4= O 2 M CO 2 CH 4 Fe(III) Fe(II) SR Fe. R CO 2 NR O 2 H 2 O
- Slides: 50