DEFINISI KIMIA ANALISIS CABANG ILMU KIMIA YG MEMPELAJARIMENDASARI

DEFINISI KIMIA ANALISIS : CABANG ILMU KIMIA YG MEMPELAJARI&MENDASARI TTG CARA ANALISIS DAN PEMISAHAN BAHAN.

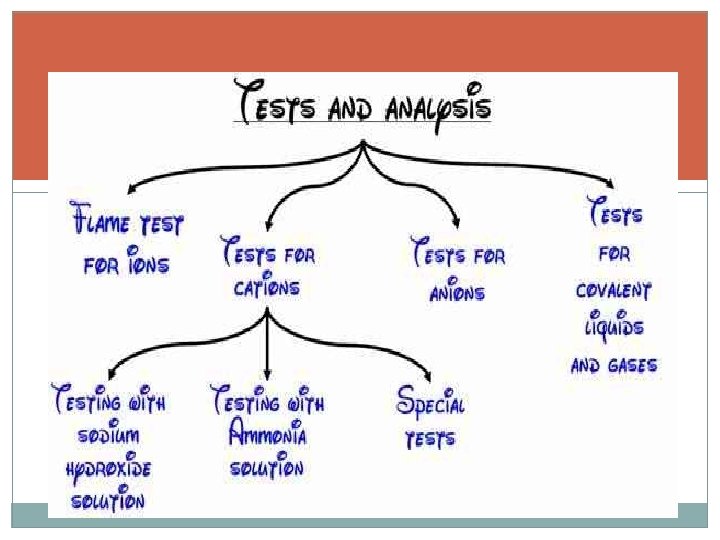
PENGGOLONGAN TEKNIK ANALISIS KUALITATIF Menentukan dan mengidentifikasi keberadaan suatu unsur/senyawa kimia baik organik maupun inorganik ANALISIS KUANTITATIF Mengetahui jumlah suatu unsur/senyawa dlm suatu cuplikan

A. Senyawa obat maupun bahan pembantu (eksipien) dalam suatu sediaan obat selain terdiri dari bahan organik juga terdapat beberapa bahan anorganik. B. Unsur logam dalam larutannya akan membentuk ion positif (kation), sedangkan unsur non logam akan membentuk ion negatif (anion). C. Untuk identifikasi dapat digunakan pendekatan melalui pengamatan warna, bau, terbentuknya gelembung gas ataupun endapan, reaksi asam-basa, redoks, kompleks.

Analisis cara kering … (1) � PERUBAHAN PADA PEMANASAN sedikit zat dalam tabung uji dipanaskan perlahan-lahan dan akan terjadi perubahan yang dapat diamati. Kesimpulan Pengarangan karena pembakaran dan terbentuk karbondioksida Zat-zat organik Hitam tapi tidak disertai pembakaran dan bau Garam Cu, Mn, Ni Kuning (panas), putih (dingin) Zn. O dan garam-garam Zn Kuning coklat (panas), kuning (dingin) Sn. O 2 dan Bi. O 3 Kuning (panas / dingin) Pb. O dan garam Pb Coklat (panas / dingin) Cd. O dan garam Cd Merah hitam (panas), coklat (dingin) Fe 2 O 3 Putih (panas / dingin) Garam Na, K, Ba, Ca, Mg, Pb
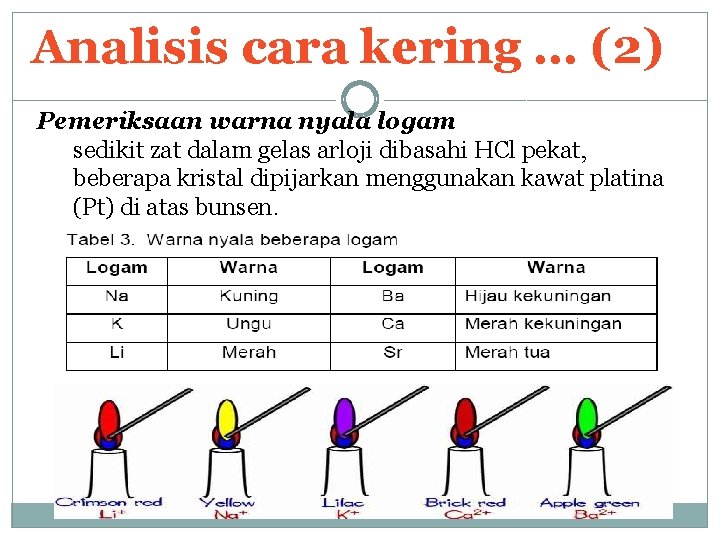
Analisis cara kering … (2) Pemeriksaan warna nyala logam sedikit zat dalam gelas arloji dibasahi HCl pekat, beberapa kristal dipijarkan menggunakan kawat platina (Pt) di atas bunsen.

Analisis cara basah HASIL REAKSI DAPAT DIKETAHUI DENGAN MENGAMATI ADANYA PERUBAHAN YANG TERJADI, YANG PADA UMUMNYA BERUPA TERBENTUKNYA ENDAPAN, TIMBULNYA GAS, DAN PERUBAHAN WARNA.

Reaksi pengendapan Ksp adalah tetapan kesetimbangan untuk kelarutan suatu senyawa ionik yang sukar larut, ksp adalah tetapan kesetimbangan untuk kelarutan suatu senyawa ionik yang sukar larut. Mm. An(s) m M+(aq) + n A-(aq) Ksp = [M+]m [A-]n

REDOKS 1. 2. 3. 4. KALIUM PERMANGANAT KALIUM KROMAT ASAM NITRAT HIDROGEN PEROKSIDA

REAKSI PEMBENTUKAN KOMPLEKS

ANALISIS KATION � Menurut sistematika berikut, kation digolongkan berdasarkan atas perbedaan kelarutan dari garam klorida, sulfida dan karbonat sebagai berikut : Gol I (Gol. Asam Klorida), II (Gol. Asam Sulfida), III (Gol. Amonium Sulfida), IV (Gol. Amonium Karbonat), V (Gol. Sisa). Golongan 4 , dapat mengendap dengan larutan Amonium Karbonat

Lab Procedures For Qualitative Kation Analysis Solution containing ions of all cation groups + HCl encer Larut + H 2 S (p. H 0, 5) filtration Mengendap : Cu. S, Cd. S, Hg. S, + Amonium polisulfida filtration Bi 2 S 3 (Gol. II A), , Sn. S 2, Sb 2 Sb 3 (Gol. II B) (Gol II B larut) + NH 4 OH + NH 4 Cl + (NH 4)2 S (p. H 9) filtration Larut + (NH 4)2 CO 3 Mengendap : Ag. Cl, Hg 2 Cl 2, Pb. Cl 2 (Gol. I) filtration Larutan : Na+, K+, NH 4+ ions (Gol. V) Mengendap : Co. S, Fe. S, Mn. S, Ni. S, Zn. S, Al(OH)3, Cr(OH)3 (Gol. III) Mengendap : Ba. CO 3, Ca. CO 3, Sr. CO 3 (Gol. IV)

ANALISIS KATION GOLONGAN I larut dalam suhu panas atau dengan H 2 SO 4 membentuk endapan putih Pb. SO 4
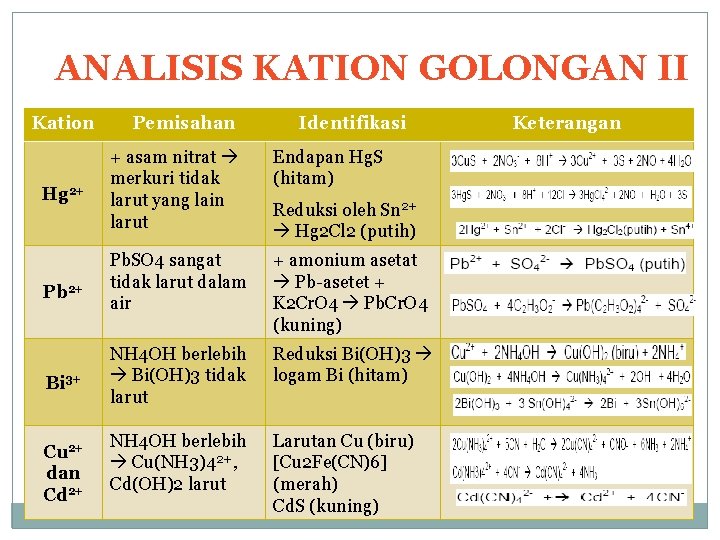
ANALISIS KATION GOLONGAN II Kation Hg 2+ Pb 2+ Bi 3+ Cu 2+ dan Cd 2+ Pemisahan Identifikasi + asam nitrat merkuri tidak larut yang lain larut Endapan Hg. S (hitam) Pb. SO 4 sangat tidak larut dalam air + amonium asetat Pb-asetet + K 2 Cr. O 4 Pb. Cr. O 4 (kuning) NH 4 OH berlebih Bi(OH)3 tidak larut Reduksi Bi(OH)3 logam Bi (hitam) NH 4 OH berlebih Cu(NH 3)42+ , Cd(OH)2 larut Larutan Cu (biru) [Cu 2 Fe(CN)6] (merah) Cd. S (kuning) Reduksi oleh Sn 2+ Hg 2 Cl 2 (putih) Keterangan

ANALISIS KATION GOLONGAN III Kation Fe 2+ Co 2+ Mn 2+ Al 3+ dan Cr 3+ Pemisahan Identifikasi H 2 SO 4 hidoksida besi larut K 4 Fe(CN)6 (biru prusian) Fe(SCN)63(merah) H 2 SO 4 hidoksida Co lambat larut + KSCN dalam alkohol kompleks Co(SCN)2 - (biru), H 2 SO 4 hidoksida Mn lambat laru Oksidasi Mn 2+ Mn. O 4 - (ungu dg Na. Bi. O 3) + Na. OH larut + asam nitrat + cromat Cr 2 O 72(jingga) + NH 4(OH) endapan Al (putih) Keterangan perlu ditambah Na. F Fe. F 63(tidak berwarna)
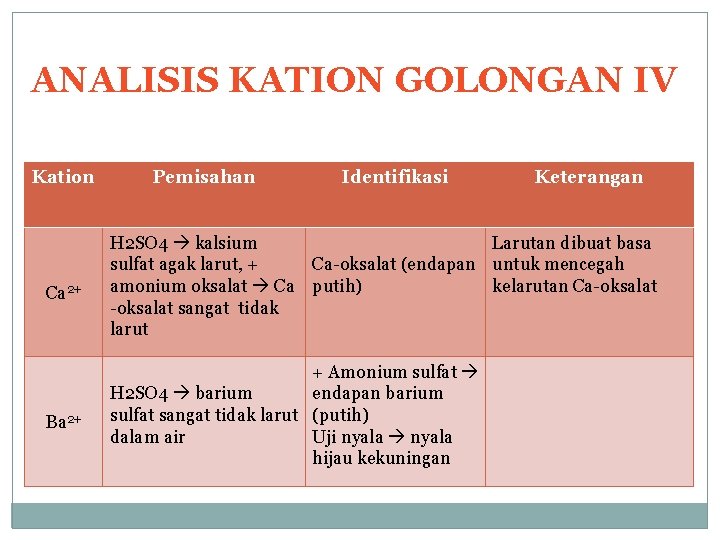
ANALISIS KATION GOLONGAN IV Kation Pemisahan Identifikasi Keterangan Ca 2+ H 2 SO 4 kalsium Larutan dibuat basa sulfat agak larut, + Ca-oksalat (endapan untuk mencegah amonium oksalat Ca putih) kelarutan Ca-oksalat sangat tidak larut Ba 2+ + Amonium sulfat H 2 SO 4 barium endapan barium sulfat sangat tidak larut (putih) dalam air Uji nyala hijau kekuningan

ANALISIS KATION GOLONGAN V Kation Mg 2+ Na+ , K+ , NH 4+ Pemisahan Identifikasi + Na 2 HPO 4 keadaan basa Mg. NH 4 PO 4 (mengendap) + pereaksi magneson I / II + Na. OH Mg(OH)2 (putih) mengadsorbsi magneson (biru) Tidak mengendap dengan pereaksi sebelumnya Uji nyala Na+ (kuning), K+ (merah keunguan) Gas NH 4+ (bau amoniak) Keterangan



ANALISIS ANION GOLONGAN SULFAT + PEREAKSI BACL 2 GARAM BARIUM TAK LARUT AIR BERWARNA PUTIH, KECUALI BACR 2 O 4 (KUNING) Golongan Halida + Asam Nitrat + Perak Nitrat Garam Perak Tak Larut Air Berwarna : Ag. Cl (putih), Ag. Br (kuning), Ag. I (kuning muda)


ANALISIS OBAT - pemeriksaan organoleptis yaitu pengamatan pendahuluan dengan menggunakan indera kita, dilihat, diraba kehalusannya dengan ujung jari, dibau dan dirasakan - Kelarutan. Zat dicoba diselidiki kelarutannya dengan bermacam-macam zat pelarut baik anorganik dan organik - fluoresensi dibawah lampu ultra violet. Bentuk serbuk dalam larutan dilihat dibawah lampu UV - Pengarangan dan pemijaran. Pengarangan bertujuan untuk mengetahui zat yang diperiksa organik atau anorganik, sedangkan pemijaran untuk mengetahui zat yang diperiksa mengandung anion atau kation - analisis elemen, dilakukan seperti pada praktikum kimia organik untuk mengetahui unsur-unsur penyusun senyawa tersebut : C, N, S, P atau unsur halogen : Cl, Br, I

- analisis gugus, perlu diidentifikasi adanya inti benzen, fenol, alkohol polivalen, gugus mereduksi, aldehid, amina aromatik, gugus sulfon, gugus aldehid, dll - analisis pendahuluan, hal ini untuk mengetahui termasuk golongan apa senyawa yang diselidiki, termasuk: golongan karbohidrat, Fenol/salisilat, anilin, barbiturat, pirazolon, sulfonamid, alkaloid, atau piridin - reaksi penjurusan, mengamati perubahan warna sampel setelah direaksikan dengan menggunakan pereaksi Fehling A dan B, Vanilin test, Fluoresensi larutan H 2 SO 4 encer, Murexide, Marquis, Virtali, Kufrifil Chen & Ko - reaksi khusus meliputi : zwikker kardizol, Hexamin, Santosin, uji borat, dan pengamatan bentuk kristal melalui mikroskop

� Here is an example of a question: A sample of a solution of an unknown was treated with dilute HCl. The white precipitate formed was filtered and washed with hot water. A few drops of KI solution were added to the hot water filtrate and a bright yellow precipitate was produced. The white precipitate remaining on the filter paper was readily soluble in NH 3 solution. What two ions could have been present in the unknown? (A) Ag+ and Hg 22+ (B) Ag+ and Pb 2+ (C) Ba 2+ and Ag+ (D) Ba 2+ and Hg 22+ (E) Ba 2+ and Pb 2+ Answer : What happens at each step? Solution – Ag+ forms a precipitate with chlorides (Ag. Cl), so what is the other metal? Think of a metal that would likely be insoluble with I- Pb 2+ is a good choice because in our labs, it formed mostly yellow/orange precipitates.

TERIMA KASIH WASSALAMUALAIKUM. . .
- Slides: 25