Dalle soluzioni alla chimica del carbonio Gruppi funzionali

Dalle soluzioni alla chimica del carbonio

Gruppi funzionali e polimeri di sintesi Capitolo 15 Unità 48 Derivati funzionali degli idrocarburi 15. 1 Composti monofunzionali e polifunzionali 15. 2 Gli alogenuri alchilici e arilici 15. 3 Gli alcoli 15. 4 Gli alcoli più importanti 15. 5 I fenoli 15. 6 I tioli 15. 7 Gli eteri 15. 8 Le aldeidi 15. 9 I chetoni Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 2

Gruppi funzionali e polimeri di sintesi Capitolo 15 15. 10 15. 11 15. 12 15. 13 15. 14 Gli acidi carbossilici più importanti Gli acidi grassi Gli esteri e le anidridi acide Le ammine Unità 49 I polimeri 15. 15 Polimeri di addizione e di condensazione 15. 16 Polimeri di addizione 15. 17 Le materie plastiche 15. 18 Polimeri di condensazione Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 3

15. 1 Composti monofunzionali e polifunzionali I composti organici possono essere suddivisi in base al gruppo funzionale presente, che ne condiziona le caratteristiche. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 4

15. 1 Composti monofunzionali e polifunzionali I composti monofunzionali contengono un solo gruppo funzionale nella loro molecola e danno le reazioni tipiche di quel gruppo. I composti polifunzionali contengono più gruppi funzionali nella loro molecola e danno tutte le reazioni tipiche dei gruppi presenti. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 5

15. 2 Gli alogenuri alchilici e arilici Gli alogenuri alchilici e gli alogenuri arilici possono essere considerati derivati dalla sostituzione di un atomo di idrogeno, rispettivamente di un alcano a catena aperta o di un idrocarburo aromatico, con un atomo di un alogeno. Danno reazione di sostituzione: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 6

15. 2 Gli alogenuri alchilici e arilici Sono importanti alogenuri: il cloroformio CHCl 3, il tetracloruro di carbonio CCl 4, il Freon® CF 2 Cl 2, il DDT e la diossina. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 7

15. 3 Gli alcoli possono essere considerati derivati dagli alcani per sostituzione di un idrogeno con il gruppo ossidrilico �OH. Hanno formula generale R �OH. Si classificano in primari, secondari o terziari sulla base del numero di atomi di carbonio legati al carbonio che porta il gruppo ossidrilico. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 8

15. 3 Gli alcoli Il gruppo �OH può formare legami idrogeno: gli alcoli a corta catena sono solubili in acqua, se aumenta il numero degli atomi di carbonio la solubilità diminuisce. Gli alcoli a basso PM sono liquidi, quelli a lunga catena solidi. La nomenclatura IUPAC prescrive il suffisso -olo. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 9

15. 3 Gli alcoli sono molto più reattivi degli alcani, perché la presenza dell’ossigeno provoca una polarizzazione dei legami. L’atomo di ossigeno del gruppo ossidrilico è nucleofilo e reagisce quindi con atomi elettrofili come i metalli alcalini. Si forma uno ione alcossido (RO–), una base molto forte. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 10

15. 3 Gli alcoli sono preparati tramite riduzione catalitica delle aldeidi e dei chetoni e l’idrolisi alcalina degli alogenuri alchilici. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 11

15. 4 Gli alcoli più importanti Il metanolo è un importante solvente organico. L’etanolo è utilizzato come disinfettante, come solvente, nei profumi e nei liquori. Può essere ottenuto attraverso la fermentazione alcolica ad opera dei lieviti, che trasformano il glucosio. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 12

15. 4 Gli alcoli più importanti Si chiamano polialcoli i composti con più gruppi alcolici. Il più importante polialcol è il glicerolo, detto comunemente glicerina, un comune componente delle creme per la pelle. I grassi e gli oli sono sostanze derivate dal glicerolo. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 13

15. 5 I fenoli sono composti organici che hanno nella molecola uno o più gruppi ossidrilici �OH legati a un anello benzenico. Il primo componente di questa classe di composti è chiamato fenolo. A differenza degli alcoli sono acidi deboli. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 14

15. 6 I tioli Il gruppo funzionale dei tioli o tioalcoli è il gruppo sulfidrilico o tiolico �SH in cui l’atomo di zolfo sostituisce quello di ossigeno. Hanno formula generale R �SH. Possono essere considerati derivati dall’acido solfidrico H 2 S per sostituzione di un idrogeno con un radicale alchilico. L’attività di molti enzimi è legata alla presenza di gruppi �SH. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 15

15. 7 Gli eteri hanno formula generale R �O �R′. I due radicali R e R′ possono essere uguali o diversi; Non formano legami idrogeno, per cui, essendo poco polari la loro solubilità in acqua è limitata e la temperatura di ebollizione è bassa. Sono poco reattivi e il loro uso è in genere quello di solvente organico. Il più importante è l’etere etilico. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 16

15. 8 Le aldeidi sono composti organici caratterizzati dal gruppo carbonilico L’atomo di carbonio è legato ad almeno un atomo di idrogeno. Le aldeidi hanno formula generale R �CHO e il gruppo �CHO è chiamato gruppo aldeidico. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 17
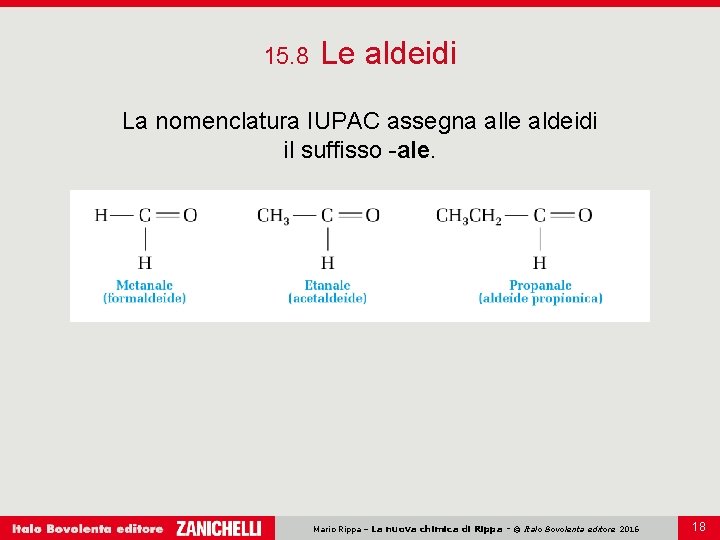
15. 8 Le aldeidi La nomenclatura IUPAC assegna alle aldeidi il suffisso -ale. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 18
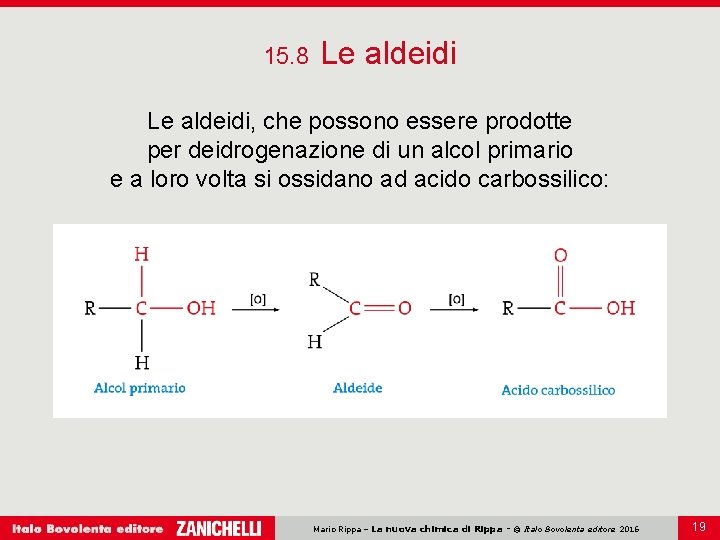
15. 8 Le aldeidi, che possono essere prodotte per deidrogenazione di un alcol primario e a loro volta si ossidano ad acido carbossilico: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 19
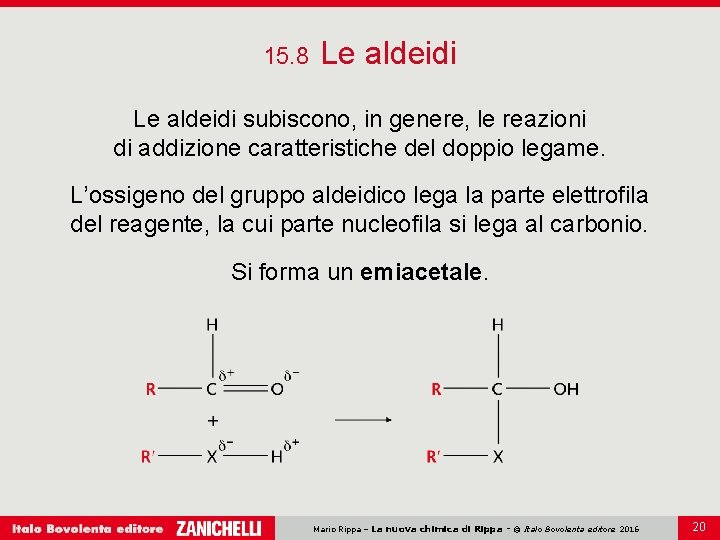
15. 8 Le aldeidi subiscono, in genere, le reazioni di addizione caratteristiche del doppio legame. L’ossigeno del gruppo aldeidico lega la parte elettrofila del reagente, la cui parte nucleofila si lega al carbonio. Si forma un emiacetale. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 20

15. 8 Le aldeidi possono essere facilmente ridotte ad alcoli primari in presenza di catalizzatori e di agenti riducenti, come idruri o idrogeno molecolare: La più semplice aldeide è il metanale H �CO, detto comunemente formaldeide, un gas incolore di odore pungente, solubilissimo in acqua. La sua soluzione acquosa è chiamata formalina. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 21

15. 9 I chetoni Anche i chetoni contengono il gruppo carbonilico. Nei chetoni il carbonio del gruppo carbonilico è legato attraverso due legami singoli a due atomi di carbonio. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 22
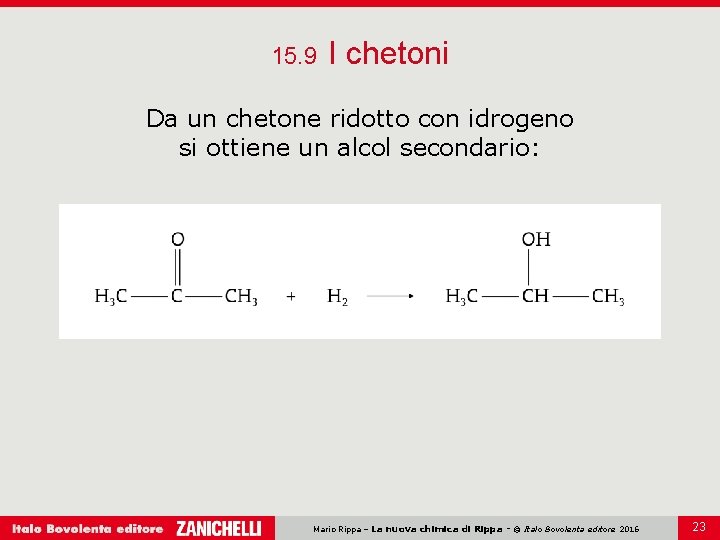
15. 9 I chetoni Da un chetone ridotto con idrogeno si ottiene un alcol secondario: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 23

15. 9 I chetoni La nomenclatura IUPAC prescrive il suffisso -one. L’acetone è un liquido volatile, di odore grato, infiammabile e molto solubile in acqua. È un ottimo solvente per molti composti organici, per vernici, lacche e celluloide. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 24

15. 10 Gli acidi carbossilici Il gruppo carbossilico �COOH è il gruppo funzionale degli acidi carbossilici, che hanno formula generale R �COOH. La nomenclatura IUPAC assegna agli acidi carbossilici il suffisso -oico aggiunto al nome dell’alcano di partenza, preceduto dal termine acido. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 25

15. 10 Gli acidi carbossilici sono acidi deboli, che trattati con una base formano un sale e acqua: Gli acidi carbossilici hanno in genere punti di ebollizione elevati, in quanto possono stabilire legami idrogeno: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 26

15. 10 Gli acidi carbossilici Gli acidi si ottengono per ossidazione di un alcol primario o di un’aldeide: Gli acidi danno luogo a reazioni di sostituzione formando nuove classi di sostanze. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 27

15. 10 Gli acidi carbossilici Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 28

15. 11 Gli acidi carbossilici più importanti L’acido formico H �COOH è stato chiamato così perché isolato per la prima volta dalle formiche. L’azione irritante delle punture di molti insetti e delle ortiche è dovuta appunto all’acido formico. L’acido acetico CH 3 �COOH è stato isolato per la prima volta dall’aceto, di cui costituisce dal 5 al 7%. Acido formico e acido acetico sono solubili in acqua in tutte le proporzioni. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 29

15. 11 Gli acidi carbossilici più importanti L’acido propionico CH 3 CH 2 �COOH si forma nella maturazione dei formaggi. Uno dei componenti caratteristici del burro è un derivato dell’acido butirrico CH 3 CH 2 �COOH. L’acido benzoico C 6 H 5 �COOH è il più semplice acido carbossilico aromatico. Un suo importante derivato è l’acido acetilsalicilico, l’aspirina. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 30

15. 11 Gli acidi carbossilici più importanti Importanti acidi bicarbossilici sono: Tra gli acidi tricarbossilici ricordiamo l’acido citrico, che conferisce l’aroma e l’acidità al succo di limone. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 31

15. 12 Gli acidi grassi Sono detti acidi grassi gli acidi carbossilici alifatici insolubili in acqua a causa della lunga catena carboniosa. Gli acidi grassi naturali contengono un numero pari di atomi di carbonio. Sono acidi grassi saturi: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 32

15. 12 Gli acidi grassi Sono acidi grassi insaturi: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 33
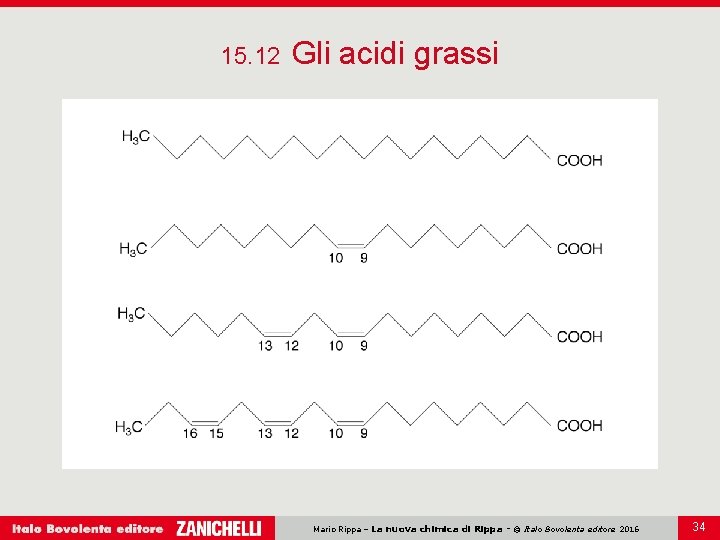
15. 12 Gli acidi grassi Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 34

15. 12 Gli acidi grassi saturi sono composti relativamente stabili, in quanto gli atomi di carbonio della catena sono uniti da legami semplici. Gli acidi grassi insaturi sono più reattivi a causa della presenza del doppio legame. Gli acidi grassi insaturi sono più facilmente ossidabili in corrispondenza del doppio legame. L’ossidazione causa la scomposizione dell’acido grasso in due molecole sature a catena più breve (irrancidimento). La riduzione con idrogeno trasforma un acido grasso insaturo in acido grasso saturo. Questo processo si chiama idrogenazione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 35

15. 13 Gli esteri e le anidridi acide Gli esteri sono composti che derivano dagli acidi carbossilici e hanno formula generale R �C(=O)O �R′. Il nome si ottiene aggiungendo il suffisso -ato al tema dell’acido corrispondente, seguito dal nome del radicale proveniente dall’alcol. Si ottengono dalla reazione di esterificazione di un acido carbossilico con un alcol: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 36

15. 13 Gli esteri e le anidridi acide Una classe importante di derivati degli acidi carbossilici è rappresentata dalle anidridi acide. Il termine anidride significa «senza acqua» . Le anidridi acide si possono formare dalla condensazione di un acido carbossilico con se stesso, eliminando una molecola d’acqua: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 37

15. 14 Le ammine sono derivati organici dell’ammoniaca NH 3. Se sostituiamo uno, due o tutti e tre gli atomi di idrogeno dell’ammoniaca con uno, due o tre radicali, abbiamo rispettivamente le ammine primarie, secondarie e terziarie: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 38

15. 14 Le ammine A causa del doppietto elettronico sull’atomo di azoto le ammine sono basiche e l’atomo di azoto è un nucleofilo. L’anilina C 6 H 5 NH 2 è uno dei prodotti base per la preparazione di colori, coloranti e sostanze farmaceutiche. Le ammine reagiscono con gli acidi carbossilici e dalla loro unione per condensazione si ottiene una famiglia di composti, le ammidi, caratterizzati dal gruppo funzionale R — CO — NH 2. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 39

15: 15 Polimeri di addizione e di condensazione Il processo di formazione di grandi molecole con elevato peso molecolare a partire da piccole unità è detto polimerizzazione. Le grandi molecole ad altissimo peso molecolare che si formano a partire dalla singola unità, detta monomero, sono i polimeri. A seconda delle condizioni in cui si svolge la reazione di polimerizzazione si ottengono polimeri con caratteristiche diverse. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 40

15: 15 Polimeri di addizione e di condensazione A seconda del meccanismo con cui avviene la polimerizzazione si possono avere due tipi di polimeri: i polimeri di addizione, se la polimerizzazione avviene a seguito della trasformazione di doppi legami in legami semplici; i polimeri di condensazione quando si uniscono monomeri con gruppi funzionali diversi, che reagiscono eliminando molecole d’acqua. In base ai loro usi e alle loro proprietà, i polimeri sono classificati come: materiali gommosi o elastomeri; film flessibili; tessuti sintetici e fibre; resine o plastiche. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 41

15: 16 Polimeri di addizione Nei polimeri di addizione, se il monomero è un composto insaturo come l’etene (CH 2 = CH 2), il doppio legame si rompe e si ottengono due atomi di carbonio con un elettrone spaiato. Si ha un’addizione radicalica. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 42

15: 16 Polimeri di addizione Alcuni composti chiamati perossidi organici R — O — R sono utilizzati come iniziatori di reazioni di polimerizzazione radicalica. Quando gli alcheni di base sono diversi si forma un copolimero. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 43
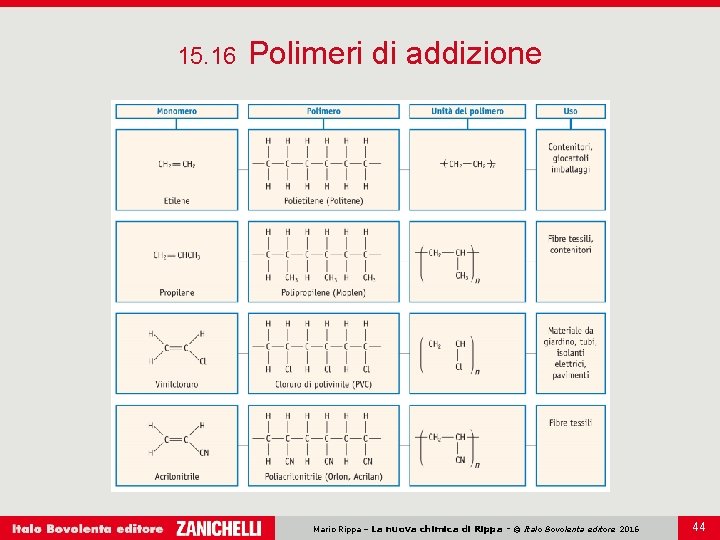
15. 16 Polimeri di addizione Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 44
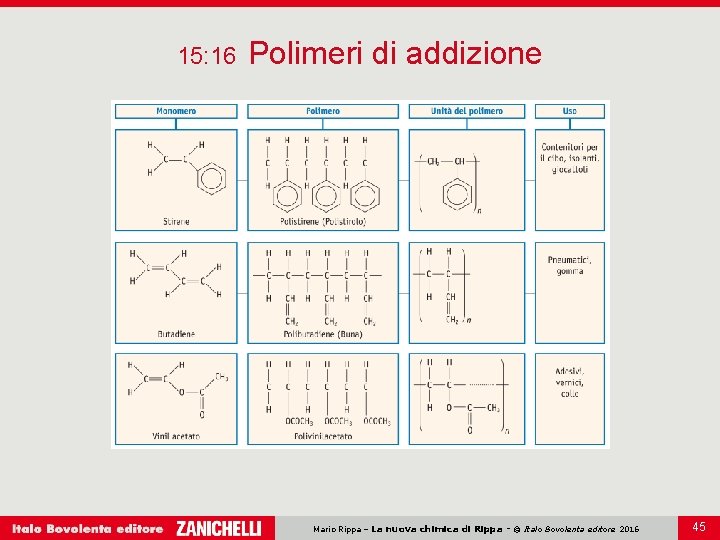
15: 16 Polimeri di addizione Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 45

15. 17 Le materie plastiche sono polimeri artificiali che possono essere deformati e modellati a piacimento finché sono allo stato fluido. Le materie plastiche sono termoplastiche se sono deformabili a caldo e rigide a freddo, ma per riscaldamento ritornano plastiche. Termoindurenti se non sono più deformabili una volta assunta una forma per riscaldamento e raffreddate. Alcune materie plastiche sono trasformate in fibre e sono utilizzate per la fabbricazione di tessuti e corde. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 46

15. 18 Polimeri di condensazione I polimeri di condensazione si formano quando due gruppi funzionali come il gruppo alcolico, il gruppo carbossilico o il gruppo amminico reagiscono tra loro con reazioni di condensazione a catena. Ognuna di queste molecole ha una doppia possibilità di unione, una in testa e una in coda. La struttura generale di un polimero di condensazione è: continua ~ A – B – A – B ~ continua Si formano in questo modo poliammidi, poliesteri, policarbonati e poliuretani. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 47
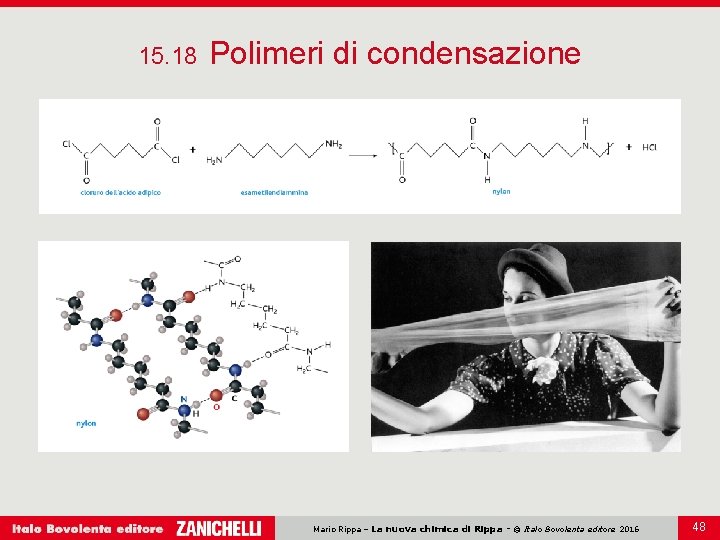
15. 18 Polimeri di condensazione Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 48
- Slides: 48