Dalle soluzioni alla chimica del carbonio Capitolo 11

Dalle soluzioni alla chimica del carbonio

Capitolo 11 Acidi e basi Unità 35 Teorie sugli acidi e le basi 11. 1 La teoria di Arrhenius 11. 2 Acidi e basi secondo Brønsted-Lowry 11. 3 Acidi e basi secondo Lewis Unità 36 L’equilibrio acido-base 11. 4 La ionizzazione e il prodotto ionico dell’acqua 11. 5 Soluzioni acide, basiche e neutre 11. 6 Equilibri di dissociazione di acidi e basi 11. 7 Elettronegatività e comportamento acido-base Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 2

Capitolo 11 Acidi e basi Unità 37 Il p. H 11. 8 La scala del p. H 11. 9 Calcolo del p. H delle soluzioni 11. 10 Reazioni di neutralizzazione acido-base Unità 38 Il comportamento acido-base dei sali 11. 11 L’idrolisi salina 11. 12 Le soluzioni tampone Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 3

Capitolo 11 Acidi e basi Unità 39 La concentrazione di acidi e basi nelle soluzioni 11. 13 Gli indicatori di p. H 11. 14 La titolazione acido-base 11. 15 Equivalente chimico e normalità Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 4

11. 1 La teoria di Arrhenius Acidi e basi sono tra le sostanze più comuni presenti in natura e sono normalmente presenti nelle nostre case. A B Acidi e soluzioni acide (A) e basi e soluzioni basiche (B) sono comunemente utilizzati per la pulizia della casa e nel settore alimentare. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 5

11. 1 La teoria di Arrhenius Nel 1675 Boyle descrisse gli acidi come le sostanze che: hanno sapore aspro; reagiscono con i metalli liberando idrogeno; sono solventi; danno reazione di neutralizzazione con le basi; colorano di rosso la cartina tornasole. Le basi invece: sono amare; danno reazione di neutralizzazione con gli acidi; colorano di blu la cartina tornasole. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 6

11. 1 La teoria di Arrhenius Fu Arrhenius a dare una prima spiegazione al comportamento acido e basico di alcune sostanze. Egli osservò che gli acidi e le basi in soluzione conducevano la corrente elettrica, perché davano luogo alla formazione di ioni. Secondo Arrhenius gli acidi sono sostanze capaci di rilasciare in acqua idrogenioni H+, mentre le basi in acqua liberano ioni idrossido OH–. Acidi: HCl(aq) → H+(aq) + Cl–(aq) HNO 3(aq) → H+(aq) + NO– 3(aq) Basi: Na. OH(aq) → Na+(aq) + OH–(aq) Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 7

11. 1 La teoria di Arrhenius Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 8

11. 1 La teoria di Arrhenius Quando un acido in acqua si ionizza, lo ione H+ si lega tramite un legame dativo all’atomo di ossigeno di una molecola di acqua. Si forma così il catione H 3 O+, chiamato ione ossonio o ione idronio. CO 2 + 2 H 2 O ⇄ H 3 O+ + HCO 3– NH 3 + H 2 O ⇄ NH 4+ + OH– Un acido secondo Arrhenius è una sostanza che incrementa la concentrazione di ioni H 3 O+ in acqua; una base secondo Arrhenius è una sostanza che incrementa la concentrazione di ioni OH– in acqua. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 9
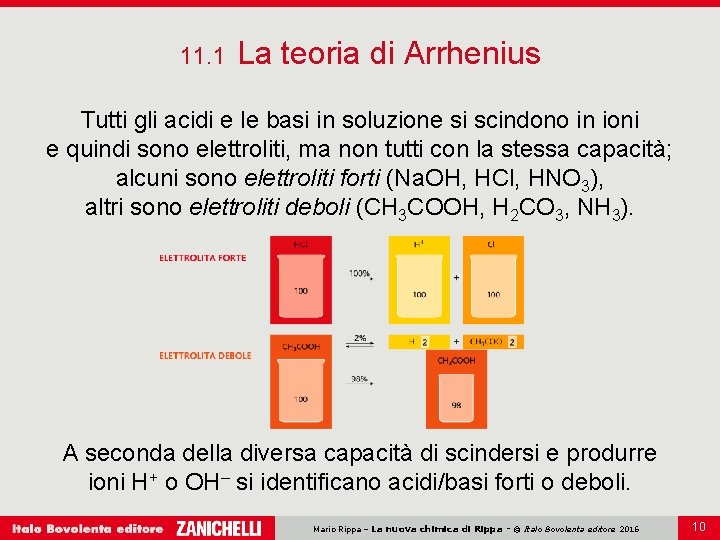
11. 1 La teoria di Arrhenius Tutti gli acidi e le basi in soluzione si scindono in ioni e quindi sono elettroliti, ma non tutti con la stessa capacità; alcuni sono elettroliti forti (Na. OH, HCl, HNO 3), altri sono elettroliti deboli (CH 3 COOH, H 2 CO 3, NH 3). A seconda della diversa capacità di scindersi e produrre ioni H+ o OH– si identificano acidi/basi forti o deboli. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 10

11. 2 Acidi e basi secondo Brønsted-Lowry Secondo la teoria di Brønsted-Lowry, un acido, che può essere una molecola o uno ione, rilascia un idrogenione a condizione che possa trasferirlo a una base, che è un’altra molecola o un altro ione. Un acido è una specie chimica capace di cedere un idrogenione a una base; una base è una specie chimica in grado di accettare un idrogenione da un acido. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 11
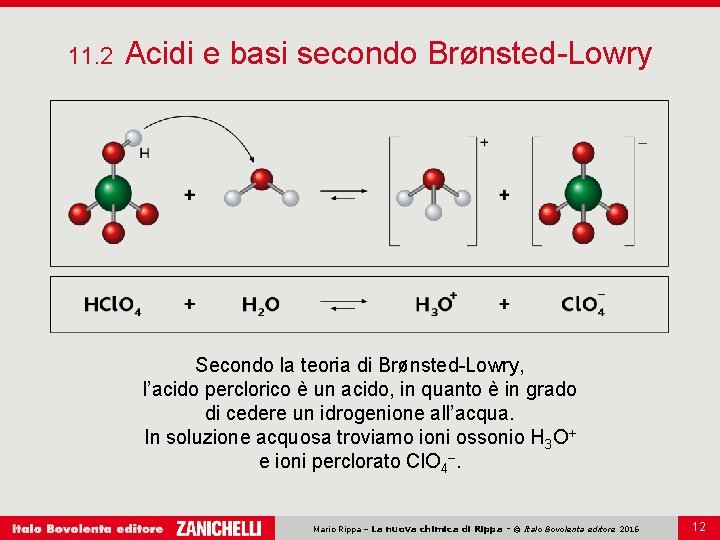
11. 2 Acidi e basi secondo Brønsted-Lowry Secondo la teoria di Brønsted-Lowry, l’acido perclorico è un acido, in quanto è in grado di cedere un idrogenione all’acqua. In soluzione acquosa troviamo ioni ossonio H 3 O+ e ioni perclorato Cl. O 4–. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 12

11. 2 Acidi e basi secondo Brønsted-Lowry Una reazione tra un acido e una base comporta il trasferimento di un idrogenione da una specie chimica a un’altra. Quando un acido perde l’idrogenione si trasforma nella sua base coniugata. Quando la base accetta l’idrogenione si trasforma nel suo acido coniugato. Le due specie chimiche differiscono per un idrogenione costituiscono una coppia coniugata acido-base. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 13
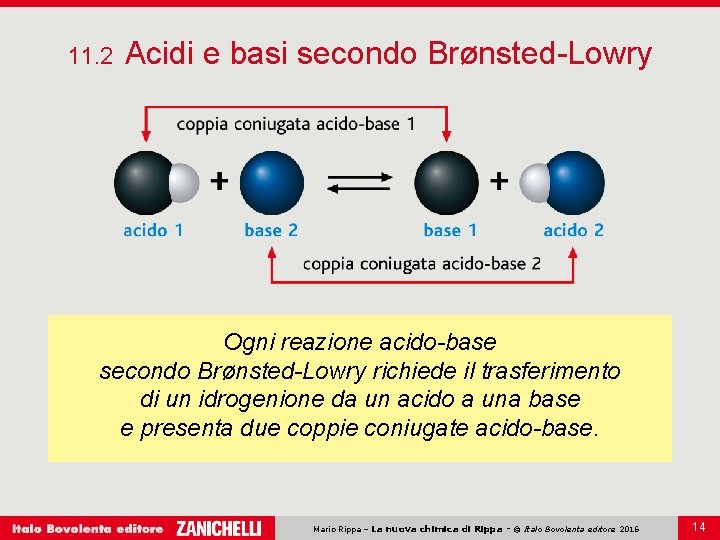
11. 2 Acidi e basi secondo Brønsted-Lowry Ogni reazione acido-base secondo Brønsted-Lowry richiede il trasferimento di un idrogenione da un acido a una base e presenta due coppie coniugate acido-base. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 14

11. 3 Acidi e basi secondo Lewis Una definizione più generale e più ampia di acido e base fu proposta nel 1930 da Gilbert Lewis. Un acido di Lewis è una specie in grado di accettare un doppietto elettronico da una base di Lewis per formare legame dativo. Una base di Lewis è una specie in grado di donare un doppietto elettronico a un acido di Lewis per formare un legame dativo. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 15

11. 3 Acidi e basi secondo Lewis I composti che si formano in queste reazioni sono chiamati complessi o composti di coordinazione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 16

11. 3 Acidi e basi secondo Lewis Sono reazioni acido-base secondo Lewis quella (A) dell’acido H+ con la base acqua, quella (B) dell’acido H+ con la base ammoniaca, quella (C) dell’acido Al. Cl 3 con la base ammoniaca, quella (D) del generico metallo M++ con la base acqua. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 17

11. 3 Acidi e basi secondo Lewis Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 18
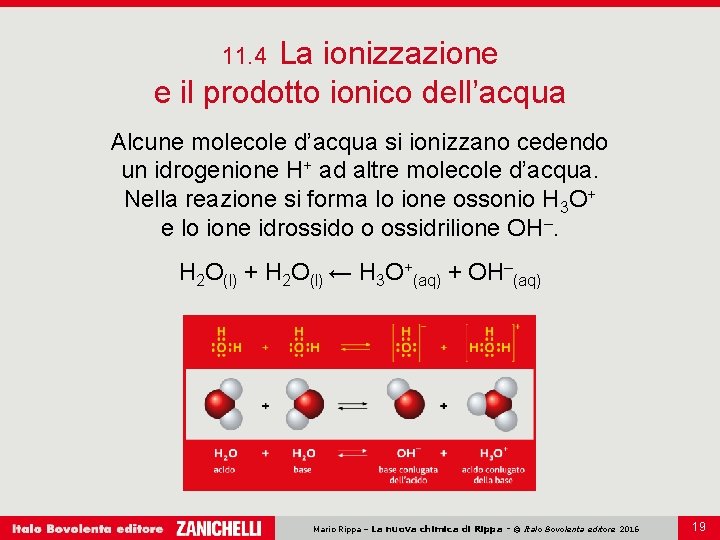
La ionizzazione e il prodotto ionico dell’acqua 11. 4 Alcune molecole d’acqua si ionizzano cedendo un idrogenione H+ ad altre molecole d’acqua. Nella reazione si forma lo ione ossonio H 3 O+ e lo ione idrossido o ossidrilione OH–. H 2 O(l) + H 2 O(l) ← H 3 O+(aq) + OH–(aq) Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 19

La ionizzazione e il prodotto ionico dell’acqua 11. 4 L’acqua è un elettrolita anfotero, in quanto si può comportare sia da acido che da base. La reazione di ionizzazione dell’acqua è reversibile e l’equilibrio è spostato verso sinistra. Il prodotto delle concentrazioni dello ione ossonio e dello ione idrossido in acqua è chiamato prodotto ionico dell’acqua Kw e ha il valore costante di 1, 0· 10– 14 a 25 °C Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 20

La ionizzazione e il prodotto ionico dell’acqua 11. 4 Nell’acqua la concentrazione dello ione ossonio è uguale a quella dello ione idrossido ed è 1, 0· 10– 7 M. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 21

11. 5 Soluzioni acidi, basiche e neutre Una soluzione neutra ha la concentrazione degli ioni ossonio uguale a quella degli ioni idrossido. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 22

11. 5 Soluzioni acidi, basiche e neutre Una soluzione acida contiene ioni ossonio in concentrazione superiore agli ioni idrossido, cioè [H 3 O+] è maggiore di 10– 7 M. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 23

11. 5 Soluzioni acidi, basiche e neutre Una soluzione basica contiene ioni idrossid in concentrazione superiore agli ioni ossonio, cioè [OH–] è maggiore di 10– 7 M. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 24
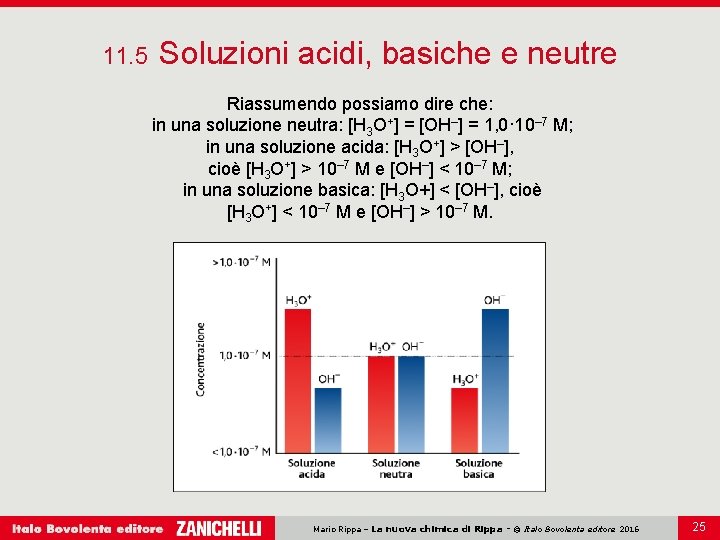
11. 5 Soluzioni acidi, basiche e neutre Riassumendo possiamo dire che: in una soluzione neutra: [H 3 O+] = [OH–] = 1, 0· 10– 7 M; in una soluzione acida: [H 3 O+] > [OH–], cioè [H 3 O+] > 10– 7 M e [OH–] < 10– 7 M; in una soluzione basica: [H 3 O+] < [OH–], cioè [H 3 O+] < 10– 7 M e [OH–] > 10– 7 M. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 25

11. 6 Equilibri di dissociazione di acidi e basi Acidi e basi che in acqua sono molto dissociati sono detti acidi forti e basi forti. Per un acido o per una base forte si può assumere che la concentrazione degli ioni H 3 O+ o degli ioni OH– in soluzione sia uguale alla concentrazione dell’acido o della base prima della dissociazione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 26

11. 6 Equilibri di dissociazione di acidi e basi Acidi e basi che in acqua sono parzialmente dissociati sono detti acidi deboli e basi deboli. Un acido debole in acqua ha la concentrazione degli ioni H 3 O+ sempre molto inferiore rispetto alla concentrazione dell’acido prima della dissociazione; stessa situazione vale per gli ioni OH– di una base debole. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 27

11. 6 Equilibri di dissociazione di acidi e basi L’equilibrio della dissociazione di un acido o di una base forte è fortemente spostato a sinistra e il valore della costante K è basso: K < 1. La costante di dissociazione degli acidi è detta costante di dissociazione dell’acido Ka, mentre Kb è la costante di dissociazione della base. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 28
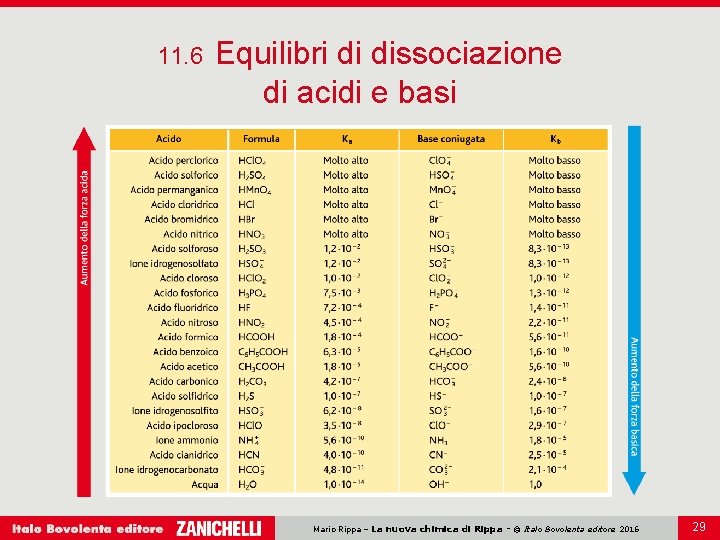
11. 6 Equilibri di dissociazione di acidi e basi Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 29

11. 6 Equilibri di dissociazione di acidi e basi Un valore elevato di Ka indica che i prodotti nella reazione di dissociazione sono favoriti rispetto ai reagenti e quindi l’acido è forte; più forte è l’acido, più debole è la sua base coniugata; più debole è l’acido, più forte è la sua base coniugata; maggiore è il valore di Ka in una coppia acido-base coniugata, minore è il valore di Kb, e viceversa; il prodotto Ka· Kb è uguale a 10– 14. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 30

11. 6 Equilibri di dissociazione di acidi e basi Gli acidi che possono cedere un solo idrogenione sono detti acidi monoprotici; gli acidi che possono cedere più idrogenioni sono detti acidi poliprotici. In particolare si dicono diprotici, triprotici o tetraprotici a seconda che siano in grado di cedere due, tre o quattro idrogenioni. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 31
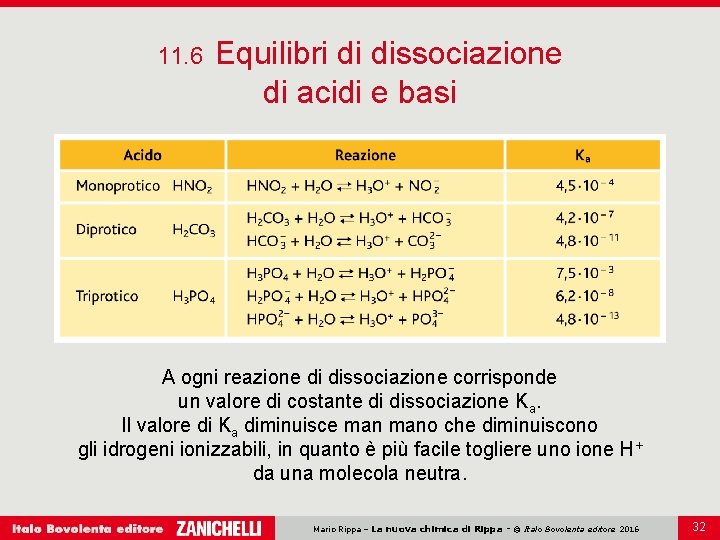
11. 6 Equilibri di dissociazione di acidi e basi A ogni reazione di dissociazione corrisponde un valore di costante di dissociazione Ka. Il valore di Ka diminuisce mano che diminuiscono gli idrogeni ionizzabili, in quanto è più facile togliere uno ione H+ da una molecola neutra. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 32

11. 6 Equilibri di dissociazione di acidi e basi Le basi che possono cedere un solo ione idrossido sono dette basi monoprotiche. Le basiche possono cedere più ioni idrossido sono dette basi polibasiche. In particolare si dicono dibasiche o tribasiche a seconda che siano in grado di ceder due o tre ioni idrossido. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 33
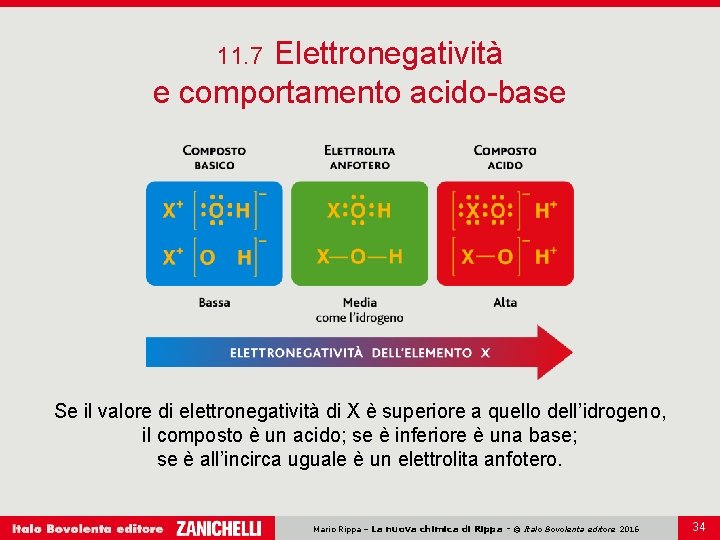
Elettronegatività e comportamento acido-base 11. 7 Se il valore di elettronegatività di X è superiore a quello dell’idrogeno, il composto è un acido; se è inferiore è una base; se è all’incirca uguale è un elettrolita anfotero. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 34

Elettronegatività e comportamento acido-base 11. 7 La formula di un composto può dare indicazioni sul comportamento acido o basico della sostanza. Un generico composto X — O — H si comporta da acido, da base o da elettrolita anfotero a seconda che X abbia, rispettivamente, un valore alto, basso o medio di elettronegatività. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 35

Elettronegatività e comportamento acido-base 11. 7 Le formule degli acidi e delle basi possono fornire indicazioni sulla loro forza. Consideriamo tre composti del tipo generico HOX, in cui X è un elemento del gruppo 17 del Sistema periodico: acido ipocloroso H �O �Cl acido ipobromoso H �O �Br acido ipoiodoso H �O �I Il cloro, che ha un’elettronegatività maggiore di quella degli altri due elementi, ha maggiore tendenza ad attirare su di sé gli elettroni di legame. L’acido ipocloroso è più dissociato e più forte. L’acido ipoiodoso è il meno dissociato e il meno forte dei tre, poiché lo iodio è l’elemento meno elettronegativo. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 36

Elettronegatività e comportamento acido-base 11. 7 Per quanto riguarda gli idrossidi, sono basi più forti gli idrossidi più solubili e gli idrossidi in cui il metallo ha un valore di elettronegatività minore. Negli ossiacidi, l’acidità aumenta all’aumentare degli atomi di ossigeno legati tramite legame dativo al non-metallo. Ogni ossigeno legato con legame dativo al cloro attira su di sé gli elettroni di legame. L’atomo di cloro attira con più forza gli elettroni del legame covalente Cl–O, facendo spostare verso l’ossigeno gli elettroni del legame O–H. La dissociazione degli ioni H+ aumenta e aumenta la forza dell’acido. L’acido ipocloroso è debolissimo, l’acido perclorico è invece fortissimo. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 37

11. 8 La scala del p. H L’acidità e la basicità delle soluzioni è espressa tramite la concentrazione molare degli ioni H 3 O+ e degli ioni OH–, calcolata su scala logaritmica. Il p. H di una soluzione è il logaritmo negativo in base 10 della concentrazione dello ione ossonio, cioè p. H = –log 10 [H 3 O+]. Il p. OH di una soluzione è il logaritmo negativo in base 10 della concentrazione dello ione idrossido, cioè p. OH = –log 10 [OH–]. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 38

11. 8 La scala del p. H Poiché il prodotto ionico dell’acqua Kw è costante in tutte le soluzioni, ed è uguale a 1, 0· 10– 14, per tutte le soluzioni i valori di p. H e p. OH devono essere tali che la loro somma sia uguale a 14: p. H + p. OH = p. Kw = 14 Una soluzione è acida se il p. H è minore di 7, neutra se il p. H è uguale a 7, basica se il p. H è maggiore di 7. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 39
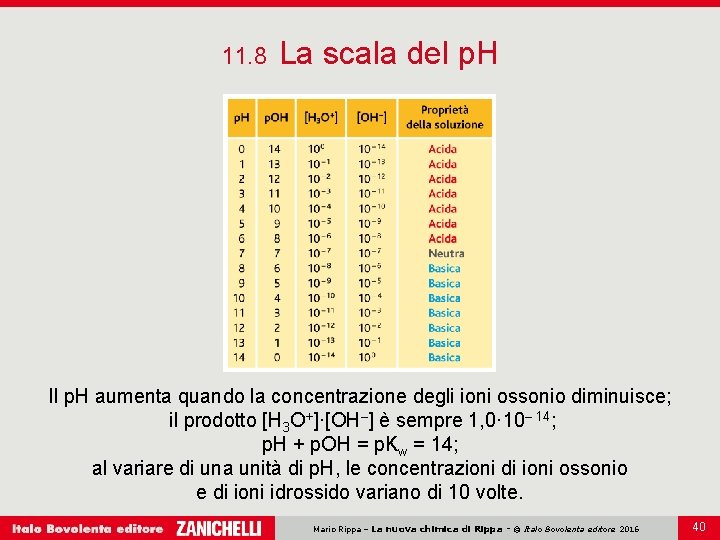
11. 8 La scala del p. H Il p. H aumenta quando la concentrazione degli ioni ossonio diminuisce; il prodotto [H 3 O+]·[OH–] è sempre 1, 0· 10– 14; p. H + p. OH = p. Kw = 14; al variare di una unità di p. H, le concentrazioni di ioni ossonio e di ioni idrossido variano di 10 volte. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 40
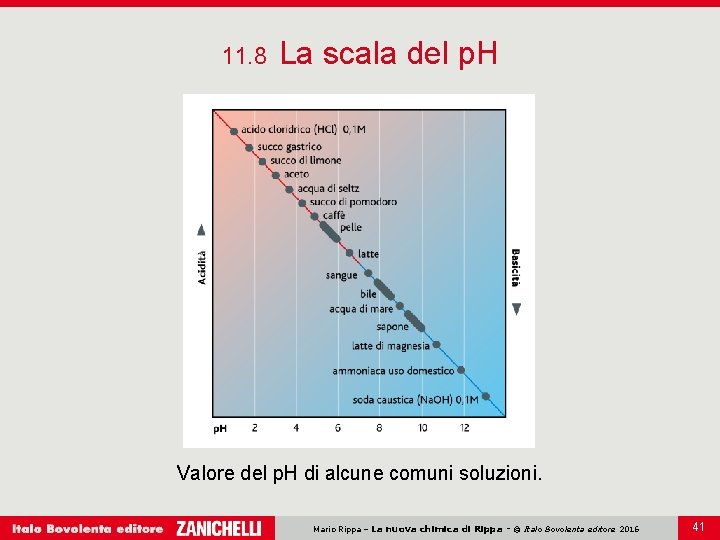
11. 8 La scala del p. H Valore del p. H di alcune comuni soluzioni. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 41

11. 8 La scala del p. H Per la misura rapida e diretta del p. H delle soluzioni si usa uno strumento chiamato p. H-metro. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 42

11. 9 Calcolo del p. H delle soluzioni Nel caso di acidi e basi forti la concentrazione dello ione ossonio o dello ione idrossido è uguale a quella dell’elettrolita di partenza. p. H = –log[H 3 O+] = –log. Ca p. OH = –log[OH-] = –log. Cb In pratica, per una soluzione 0, 1 M di un acido forte come l’acido nitrico HNO 3 p. H = –log [H 3 O+] = –log 10– 1 = – (– 1) = 1 Per una soluzione 0, 1 M di Na. OH, che è una base forte: p. OH = –log [OH–] = –log 10– 1 = – (– 1) = 1 Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 43

11. 9 Calcolo del p. H delle soluzioni Nel caso di acidi o di basi deboli, che si dissociano parzialmente in soluzione acquosa, la concentrazione di ioni ossonio o di ioni idrossido in soluzione è sempre inferiore alla concentrazione dell’elettrolita di partenza. Il p. H di un acido debole è sempre più alto del p. H di un acido forte alla stessa concentrazione e il p. OH di una base debole è sempre più basso del p. OH di una base forte alla stessa concentrazione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 44

11. 10 Reazioni di neutralizzazione acido-base La reazione tra un acido e una base prende il nome di reazione di neutralizzazione. In una reazione di neutralizzazione una soluzione di una base aggiunta a una quantità equimolare di un acido in soluzione, o viceversa, produce una soluzione di un sale in acqua. HCl + Na. OH → Na. Cl + H 2 O acido base sale acqua Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 45

11. 10 Reazioni di neutralizzazione acido-base Mescolando due soluzioni equimolari di HCl e Na. OH, tutti gli ioni idrossido si uniscono con gli ioni ossonio formando molecole di acqua. La soluzione ottenuta ha p. H = 7 e contiene ioni sodio e ioni cloruro. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 46

11. 11 L’idrolisi salina Le soluzioni acquose di alcuni sali non sono neutre. Il fenomeno per cui la soluzione di un sale è acida o basica si chiama idrolisi salina. La reazione di idrolisi acida avviene nelle soluzioni dei sali provenienti da un acido forte e una base debole; la reazione di idrolisi basica avviene nelle soluzioni dei sali provenienti da un acido debole e una base forte. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 47

11. 11 L’idrolisi salina Nel caso del cloruro di ammonio, un sale che possiamo considerare come proveniente da un acido forte (HCl) e una base debole (NH 3), avviene una reazione di idrolisi acida. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 48

11. 11 L’idrolisi salina Nel caso dell’acetato di sodio, un sale che consideriamo come proveniente da una base forte (Na. OH) e un acido debole (CH 3 COOH), avviene una reazione di idrolisi basica. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 49
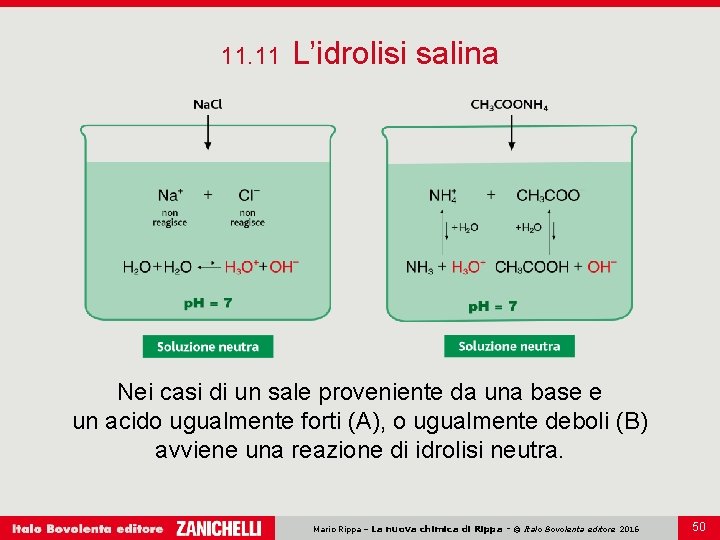
11. 11 L’idrolisi salina Nei casi di un sale proveniente da una base e un acido ugualmente forti (A), o ugualmente deboli (B) avviene una reazione di idrolisi neutra. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 50

11. 12 Le soluzioni tampone Alcune soluzioni sono in grado di limitare le variazioni di p. H quando vengono aggiunti acidi o basi. Il sistema chimico ottenuto unendo un acido debole a un suo sale con una base forte è in grado di catturare eventuali ioni H 3 O+ e OH– aggiunti, impedendo che il p. H cambi, ed è chiamato soluzione tampone. Una soluzione tampone, costituita da un acido debole e da un suo sale con una base forte o da una base debole e un suo sale con un acido forte, è un sistema in grado di limitare la variazione del p. H di una soluzione in seguito all’aggiunta di un acido o di una base. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 51

11. 12 Le soluzioni tampone Aggiungendo piccole quantità di acido o di base all’acqua si ha una notevole variazione del p. H. Se le stesse aggiunte sono fatte a una soluzione tampone, ad esempio di acido acetico CH 3 COOH e acetato di sodio CH 3 COONa, il p. H varia di poco. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 52

11. 12 Le soluzioni tampone Per le soluzioni tampone formate da un acido debole e da un suo sale con una base forte la concentrazione degli ioni H 3 O+ si ricava moltiplicando la Ka per il rapporto tra le moli di acido na e quelle del sale ns, in quanto il volume della soluzione in cui si trovano il sale e l’acido è lo stesso. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 53

11. 12 Le soluzioni tampone Per le soluzioni tampone formate da una base debole e da un suo sale con un acido forte: Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 54

11. 13 Gli indicatori di p. H Alcune sostanze assumono colori diversi a seconda del p. H e sono chiamate indicatori di p. H. Gli indicatori di p. H sono acidi deboli, le cui molecole assumono colori diversi a seconda che siano in forma dissociata o indissociata, dal cui colore è possibile risalire al p. H della soluzione. Per il principio dell’equilibrio mobile, l’aggiunta o la sottrazione di ioni ossonio alla soluzione fa spostare l’equilibrio, e fa cambiare il colore della soluzione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 55
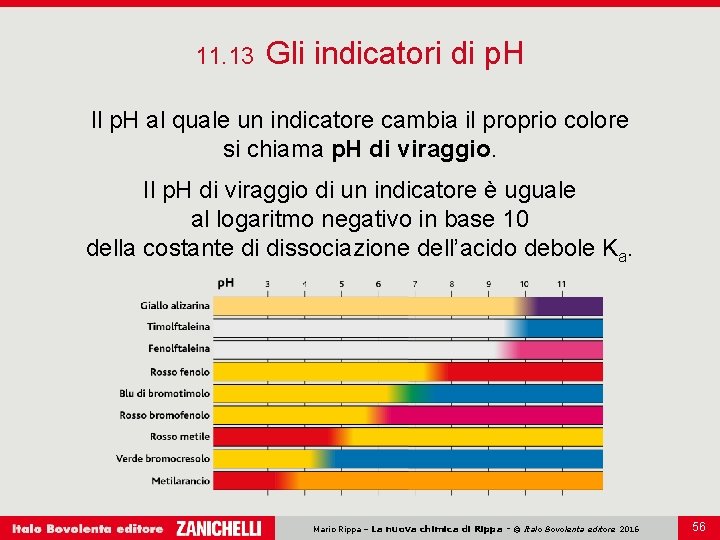
11. 13 Gli indicatori di p. H Il p. H al quale un indicatore cambia il proprio colore si chiama p. H di viraggio. Il p. H di viraggio di un indicatore è uguale al logaritmo negativo in base 10 della costante di dissociazione dell’acido debole Ka. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 56

11. 14 La titolazione acido base Il titolo di una soluzione indica il valore della sua concentrazione. Si chiama titolazione acido-base la determinazione della concentrazione di un acido mediante l’aggiunta di una base a titolo noto, o viceversa. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 57
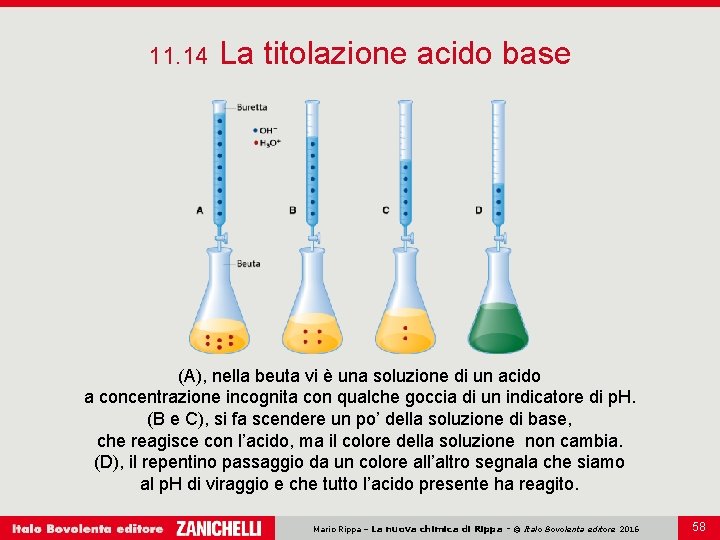
11. 14 La titolazione acido base (A), nella beuta vi è una soluzione di un acido a concentrazione incognita con qualche goccia di un indicatore di p. H. (B e C), si fa scendere un po’ della soluzione di base, che reagisce con l’acido, ma il colore della soluzione non cambia. (D), il repentino passaggio da un colore all’altro segnala che siamo al p. H di viraggio e che tutto l’acido presente ha reagito. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 58

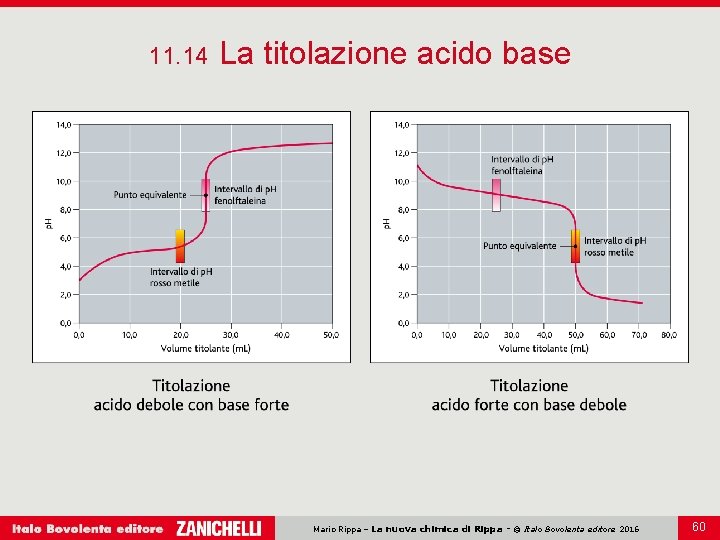
11. 14 La titolazione acido base Le curve di titolazione acido-base rappresentano l’andamento del p. H della soluzione di titolando in funzione del volume di titolante aggiunto. Dalla curva di titolazione è possibile individuare il punto equivalente, che varia a seconda della forza degli acidi e basi in gioco. Il punto equivalente in una titolazione corrisponde al punto in cui le moli del titolante sono stechiometricamente uguali a quelle del titolando. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 59
11. 14 La titolazione acido base Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 60

11. 14 La titolazione acido base La scelta dell’indicatore da utilizzare durante una titolazione deve essere opportunamente valutata in base alla posizione del punto equivalente. Di volta in volta l’indicatore di p. H più opportuno è quello in cui l’intervallo di viraggio comprende il punto equivalente della curva in esame. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 61

11. 15 Equivalente chimico e normalità Una mole di acido monoprotico, per esempio HCl, diprotico, per esempio H 2 SO 4, o triprotico, per esempio H 3 PO 4, è capace di cedere rispettivamente una, due o tre moli di ioni ossonio. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 62

18. 17 Equivalente chimico e normalità Si chiama equivalente chimico la quantità di un acido che rilascia una mole di ioni ossonio o la quantità di una base che reagisce con una mole di ioni ossonio. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 63
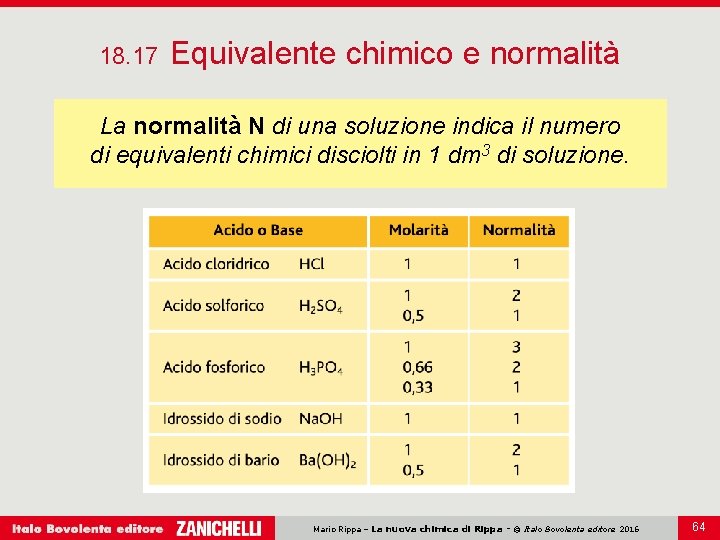
18. 17 Equivalente chimico e normalità La normalità N di una soluzione indica il numero di equivalenti chimici disciolti in 1 dm 3 di soluzione. Mario Rippa – La nuova chimica di Rippa - © Italo Bovolenta editore 2016 64
- Slides: 64