DALLE LEGGI DELLA CHIMICA ALLA TEORIA ATOMICA VERSO





- Slides: 15

DALLE LEGGI DELLA CHIMICA ALLA TEORIA ATOMICA

VERSO IL CONCETTO DI ATOMO Leucippo (450 a. C. ) “La materia, non è continua come sembra, ma è formata da particelle piccolissime” Democrito (460/370 a. C. ) Denominò atomi queste particelle piccolissime Su base filosofica Due secoli dopo, 1803, nasce Dalton nasce la Moderna Teoria Atomica Su base sperimentale

Lavoisier: legge di conservazione della massa. “In una reazione chimica, la massa dei reagenti è esattamente uguale alla massa dei prodotti” KI + Pb(NO 3 )2 K (NO 3) + Pb. I 2

Proust: legge delle proporzioni definite. “In un composto, gli elementi che lo costituiscono sono presenti secondo rapporti in massa costanti e definiti. ”

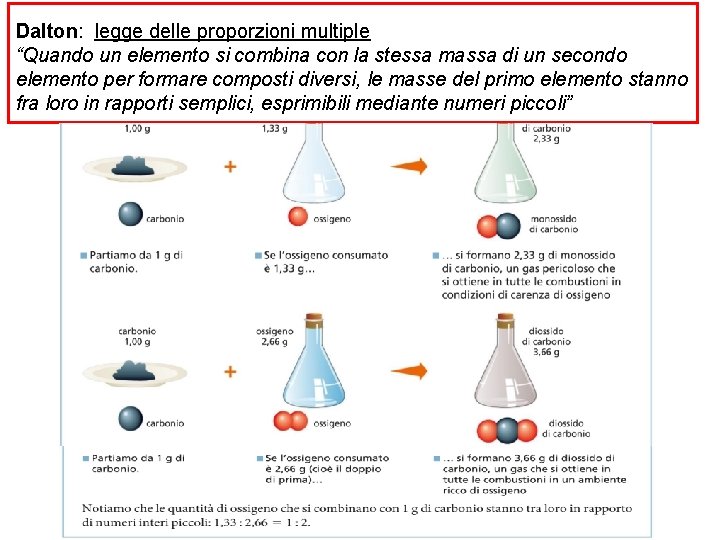
Dalton: legge delle proporzioni multiple “Quando un elemento si combina con la stessa massa di un secondo elemento per formare composti diversi, le masse del primo elemento stanno fra loro in rapporti semplici, esprimibili mediante numeri piccoli”

IL MODELLO ATOMICO DI DALTON 1. La materia è fatta di atomi piccolissimi, che sono invisibili e indistruttibili. 2. Tutti gli atomi di uno stesso elemento sono identici ed hanno la stessa massa. 3. Gli atomi di un elemento non possono essere convertiti in atomi di altri elementi. 4. Gli atomi di un elemento si combinano solo con numeri interi di atomi di altri elementi. 5. Gli atomi non possono essere né creati né distrutti, ma si trasferiscono interi da un composto all’altro.

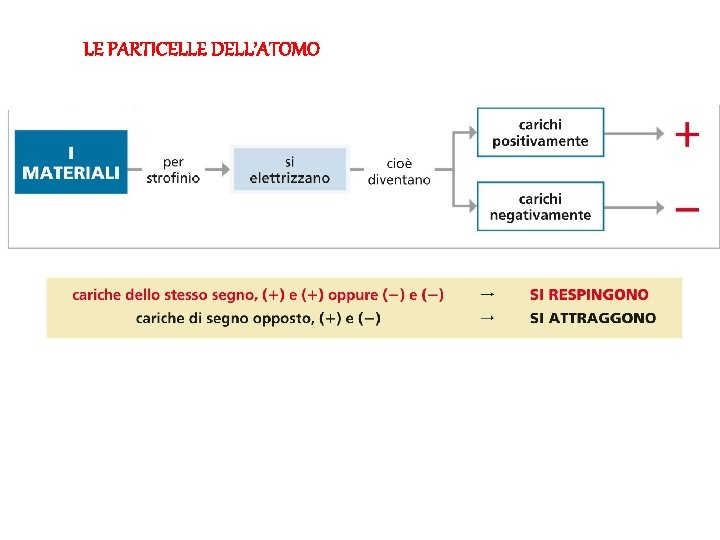
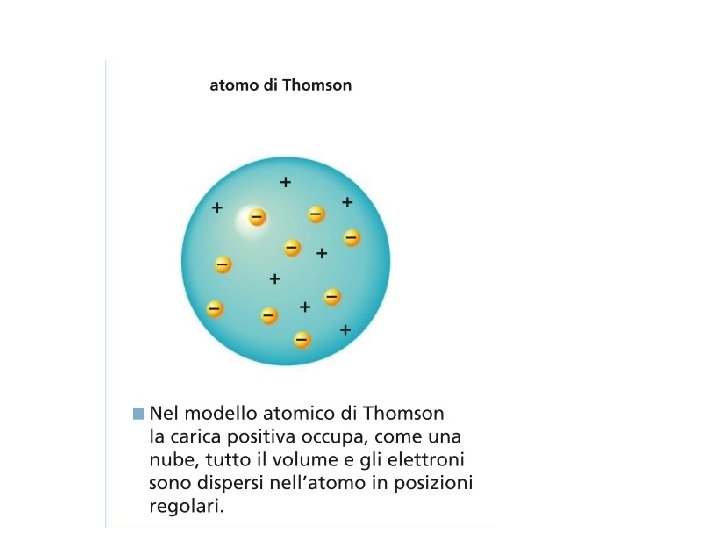
LE PARTICELLE DELL’ATOMO

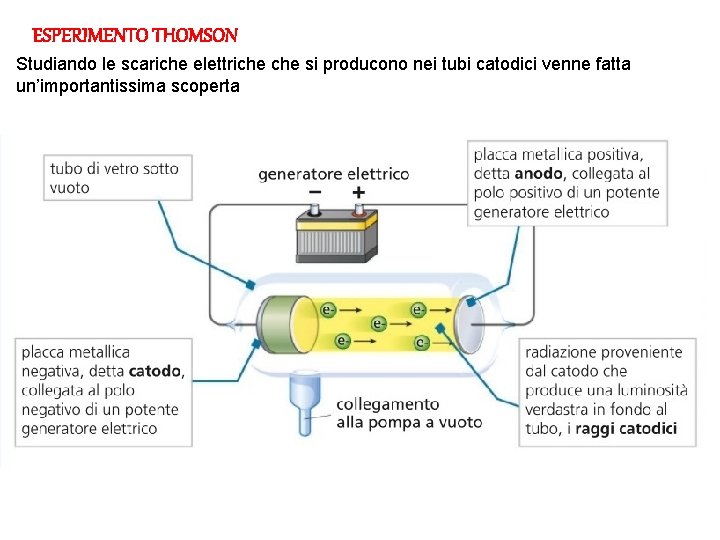
ESPERIMENTO THOMSON Studiando le scariche elettriche si producono nei tubi catodici venne fatta un’importantissima scoperta

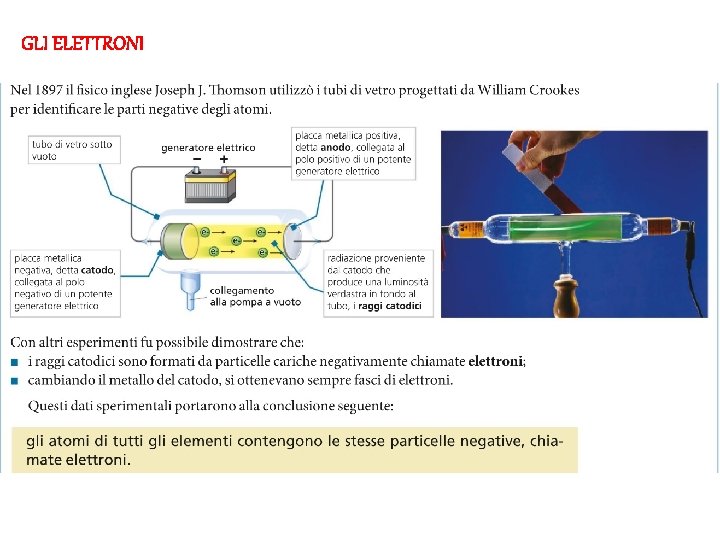
GLI ELETTRONI

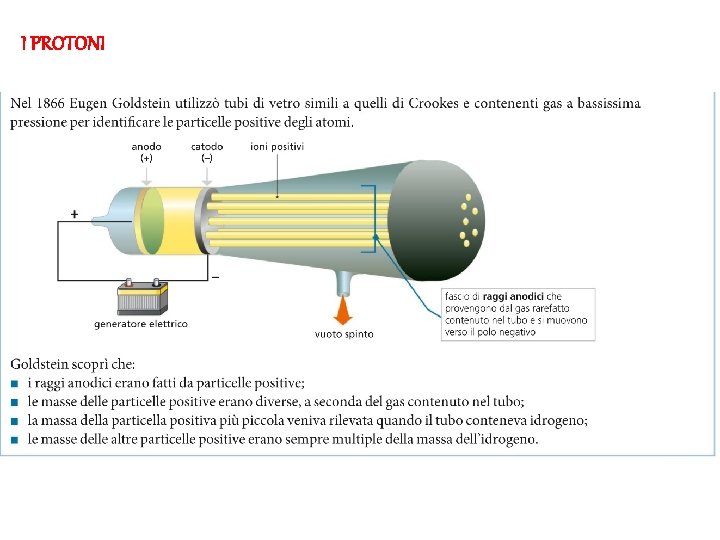
I PROTONI

I PROTONI I protoni sono le più piccole particelle con carica positiva che sono presenti in tutti gli atomi. • la massa del protone è molto più grande di quella dell’elettrone, ma la carica elettrica positiva del protone ha lo stesso valore di quella negativa dell’elettrone. • In ogni atomo il numero di protoni è uguale a quello degli elettroni; in questo modo l’atomo è elettricamente neutro.

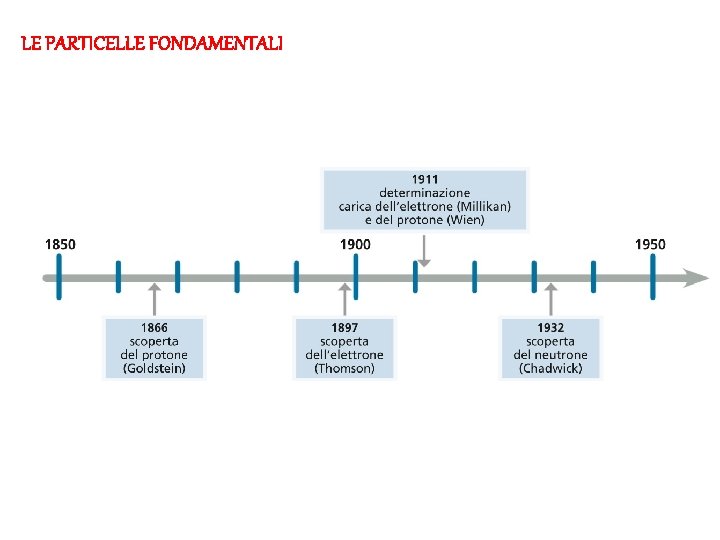
LE PARTICELLE FONDAMENTALI


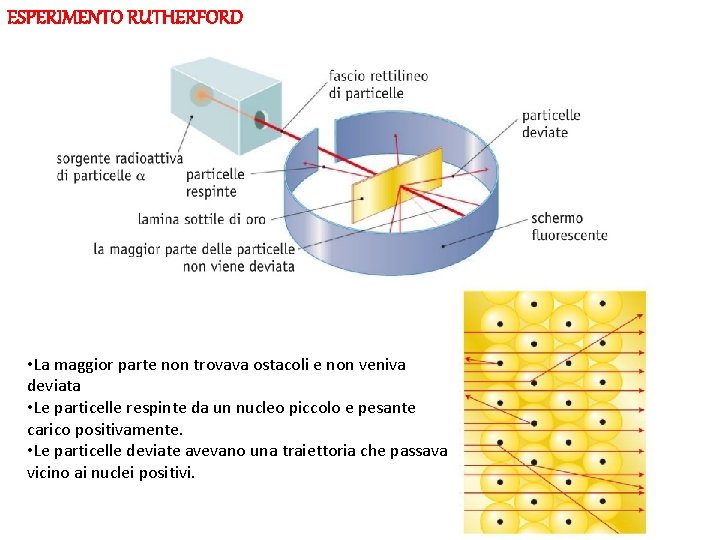
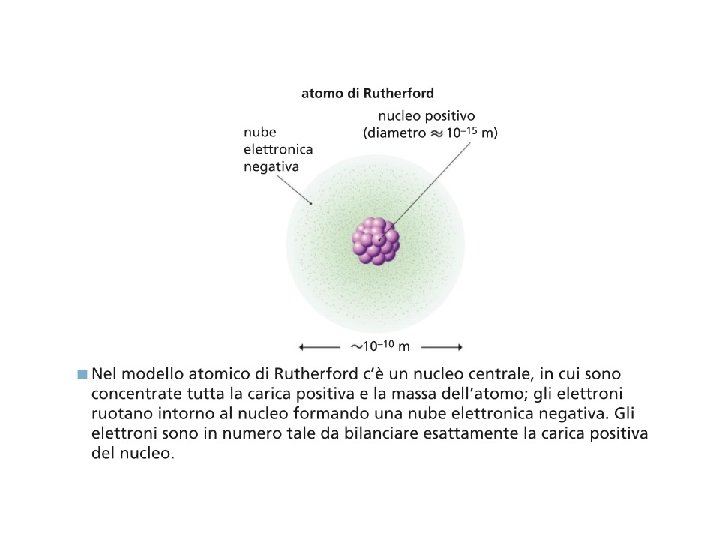
ESPERIMENTO RUTHERFORD • La maggior parte non trovava ostacoli e non veniva deviata • Le particelle respinte da un nucleo piccolo e pesante carico positivamente. • Le particelle deviate avevano una traiettoria che passava vicino ai nuclei positivi.
