d PRVKY Skupina V I I B Skupina
d – PRVKY Skupina V I I. B

Skupina V I I. B Mangan, Technecium, Rhenium konfigurace Mn 4 s 2 3 d 5 Prvek I r (pm) b. t. (K) Mn 717 126 7, 21 1517 Tc 703 136 11, 50 2600 Re 760 137 21, 00 3450 Oxidační čísla + I I … + V I I Re 2 O 7

Mangan Mn. – 0, 085 % Fe > Ti > Mn Mn. O 2 – pyrolusit techn. Fe + Mn (80 %) slitina ferromangan výroba Mn. O 2 + Fe 2 O 3 + dolomit + uhlí. Mn + S Mn. S – zlepšuje vlastnosti ocelí Mn + S , N 2 , O 2 (Mn 3 O 4 ) Oxidy Mn. O – manganosit (zelený), struktura Na. Cl . . nestechiometrické ; Mn. CO 3 Mn. O 1, 13. Mn(OH)2 (bílý) Mn. O(OH) Mn 2 O 3 – braunit ; Mn. O 2 Mn 2 O 3 200 °C
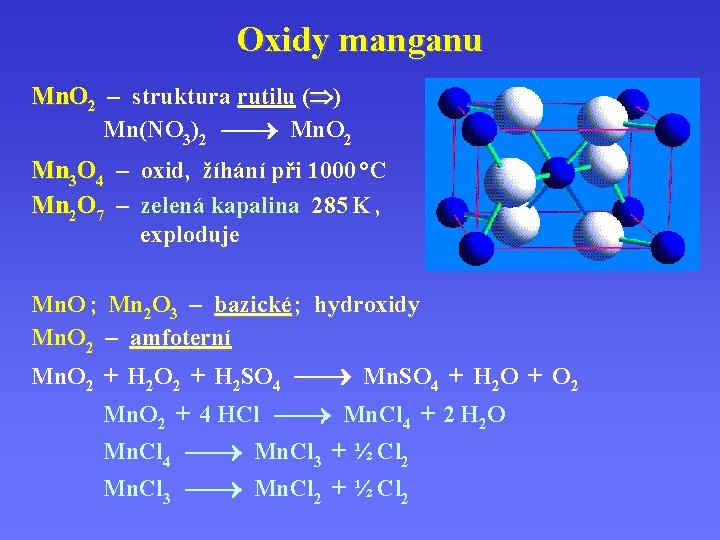
Oxidy manganu Mn. O 2 – struktura rutilu ( ) Mn(NO 3)2 Mn. O 2. Mn 3 O 4 – oxid, žíhání při 1000 °C Mn 2 O 7 – zelená kapalina 285 K , exploduje Mn. O ; Mn 2 O 3 – bazické ; hydroxidy Mn. O 2 – amfoterní Mn. O 2 + H 2 SO 4 Mn. SO 4 + H 2 O + O 2 Mn. O 2 + 4 HCl Mn. Cl 4 + 2 H 2 O Mn. Cl 4 Mn. Cl 3 + ½ Cl 2 Mn. Cl 3 Mn. Cl 2 + ½ Cl 2

Mangan – oxidační čísla Mn(II) II Mn. S – struktura Na. Cl Mn. Cl 2 ; Mn. Cl 2 · 4 H 2 O ; Mn. SO 4 · 7 H 2 O (5 H 2 O) schoenity Mn. CO 3 Mn. O + CO 2 Mn(III) Mn. F 3 nejstálejší Mn 2(SO 4)3 · H 2 O · H 2 SO 4 ; H[Mn(SO 4)2] · 2 H 2 O. Mn(IV) – soli nestálé K 2[Mn. Cl 6] , Mn(SO 4)2 Mn(V) Na 3[Mn. O 4] · 10 H 2 O Mn. O 2 + soda + ledek modré zabarvení. Mn(VI) VI Mn(VII) VII. K 2 Mn. O 4 KMn. O 4 zelený Mn. O 4– + 8 H+ + 5 e– Mn 2+ + 4 H 2 O 2 Mn. O 4– + 4 H+ + 3 e– Mn. O 2 + 2 H 2 O 4 Mn. O 4– + 4 OH– 4 Mn. O 42– + O 2 + 2 H 2 O
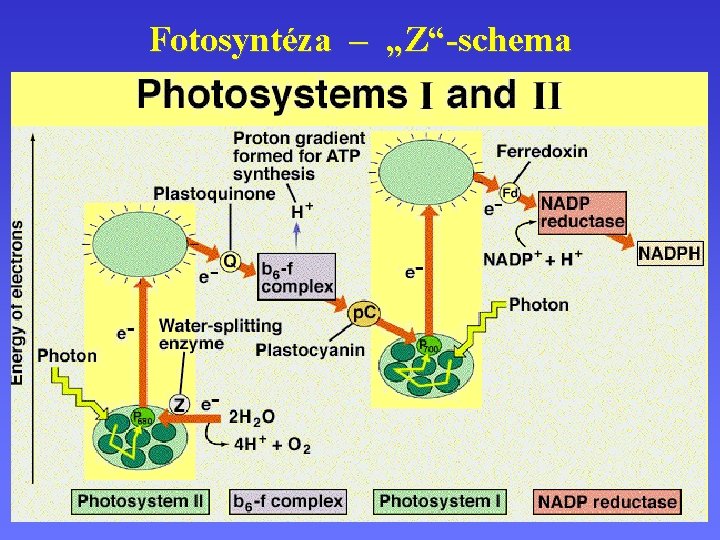
Fotosyntéza – „Z“-schema
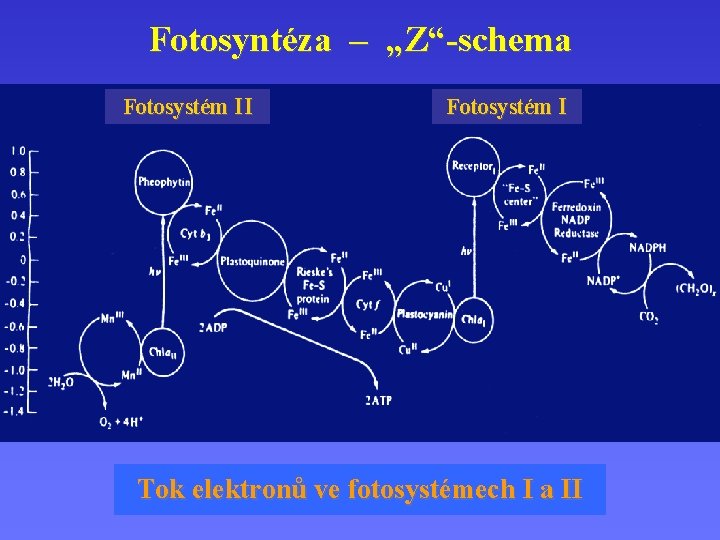
Fotosyntéza – „Z“-schema Fotosystém II Fotosystém I Tok elektronů ve fotosystémech I a II
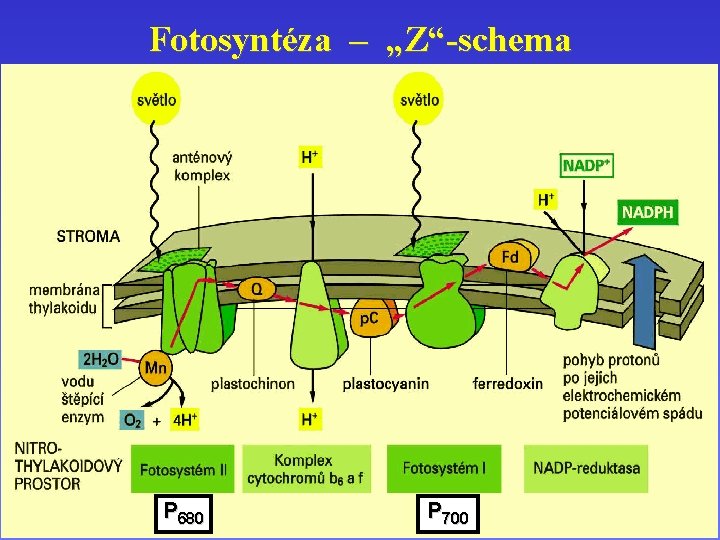
Fotosyntéza – „Z“-schema P 680 P 700
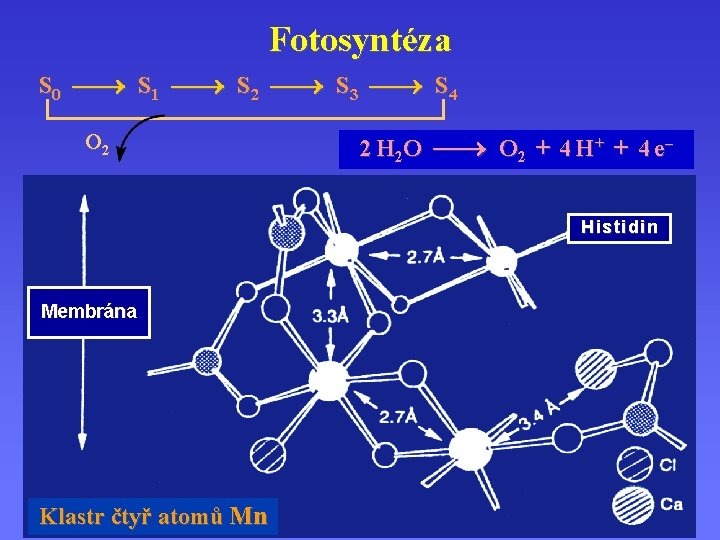
Fotosyntéza S 0 S 1 S 2 S 3 S 4 O 2 2 H 2 O O 2 + 4 H + + 4 e– Histidin Membrána Klastr čtyř atomů Mn
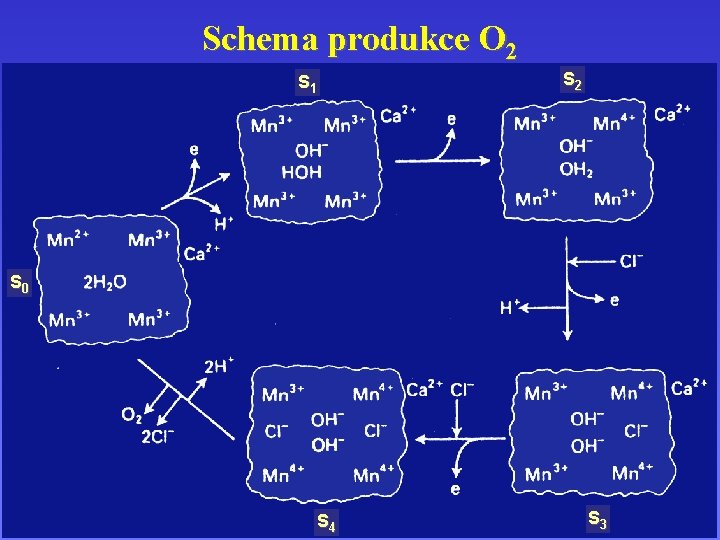
Schema produkce O 2 S 1 S 2 S 0 S 4 S 3

Technecium, Rhenium 91 Tc – štěpný produkt U (6 %) , 1939 99 m. Tc z Mo ; 100 MW 2, 5 g 99 Tc denně Tc. O 2 — Tc 2 O 7 — Tc 2 S 7. Re – 1925 z molybdenitu (20 ppm). . z letavých prachů Mo. S 2 (Re 2 O 7) Re 2 O 3 – nestálý Re. O 2 Re 2 O 7 Tc. O 2 nejstálejší, černý stálý, žlutý Tc 2 O 7 stálý, žlutý H Tc. O 4 – červená krystalická látka ; Tc 2 O 7 v H 2 O H Re. O 4 – žlutozelená jen slabé oxidační vlastnosti. Halogenidy: Halogenidy Re 3 Cl 9 . . Hydridy: Hydridy K 2 Re. H 9
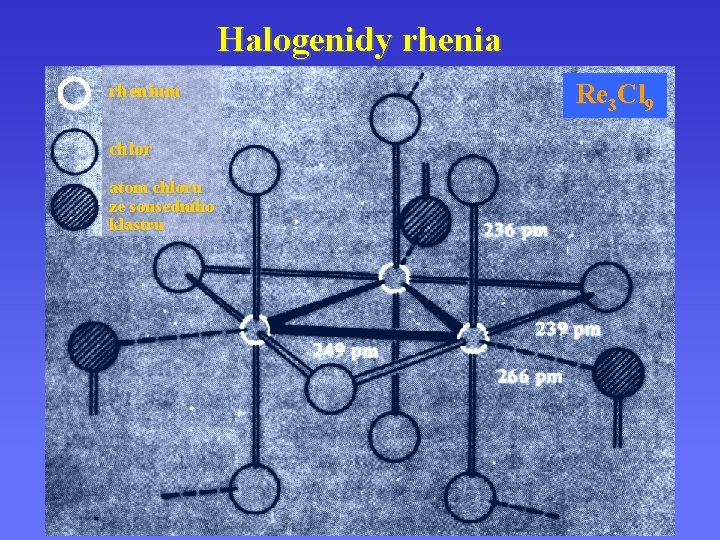
Halogenidy rhenia rhenium chlor atom chloru ze sousedního klastru Re 3 Cl 9
![Hydridy rhenia vodík rhenium [Re. H 9]2– Hydridy rhenia vodík rhenium [Re. H 9]2–](http://slidetodoc.com/presentation_image_h2/f10c5d0b336e69c7ffd7a489dcf67c0a/image-13.jpg)
Hydridy rhenia vodík rhenium [Re. H 9]2–
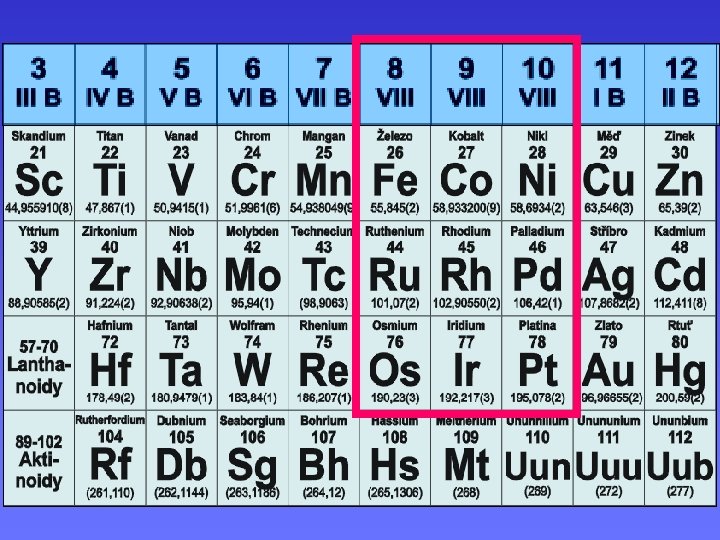
d – PRVKY Skupina V I I I

Skupina V I I I Mn Fe Co Ni Cu triáda železa r Ru Rh Pd Ag lehké Pt kovy 12 Os Ir Pt Au těžké Pt kovy 22 vysoké body tání ; slitiny ; intermetalické sloučeniny katalyzátory ; rozpouštění H 2 ; proměnlivá oxidační čísla Prvek r 2+ (pm) b. t. (K) Oxidační čísla Příklady Fe 76 1810 – II, 0, III, + VI [Fe(CO)6]2– , K 2 Fe. O 4 Co 74 1760 – I, III, + IV [Co(CO)4]– , [Co. F 6]2– Ni 72 1720 0, II, + IV K 2 Ni. F 6

Železo Fe. – 5, 1 % Fe 2 O 3 krevel, Fe 3 O 4 magnetovec, Fe. S 2 – pyrit, Fe. CO 3 ocelek. . výroba: čisté Fe – redukce H 2 z oxidů Fe 2 O 3 + CO Fe + CO 2 C CO obsah 4 % C; 2, 5 % Si; 2, 5 % Mn. . 1 % P; 0, 1 % S; ocel C < 1 % Koroze 4 Fe + 2 H 2 O + 3 O 2 2 Fe 2 O 3 · H 2 O

Sloučeniny železa sloučeniny. . Fe 2+ – stálé v H+ Fe 3+ – stálejší Fe 2+ – Fe. O; Fe. S 2 [Fe(H 2 O)6]2+ Fe. O – (struktura Na. Cl) – modrozelený Fe. SO 4 · 7 H 2 O ; Fe. Cl · 4 H 2 O (Br–, I–). 2+ + 2 OH– Fe(OH) Fe 2. (NH 4)2 Fe. SO 4 · 6 H 2 O inertní Mohrova sůl Fe 3+ [Fe(H 2 O)6]3+. . [Fe(OH)(H 2 O)5]2+ žlutý až červený amoniak Fe 3+ + 3 OH– Fe(OH)3 ; Na. OH + KFe. O 2 Fe 2 O 3 + KOH + Cl 2 K 2 Fe. O 4
![Koordinační sloučeniny železa [Fe. Cl 4]– – slabý, tetraedrický K 4[Fe(CN)6] – žlutá krevní Koordinační sloučeniny železa [Fe. Cl 4]– – slabý, tetraedrický K 4[Fe(CN)6] – žlutá krevní](http://slidetodoc.com/presentation_image_h2/f10c5d0b336e69c7ffd7a489dcf67c0a/image-18.jpg)
Koordinační sloučeniny železa [Fe. Cl 4]– – slabý, tetraedrický K 4[Fe(CN)6] – žlutá krevní sůl K 3[Fe(CN)6] – červená krevní sůl (nízkospinový). . . Fe 3+ + [Fe(CN)6]4 – modrá sraženina Berlínská modř Fe 2+ + [Fe(CN)6]3– modrá sraženina Turnbullova modř. Fe 3+ + 6 SCN– [Fe(SCN)6]3–. prusidy Na 2[Fe(CN)5 NO] · 2 H 2 O nitroprusid sodný . . Fe + cyklopentadien FERROCEN Fe
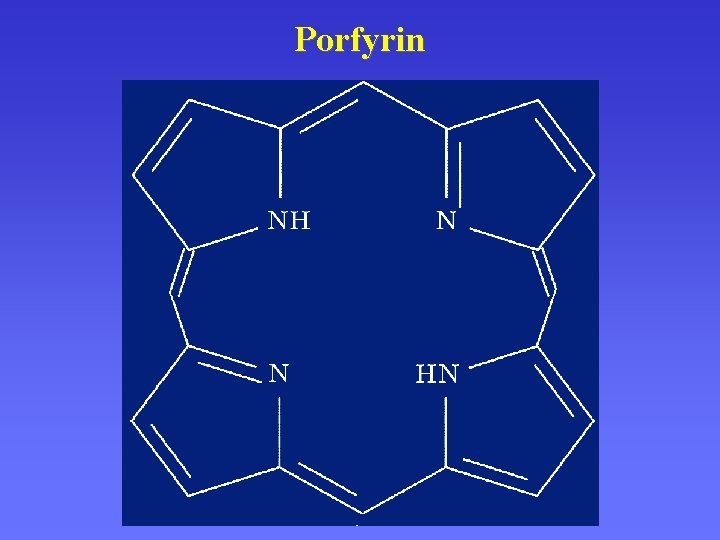
Porfyrin
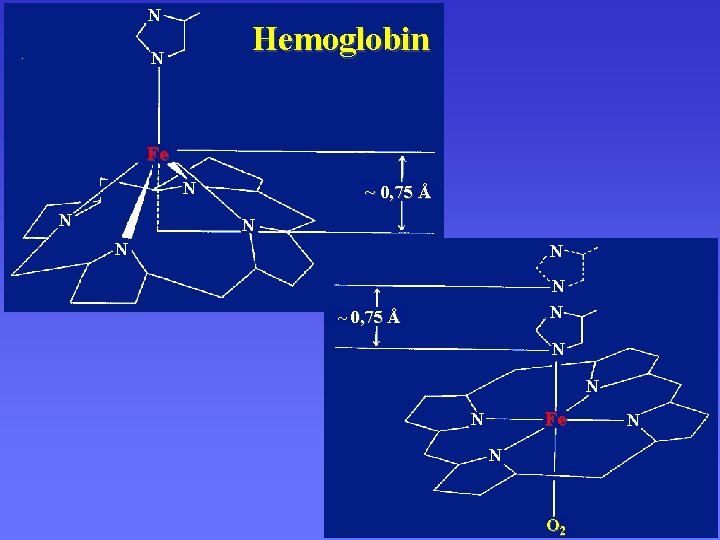
N Hemoglobin N Fe N N ~ 0, 75 Å N N Fe N N O 2 N
![Hemoglobin a hem 2 [Fe(Pf )]2+ + ½ O 2 [Fe(Pf ) – O Hemoglobin a hem 2 [Fe(Pf )]2+ + ½ O 2 [Fe(Pf ) – O](http://slidetodoc.com/presentation_image_h2/f10c5d0b336e69c7ffd7a489dcf67c0a/image-21.jpg)
Hemoglobin a hem 2 [Fe(Pf )]2+ + ½ O 2 [Fe(Pf ) – O – Fe(Pf )]
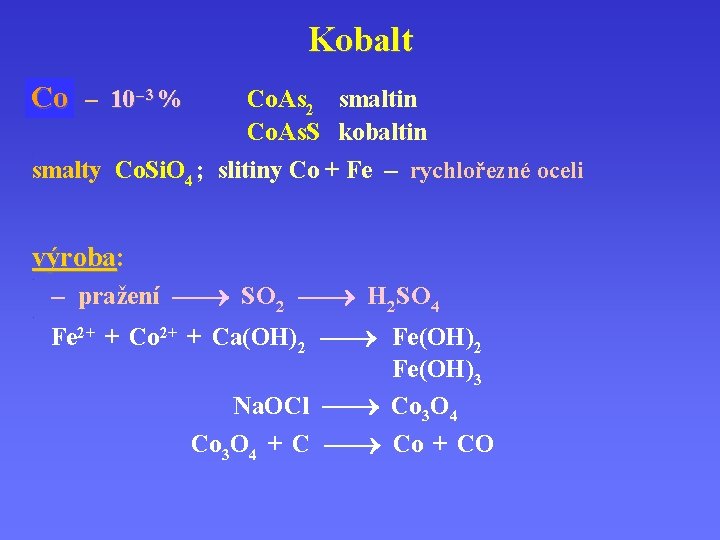
Kobalt Co – 10 – 3 % Co. As 2 smaltin Co. As. S kobaltin . smalty Co. Si. O 4 ; slitiny Co + Fe – rychlořezné oceli výroba: výroba. . – pražení SO 2 H 2 SO 4 Fe 2+ + Co 2+ + Ca(OH)2 Fe(OH)2 Fe(OH)3 Na. OCl Co 3 O 4 + C Co + CO
![Sloučeniny kobaltu Co 2+ – oxid Co. O ; Co. S. [Co(H 2 O)6]2+ Sloučeniny kobaltu Co 2+ – oxid Co. O ; Co. S. [Co(H 2 O)6]2+](http://slidetodoc.com/presentation_image_h2/f10c5d0b336e69c7ffd7a489dcf67c0a/image-23.jpg)
Sloučeniny kobaltu Co 2+ – oxid Co. O ; Co. S. [Co(H 2 O)6]2+ růžový. [Co. Cl 4]2– modrý Co. Cl 2 · 6 H 2 O ; Co. SO 4 · 7 H 2 O ; Co(NO 3)2 · 6 H 2 O Co 3+ – Co 2 O 3 ; Co. F 3 · 3, 5 H 2 O. stabilisace. . O 2 [Co(NH 3)6]2+ [Co(NH 3)6]3+ K 3[Co(NO 2)6] ; vitamin B -12 (kobalamin)
![Komplexní sloučeniny kobaltu Opticky aktivní komplex [Co(NH 3)4(H 2 O)Cl]SO 4 Komplexní sloučeniny kobaltu Opticky aktivní komplex [Co(NH 3)4(H 2 O)Cl]SO 4](http://slidetodoc.com/presentation_image_h2/f10c5d0b336e69c7ffd7a489dcf67c0a/image-24.jpg)
Komplexní sloučeniny kobaltu Opticky aktivní komplex [Co(NH 3)4(H 2 O)Cl]SO 4
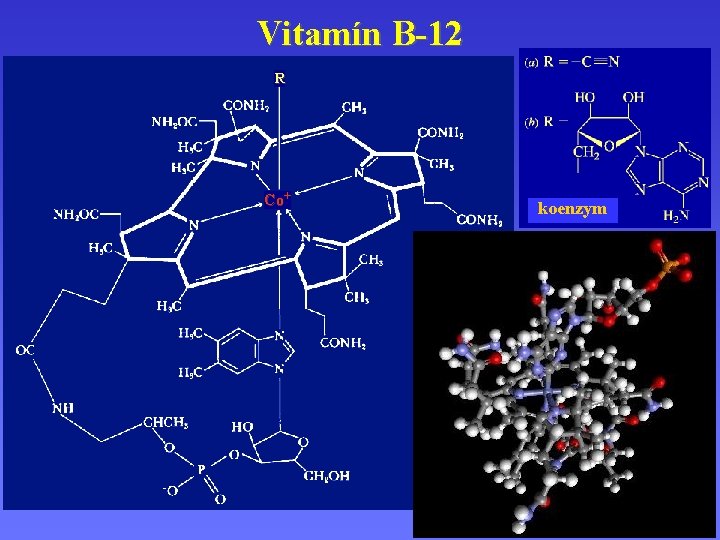
Vitamín B-12 R Co+ koenzym
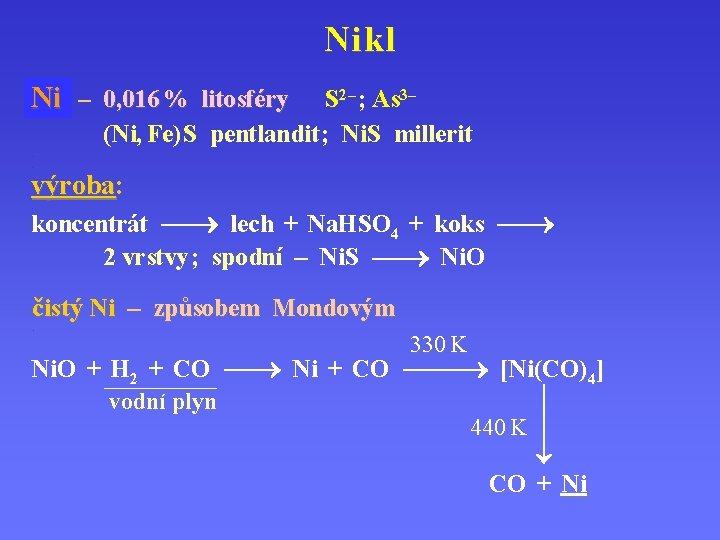
Nikl Ni – 0, 016 % litosféry S 2– ; As 3– (Ni, Fe) S pentlandit ; Ni. S millerit . . výroba: výroba. koncentrát lech + Na. HSO 4 + koks 2 vrstvy ; spodní – Ni. S Ni. O čistý Ni – způsobem Mondovým. 330 K Ni. O + H 2 + CO Ni + CO [Ni(CO)4] vodní plyn 440 K ————————— CO + Ni
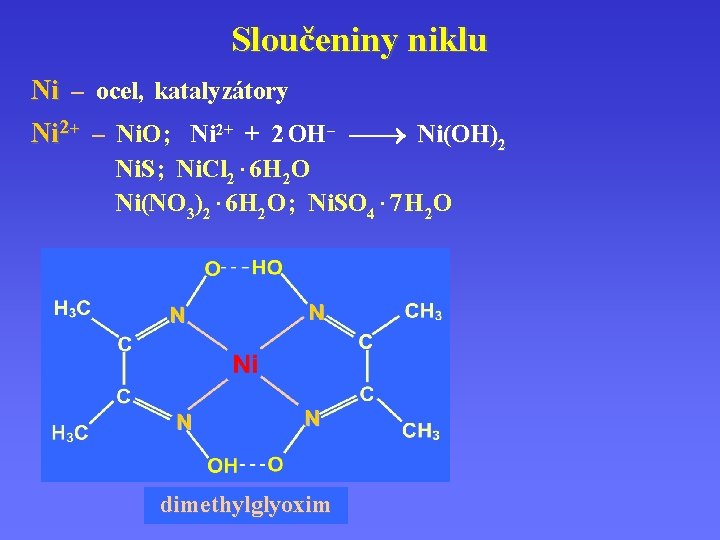
Sloučeniny niklu Ni – ocel, katalyzátory. Ni 2+ – Ni. O ; Ni 2+ + 2 OH– Ni(OH)2 Ni. S ; Ni. Cl 2 · 6 H 2 O Ni(NO 3)2 · 6 H 2 O ; Ni. SO 4 · 7 H 2 O dimethylglyoxim
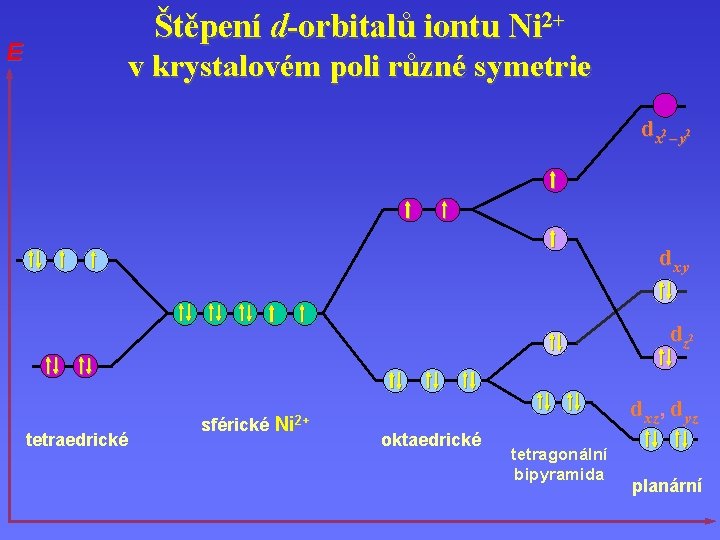
E Štěpení d-orbitalů iontu Ni 2+ v krystalovém poli různé symetrie dx 2 – y 2 dx y d z 2 tetraedrické sférické Ni 2+ dx z , dy z oktaedrické tetragonální bipyramida planární
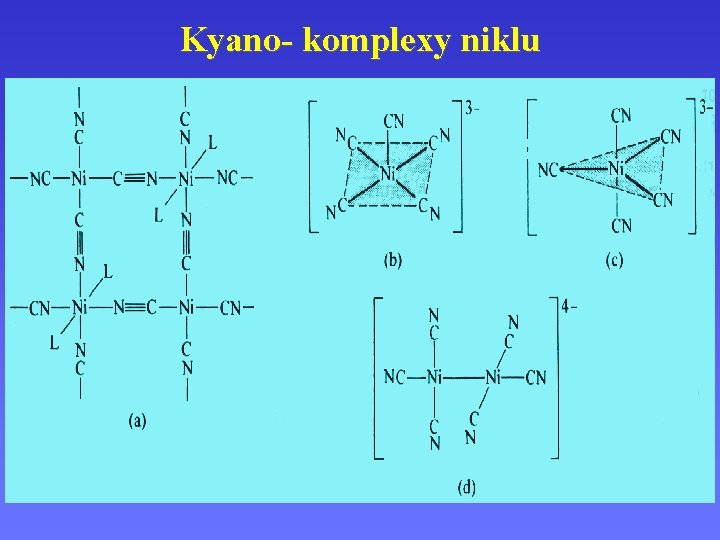
Kyano- komplexy niklu
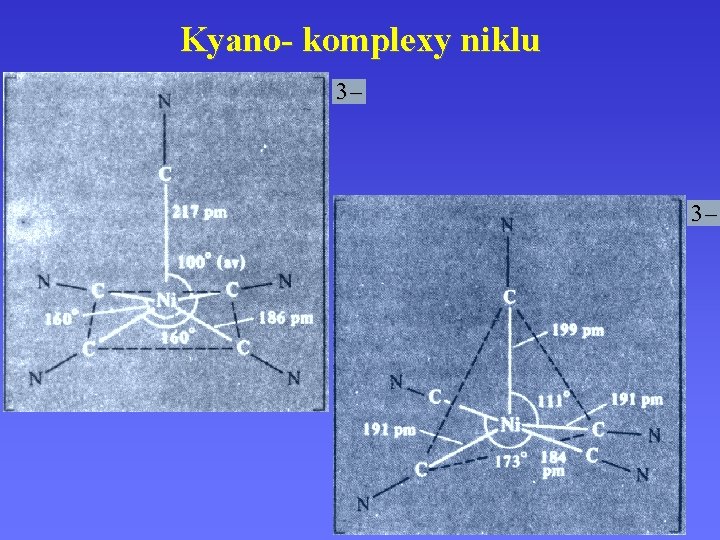
Kyano- komplexy niklu 3– 3–
- Slides: 30