d PRVKY Skupina V B Skupina V B
d – PRVKY Skupina V. B

Skupina V. B Vanad, Niob, Tantal konfigurace V 4 s 2 3 d 3 Prvek I r 5+ (pm) b. t. (K) V 651 56 2190 6, 11 Nb 654 70 2770 8, 57 Ta 675 73 3270 16, 60 4 M + 5 O 2 2 M 2 O 5 ; VN

Skupina V. B V. – 0, 02 % 60 minerálů K(UO 2)VO 4 karnotit Pb 5(VO 4)Cl vanadinit NH 4 Cl Pb 5(VO 4)Cl + Na. Cl Na. VO 3 NH 4 VO 3 V 2 O 5 + 5 Ca. O + 2 V. elektrolýza Na. Cl – Li. Cl – VCl 2 Nb ; Ta – 10 – 4 , 10 – 5 % [V(CO)6]– [V(CO)6] [V(bpy)3]+ [V(CN)6]4– [V(NH 3)6]3+ K 2[VCl 6] VOCl 3 –I 0 +I + III + IV +V
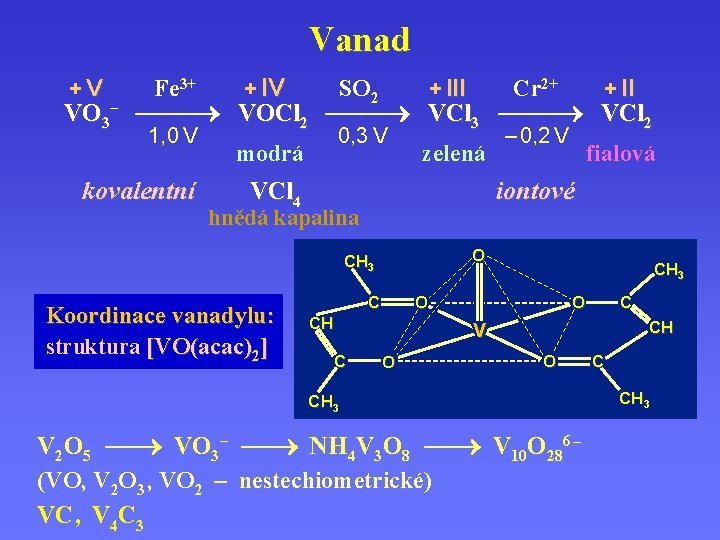
Vanad +V Fe 3+ + IV SO 2 + III Cr 2+ + II VO 3– VOCl 2 VCl 3 VCl 2 1, 0 V kovalentní 0, 3 V modrá zelená hnědá kapalina O CH 3 C CH 3 O O CH C fialová iontové VCl 4 Koordinace vanadylu: struktura [VO(acac)2] – 0, 2 V C CH V O O CH 3 V 2 O 5 VO 3– NH 4 V 3 O 8 V 10 O 286 – (VO, V 2 O 3 , VO 2 – nestechiometrické) VC , V 4 C 3 C CH 3
![Vanadičnany, vanadyly p. H 12 p. H 10 p. H 9 [VO 4]3– [VO Vanadičnany, vanadyly p. H 12 p. H 10 p. H 9 [VO 4]3– [VO](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-5.jpg)
Vanadičnany, vanadyly p. H 12 p. H 10 p. H 9 [VO 4]3– [VO 3 · OH]2– [V 2 O 6 · OH]3– [V 3 O 9]3– p. H 7 p. H 6, 5 p. H 2, 2 p. H < 1 7 6, 5 2, 2 <1 [V 5 O 14]3– V 2 O 5 · n H 2 O [V 10 O 28]6– [VO 2]+ Struktura aniontu V 10 O 286– tvořený 10 oktaedry VO 6 (2 jsou zakryty)

V 2 O 5 Vanadičnany V 10 O 246 – ? V 2 O 74 – H 2 V 10 O 284 – V 4 O 124 – ? HV 10 O 285 – V 3 O 93 – ? VO 43 – VO 2+ HVO 42 – H 2 VO 4– p. H H 3 VO 4 ? V(OH)4 ?
![Vanadičnany V alkalickém roztoku: roztoku [VO 4] 3 – + H+ [HVO 4] 2 Vanadičnany V alkalickém roztoku: roztoku [VO 4] 3 – + H+ [HVO 4] 2](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-7.jpg)
Vanadičnany V alkalickém roztoku: roztoku [VO 4] 3 – + H+ [HVO 4] 2 – 2 [HVO 4] 2 – [V 2 O 7] 4 – + H 2 O [HVO 4] 2 – + H+ [H 2 VO 4] – 3 [H 2 VO 4] – [V 2 O 9] 3 – + 3 H 2 O 4 [H 2 VO 4] – [V 4 O 12] 4 – + 4 H 2 O. V kyselém roztoku: roztoku. 10 [V 3 O 9] 3 – + 15 H+ [H 2 VO 4] – + H+ [HV 10 O 28] 5 – + H+ H 3 VO 4 + H+ [H 2 V 10 O 28] 4 – + H+ 3 [HV 10 O 28] 5 – + 6 H 2 O H 3 VO 4 [H 2 V 10 O 28] 4 – VO 2+ + 2 H 2 O 10 VO 2+ + 8 H 2 O
![Niob, Tantal X M (Nb, Ta) Komplexní částice [M 6 Cl 12] n + Niob, Tantal X M (Nb, Ta) Komplexní částice [M 6 Cl 12] n +](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-8.jpg)
Niob, Tantal X M (Nb, Ta) Komplexní částice [M 6 Cl 12] n +
d – PRVKY Skupina V I. B

Skupina V I. B Chrom, Molybden, Wolfram konfigurace Cr 4 s 1 3 d 5 Prvek I r 4+ r (pm) b. t. (K) Cr 653 55 127 7, 14 2180 Mo 692 68 139 10, 80 2840 W 770 68 139 19, 30 3680

Chrom Cr. . – kov – chemicky odolný Fe. O · Cr 2 O 3 chromit, Pb. Cr. O 4 krokoit výroba: výroba Fe. O · Cr 2 O 3 + 4 C Fe + 2 Cr + 4 CO ferochrom čistý Na 2 Cr 2 O 7 + C Cr 2 O 3 + Na 2 CO 3 + CO. Cr 2 O 3 + 2 Al 2 O 3 + 2 Cr
![chemie. Chrom 3 d 5 4 s 1 ; Na 2[Cr(CO)5] ; [Cr(CO)6] oxidační chemie. Chrom 3 d 5 4 s 1 ; Na 2[Cr(CO)5] ; [Cr(CO)6] oxidační](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-12.jpg)
chemie. Chrom 3 d 5 4 s 1 ; Na 2[Cr(CO)5] ; [Cr(CO)6] oxidační čísla I I; I I I; V I. Cr(II) II Cr. SO 4 · 5 H 2 O --- Cu. SO 4 · 5 H 2 O. Cr oxidace na vzduchu 4 Cr 2+ + O 2 + 4 H+ 4 Cr 3+ + 2 H 2 O Cr 3+ + H • 4 Cr 2+ + H+ ( Zn + 2 H+ Zn 2+ + 2 H • ) Cr 3 + Cr 2 O 3 – chromová zeleň Cr octan chromnatý Cr. X 3 · 6 H 2 O zelená ; [Cr(H 2 O)6]Cl 3 fialová KCr(SO 4)2 · 12 H 2 O ; oktaedrické okolí. . Cr(IV) Cr. O 2 – feromagnetický (záznamová média)
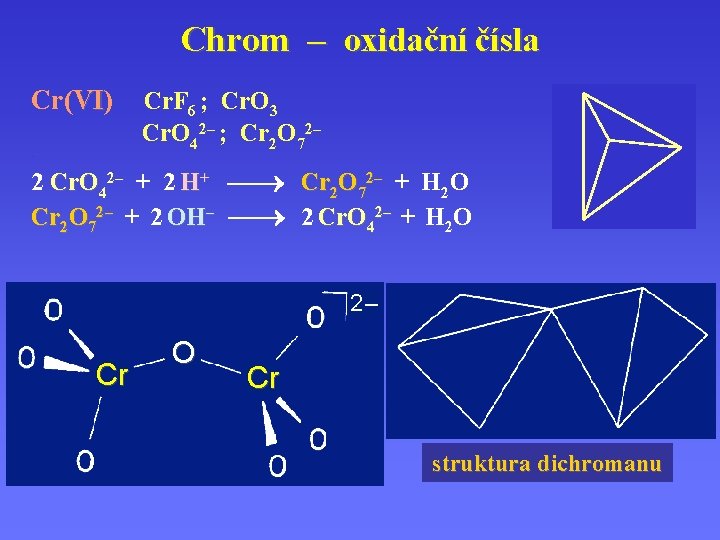
Chrom – oxidační čísla Cr(VI). Cr. F 6 ; Cr. O 3 Cr. O 42– ; Cr 2 O 72– 2 Cr. O 42– + 2 H+ Cr 2 O 72– + H 2 O Cr 2 O 72– + 2 OH– 2 Cr. O 42– + H 2 O 2– Cr O Cr struktura dichromanu

Cr(VI), Chromany oxidační vlastnosti – chromsírová směs. Cr 2 O 72– + 6 Fe 2+ + 14 H+ 2 Cr 3+ + 6 Fe 3+ + 7 H 2 O Cr 2 O 72– + 6 I– + 14 H+ 2 Cr 3+ + 2 I 2 + 7 H 2 O K 2 Cr 2 O 7 + 3 H 2 S + 4 H 2 SO 4 3 S + Cr 2(SO 4)3 + K 2 SO 4 + 7 H 2 O Peroxokomplexy. – + Cr. O(O ) + H O HCr. O + H 4 2 2 2. H 2 Cr. O 8 – červenohnědý (OH–)
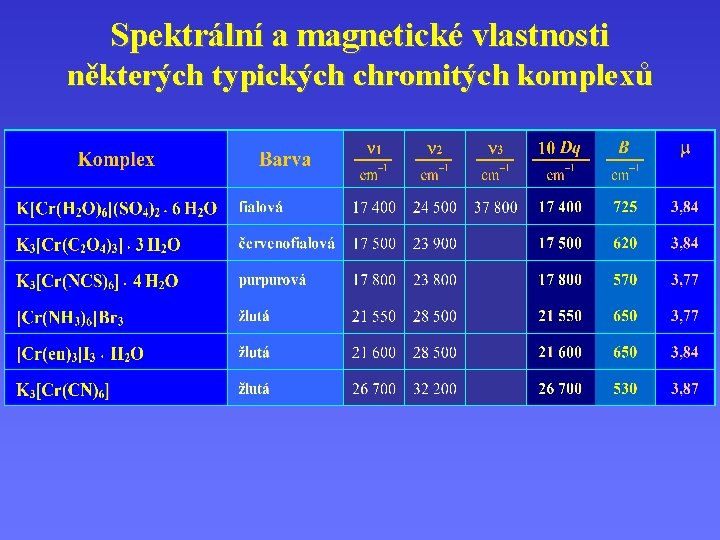
Spektrální a magnetické vlastnosti některých typických chromitých komplexů
![Spektrální a magnetické vlastnosti některých typických chromitých komplexů OH 2+ ] OH )5 [Cr(H Spektrální a magnetické vlastnosti některých typických chromitých komplexů OH 2+ ] OH )5 [Cr(H](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-16.jpg)
Spektrální a magnetické vlastnosti některých typických chromitých komplexů OH 2+ ] OH )5 [Cr(H 2 O)6]3+ O r(H 2 [(H 2 O)4 Cr OH [C – H+ [Cr(H 2 O)5 OH]2+ + H+ [Cr (H p. K ~ 4 [ (NH 3)5 – OH – Cr(NH 3)5 ]5+ červený Cr(H 2 O)4]4+ + 2 H 2 O OH 2 O) 6 ] 3+ OH – H+ [(H 2 O)5 Cr Cr(H 2 O)5]5+ + H 2 O [ (NH 3)5 – O – Cr(NH 3)5 ]4+ modrý
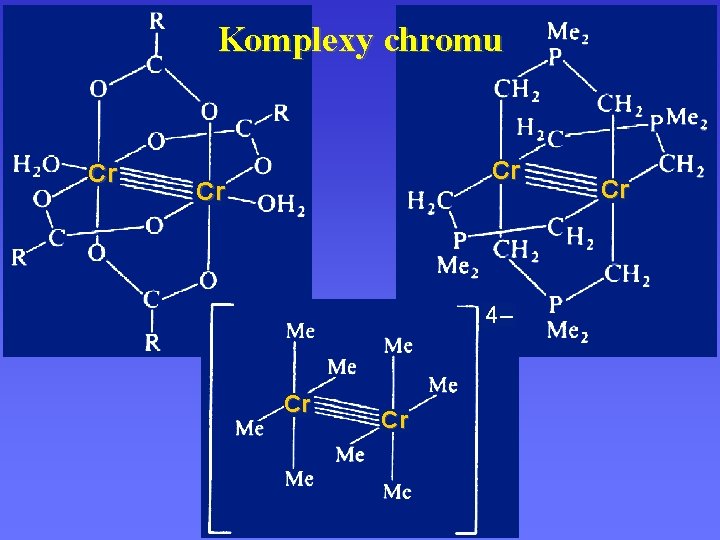
Komplexy chromu Cr Cr Cr 4– Cr Cr Cr
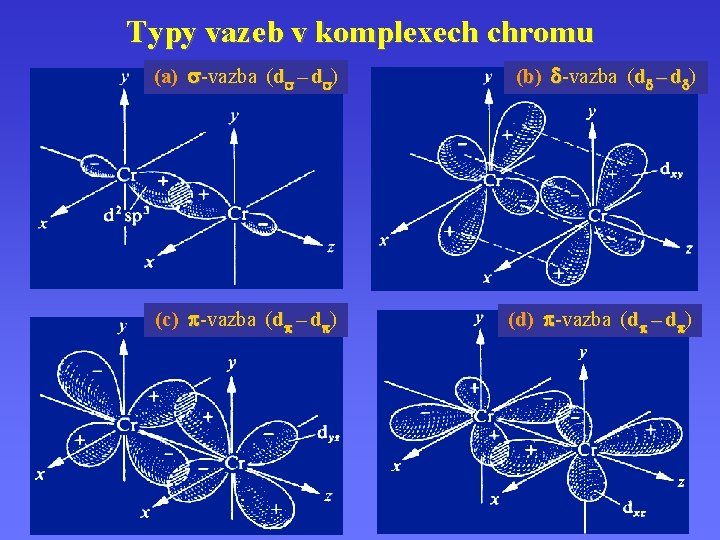
Typy vazeb v komplexech chromu (a) -vazba (d – d ) (b) -vazba (d – d ) (c) -vazba (d – d ) (d) -vazba (d – d )

Molybden, Wolfram Mo, Mo W – litosféra 10 – 4 %. Mo. S 2 molybdenit, (Fe, Mn) WO 4 wolframit Pb. Mo. O 4 wulferit, Ca. WO 4 – scheelit Mo. S 2 + 7/ 2 O 2 Mo. O 3 + 2 SO 2. 2 Fe. WO 4 + 2 Na 2 CO 3 + ½ O 2 2 Na 2 WO 4 + Fe 2 O 3 + 2 CO 2 Na 2 WO 4 + 2 HCl WO 3 + H 2 O + 2 Na. Cl WO 3 + 3 H 2 W + 3 H 2 O Použití: Použití katalýza – Mo, ocel, žárovky. oxidační čísla I I; I I I; V I

Sloučeniny molybdenu a wolframu Oxidy – MO 3 Mo. O 3 · 2 H 2 O ; bílý WO 3 – žlutý Wolframany, stálé – jen velmi slabé oxidační vlastnosti Mo. O 2 – redukcí H 2 , NH 3. . Sulfidy – afinita k síře, biogenní prvek Halogenidy – velké množství, . oxidační čísla I I I; I V; V I, dále můstkové W 6 Cl 12 Mo. F 6 , WF 6 – velice reaktivní WCl 6 – stálejší ; hydrolýza H 2 O
![Halogenidy molybdenu a wolframu ]4+ Klastr [M 6 X 8 M II X– Halogenidy molybdenu a wolframu ]4+ Klastr [M 6 X 8 M II X–](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-21.jpg)
Halogenidy molybdenu a wolframu ]4+ Klastr [M 6 X 8 M II X–

Sloučeniny molybdenu a wolframu Nestechiometrické sloučeniny oxidy – Mo. O 2, 0(OH) Mo. O 2, 5(OH)0, 5. . modré Působení redukčních činidel na H+ roztok Mo. O 42– „wolframové bronzy“ n ~ 0, 9 zlatožluté n ~ 0, 3 modrá chemicky inertní ; K 0, 26 Mo 1, 0 O 3 polovodič Redukce WO 42– Nan. WO 3.

Molybdenany a wolframamy isopolykyseliny – polyanionty Mo. O 6 ; WO 6 Mo 7 O 246 – ; HW 6 O 215 – . 6 Mo. O 42 – 7 Mo. O 42 – 8 Mo. O 42 – 36 Mo. O 42 – + + 10 H+ 8 H+ 12 H+ 64 H+ Mo 6 O 192 – Mo 7 O 246 – Mo 8 O 264 – Mo 36 O 1128 – p. H 6 p. H 2 p. H 6 – 7 p. H 3, 3 + + 5 H 2 O 4 H 2 O 6 H 2 O 32 H 2 O p. H < 1 [Mo. O 4]2– [Mo 7 O 24]6– [Mo 8 O 26]4– Mo. O 3 · 2 H 2 O p. H < 1 [WO 4]2– [HW 6 O 21]5– [H 3 W 6 O 21]3– WO 3 · 2 H 2 O isopolykyseliny
![Molybdenany – příklady [Mo 2 O 72 – ]n Molybdenany – příklady [Mo 2 O 72 – ]n](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-24.jpg)
Molybdenany – příklady [Mo 2 O 72 – ]n
![Molybdenany – příklady [Mo 8 O 26]4 – [Mo 7 O 24]6 – Molybdenany – příklady [Mo 8 O 26]4 – [Mo 7 O 24]6 –](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-25.jpg)
Molybdenany – příklady [Mo 8 O 26]4 – [Mo 7 O 24]6 –
![Wolframamy [WO 4]2 – p. H ~ 6 [HW 6 O 21]5 – dny Wolframamy [WO 4]2 – p. H ~ 6 [HW 6 O 21]5 – dny](http://slidetodoc.com/presentation_image_h2/9673129bb93ea00e99728b411caf5afb/image-26.jpg)
Wolframamy [WO 4]2 – p. H ~ 6 [HW 6 O 21]5 – dny / týdny parawolframan (A) parawolframan (B nebo Z) p. H ~ 4 [HW 6 O 203 –]n pseudo- metawolframan p. H ~ 1 WO 3 · 2 H 2 O [H 6 W 12 O 42]10 – týdny / měsíce [H 6 W 12 O 40]6 – metawolframan Reakční schema kondenzace parawolframanových iontů ve vodných roztocích
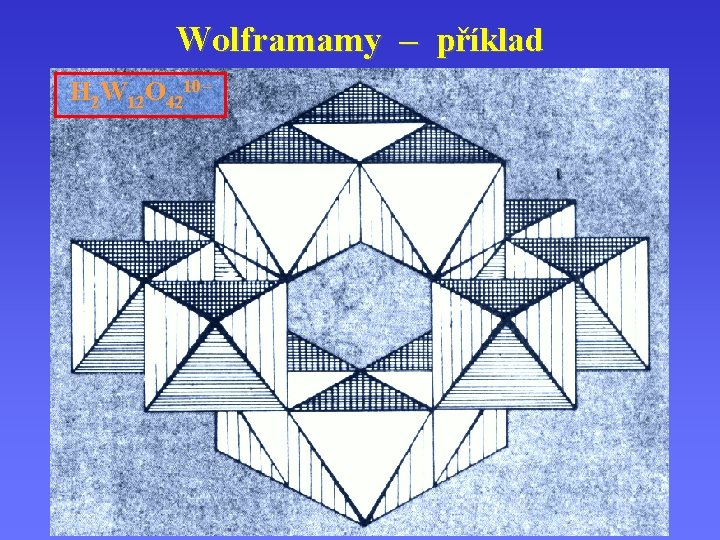
Wolframamy – příklad H 2 W 12 O 4210 –
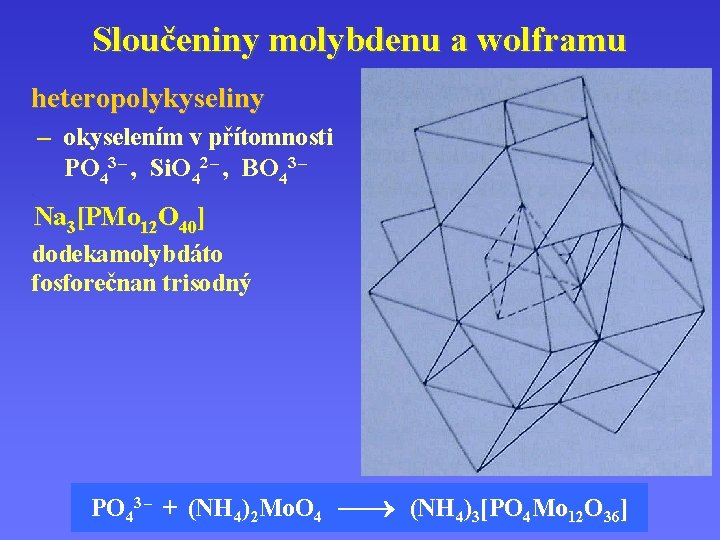
Sloučeniny molybdenu a wolframu heteropolykyseliny. . – okyselením v přítomnosti PO 43 – , Si. O 42 – , BO 43 – Na 3[PMo 12 O 40] . dodekamolybdáto fosforečnan trisodný PO 43 – + (NH 4)2 Mo. O 4 (NH 4)3[PO 4 Mo 12 O 36]
- Slides: 28