Czym jest Cerebrolysin Cerebrolysin jest zbalansowanym preparatem niskoczsteczkowych


Czym jest Cerebrolysin? • Cerebrolysin jest zbalansowanym preparatem niskocząsteczkowych peptydów o właściwościach neurotroficznych. Peptydy są podobne lub identyczne do tych, które są wytwarzane endogennie u człowieka. • Nowym spojrzeniem na terapie zaburzeń mózgu poprzez mechanizm działania naśladujący naturalne czynniki neurotroficzne i neuroprotekcyjne.

Cerebrolysin a rozwój medycyny • Zdolności regeneracyjne mózgu nie podlegają wątpliwości • Procesy neurodegeneracyjne są złożone • Wiele czynników neurotroficznych: NGF i BDNF poznane najlepiej • Nadzieja - peptydy działające jak czynniki neurotroficzne – badania • Badania nad Cerebrolysin przy współpracy Instytutu Lotów Kosmicznych USA i Sił Powietrznych Wielkiej Brytanii • CASTA – badanie w udarze niedokrwiennym, południowowschodnia Azja, monitorowane przez USA

Na co działa Cerebrolysin? BEZPOŚREDNIO NA NEURONY Stymuluje wzrost i rozgałęzianie neuronów Działa na złożone zaburzenia powstałe na skutek urazu lub neurodegeneracji – działanie plejotropowe (wielotorowe) Przekracza barierę krew-mózg (masa molekularna 10 k. D ) Jest bezpieczna dla mózgu i całego organizmu.

Znaczenie pokonywania bariery krew mózg (BBB) • Filtracja molekuł o zbyt dużej wadze w procesie produkcyjnym koncentratu cerebrolysin • Masa molekularna 10 k. D pozwala na przekroczenie bariery krew-mózg (BBB) – pierwsza substancja na świecie • Peptydy dostają się bezpośrednio do źródła choroby, działają wspomagająco i stymulująco na wzrost i rozgałęzianie neuronów • Zwiększa się liczba cząsteczek transportujących glukozę przez barierę krew-mózg • Wyrównywanie deficytu energetycznego związanego z chorobą

Cerebrolysin w leczeniu ostrych i przewlekłych zaburzeń OUN • Hamowanie procesów neurodegeneracyjnych 1, 2, 3, 4 REDUKCJA FORMOWANIA PŁYTEK AMYLOIDALNYCH Redukcja transportu APP do końcówek synaptycznych w chorobie Alzheimera REDUKCJA PROCESÓW NEKROTYCZNYCH I APOPTOTYCZNYCH Redukcja formowania wolnych rodników, procesów zapalnych , inhibicja kalpainy) • Stymulowanie naturalnych mechanizmów obronnych 5, 6, 7, 8 NEUROPLASTYCZNOŚĆ NEUROGENEZA NEUROPROTEKCJA poprawa procesów neuroregeneracyjnych, poprawa przeżywalności neuronów, wyższa gęstosć synaptyczna, poprawa integralności obwodów neuronalnych

Źródła • • • 1 Rockenstein et al. , J. Neursci Res. 2006; 83: 1252 -61 2 Wronski et al. , J, Neural Transm. 2000; 107: 145 -57 3 Sugita et al. , No To Shinkei, 1993; 45/4: 325 -331 4 Alvarez et al. , J Neural transm Suppl. 2000; 59: 281 -92 5 Masliah et al. , Pharmacol Biochem Behav, 1999; 62: 239 -45 • 6 Tatebayashi et al. , Acta Neuropathol (Berl). 2003; 105: 225 -327 • 7 Rockenstein et al. , J Neural Transm, 2003; 110: 131327 • 8 Harbauer et al. , J Neural Transm. 2001; 108: 459 -73
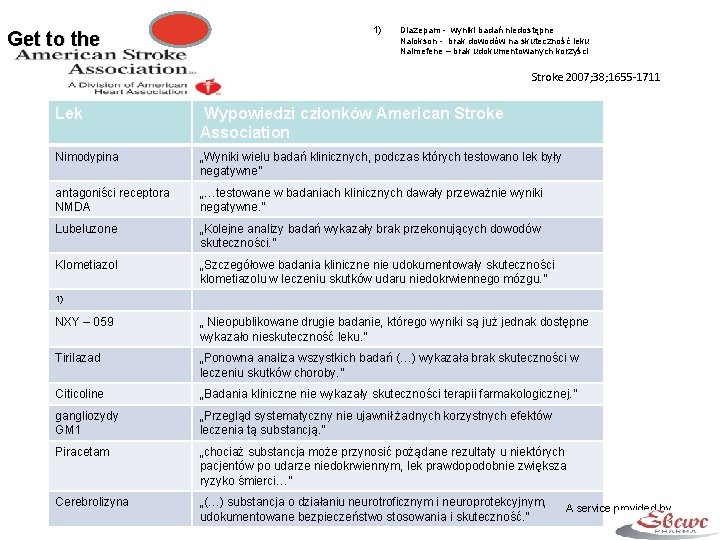
Get to the 1) Diazepam - wyniki badań niedostępne Nalokson - brak dowodów na skuteczność leku Nalmefene – brak udokumentowanych korzyści Stroke 2007; 38; 1655 -1711 Lek Wypowiedzi członków American Stroke Neuroprotekcja Association Nimodypina „Wyniki wielu badań klinicznych, podczas których testowano lek były negatywne” antagoniści receptora NMDA „…testowane w badaniach klinicznych dawały przeważnie wyniki negatywne. ” Lubeluzone „Kolejne analizy badań wykazały brak przekonujących dowodów skuteczności. ” Klometiazol „Szczegółowe badania kliniczne nie udokumentowały skuteczności klometiazolu w leczeniu skutków udaru niedokrwiennego mózgu. ” 1) NXY – 059 „ Nieopublikowane drugie badanie, którego wyniki są już jednak dostępne wykazało nieskuteczność leku. ” Tirilazad „Ponowna analiza wszystkich badań (…) wykazała brak skuteczności w leczeniu skutków choroby. ” Citicoline „Badania kliniczne nie wykazały skuteczności terapii farmakologicznej. ” gangliozydy GM 1 „Przegląd systematyczny nie ujawnił żadnych korzystnych efektów leczenia tą substancją. ” Piracetam „chociaż substancja może przynosić pożądane rezultaty u niektórych pacjentów po udarze niedokrwiennym, lek prawdopodobnie zwiększa ryzyko śmierci…” Cerebrolizyna „(…) substancja o działaniu neurotroficznym i neuroprotekcyjnym, udokumentowane bezpieczeństwo stosowania i skuteczność. ” A service provided by
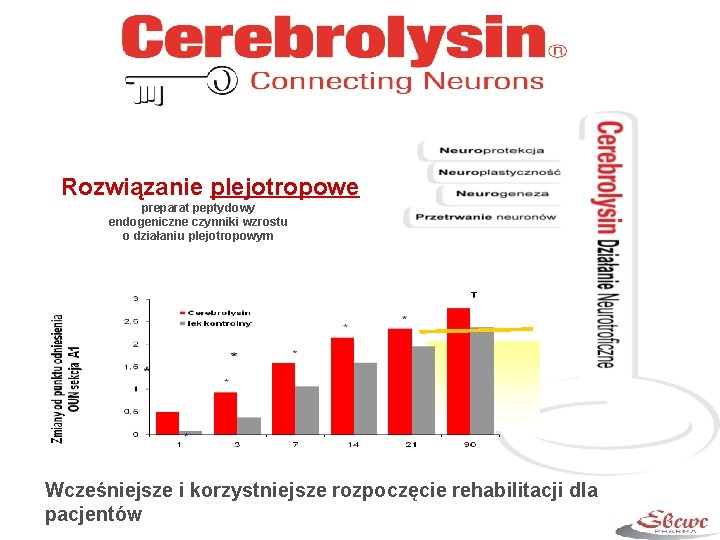
Rozwiązanie plejotropowe preparat peptydowy endogeniczne czynniki wzrostu o działaniu plejotropowym Wcześniejsze i korzystniejsze rozpoczęcie rehabilitacji dla pacjentów
Zastosowanie • Udar mózgu , powikłania poudarowe • Rehabilitacja poudarowa, demencja poudarowa, depresja poudarowa, niedowłady • Urazy mózgowo-czaszkowe , wstrząśnienie mózgu • Rehabilitacja pourazowa • otępienie typu alzheimerowskiego oraz naczyniowego • Inne zespoły organiczne , metaboliczne i neurodegeneracyjne mózgu , szczególnie • Stosowana u dzieci: ADHD, autyzm, wstrząśnienie mózgu, urazy mechaniczne mózgu, urazy okołoporodowe

AD: poprawa funkcji poznawczych: poprawa 4. 1 punkty w skali ADAS-cog+ Poprawa: 4, 1 punkty ADAS-cog+ : change to baseline – ITT Analysis 1) Stała poprawa na co najmniej 6 miesięcy. Stabilizacja nawet po 2 miesiącach po zakończeniu leczenia Alvarez et al, 2006
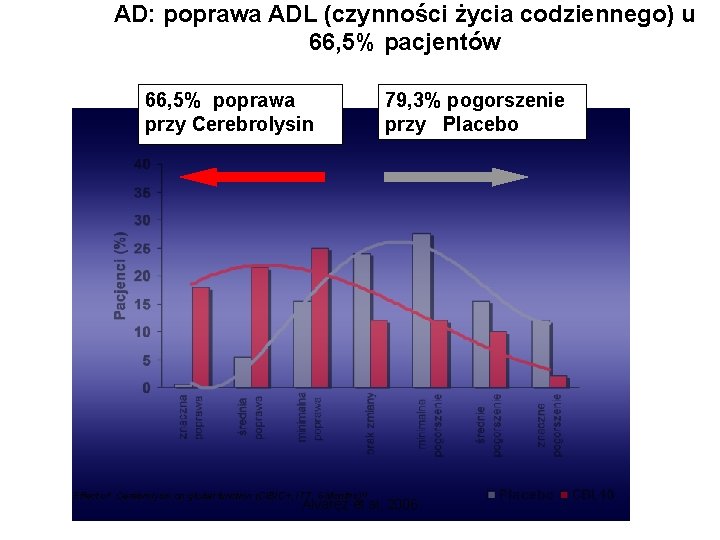
AD: poprawa ADL (czynności życia codziennego) u 66, 5% pacjentów 66, 5% poprawa przy Cerebrolysin 79, 3% pogorszenie przy Placebo Effect of Cerebrolysin on global function (CIBIC+, ITT, 6 Months) Alvarez et al, 2006 1)
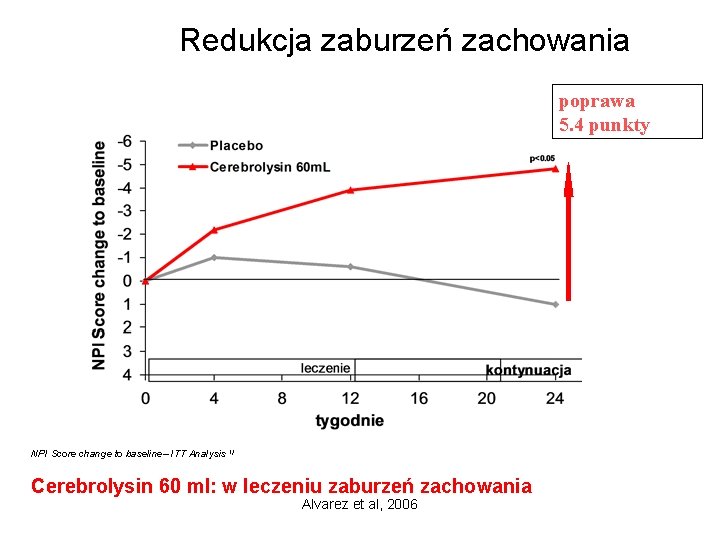
Redukcja zaburzeń zachowania poprawa 5. 4 punkty NPI Score change to baseline– ITT Analysis 1) Cerebrolysin 60 ml: w leczeniu zaburzeń zachowania Alvarez et al, 2006

AD: ADAS-cog – zmiana w stosunku do podstawy (ITT) – Alvarez 2006 (dawkowanie) Dose-finding study, Alvarez 2006

Udar niedokrwienny: The MCA Stroke Trial poprawa funkcji motorycznych Ladurner et al, 2005 * p<0. 05; T p<0. 1
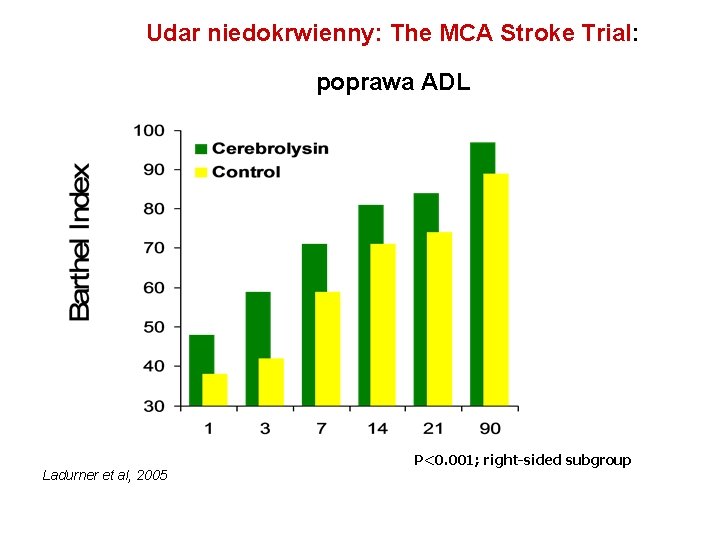
Udar niedokrwienny: The MCA Stroke Trial: poprawa ADL Ladurner et al, 2005 P<0. 001; right-sided subgroup

W Demencji Naczyniowej Preliminary results of the Russian phase IV trial (randomized, double-blind, placebo-controlled)
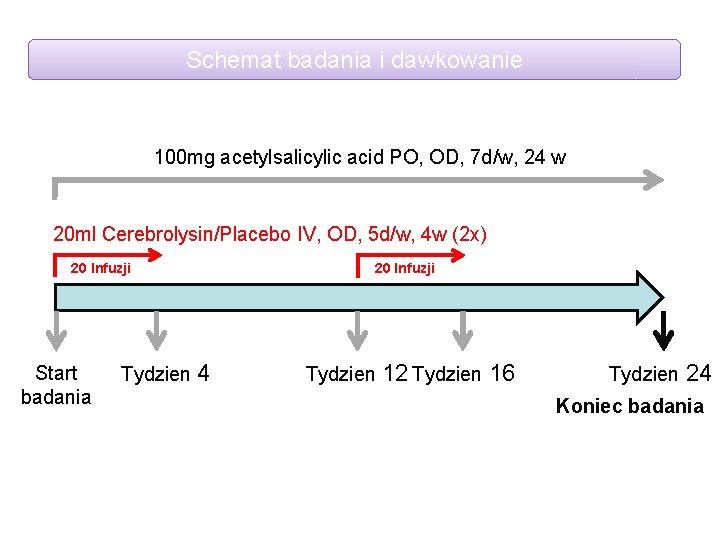
Schemat badania i dawkowanie 100 mg acetylsalicylic acid PO, OD, 7 d/w, 24 w 20 ml Cerebrolysin/Placebo IV, OD, 5 d/w, 4 w (2 x) 20 Infuzji Start badania Tydzien 4 20 Infuzji Tydzien 12 Tydzien 16 Tydzien 24 Koniec badania
Efficacy criteria Primary efficacy criteria: ADAS-COG+ change score from baseline to week 24 (ITT; LOCF) CIBIC+ score distribution at week 24 (ITT; LOCF) Secondary efficacy criteria: MMSE, ADCS-ADL, Clock-Drawing Test, Trial-Making Test Safety criteria: Adverse events, vital signs, laboratory tests (hematology, blood chemistry, urinalysis)
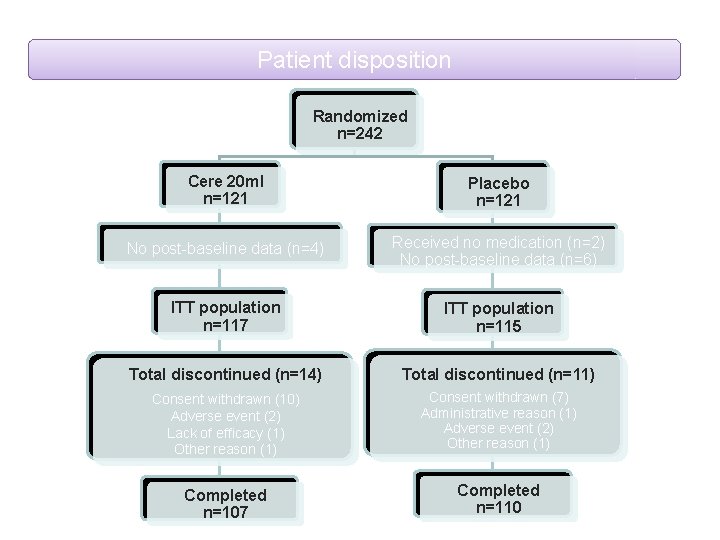
Patient disposition Randomized n=242 Cere 20 ml n=121 Placebo n=121 No post-baseline data (n=4) Received no medication (n=2) No post-baseline data (n=6) ITT population n=117 ITT population n=115 Total discontinued (n=14) Total discontinued (n=11) Consent withdrawn (10) Adverse event (2) Lack of efficacy (1) Other reason (1) Consent withdrawn (7) Administrative reason (1) Adverse event (2) Other reason (1) Completed n=107 Completed n=110
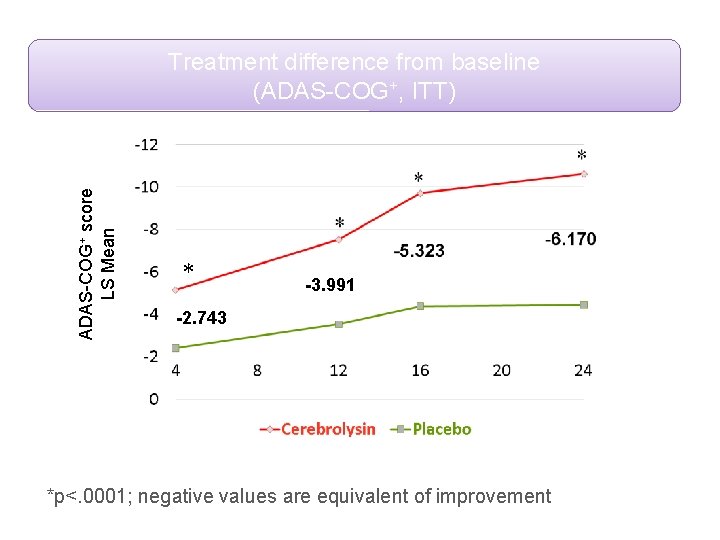
ADAS-COG+ score LS Mean Treatment difference from baseline (ADAS-COG+, ITT) * -3. 991 -2. 743 *p<. 0001; negative values are equivalent of improvement
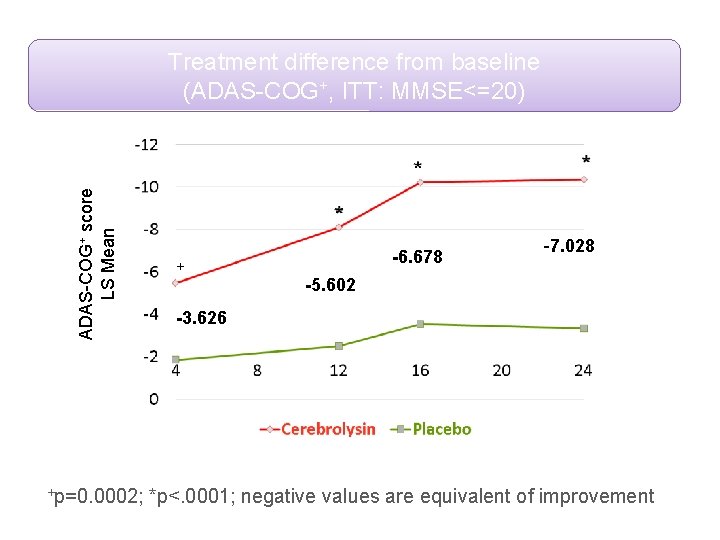
ADAS-COG+ score LS Mean Treatment difference from baseline (ADAS-COG+, ITT: MMSE<=20) + -6. 678 -7. 028 -5. 602 -3. 626 +p=0. 0002; *p<. 0001; negative values are equivalent of improvement

Effects of Cerebrolysin on global function (CIBIC+, ITT, week 24) Values are n; p<. 0001

Effects of Cerebrolysin on global function (CIBIC+, ITT: MMSE<=20, week 24) Values are n; p<. 0001

In Alzheimer‘s Disease Preliminary results of the Spanish phase IV trial (A randomized , double-blind, clinical trial to compare the safety and efficacy of Cerebrolysin and Aricept (Donepezil) and a combination therapy in patients with probable Alzheimer’s Disease)
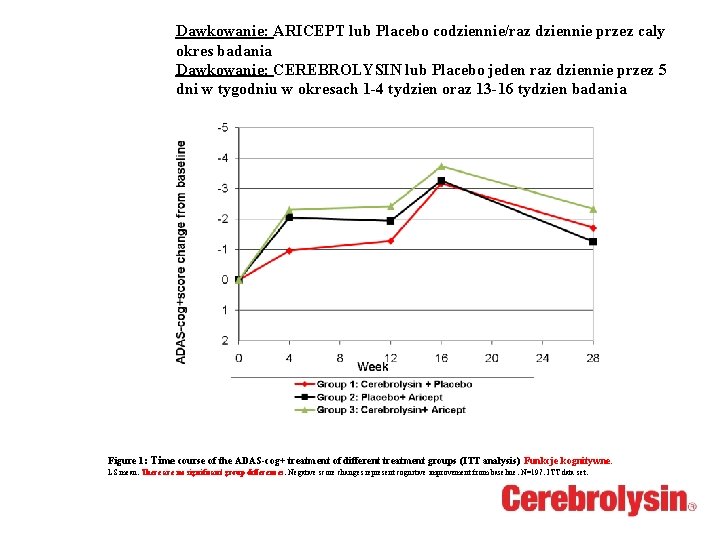
Dawkowanie: ARICEPT lub Placebo codziennie/raz dziennie przez caly okres badania Dawkowanie: CEREBROLYSIN lub Placebo jeden raz dziennie przez 5 dni w tygodniu w okresach 1 -4 tydzien oraz 13 -16 tydzien badania Figure 1: Time course of the ADAS-cog+ treatment of different treatment groups (ITT analysis) Funkcje kognitywne. LS mean. There are no significant group differences. Negative score changes represent cognitive improvement from baseline. N=197. ITT data set.
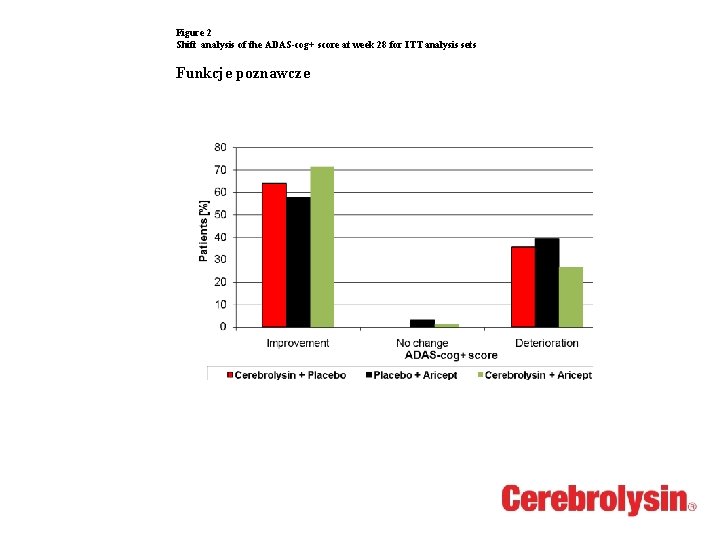
Figure 2 Shift analysis of the ADAS-cog+ score at week 28 for ITT analysis sets Funkcje poznawcze
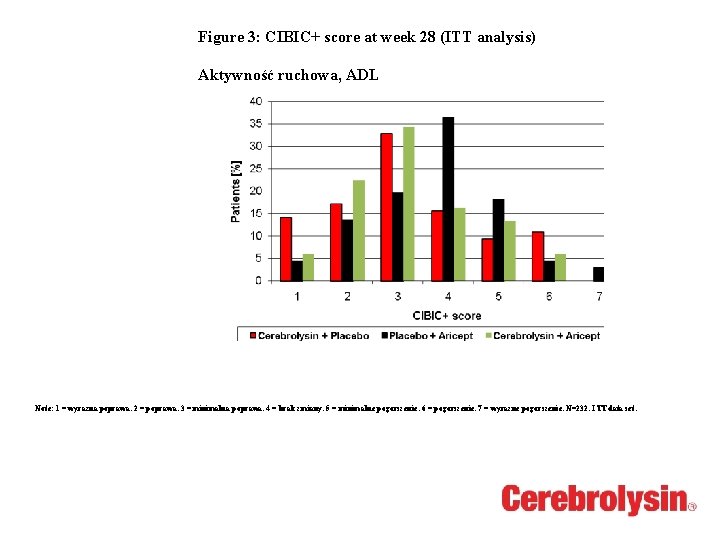
Figure 3: CIBIC+ score at week 28 (ITT analysis) Aktywność ruchowa, ADL Note: 1 = wyrazna poprawa. 2 = poprawa. 3 = minimalna poprawa. 4 = brak zmiany. 5 = minimalne pogorszenie. 6 = pogorszenie. 7 = wyrazne pogorszenie. N=232. ITT data set.

Postać farmaceutyczna oraz rodzaj i zawartość opakowania • Roztwór do wstrzykiwań i infuzji • Opakowania (ceny dla pacjenta za opakowanie) - 10 ampułek po 1 ml ( 29 zł) - 5 ampułek po 5 ml ( 60 zł ) - 5 ampułek po 10 ml ( 95 zł )

CYKLE LECZENIA • Demencja – optymalna dawka 10 ml przez 5 dni w tygodniu przez 4 tygodnie , powtarzanie po 3 miesiącach Demencja – do 30 ml • Rehabilitacja poudarowa dawka optymalna 30 ml, przez 5 dni w tygodniu przez 4 tygodnie, powtórzenie po 3 miesiącach Rehab. – do 50 ml • Udar niedokrwienny: 30 ml przez 2 tyg (przez pierwsze 2 dni można podawać 50 ml) Podawanie: 10 ml domięśniowo (2 x 5 ml) 10 ml dożylnie nierozcieńczone

KOSZT TERAPII CEREBROLYSIN • Koszt jednego cyklu terapii – 1 miesiąc 4 opakowania 10 ml x 100 zł = 400 zł Zalecana ilość powtórzeń: 3 razy w roku (2 razy w roku) • Roczny koszt terapii: 400 zł x 3 = 1200 zł - 3 razy w roku 400 zł x 2 = 800 zł – 2 razy w roku Średni miesięczny koszt: • 1200 zł : 12 miesięcy = 100 zł • (800 zł : 12 miesięcy = ok. 60 zł)

Dawkowanie i sposób podawania - pozostałe Dawki od 10 ml – do 50 ml są zalecane wyłącznie w powolnym wlewie dożylnym po rozcieńczeniu standardowym roztworem do infuzji . - Czas trwania wlewu powinien wynosić 15 - 60 minut. - Dawki do 30 ml należy podawać w 50 ml Na. Cl, większe dawki w 100 ml Na. Cl
- Slides: 32