Cytotoxicit mdiation cellulaire La lyse dune cellule cible

Cytotoxicité à médiation cellulaire • La lyse d’une cellule cible sans l’intervention d’anticorps par la libération polarisée de perforines et l’induction de l’apoptose (granzymes et Fas. Ligand) • Une machinerie utilisée par deux cellules cytotoxiques voisines – L’ancêtre : la cellule natural killer (NK) – Sa descendante « moderne » : le lymphocyte T cytotoxique • La machinerie est la même mais le trigger est différent – Pour le lymphocyte T cytotoxique : TCR – Pour la NK : ?

« licence to kill » des NK? • La reconnaissance de PAMP sur les cellules infectées ou de ligands anormaux sur certaines cellules tumorales joue un rôle mais n’est pas suffisant (nécessaire mais pas suffisant) • comment reconnaître une cellule transformée ou infectée par un virus quand on n’a pas de TCR?

Base moléculaire de la discrimination par les cellules NK • comment reconnaître une cellule transformée ou infectée par un virus quand on n’a pas de TCR? – la cellule NK perçoit l’absence d’une structure normalement présente sur la plupart des cellules saines de l’organisme
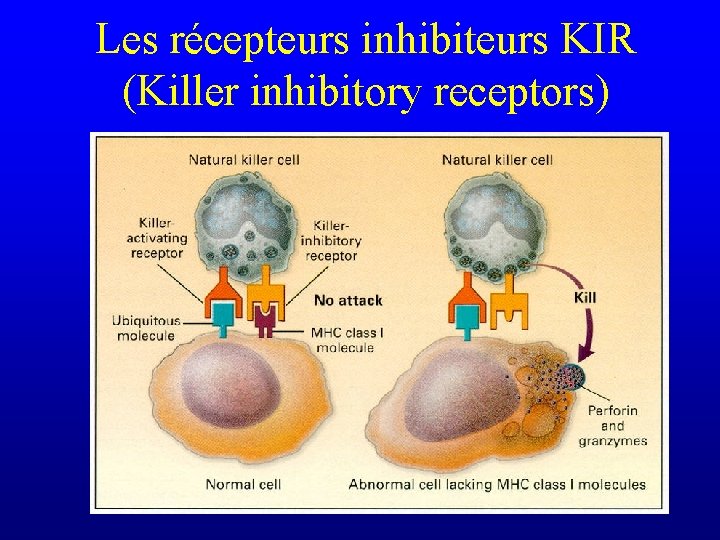
Les récepteurs inhibiteurs KIR (Killer inhibitory receptors)

La perte des molécules MHC de classe I est un moyen fréquemment utilisé par les cellules tumorales ou par les cellules infectées par des virus pour échapper au contrôle des lymphocytes T cytotoxiques CD 8+. . .

cela rend les cellules en question plus sensibles à l’activité des NK. L’évolution a conservé les NK aux côtés des lymphocytes T cytotoxiques pour contrecarrer les mécanismes d’échappement des virus. . .

« Cellules K » et ADCC • ADCC = antibody dependent cell-mediated cytotoxicity
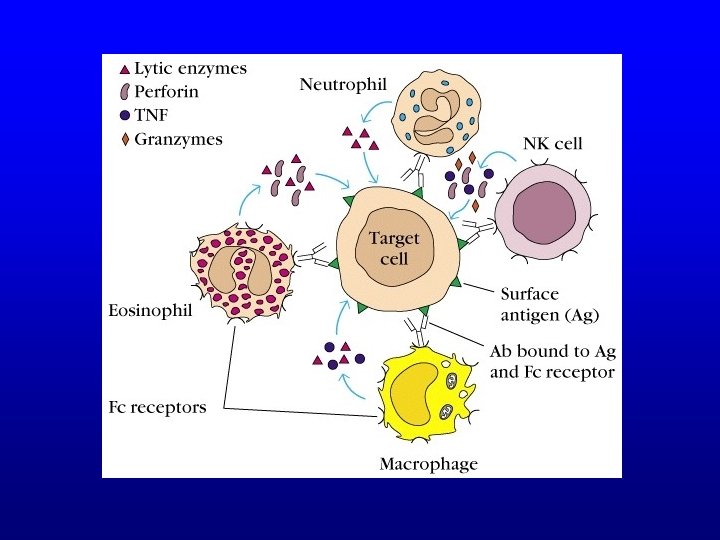

« Cellules K » et ADCC • ADCC = antibody dependent cell-mediated cytotoxicity • Les cellules K correspondent à une fonction particulière que peuvent exercer plusieurs types cellulaires (NK, macrophages, polynucléaires) • Les cellules K ne sont pas une lignée en soi

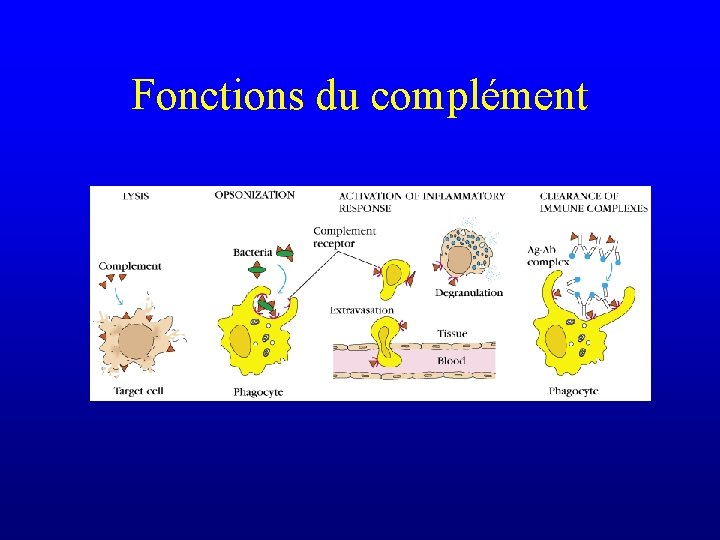
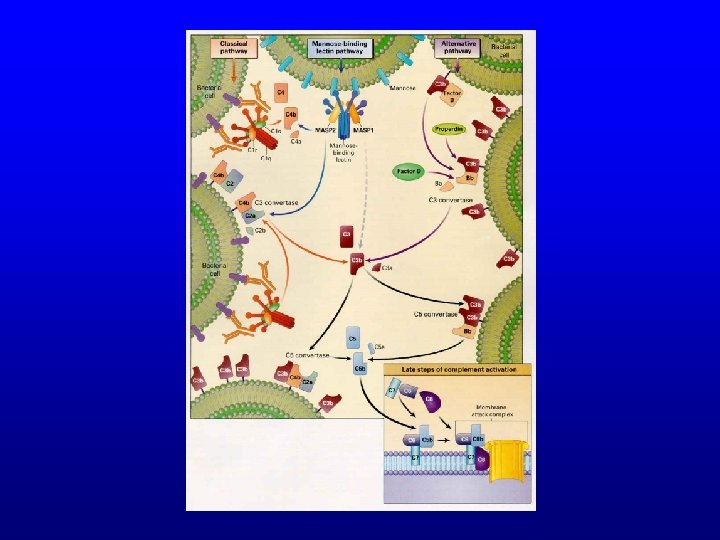
Complément

Complément • Jules Bordet, Paul Ehrlich – complément à l’action bactéricide des immunoglobulines (anticorps) • Système complexe de plus de trente protéines plasmatiques et membranaires
Fonctions du complément

Les protéines du complément • synthétisées majoritairement dans le foie • souvent des proenzymes (ou zymogènes) – dénomination selon l’ordre de découverte pas nécessairement selon un ordre logique (malheureusement) – activation par protéolyse avec séparation d’un fragment inhibiteur et d’un fragment catalytique

Les protéines du complément • Fragment inhibiteur – le plus petit – appelé. . . a – action à distance sur l’activation et le chémotactisme des phagocytes • Fragment catalytique (sérine protéase) – le plus gros – appelé. . . b – action enzymatique locale (à la surface de l’agent pathogène) (nouvelle nomenclature : fragment catalytique de C 2 = C 2 b)
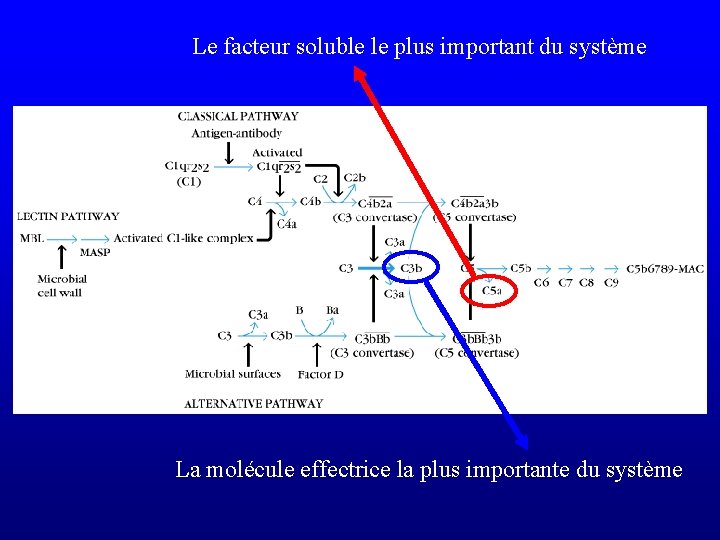
Le facteur soluble le plus important du système La molécule effectrice la plus importante du système
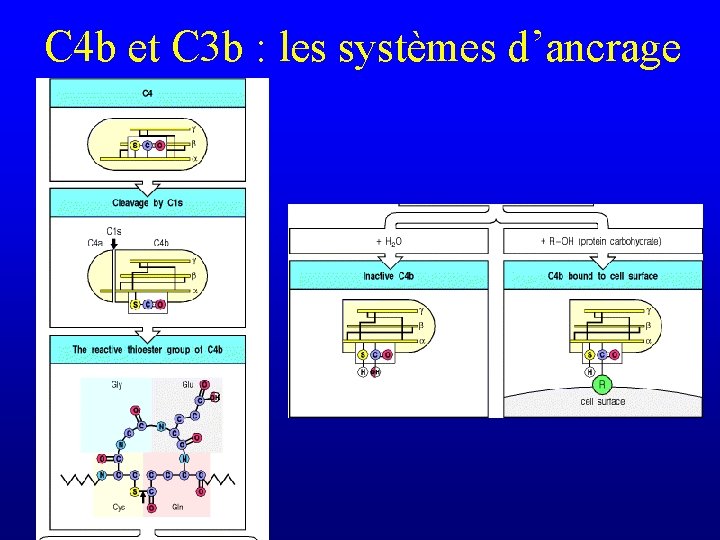
C 4 b et C 3 b : les systèmes d’ancrage

Voie classique : intervention de la collectine C 1 q • Collectines : molécules ancestrales à activité lectine • Interagit avec plusieurs ligands mais en particulier avec des ligands présents sur les immunoglobulines et en particulier sur les complexes immuns • Activation : reconnaissance d’un antigène par un anticorps spécifique – formation d’un complexe immun • La portion Fc d’une immunoglobuline libre (sans antigène fixé sur le Fab) est incapable de lier C 1 q.

Voie classique : le complexe C 1 • C 1 est formé de trois molécules distinctes – C 1 q : dépourvu d’activité enzymatique, se lie au domaine Fc des Ig. M et des Ig. G – C 1 r : sérine protéase – C 1 s : sérine protéase

Le complexe C 1
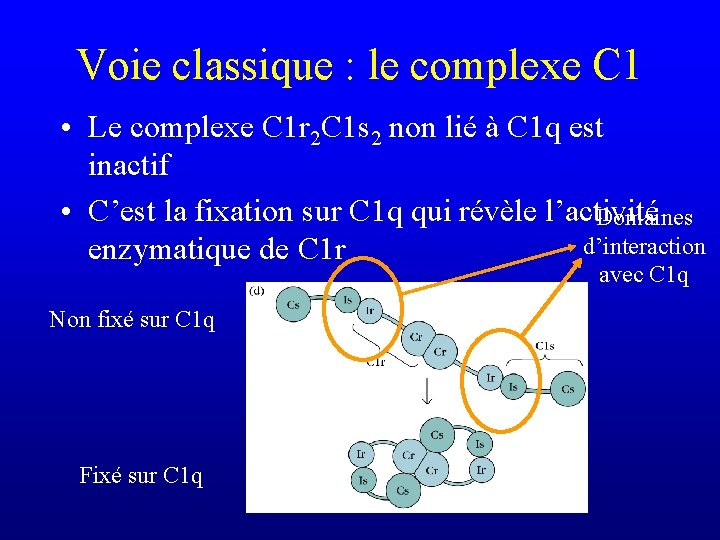
Voie classique : le complexe C 1 • Le complexe C 1 r 2 C 1 s 2 non lié à C 1 q est inactif • C’est la fixation sur C 1 q qui révèle l’activité Domaines d’interaction enzymatique de C 1 r avec C 1 q Non fixé sur C 1 q Fixé sur C 1 q
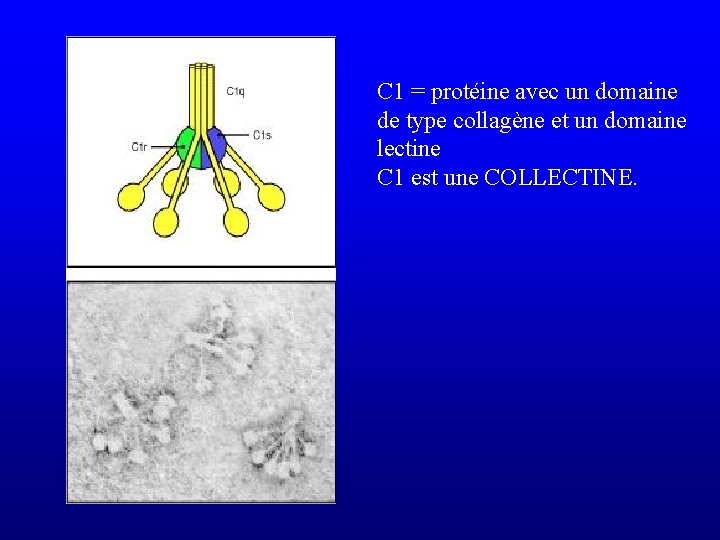
C 1 = protéine avec un domaine de type collagène et un domaine lectine C 1 est une COLLECTINE.

Lectine • Se dit de toute protéine ou glycoprotéine, d’origine animale ou végétale possédant au moins un domaine non catalytique de fixation réversible à un mono- ou à un oligosaccharide spécifique, et ce à l’exclusion des immunoglobulines

Le complexe C 1 • Pour que C 1 r 2 C 1 s 2 puisse se lier à C 1 q, il faut que C 1 q subisse lui-même un changement de conformation • La fixation de C 1 q, notamment sur des complexes immuns permet ce changement de conformation

Le complexe C 1 • Complexes immuns à Ig. M – les Ig. M sont des pentamères – chaque molécule d’Ig. M possède au moins trois sites de fixation au C 1 q • les Ig. M activent très efficacement le complément
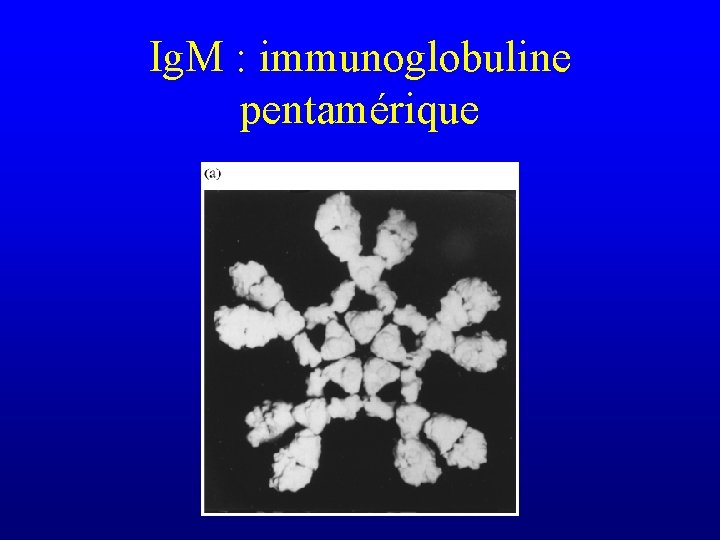
Ig. M : immunoglobuline pentamérique

Le complexe C 1 • Complexes immuns à Ig. M – les Ig. M sont des pentamères – chaque molécule d’Ig. M possède trois sites de fixation au C 1 q • les Ig. M activent très efficacement le complément – Les sites de fixation au C 1 q ne sont exposés que si l’Ig. M est liée à un antigène
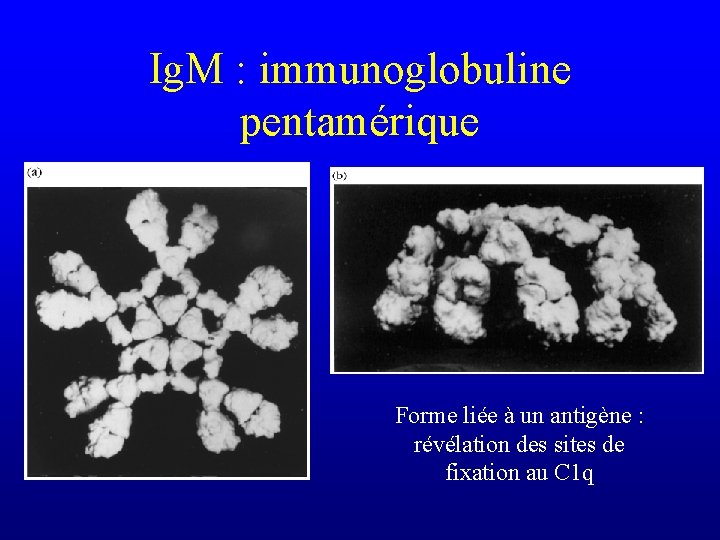
Ig. M : immunoglobuline pentamérique Forme liée à un antigène : révélation des sites de fixation au C 1 q

Le complexe C 1 • Complexes immuns à Ig. G – les Ig. G sont des monomères – chaque molécule d’Ig. G possède un seul site de fixation au C 1 q – La liaison de C 1 q à une seule Ig. G n’est pas suffisante pour modifier sa conformation • les Ig. G sont beaucoup moins efficaces que les Ig. M pour activer le complément

Le complexe C 1 • La liaison de C 1 q à deux Ig ou plus n’est possible que si ces dernières appartiennent à un même complexe immun ou si elles sont fixées sur une même surface

Liaison de C 1 q à des Ig

Un grand classique en immunologie clinique • Le test au C 1 q – destiné à mesurer la présence de complexes immuns dans le plasma

Liaison de C 1 q à des Ig

Liaison de C 1 q à des Ig • Constitution de C 1 qr 2 s 2 C 1 s est le substrat de C 1 r et est lui-même une protéase
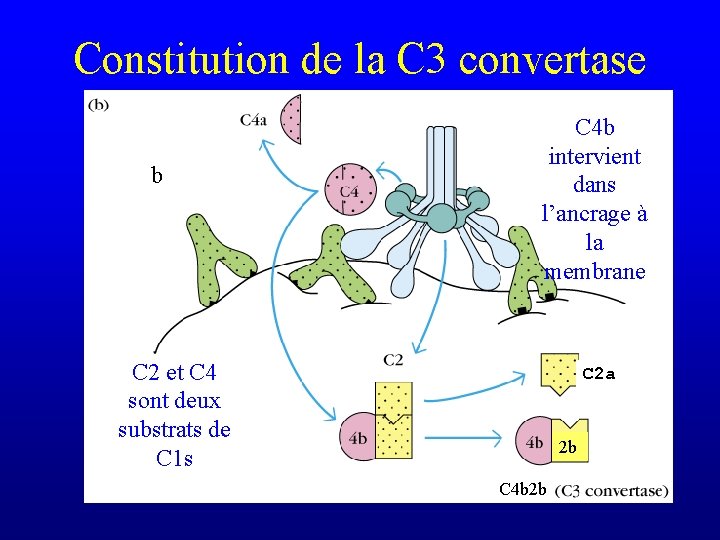
Constitution de la C 3 convertase b C 4 b intervient dans l’ancrage à la membrane C 2 et C 4 sont deux substrats de C 1 s C 2 a 2 b C 4 b 2 b
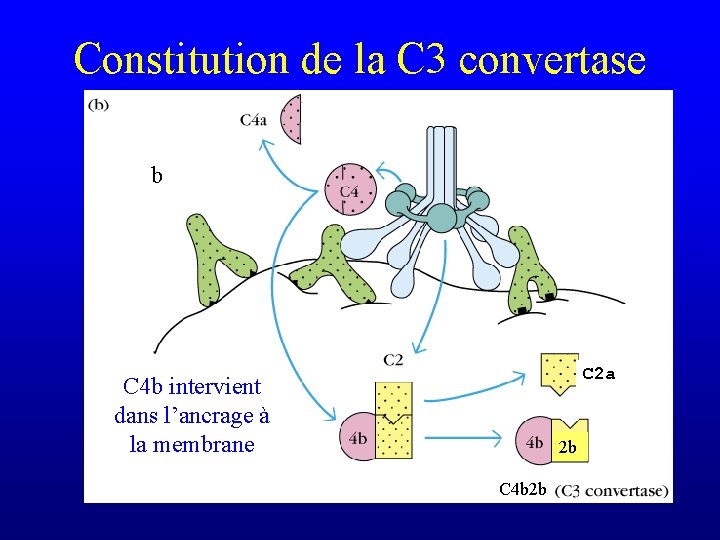
Constitution de la C 3 convertase b C 2 a C 4 b intervient dans l’ancrage à la membrane 2 b C 4 b 2 b
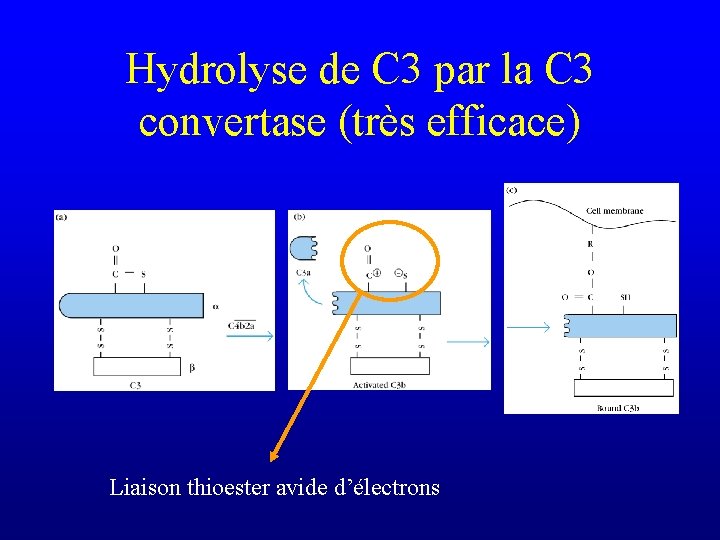
Hydrolyse de C 3 par la C 3 convertase (très efficace) Liaison thioester avide d’électrons
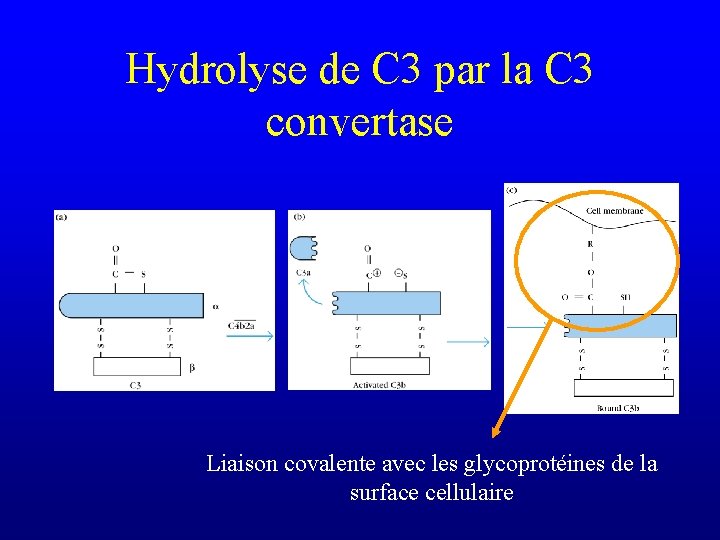
Hydrolyse de C 3 par la C 3 convertase Liaison covalente avec les glycoprotéines de la surface cellulaire
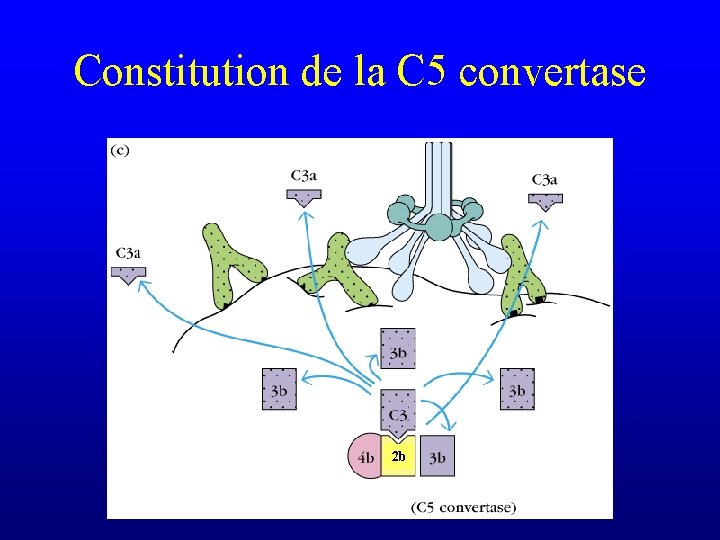
Constitution de la C 5 convertase 2 b

Génération d’une grande quantité de C 3 b qui couvre la surface bactérienne 2 b Tout le C 3 b ne se lie pas à la membrane Une partie diffuse et se fixe sur des complexes immuns solubles et des microorganismes : opsonisation
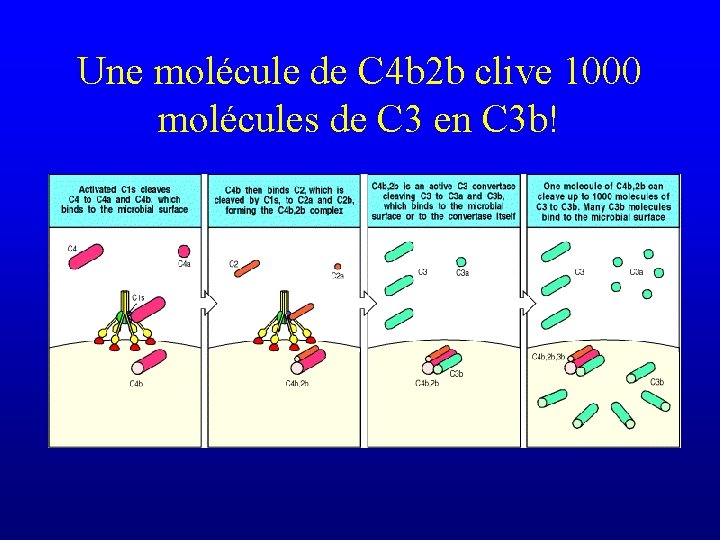
Une molécule de C 4 b 2 b clive 1000 molécules de C 3 en C 3 b!
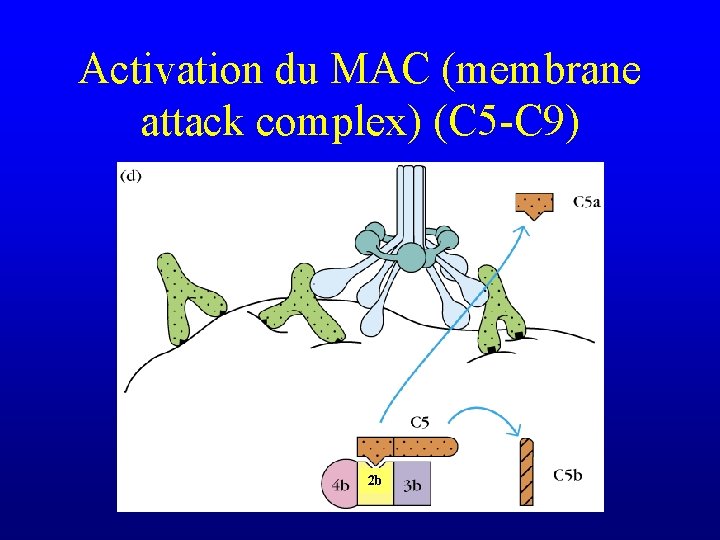
Activation du MAC (membrane attack complex) (C 5 -C 9) 2 b
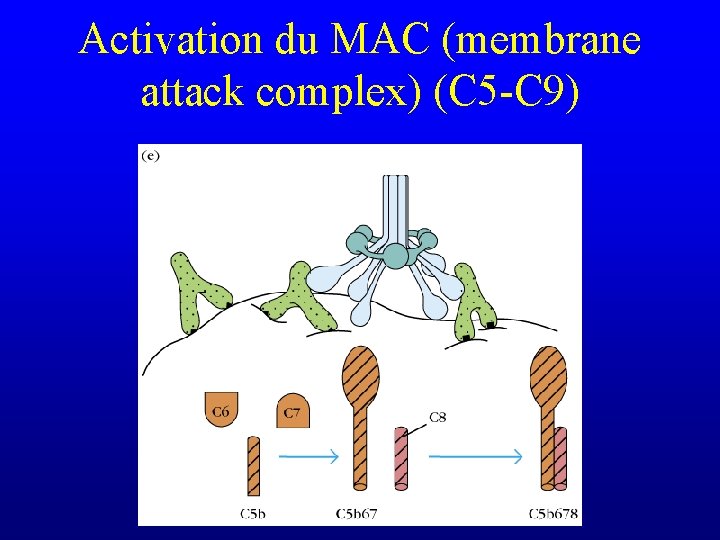
Activation du MAC (membrane attack complex) (C 5 -C 9)
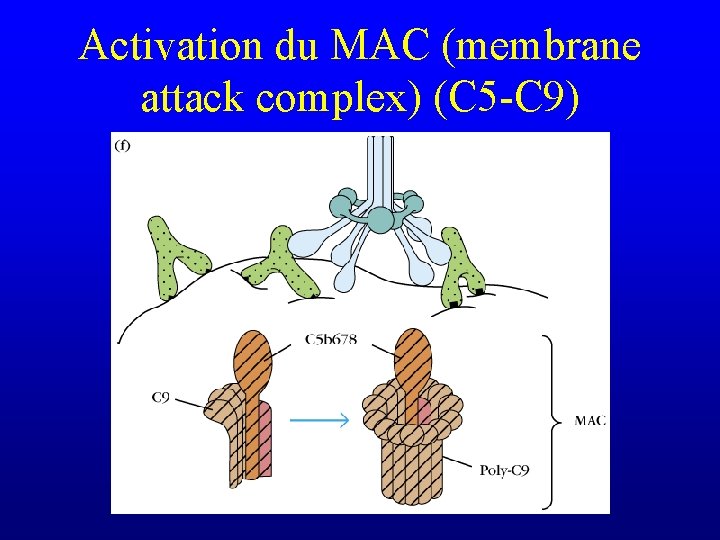
Activation du MAC (membrane attack complex) (C 5 -C 9)

Importance relative du MAC et de la génération de l’opsonine C 3 b • Le MAC est important contre un nombre limité de bactéries (neisseria notamment) • Par contre l’opsonisation par C 3 b est cruciale pour un grand nombre d’agents infectieux.

La voie classique peut parfois être activée via C 1 q mais par autre chose que des complexes immuns

Dans certains cas C 1 q peut se lier directement à certaines cellules • Certaines bactéries (certains steptocoques) • Cellules apoptotiques

Dans d’autres cas, C 1 q est activé par une protéine qui n’est pas une immunoglobuline : la CRP

CRP : C Reactive Protein • Protéine de la phase aiguë de l’inflammation (acute phase protein) • Synthétisée par le foie • Marqueur de l’inflammation très couramment utilisé en biologie clinique
CRP

CRP • Membre d’une famille de protéines très ancienne. • Se lie à la phosphocholine et aux résidus phosphocholine des polysaccharides bactériens. • Se lie aux cellules apoptotiques • Une fois lié à son ligand, peut activer le C 1 q

Une fonction importante de la voie classique du complément est l’élimination des cellules apoptotiques

Lectines • protéines ou glycoprotéines capable de se lier à certains résidus glucidiques • origine non immunitaire • capable comme un anticorps d’agglutiner ou de précipiter des cellules ou des glycoconjugués • isolées initialement chez des végétaux mais molécules voisines (lectin-like) présentes chez les bactéries et les animaux
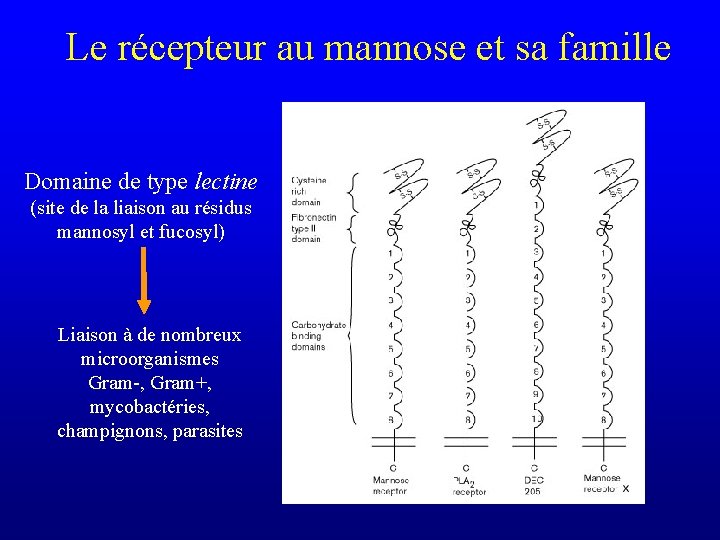
Le récepteur au mannose et sa famille Domaine de type lectine (site de la liaison au résidus mannosyl et fucosyl) Liaison à de nombreux microorganismes Gram-, Gram+, mycobactéries, champignons, parasites

Voie d’activation par la lectine liant le mannose (MBL) • Fait intervenir la MBP (mannose binding protein), une collectine de la même famille que C 1 q • MBL est donc l’équivalent de C 1 q • Une fois liée, la MBP recrute une protéase (la mannose binding protein associated protease ou MASP) qui est l’équivalent de C 1 s et dont les substrats sont C 4 et C 2
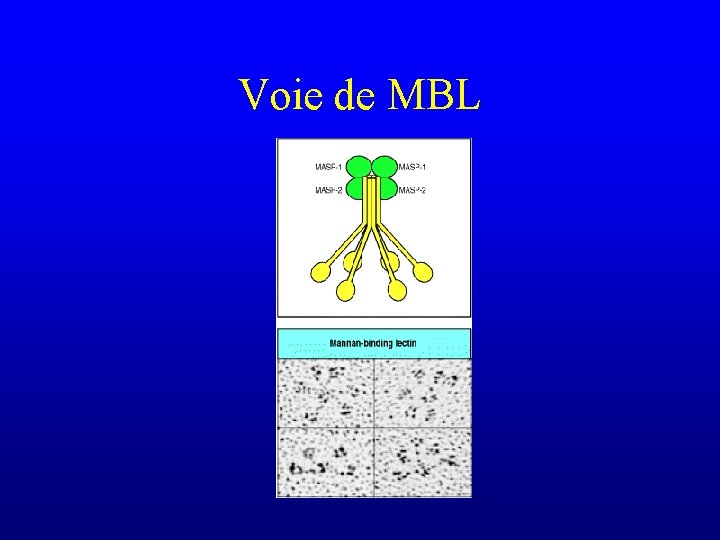
Voie de MBL

Voie alterne • Non liée à la fixation d’une collectine sur un complexe immun ou sur un pathogène donc indépendante de l’immunité adaptative • Considérée comme constituant de l’immunité naturelle • Aboutit à l’activation du MAC (formation de C 5 b sans l’intervention d’anticorps)
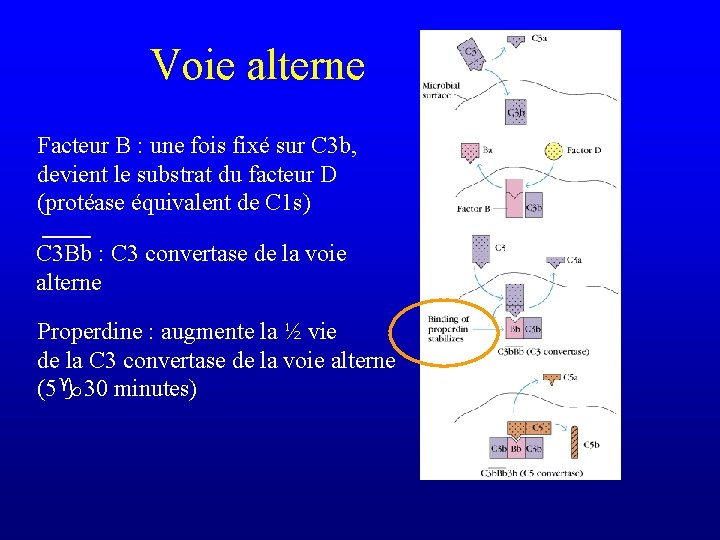
Voie alterne Facteur B : une fois fixé sur C 3 b, devient le substrat du facteur D (protéase équivalent de C 1 s) C 3 Bb : C 3 convertase de la voie alterne Properdine : augmente la ½ vie de la C 3 convertase de la voie alterne (5 30 minutes)

Voie alterne • Présence physiologique de petites quantités de C 3 b dans le plasma (hydrolyse spontanée à bas bruit de la liaison thioester instable) • Fixation de C 3 b sur toutes les cellules (y compris les cellules de l’hôte)

Régulation étroite de la voie alterne sur les cellules eukaryotes

Régulation de la voie alterne • CR 1 et DAF : empêchent l’interaction C 3 b B et déplacent C 3 b des complexes C 3 b. Bb déjà formés • Facteur I : protéase plasmatique qui clive C 3 b en i. C 3 b • CR 1, DAF et facteur H sont des cofacteurs du facteur I • L’activité du facteur H dépend du contenu cellulaire en acide sialique
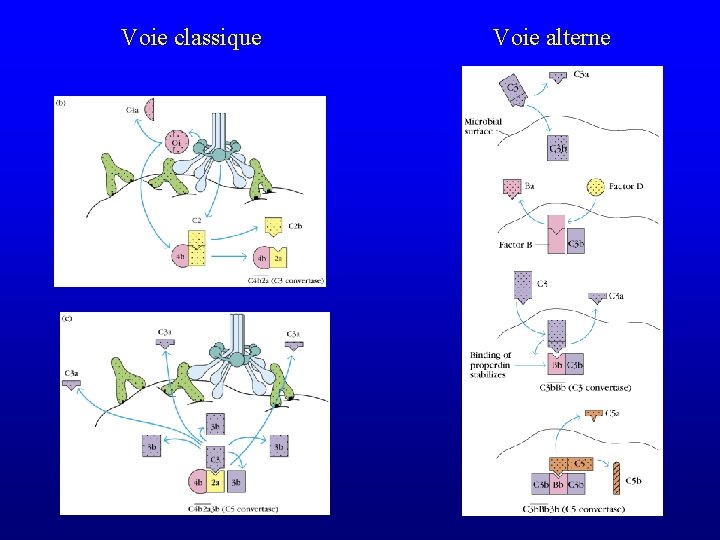
Voie classique Voie alterne

Voie classique vs. voie alterne C 4 b 2 b 3 b
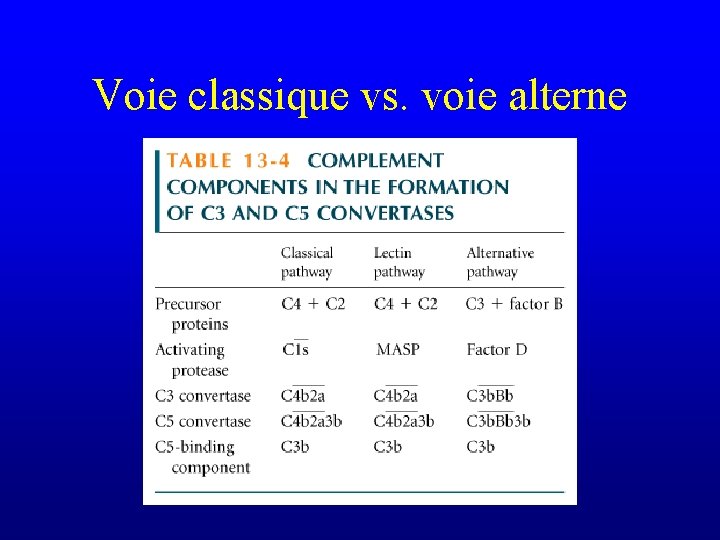
Voie classique vs. voie alterne
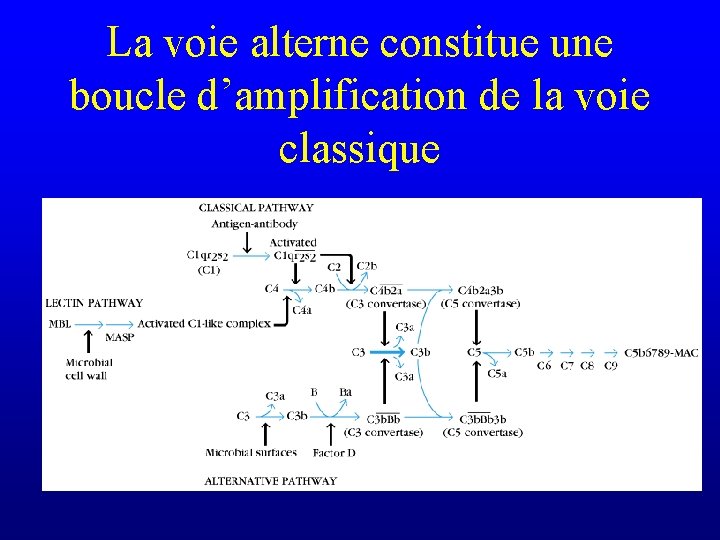
La voie alterne constitue une boucle d’amplification de la voie classique

Les trois modes d’initiation de la cascade du complément • Classique : intervention de C 1 q – Via COMPLEXES IMMUNS : le plus souvent – Via CRP (polysaccharides bactériens, cellules apoptotiques) – Directement (certaines bactéries, cellules apoptotiques)

Les trois modes d’initiation de la cascade du complément • Alterne : pas d’intervention de C 1 q – Nombreuses bactéries, champignons, virus, cellules tumorales • Mannose binding lectin – Microorganismes qui contiennent des groupes mannoses terminaux
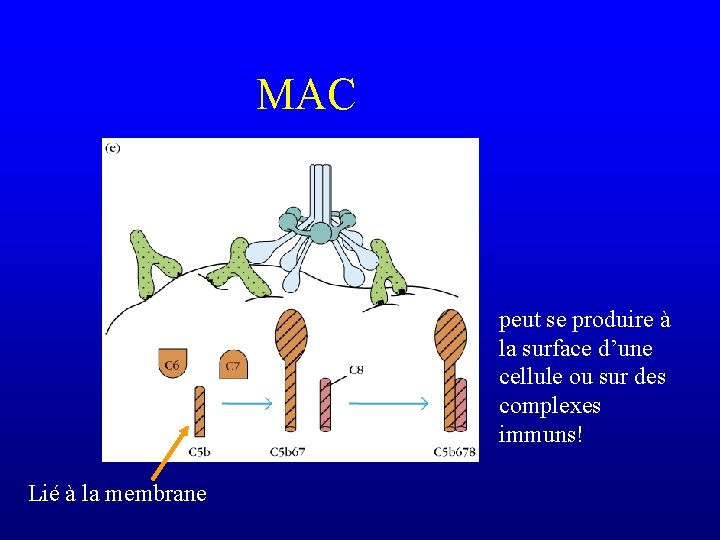
MAC peut se produire à la surface d’une cellule ou sur des complexes immuns! Lié à la membrane

MAC • Attention : si le MAC est activé par des complexes immuns libres (non cellulaires), le C 5 b 67 peut aller se fixer sur des cellules voisines (qui n’ont pas d’antigène à leur surface) – innocent bystander lysis
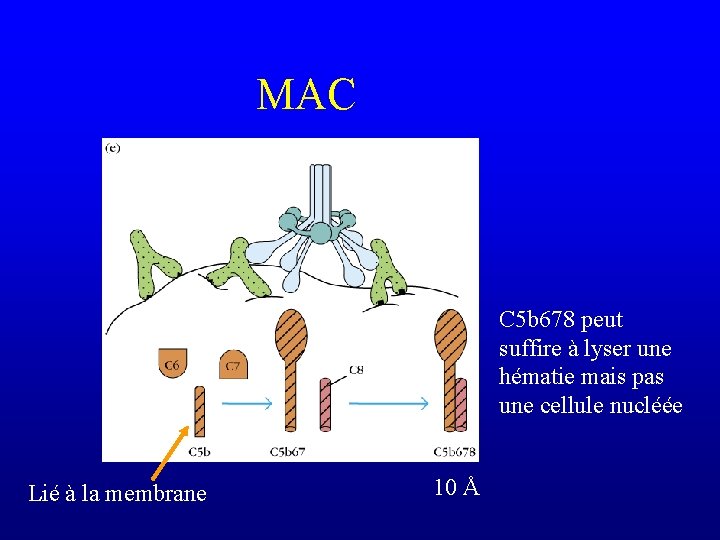
MAC C 5 b 678 peut suffire à lyser une hématie mais pas une cellule nucléée Lié à la membrane 10 Å

Activation du MAC (membrane attack complex) (C 5 -C 9) 100 Å

La régulation du complément • Une activation intempestive du complément peut tuer un individu ou altérer gravement ses organes – molécules très labiles une fois activées – nombreux systèmes de contrôle
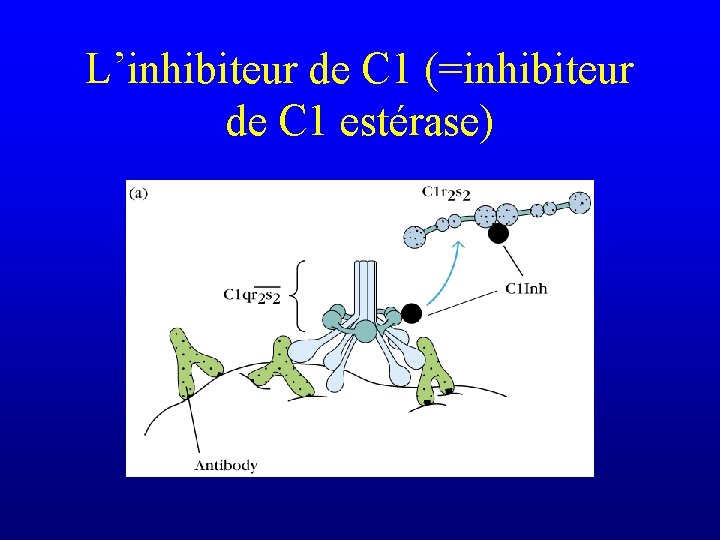
L’inhibiteur de C 1 (=inhibiteur de C 1 estérase)
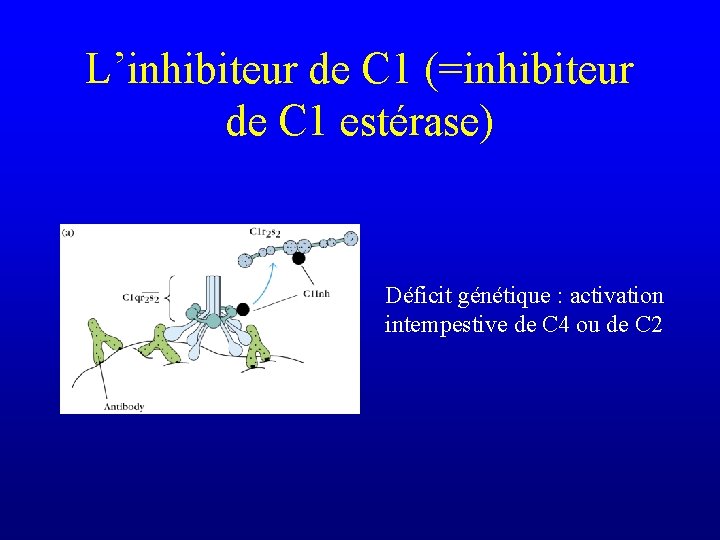
L’inhibiteur de C 1 (=inhibiteur de C 1 estérase) Déficit génétique : activation intempestive de C 4 ou de C 2

Les protéines RCA (regulator of complement activation) • Famille de protéines (toutes codées par le même chromosome) et qui régulent l’activité de la C 3 convertase – voie classique : se lient à C 4 b • une protéine soluble : C 4 BP • deux protéines membranaires : CR 1 et MCP • une protéase qui inactive C 4 b en C 4 d et C 4 c

Les protéines RCA (regulator of complement activation) • Famille de protéines (toutes codées par le même chromosome) et qui régulent l’activité de la C 3 convertase – voie alterne : se lient à C 3 b • trois protéines membranaires : CR 1, MCP, facteur H • une protéase qui inactive C 3 b en C 3 c et C 3 dg
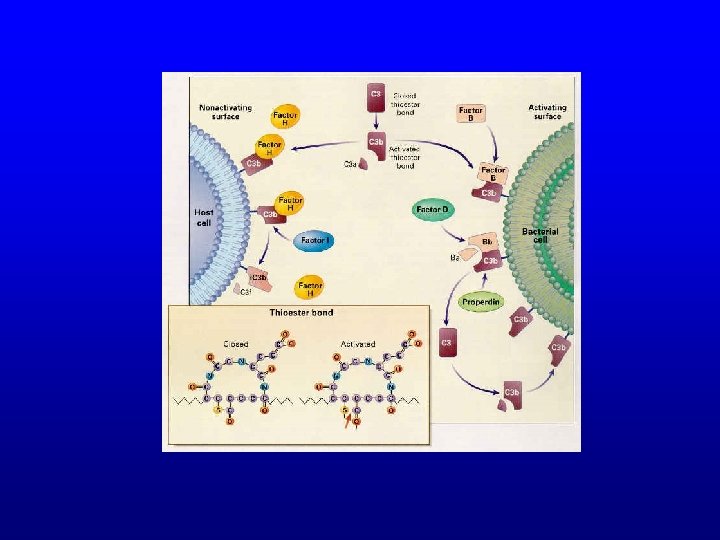

Les protéines RCA (regulator of complement activation) • Famille de protéines (toutes codées par le même chromosome) et qui régulent l’activité de la C 3 convertase (voie classique ou voie alterne) – inhibent sa formation – favorisent sa dissociation (decay) • C 4 BP, CRI, facteur H • DAF (decay accelerating factor)
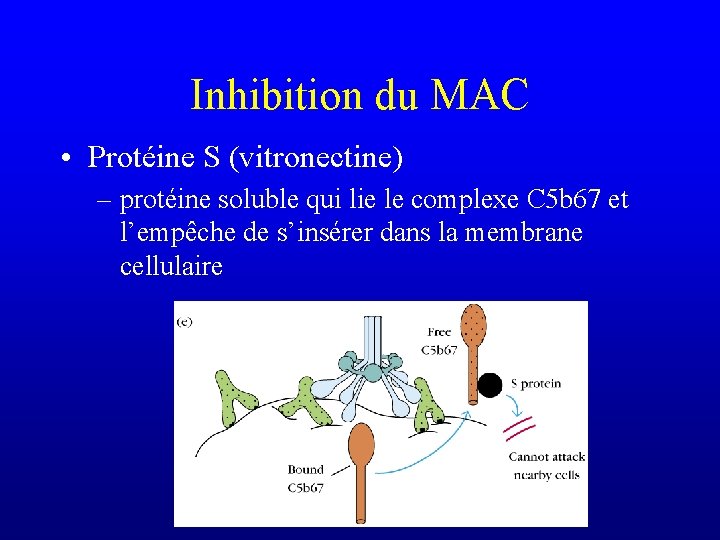
Inhibition du MAC • Protéine S (vitronectine) – protéine soluble qui lie le complexe C 5 b 67 et l’empêche de s’insérer dans la membrane cellulaire
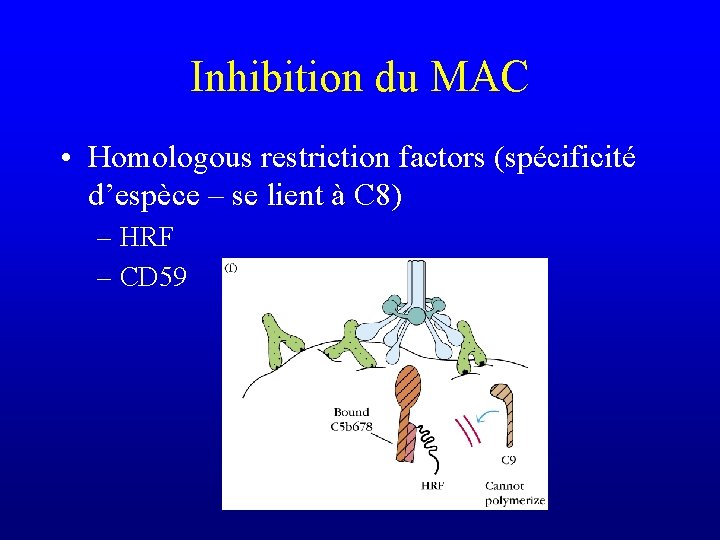
Inhibition du MAC • Homologous restriction factors (spécificité d’espèce – se lient à C 8) – HRF – CD 59
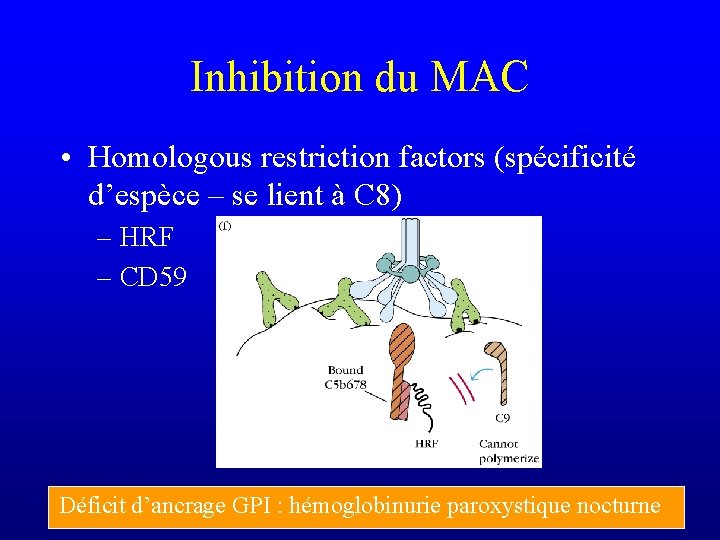
Inhibition du MAC • Homologous restriction factors (spécificité d’espèce – se lient à C 8) – HRF – CD 59 Déficit d’ancrage GPI : hémoglobinurie paroxystique nocturne

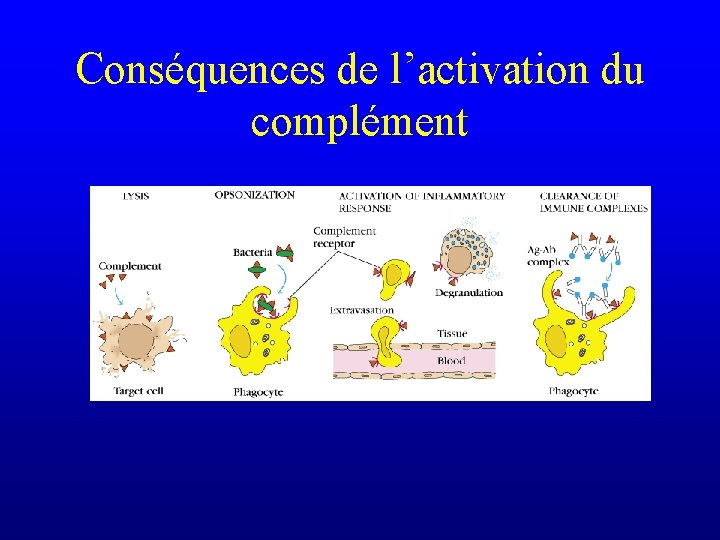
Conséquences de l’activation du complément
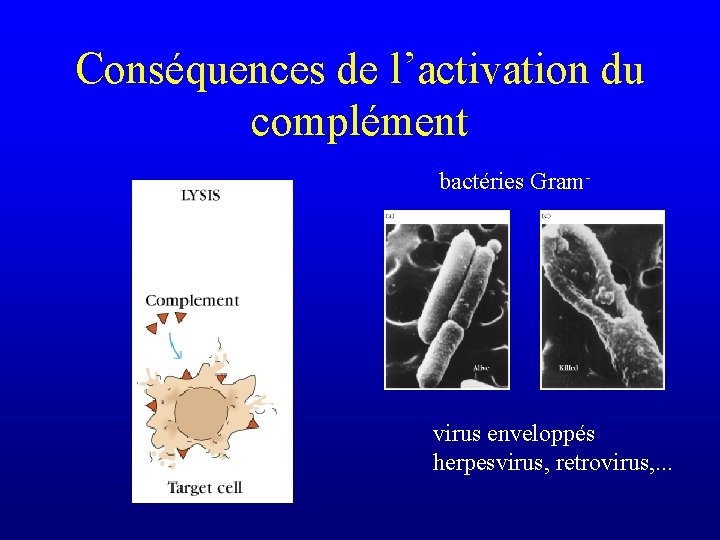
Conséquences de l’activation du complément bactéries Gram- virus enveloppés herpesvirus, retrovirus, . . .

Conséquences de l’activation du complément peu efficace contre les bactéries Gram+ et les cellules nucléées (notamment tumorales)

Conséquences de l’activation du complément • Neutralisation de certains virus par la fixation de certains composants du complément indépendemment de l’activation du MAC

Conséquences de l’activation du complément Principale opsonine : C 3 b

Conséquences de l’activation du complément Principale opsonine : C 3 b Récepteur CR 1
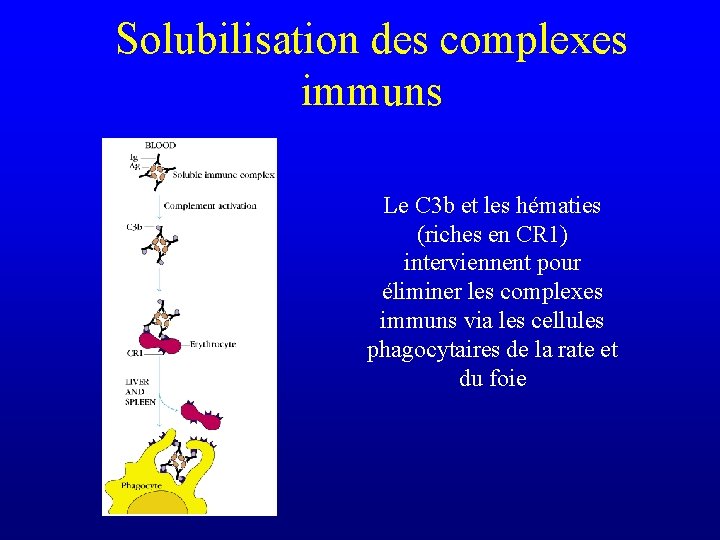
Solubilisation des complexes immuns Le C 3 b et les hématies (riches en CR 1) interviennent pour éliminer les complexes immuns via les cellules phagocytaires de la rate et du foie

Réponse inflammatoire • C 3 a, C 4 a et C 5 a sont des anaphylatoxines, des facteurs solubles qui initient la réponse inflammatoire

Inflammation • réaction défensive immédiate des tissus à l’infection ou à une agression par des agents chimiques ou physiques. Le tissu affecté est caractérisé par la perception d’une douleur, la tuméfaction, la chaleur, la rougeur et la perte de fonction

Inflammation • ceci correspond à une vasodilatation locale, une extravasation de plasma dans les espaces intercellulaires et une accumulation de leucocytes dans l’organe atteint. Les systèmes enzymatiques du plasma jouent un rôle fondamental dans la génération de médiateurs de l’inflammation

Inflammation • ces systèmes enzymatiques incluent le complément, la coagulation, la fibrinolyse et les kinines

Inflammation • Rougeur et chaleur : vasodilatation • Gonflement : extravasation de plasma et de leucocytes • Douleur : libération de médiateurs par les leucocytes au voisinage des terminaisons nerveuses

Réponse inflammatoire • C 3 a, C 4 a et surtout C 5 a sont des anaphylatoxines, des facteurs solubles qui initient la réponse inflammatoire – provoquent la dégranulation des basophiles et des mastocytes tissulaires et la libération d’amines vasoactives (en particulier d’histamine) • vasodilatation, augmentation de la perméabilité vasculaire, contraction des muscles lisses bronchiques – induisent l’adhérence des neutrophiles et des monocytes au cellules endothéliales, leur extravasation, et leur activation sur le site inflammatoire

Réponse inflammatoire • C 3 a, C 4 a et surtout C 5 a sont des anaphylatoxines, des facteurs solubles qui initient la réponse inflammatoire – activité régulée par une protéase la carboxypeptidase N – les formes des-Arg ont perdu l’essentiel de leur activité

Quizz : vrai ou faux • Une seule molécule d’Ig. M fixée sur une surface suffit à activer C 1 q de la voie classique

Quizz : vrai ou faux • C 3 a et C 3 b sont des fragments de C 3

Quizz : vrai ou faux • Les cellules nuclées sont plus résistantes à la lyse induite par le complément que les hématies

Quizz : vrai ou faux • Les virus enveloppés ne peuvent être lysés par le complément parce que leur enveloppe est résistante à la formation de pores par le MAC

Quizz : vrai ou faux • Les individus déficients en C 4 éliminent mal les complexes immuns circulants

Questions ouvertes • Pourquoi une Ig. M sérique ne peut-elle activer la voie classique?

Questions ouvertes • Quel déficit génétique aura selon vous le plus d’implications cliniques (infectieuses) – C 1 – C 3

Questions ouvertes • Certains microorganismes produisent des enzymes capables de dégrader la portion Fc des immunoglobulines. Quel avantage ces enzymes apportent-ils aux microorganismes en question?

Voies classique/alterne/lectine • Quel type de stimulus pour l’activation de chaque voie?

Voies classique/alterne/lectine • Parties communes & parties différentes?

Voies classique/alterne/lectine • Conséquences biologiques similaires ou différentes?

Systèmes de régulation • Pourquoi les globules rouges sont-ils plus sensibles au complément que les cellules nucléées? • Pourquoi les globules d’un individu ne sont-ils normalement pas lysés par le complément (innocent bystander lysis)? • Dans quelles conditions, des globules rouges peuvent-il détruits par le complément?

• • • a. C 3 b b. C 1, C 4, C 2 et C 3 c. C 9 d. C 3, facteur B et properdine e. C 1 q f. C 4 b 2 a 3 b g. C 5 b, C 6, C 7, C 8 et C 9 h. C 3 a+C 3 b i. C 3 a, C 5 a, et C 5 b. C 7 j. C 3 a, C 4 a, et C 5 a k. C 4 b 2 a i. C 3 b+B C 3 b. Bb+Ba • 1. Réaction qui produit une amplification majeure • 2. Composants précoces v. alterne • 3. Les composants du MAC • 4. Responsable de l’opsonisation • 5. Composants précoces v. classique • 6. Activité de type perforine • 7. Se lie au Fc des anticorps • 8. Activité chémotactique • 9. Activité C 3 convertase • 10. Anaphylatoxines • 11. Activité C 5 convertase • 12. Réaction catalysée par facteur D • 13. Réaction catalysée par C 1 qr 2 s 2
- Slides: 109