CURVAS TEMPORALES DE ACTIVIDAD ENZIMTICA Discusin OBJETIVOS Conocer

CURVAS TEMPORALES DE ACTIVIDAD ENZIMÁTICA Discusión

OBJETIVOS Conocer las características generales de las enzimas como catalizadores biológicos. v Adquirir la habilidad para medir la actividad de una enzima utilizando un método espectrofotométrico. v Relacionar los distintos parámetros asociados a la medición de la actividad enzimática que permiten seguir y evaluar la purificación de una enzima (actividad específica, rendimiento y enriquecimiento). v
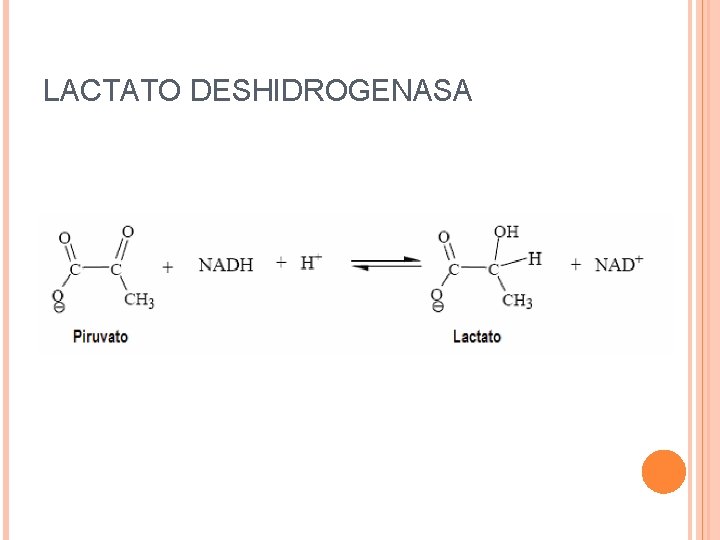
LACTATO DESHIDROGENASA
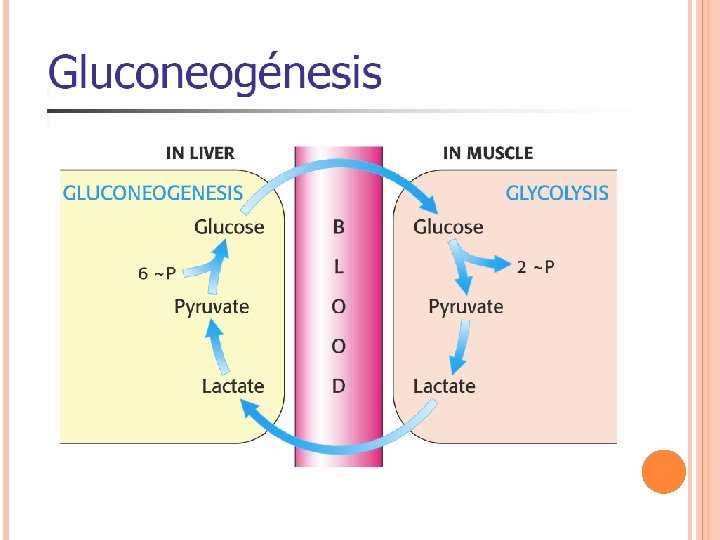
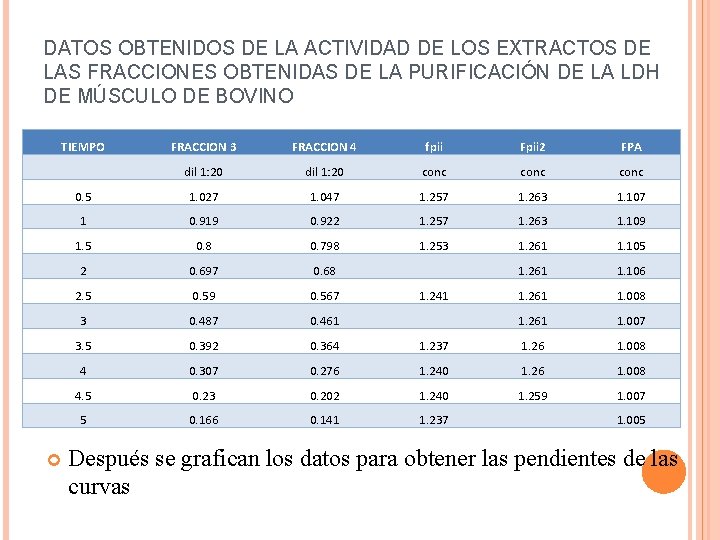
DATOS OBTENIDOS DE LA ACTIVIDAD DE LOS EXTRACTOS DE LAS FRACCIONES OBTENIDAS DE LA PURIFICACIÓN DE LA LDH DE MÚSCULO DE BOVINO TIEMPO FRACCION 3 FRACCION 4 fpii Fpii 2 FPA dil 1: 20 conc 0. 5 1. 027 1. 047 1. 257 1. 263 1. 107 1 0. 919 0. 922 1. 257 1. 263 1. 109 1. 5 0. 8 0. 798 1. 253 1. 261 1. 105 2 0. 697 0. 68 1. 261 1. 106 2. 5 0. 59 0. 567 1. 261 1. 008 3 0. 487 0. 461 1. 261 1. 007 3. 5 0. 392 0. 364 1. 237 1. 26 1. 008 4 0. 307 0. 276 1. 240 1. 26 1. 008 4. 5 0. 23 0. 202 1. 240 1. 259 1. 007 5 0. 166 0. 141 1. 237 1. 241 1. 005 Después se grafican los datos para obtener las pendientes de las curvas
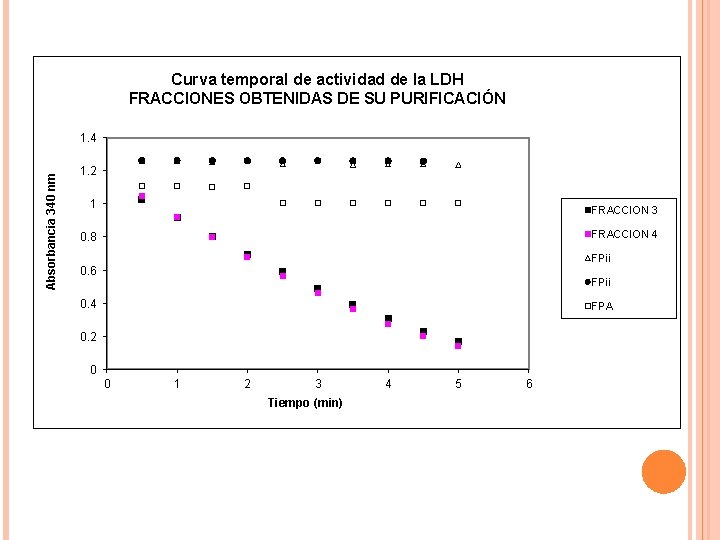
Curva temporal de actividad de la LDH FRACCIONES OBTENIDAS DE SU PURIFICACIÓN Absorbancia 340 nm 1. 4 1. 2 1 FRACCION 3 FRACCION 4 0. 8 FPii 0. 6 FPii 0. 4 FPA 0. 2 0 0 1 2 3 Tiempo (min) 4 5 6

CÁLCULOS mg proteína F 3= 0. 01812 mg (lo obtuve al considerar que había 7. 25 / L en el concentrado (datos de determinación de proteína de mi extracto) al diluir 1: 20 quedaron 0. 3625 g/ L, como añadí 50 L entonces la celda tenía 0. 01812 mg)

ACTIVIDAD DE LDH DE LAS FRACCIONES 3 Y 4 DEL PROCESO DE PURIFICACIÓN DE AL ENZIMA Fracción 3 ( mol min-1 mg-1) Fracción 4 ( mol min-1 mg-1) m 0. 1946 0. 2043 r 2 0. 99 Actividad 29. 490499 33. 293998
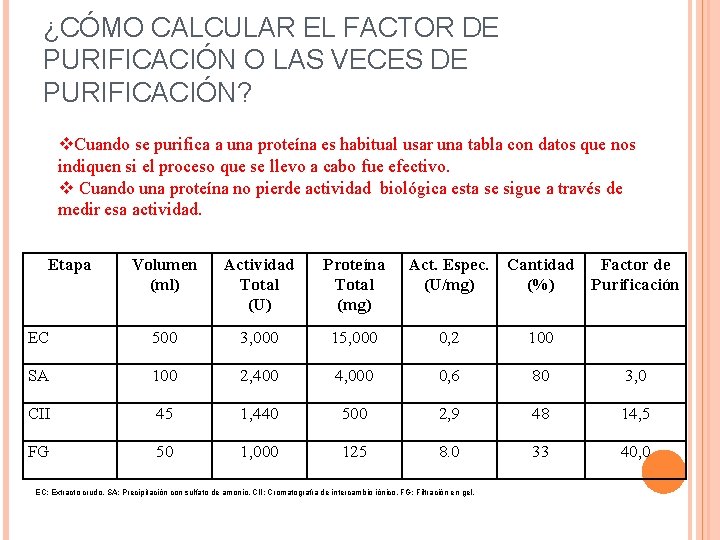
¿CÓMO CALCULAR EL FACTOR DE PURIFICACIÓN O LAS VECES DE PURIFICACIÓN? v. Cuando se purifica a una proteína es habitual usar una tabla con datos que nos indiquen si el proceso que se llevo a cabo fue efectivo. v Cuando una proteína no pierde actividad biológica esta se sigue a través de medir esa actividad. Etapa Volumen (ml) Actividad Total (U) Proteína Total (mg) Act. Espec. (U/mg) EC 500 3, 000 15, 000 0, 2 100 SA 100 2, 400 4, 000 0, 6 80 3, 0 CII 45 1, 440 500 2, 9 48 14, 5 FG 50 1, 000 125 8. 0 33 40, 0 EC: Extracto crudo. SA: Precipitación con sulfato de amonio. CII: Cromatografía de intercambio iónico. FG: Filtración en gel. Cantidad Factor de (%) Purificación
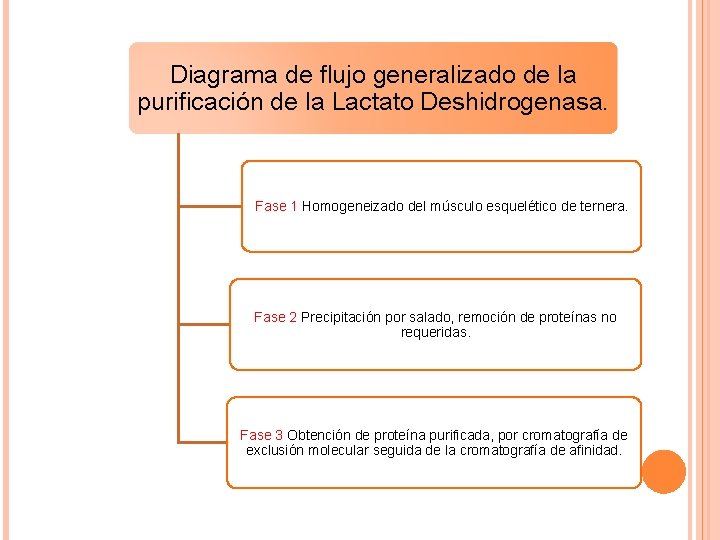
Diagrama de flujo generalizado de la purificación de la Lactato Deshidrogenasa. Fase 1 Homogeneizado del músculo esquelético de ternera. Fase 2 Precipitación por salado, remoción de proteínas no requeridas. Fase 3 Obtención de proteína purificada, por cromatografía de exclusión molecular seguida de la cromatografía de afinidad.
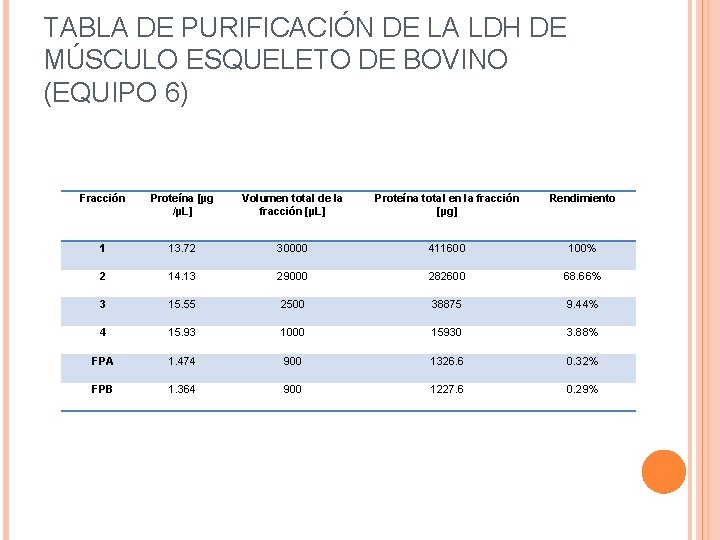
TABLA DE PURIFICACIÓN DE LA LDH DE MÚSCULO ESQUELETO DE BOVINO (EQUIPO 6) Fracción Proteína [µg /µL] Volumen total de la fracción [µL] Proteína total en la fracción [µg] Rendimiento 1 13. 72 30000 411600 100% 2 14. 13 29000 282600 68. 66% 3 15. 55 2500 38875 9. 44% 4 15. 93 1000 15930 3. 88% FPA 1. 474 900 1326. 6 0. 32% FPB 1. 364 900 1227. 6 0. 29%
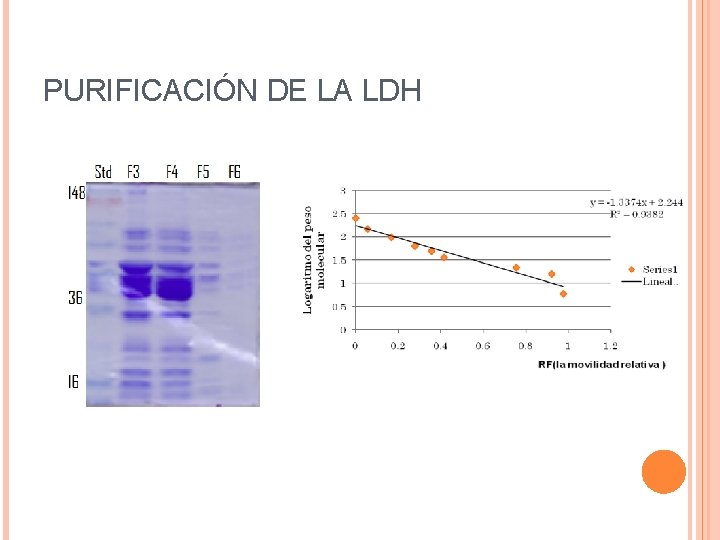
PURIFICACIÓN DE LA LDH
- Slides: 12