Curso Pr Vestibular 1 O Portal do vestibular

Curso Pré- Vestibular 1 – O Portal do vestibular! www. vestibular 1. com. br Química Professor: Albério Riccio Filho

O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria.
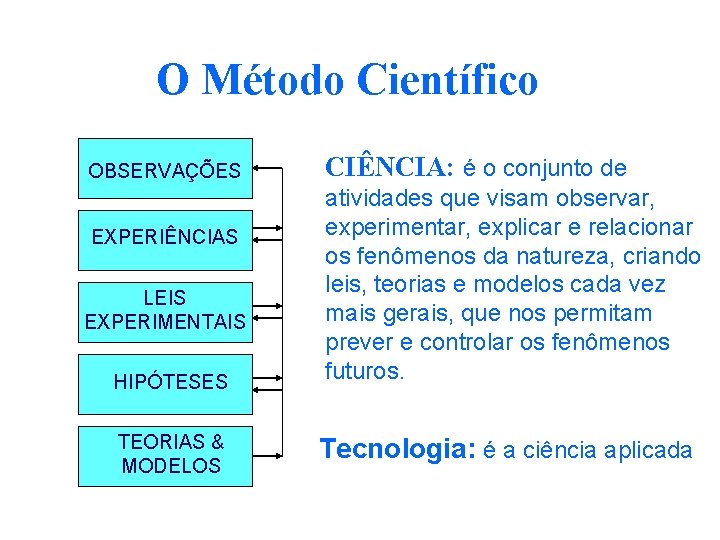
O Método Científico OBSERVAÇÕES EXPERIÊNCIAS LEIS EXPERIMENTAIS HIPÓTESES TEORIAS & MODELOS CIÊNCIA: é o conjunto de atividades que visam observar, experimentar, explicar e relacionar os fenômenos da natureza, criando leis, teorias e modelos cada vez mais gerais, que nos permitam prever e controlar os fenômenos futuros. Tecnologia: é a ciência aplicada
ESTRUTURA DA MATÉRIA A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas chamadas de átomos.
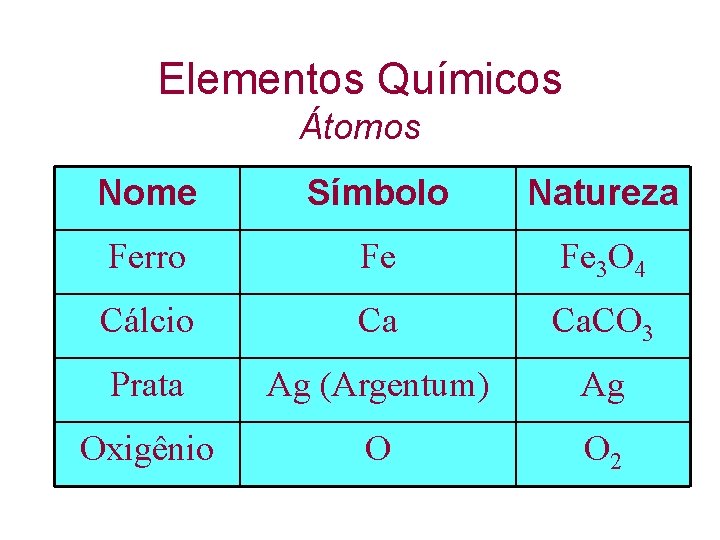
Elementos Químicos Átomos Nome Símbolo Natureza Ferro Fe Fe 3 O 4 Cálcio Ca Ca. CO 3 Prata Ag (Argentum) Ag Oxigênio O O 2
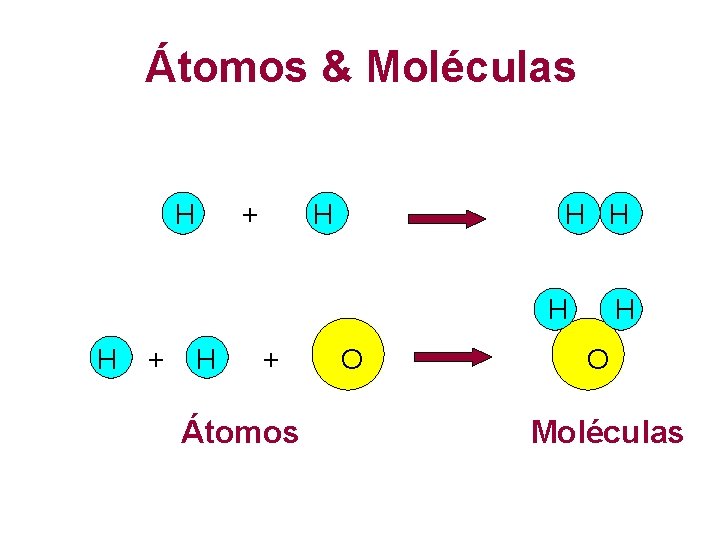
Átomos & Moléculas H + H H H + Átomos O H O Moléculas
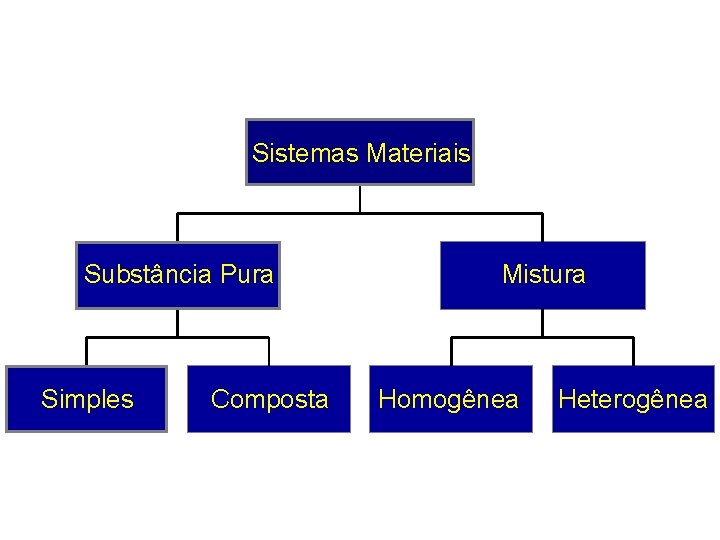
Sistemas Materiais Substância Pura Simples Composta Mistura Homogênea Heterogênea
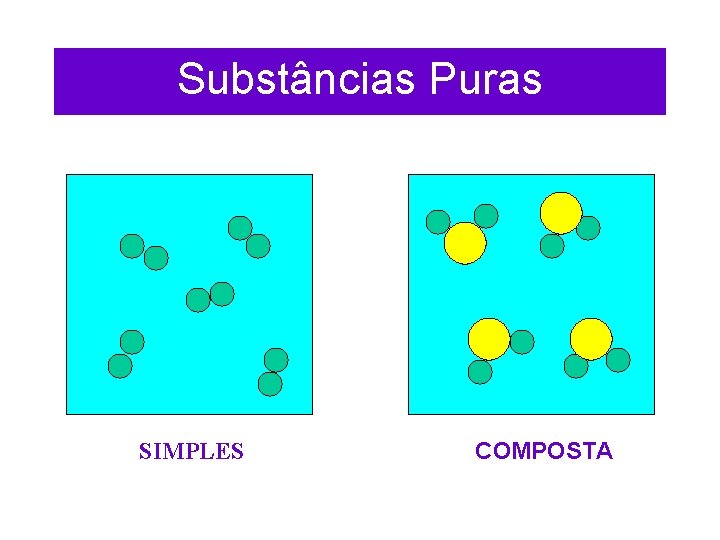
Substâncias Puras SIMPLES COMPOSTA
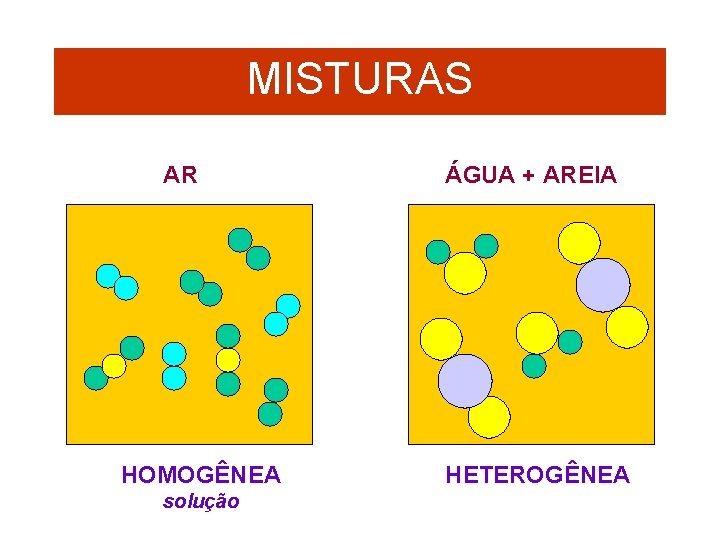
MISTURAS AR HOMOGÊNEA solução ÁGUA + AREIA HETEROGÊNEA
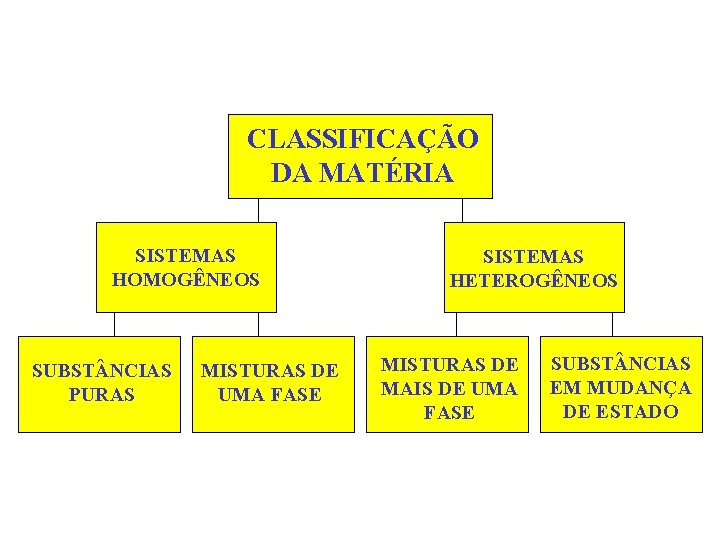
CLASSIFICAÇÃO DA MATÉRIA SISTEMAS HOMOGÊNEOS SUBST NCIAS PURAS MISTURAS DE UMA FASE SISTEMAS HETEROGÊNEOS MISTURAS DE MAIS DE UMA FASE SUBST NCIAS EM MUDANÇA DE ESTADO

OUTROS CONCEITOS v ATOMICIDADE v VARIEDADE ALOTRÓPICA v FENÔMENOS (Transformações): QUÍMICOS E FÍSICOS

ATOMICIDADE Atomicidade Substâncias Monoatômica He, Ne, Ar, Kr Diatômica H 2, N 2, HCl, CO Tetratômica P 4 (fósforo branco) Indeterminada P(verm), C(graf), metais v Atomicidade se refere ao número de átomos que compõem uma substância
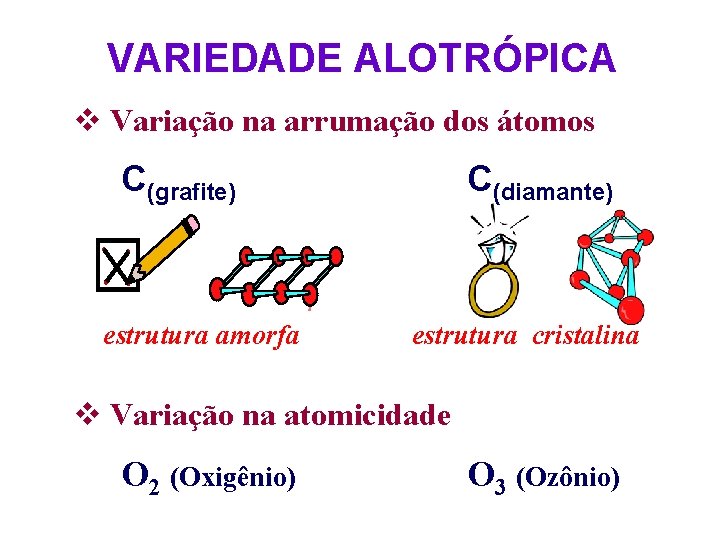
VARIEDADE ALOTRÓPICA v Variação na arrumação dos átomos C(grafite) estrutura amorfa C(diamante) estrutura cristalina v Variação na atomicidade O 2 (Oxigênio) O 3 (Ozônio)

FENÔMENO QUÍMICO Combustão do álcool etílico H 3 C- CH 2 - OH + 3 O 2 2 CO 2 + 3 H 2 O Reagentes Produtos v O fenômeno químico transforma a natureza íntima da matéria.
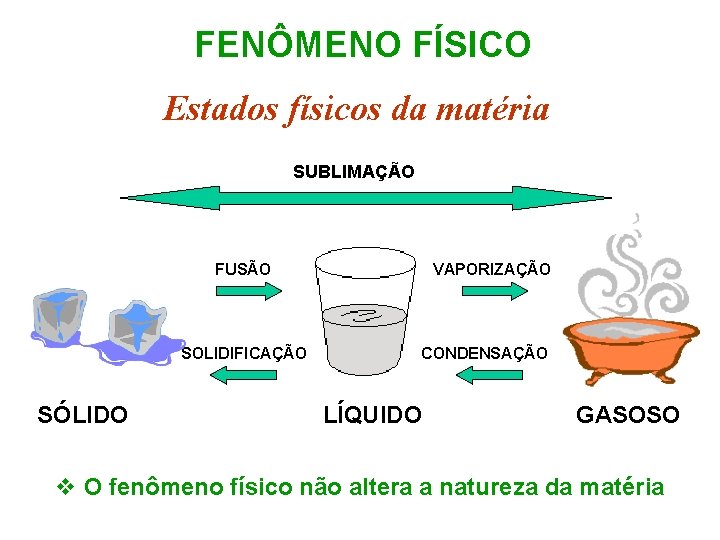
FENÔMENO FÍSICO Estados físicos da matéria SUBLIMAÇÃO FUSÃO SOLIDIFICAÇÃO SÓLIDO VAPORIZAÇÃO CONDENSAÇÃO LÍQUIDO GASOSO v O fenômeno físico não altera a natureza da matéria
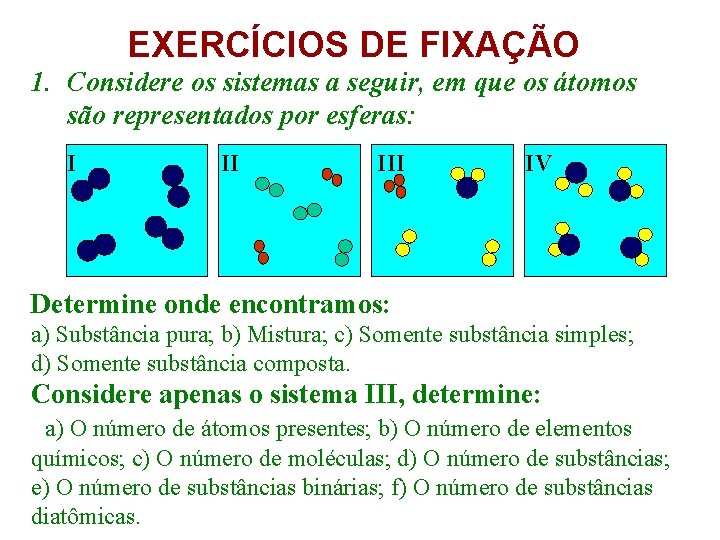
EXERCÍCIOS DE FIXAÇÃO 1. Considere os sistemas a seguir, em que os átomos são representados por esferas: I II IV Determine onde encontramos: a) Substância pura; b) Mistura; c) Somente substância simples; d) Somente substância composta. Considere apenas o sistema III, determine: a) O número de átomos presentes; b) O número de elementos químicos; c) O número de moléculas; d) O número de substâncias; e) O número de substâncias binárias; f) O número de substâncias diatômicas.

2. Considere o sistema representado abaixo. Pode-se descrever o sistema em questão como constituido por: a) Três fases e um componente. b) Duas fases e dois componentes. c) Três fases e dois componentes. d) Três fases e três componentes.

3. Os diferentes tipos de matéria podem ser classificados em dois grupos: Substâncias puras e misturas. As substâncias puras podem ser simples e compostas. Considerando esse modo de classificação, pode-se afirmar: (01) O ar atmosférico é uma substância pura. (02) A água é uma substância simples. (04) O sangue é uma mistura. (08) Uma solução de açúcar é uma mistura (16) O oxigênio e o ozônio são substâncias distintas, embora constituídas por átomos de um mesmo elemento. (32) A matéria que contém três tipos de moléculas é uma substância composta. (64) A matéria que contém apenas um tipo de molécula é uma substância simples, mesmo que cada molécula seja formada por dois átomos diferentes.

4. Observe os seguintes fatos: I – Uma pedra de naftalina deixada no armário. II – Uma vasilha com água deixada no freezer. III – Uma vasilha com água deixada no fogo. IV – O derretimento de um pedaço de chumbo quando aquecido. Nestes fatos estão relacionados corretamente os seguintes fenômenos: a) I – sublimação, II – solidificação, III – vaporização, IV – fusão. b) I – sublimação, II – solidificação, III – fusão, IV –vaporização. c) I – fusão, II – sublimação, III –vaporização, IV – solidificação. d) I – vaporização, II- solidificação, III – fusão, IV – sublimação. e) I – vaporização, II – sublimação, II –fusão, IV – solidificação.

5. Qual dos fenômenos a seguir não envolve reações químicas? a) Fusão de gelo. b) Digestão de alimentos. c) Combustão. d) Queima de vela. e) Explosão de dinamite.

PROPRIEDADES DA MATÉRIA v PROPRIEDADES GERAIS v PROPRIEDADES FUNCIONAIS v PROPRIEDADES ESPECÍFICAS:

PROPRIEDADES GERAIS v Massa v Volume v Inércia v impenetrabilidade v Dureza As propriedades gerais são comuns a todos os materiais.

PROPRIEDADES FUNCIONAIS v Hidrocarbonetos são inflamáveis. v Os ácidos têm sabor azedo. v Os sais fundidos conduzem corrente elétrica. As propriedades funcionais são aquelas apresentadas por um grupo de substâncias, chamado função química.

PROPRIEDADES ESPECÍFICAS v Ponto de Fusão / Solidificação v Ponto de Ebulição / Liquefação v Densidade ou Massa Específica v Coeficiente de Solubilidade As propriedades específicas caracterizam cada tipo de substância.

Ponto de Fusão / Solidificação v Ponto de Fusão é a temperatura em que uma substância muda do estado sólido para o estado líquido. v. Ponto de Solidificação corresponde ao processo inverso, embora as temperaturas sejam equivalentes. Obs. O PF e o PS são obtidos em uma dada pressão, quando esta não é citada, considera-se a pressão atmosférica

Ponto de Ebulição / Liquefação v Ponto de Ebulição é a temperatura em que uma substância muda do estado líquido para o estado gasoso. v. Ponto de liquefação corresponde ao processo inverso, embora as temperaturas sejam equivalentes. Obs. O PE e o PL são obtidos em uma dada pressão, quando esta não é citada, considera-se a pressão atmosférica
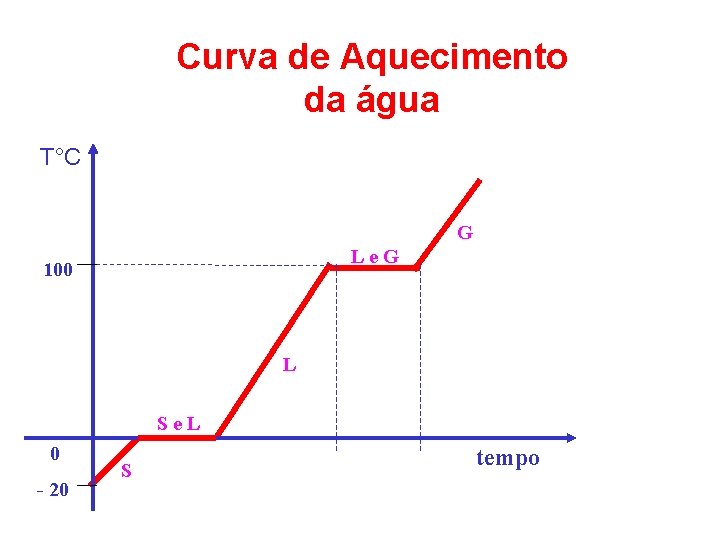
Curva de Aquecimento da água T°C G Le. G 100 L Se. L 0 - 20 S tempo
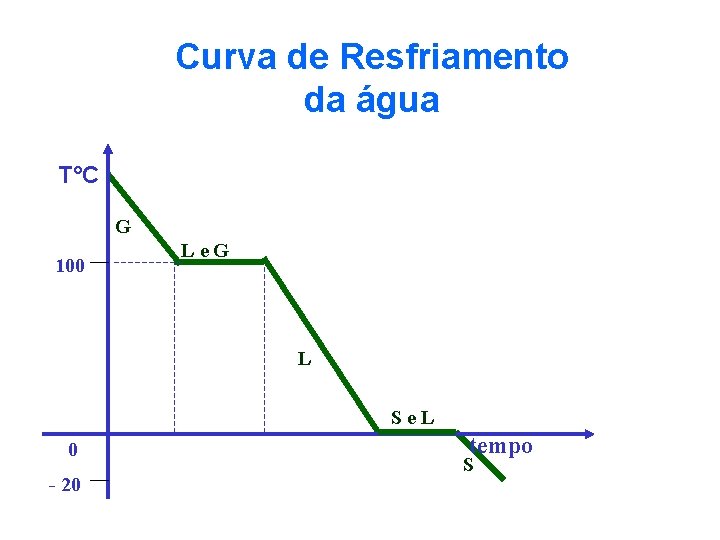
Curva de Resfriamento da água T°C G 100 Le. G L Se. L 0 - 20 tempo S
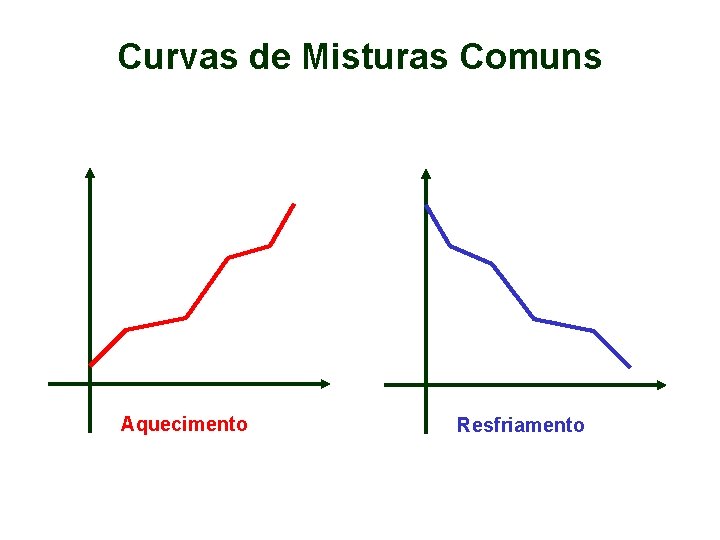
Curvas de Misturas Comuns Aquecimento Resfriamento
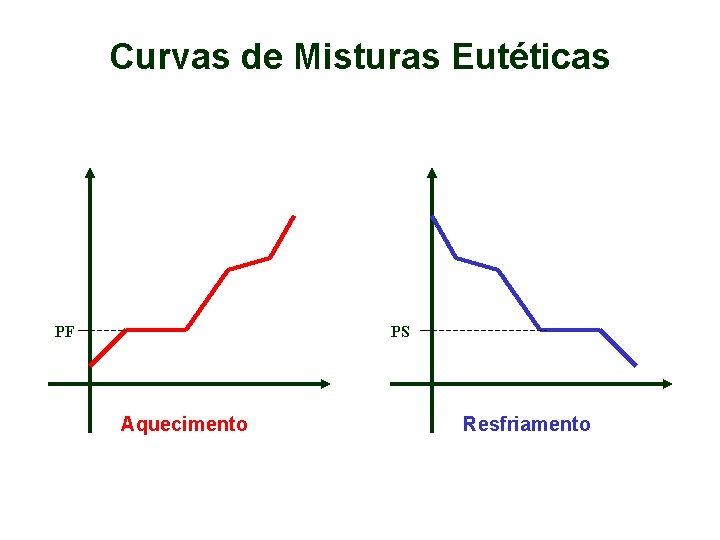
Curvas de Misturas Eutéticas PF PS Aquecimento Resfriamento
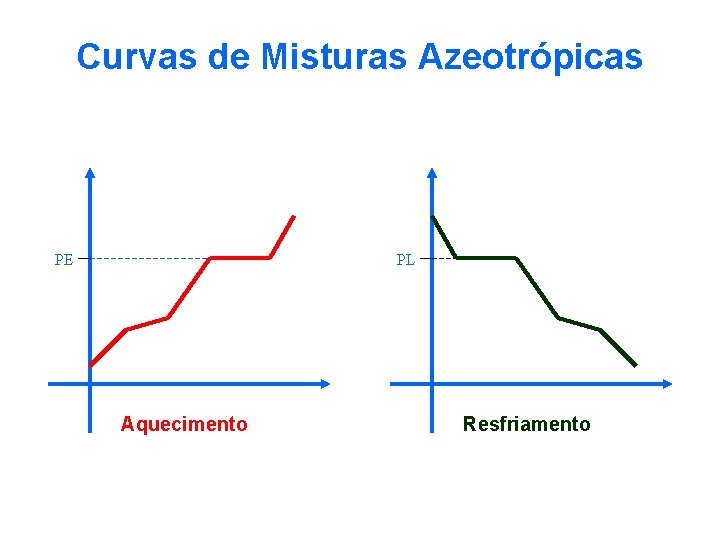
Curvas de Misturas Azeotrópicas PE PL Aquecimento Resfriamento
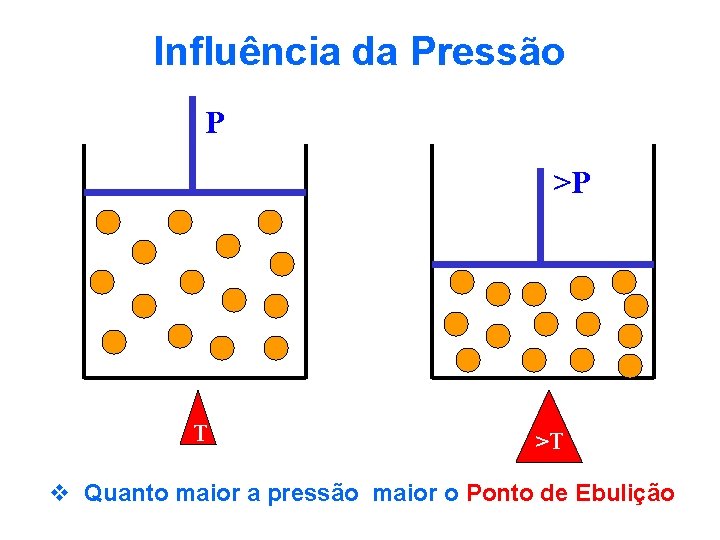
Influência da Pressão P >P T >T v Quanto maior a pressão maior o Ponto de Ebulição
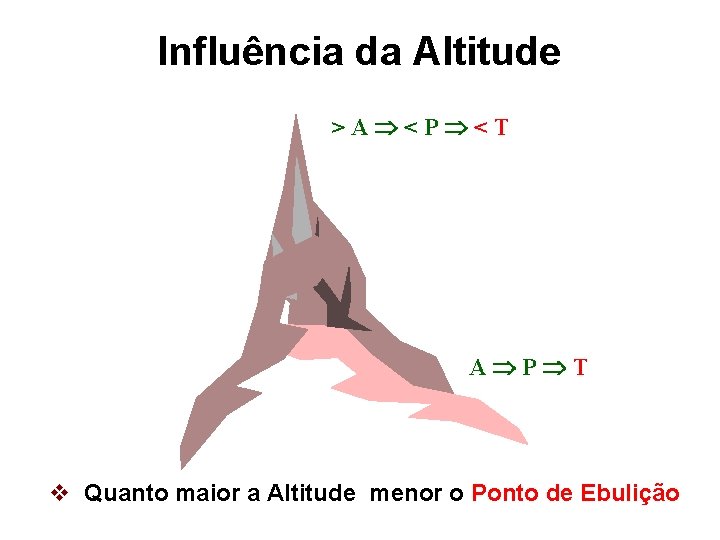
Influência da Altitude >A <P <T A P T v Quanto maior a Altitude menor o Ponto de Ebulição

Densidade v Densidade é a relação da massa pelo volume de uma substância a uma dada Temperatura e Pressão: d=m/V
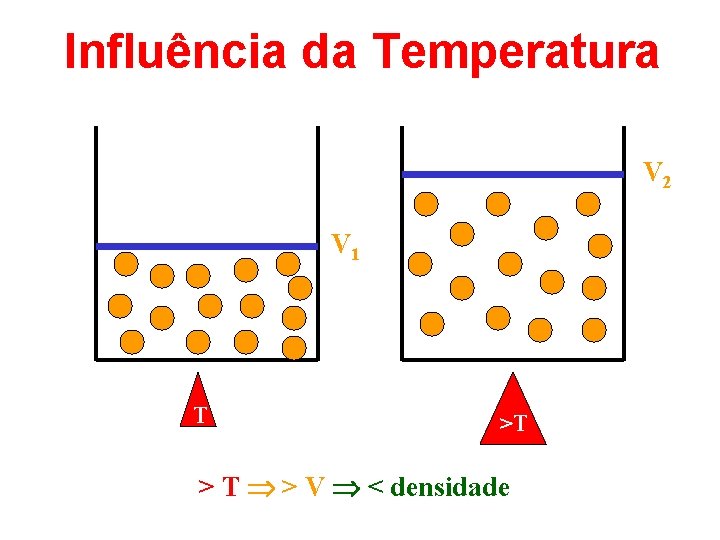
Influência da Temperatura V 2 V 1 T >T > T > V < densidade
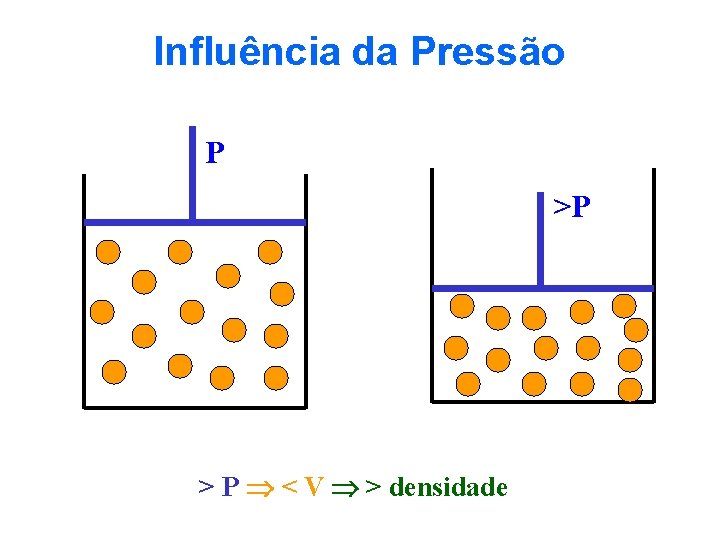
Influência da Pressão P >P > P < V > densidade
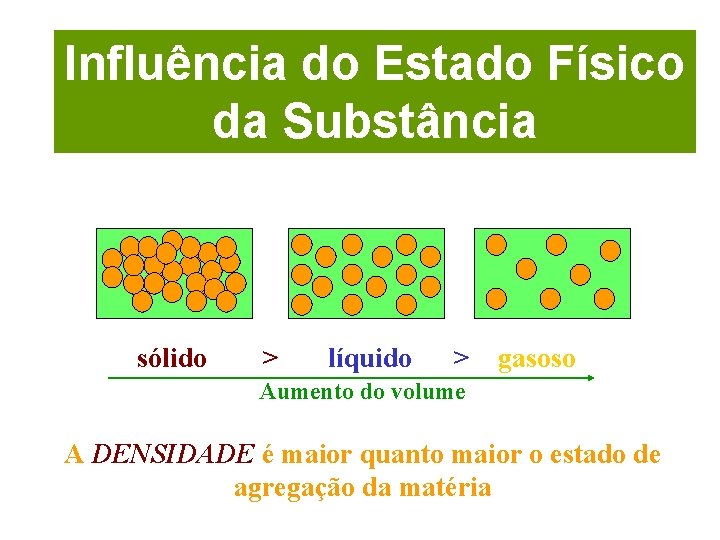
Influência do Estado Físico da Substância sólido > líquido > gasoso Aumento do volume A DENSIDADE é maior quanto maior o estado de agregação da matéria

Exceções a Regra • Água líquida é mais densa que o gelo. • Prata, Ferro e Bismuto, todos diminuem de volume quando fundidos, portanto fase líquida mais densa.
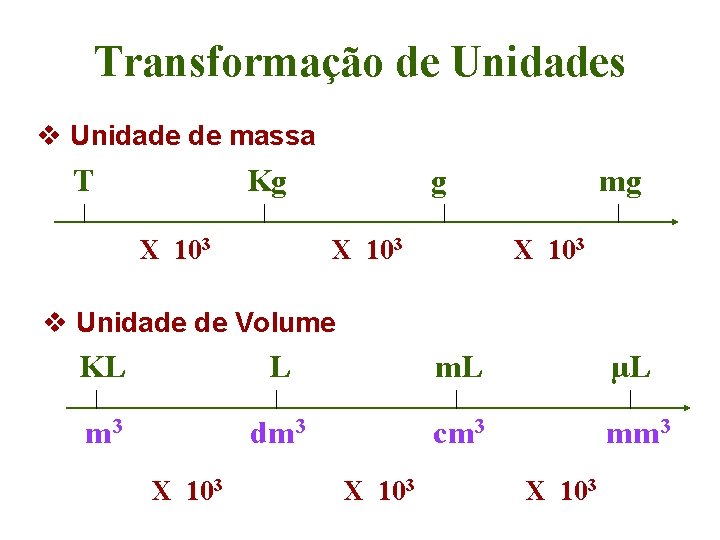
Transformação de Unidades v Unidade de massa T Kg X 103 mg X 103 v Unidade de Volume KL L m. L µL m 3 dm 3 cm 3 mm 3 X 103

Exercícios de fixação: 1) Dada a tabela: PF PE – 63°C 61°C Fenol 43°C 182°C Cloro – 101°C Clorofórmio – 34, 5°C Determine o estado físico de cada substância nas condições ambientes ( 25°C e 1 atm). Clorofórmio Fenol Cloro
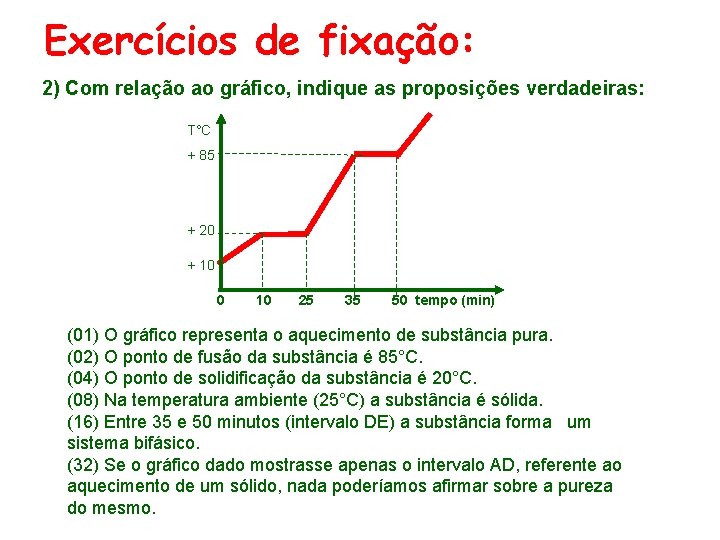
Exercícios de fixação: 2) Com relação ao gráfico, indique as proposições verdadeiras: T°C + 85 + 20 + 10 0 10 25 35 50 tempo (min) (01) O gráfico representa o aquecimento de substância pura. (02) O ponto de fusão da substância é 85°C. (04) O ponto de solidificação da substância é 20°C. (08) Na temperatura ambiente (25°C) a substância é sólida. (16) Entre 35 e 50 minutos (intervalo DE) a substância forma um sistema bifásico. (32) Se o gráfico dado mostrasse apenas o intervalo AD, referente ao aquecimento de um sólido, nada poderíamos afirmar sobre a pureza do mesmo.

Exercícios de fixação: 3) O gráfico está representando a ebulição de duas amostras, iguais ou diferentes, em experiências distintas realizadas cada uma a pressão constante. As quais foram realizadas em sistemas abertos. T°C T 1 B A T 2 tempo (min) (01) Se a amostra A e B forem idênticas, então a pressão é diferente para cada experiência. (02) Se a pressão é a mesma, então A e B poderão ser amostras idênticas em quantidades diferentes. (04) A e B são substâncias puras. (08) A e B podem ser misturas. (16) Se A e B são amostras idênticas, A foi realizada numa pressão maior que B. (32) Se A e B são amostras idênticas, A foi realizada numa altitude menor que B. (64) B pode ser uma substância pura e A, ser uma mistura azeotrópica.

Exercícios de fixação: 4) Responda a essa questão considerando três frascos contendo massas iguais de líquidos diferentes, A, B e C, cujos valores de densidade em g/m. L são respectivamente: 0, 8; 1, 0; 1, 2. I A alternativa que indica cada frasco com seu respectivo líquido é: a) I – A, II – B, III – C. II b) I – A, II – C, III – B. c) I – B, II – C, III – A. III d) I – B, II – A, III – C. e) I – C, II – B, III – A.

Exercícios de fixação: 5) (UFMG) As figuras abaixo representam densímetros como os usados em postos de gasolina. O primeiro contém etanol puro (d = 0, 8 g/cm 3). Dos dois restantes, um está cheio de etanol e água e o outro gasolina (d = 0, 7 g/cm 3), não estão necessariamente nessa ordem. Com base nessas informações, pode-se afirmar corretamente que: I II a) A densidade da bola preta é maior que 1 g/cm 3 b) A densidade da bola branca é menor que 0, 8 g/cm 3. c) A mistura no densímetro II, tem densidade menor que 0, 8 g/cm 3. d) A mistura no densímetro III, contém água. III e) As duas bolas apresentam densidade menores que 0, 7 g/cm 3.
Exercícios de fixação: 6) Uma torneira defeituosa goteja a cada 36 segundos. Sabendo-se que cada gota de água pesa 0, 25 g, quanto tempo levará para encher uma lata de 0, 01 m 3 ?

Coeficiente de Solubilidade - CS v Em geral é considerada como sendo a massa em gramas possível de ser solubilizada em 100 g de água, em uma dada Temperatura e pressão. Obs. Quando a temperatura / pressão não são indicadas, considera-se a temperatura de 25°C e pressão de 1 atm.
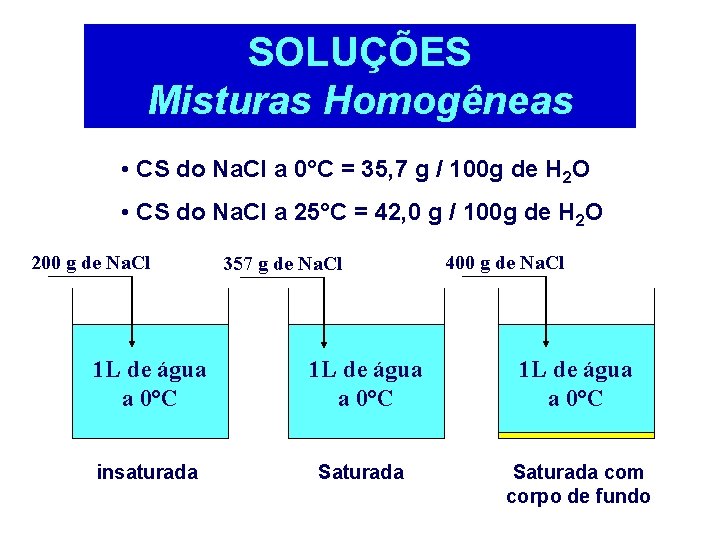
SOLUÇÕES Misturas Homogêneas • CS do Na. Cl a 0°C = 35, 7 g / 100 g de H 2 O • CS do Na. Cl a 25°C = 42, 0 g / 100 g de H 2 O 200 g de Na. Cl 357 g de Na. Cl 400 g de Na. Cl 1 L de água a 0°C insaturada Saturada com corpo de fundo
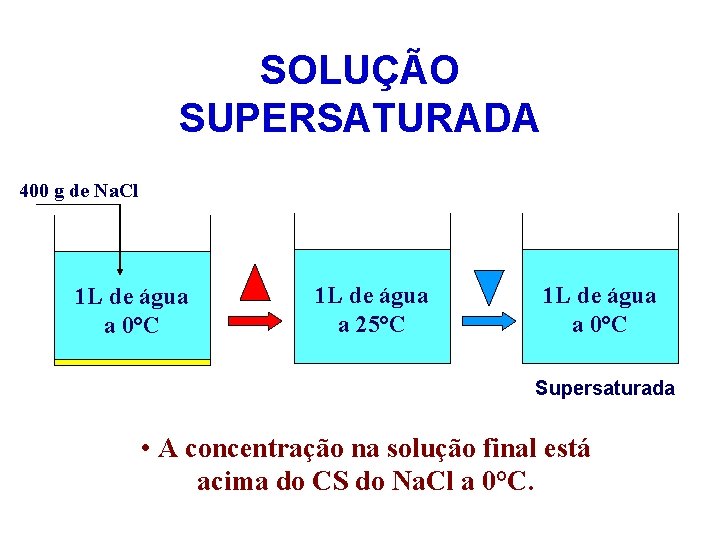
SOLUÇÃO SUPERSATURADA 400 g de Na. Cl 1 L de água a 0°C 1 L de água a 25°C 1 L de água a 0°C Supersaturada • A concentração na solução final está acima do CS do Na. Cl a 0°C.
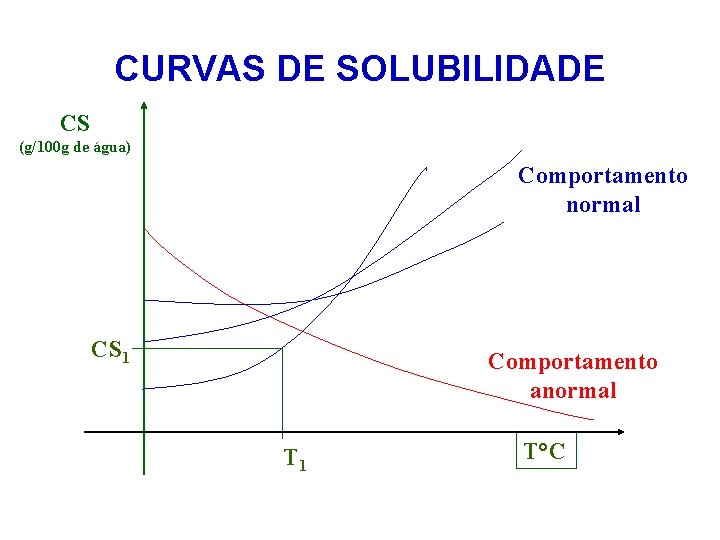
CURVAS DE SOLUBILIDADE CS (g/100 g de água) Comportamento normal CS 1 Comportamento anormal T 1 T°C

Exercícios de fixação: 1) A 18°C a solubilidade de uma substância X é de 60 g/100 m. L de água. Nessa temperatura 150 g de X foram misturados em 200 m. L de água. O sistema obtido é: a) Heterogêneo com uma fase. b) Homogêneo com duas fases. c) Uma solução aquosa com corpo de fundo. d) Heterogêneo com três substâncias. e) Apenas uma solução aquosa.

Exercícios de fixação: 2) 160 g de uma solução saturada de sacarose (C 12 H 22 O 11) a 30°C é resfriada a 0°C. Qual a massa de açúcar cristalizada? Dados: Temperatura °C CS da sacarose (g/ 100 g de água) 0° 30° 180 220
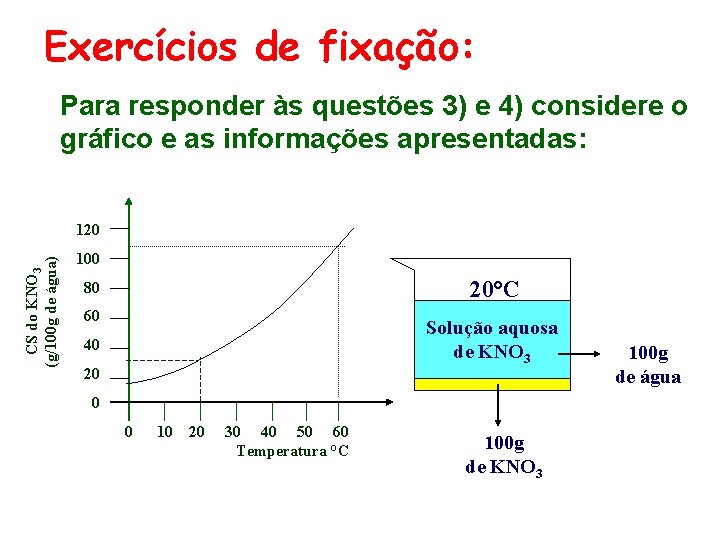
Exercícios de fixação: Para responder às questões 3) e 4) considere o gráfico e as informações apresentadas: CS do KNO 3 (g/100 g de água) 120 100 20°C 80 60 Solução aquosa de KNO 3 40 20 0 0 10 20 30 40 50 60 Temperatura °C 100 g de KNO 3 100 g de água

Exercícios de fixação: 3) Essa mistura heterogênea, inicialmente a 20°C, é aquecida até 60°C. Dessa forma: a) A solução aquosa torna-se insaturada. b) A solução aquosa torna-se saturada e restam 5 g de corpo de fundo. c) A solução aquosa continua saturada, sem corpo de fundo. d) A solução aquosa continua saturada e restam 20 g de corpo de fundo. e) A massa de KNO 3 dissolvida triplica.

Exercícios de fixação: 4) Uma maneira conveniente para se recuperar todo o KNO 3 do sistema e obter o sal sólido e puro é: a) Evaporar toda água, por aquecimento. b) Agitar a mistura e depois filtrá-la. c) Decantar a solução sobrenadante. d) Resfriar a mistura a 0°C. e) Aquecer a mistura a 40°C

ANÁLISE IMEDIATA v Definição: processos de separação de uma mistura nos seus constituintes. v Classificação dos processos: Mecânicos: separações que não envolvem transformações físicas ou químicas. Físicos: processos que envolvem mudanças de estados físicos das substâncias. Normalmente indicados nas separações de misturas homogêneas.

ANÁLISE IMEDIATA v Misturas Heterogêneas: Sólido/sólido Sólido/líquido Sólido/gás Líquido/líquido v Misturas Homogêneas: sólido/sólido/líquido/gás gás/gás

Separação de Misturas Heterogêneas Sistemas Sólido/sólido: v Catação v Peneiração ou Tamisação v Ventilação v Levigação v Separação Magnética v Dissolução Fracionada v Flotação v Fusão Fracionada

Separação de Misturas Heterogêneas Sistemas Sólido/líquido: Sistemas Líquido/líquido: v Filtração v Decantação v Centrifugação v Cristalização Fracionada Sistemas Sólido/gás: v Filtração v Decantação v Câmara de Poeira
Separação de Misturas Homogêneas Sistemas Sólido/sólido: Sistemas gás/gás: v Fusão Fracionada v. Liquefação Fracionada Sistemas Sólido/líquido: v Evaporação v Destilação Simples Sistemas Líquido/líquido: v Destilação Fracionada Sistemas Líquido/gás: v Aquecimento v Despressurização

Materiais comuns de Laboratório v Tubo de Ensaio v Funil de Büchner v Béquer v Kitassato v Erlenmeyer v Proveta v Balão de Fundo Chato v Pipeta Volumétrica v Balão Volumétrico v Pipeta Graduada v Balão de Destilação v Condensador v Funil de Decantação v Funil de Filtração v Funil Liso

Materiais comuns de Laboratório v Bureta v Garras v Dessecador v Tripé de Ferro v Vidro de Relógio v Tela de Amianto v Almofariz e Pistilo v Bastão de Vidro v Cápsula de Evaporação v Frasco de Reagente v Cadinho de Porcelana v Cadinho de Platina v Piscete v Espátula v Suporte de Ferro
- Slides: 61