CURSO DE QUMICA BSICA Prof Joo Miranda QUMICA

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

QUÍMICA BÁSICA Prof. : João Valdir Miranda

QUÍMICA BÁSICA AULA 1 Conceitos; Representações; Atomicidade; Alotropia; Sistemas puros e misturas; Fenômenos Químicos e Físicos; Mudanças de Estado Físico; Densidade; AULA 2 AULA 3 Estrutura Atômica Octeto; Ligações Químicas Isotopia; Isobaria; Isotonia; CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Tabela Periódica; Mol; Massa Atômica; Massa Molecular;

Aula 1 – CONCEITOS E REPRESENTAÇÕES QUÍMICAS Conceito de Química: Matéria: Ciência que estuda materiais, as transformações que eles podem sofrer e a energia envolvida nessas transformações. É tudo que ocupa lugar no espaço e tem massa. Elemento Químico: É um conjunto de átomos de mesmo número atômico (Z), ou número de prótons. Z = número atômico A = Massa atômica N = número de nêutrons CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
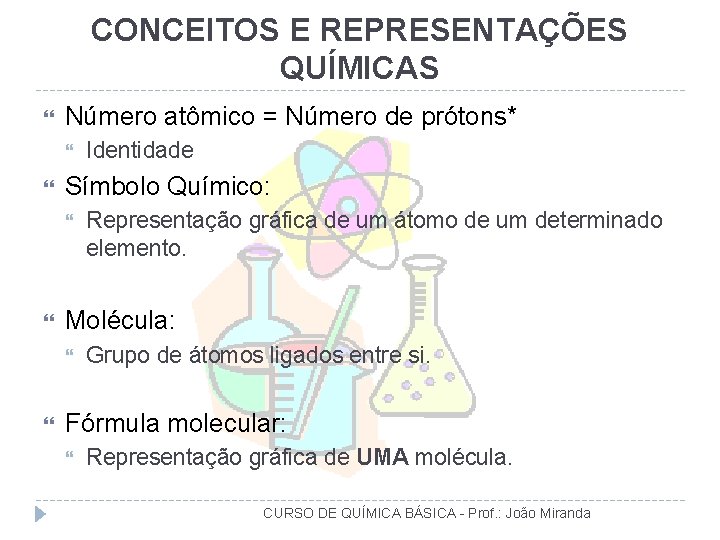
CONCEITOS E REPRESENTAÇÕES QUÍMICAS Número atômico = Número de prótons* Símbolo Químico: Representação gráfica de um átomo de um determinado elemento. Molécula: Identidade Grupo de átomos ligados entre si. Fórmula molecular: Representação gráfica de UMA molécula. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

CONCEITOS E REPRESENTAÇÕES QUÍMICAS Substância Pura: Substância Simples: Moléculas formadas por átomos de um mesmo elemento químico. Substância Composta ou Composto Químico: Conjunto de moléculas iguais. Moléculas formadas por átomos de elementos diferentes. Mistura: Conjunto de moléculas diferentes. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
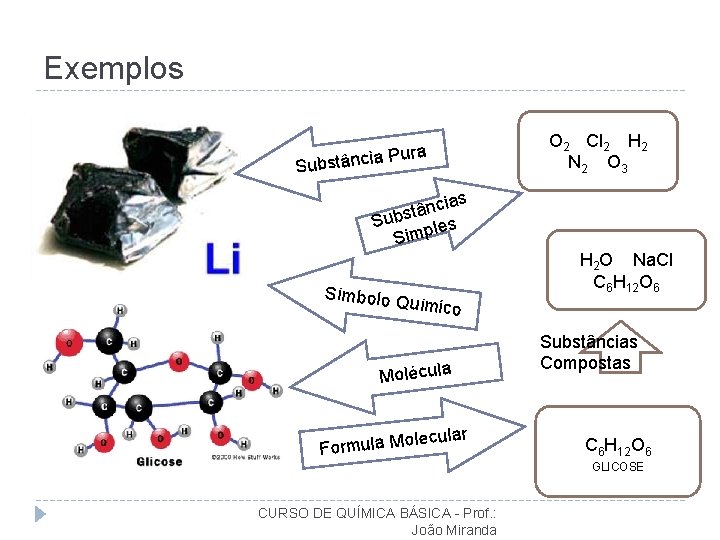
Exemplos O 2 Cl 2 H 2 N 2 O 3 a ância Pur Subst ias c n â t Subs ples Sim Símbolo Q uímico Molécula lar lecu Formula Mo H 2 O Na. Cl C 6 H 12 O 6 Substâncias Compostas C 6 H 12 O 6 GLICOSE CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
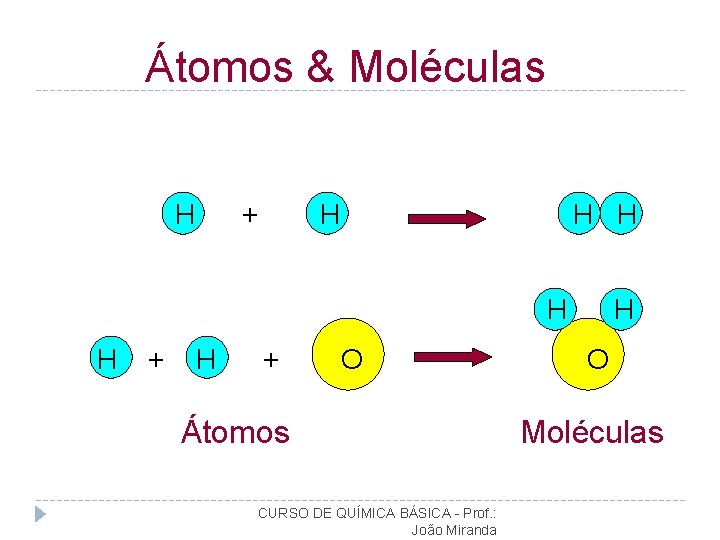
Átomos & Moléculas H + H H H + O Átomos CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda H O Moléculas
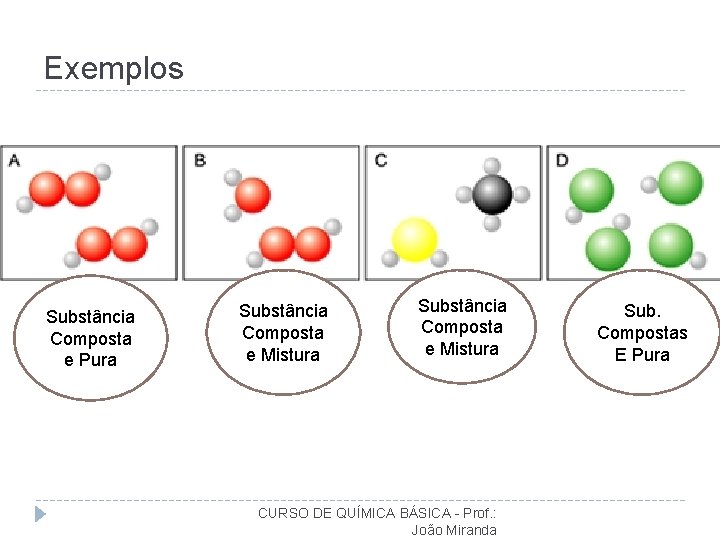
Exemplos Substância Composta e Pura Substância Composta e Mistura CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Sub. Compostas E Pura
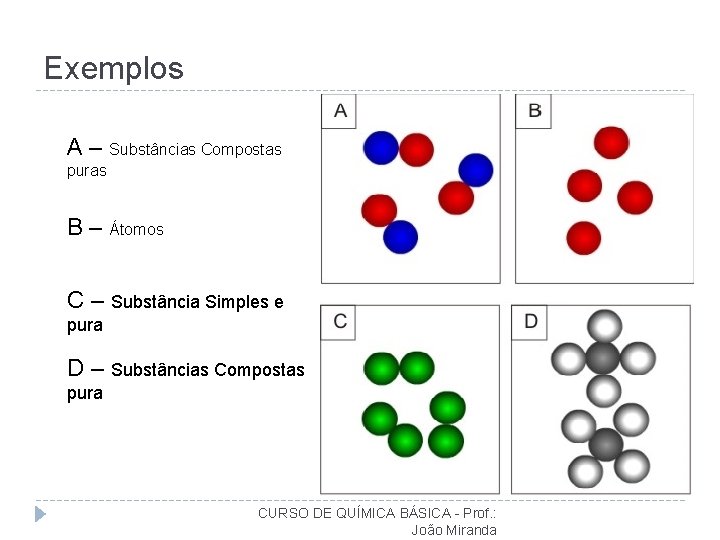
Exemplos A – Substâncias Compostas puras B – Átomos C – Substância Simples e pura D – Substâncias Compostas pura CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
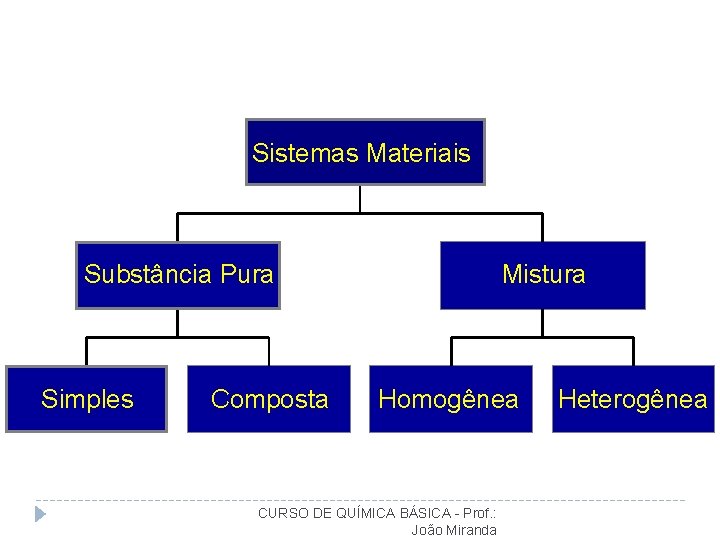
Sistemas Materiais Substância Pura Simples Composta Mistura Homogênea CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Heterogênea
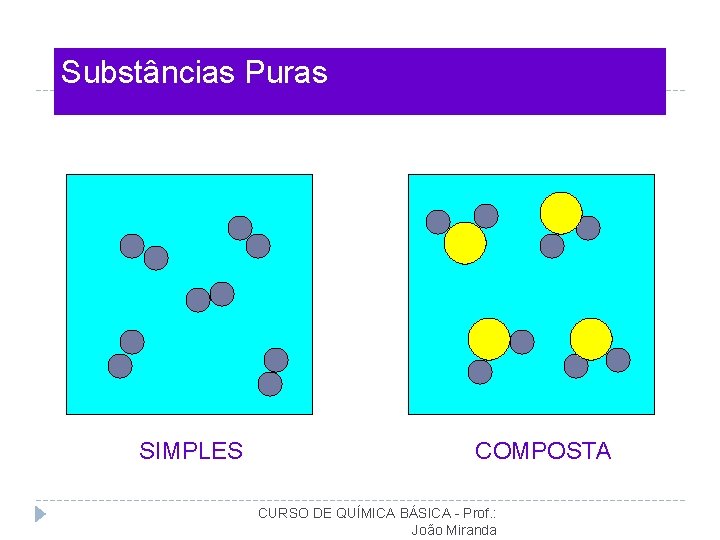
Substâncias Puras SIMPLES COMPOSTA CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
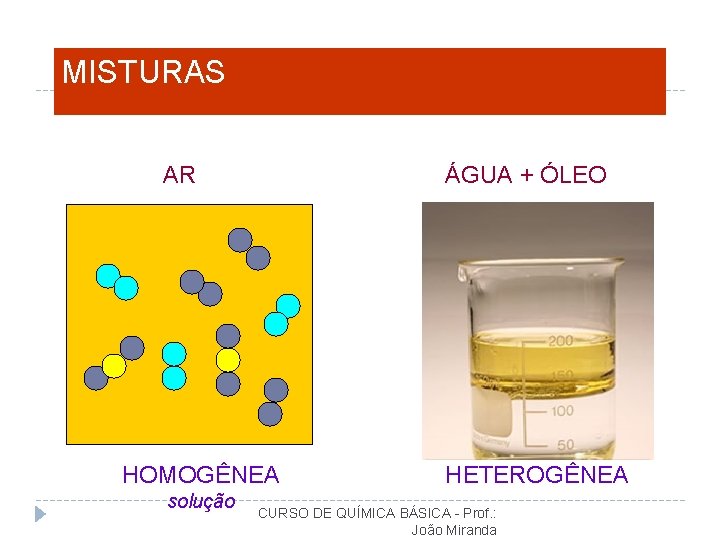
MISTURAS AR ÁGUA + ÓLEO HOMOGÊNEA solução HETEROGÊNEA CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
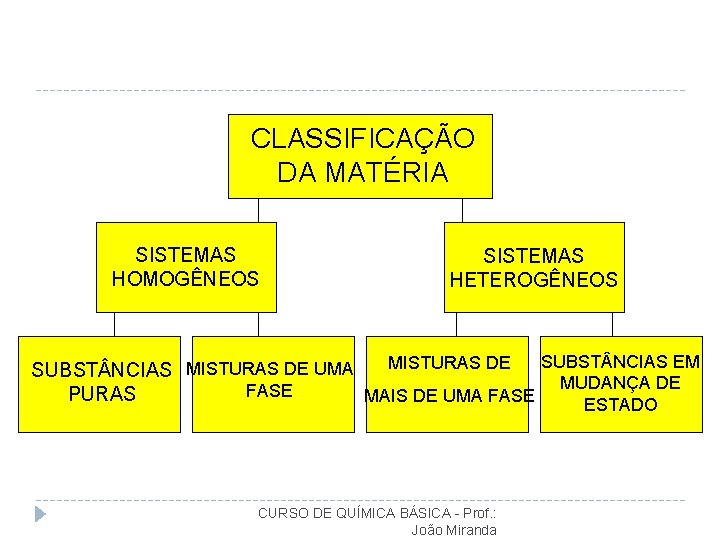
CLASSIFICAÇÃO DA MATÉRIA SISTEMAS HOMOGÊNEOS SISTEMAS HETEROGÊNEOS SUBST NCIAS EM MISTURAS DE SUBST NCIAS MISTURAS DE UMA MUDANÇA DE FASE PURAS MAIS DE UMA FASE ESTADO CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

ATOMICIDADE Atomicidade Substâncias Monoatômica He, Ne, Ar, Kr Diatômica H 2, N 2, HCl, CO Tetratômica P 4 (fósforo branco) Indeterminada P(verm), C(graf), metais v Atomicidade se refere ao número de átomos que compõem uma substância CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
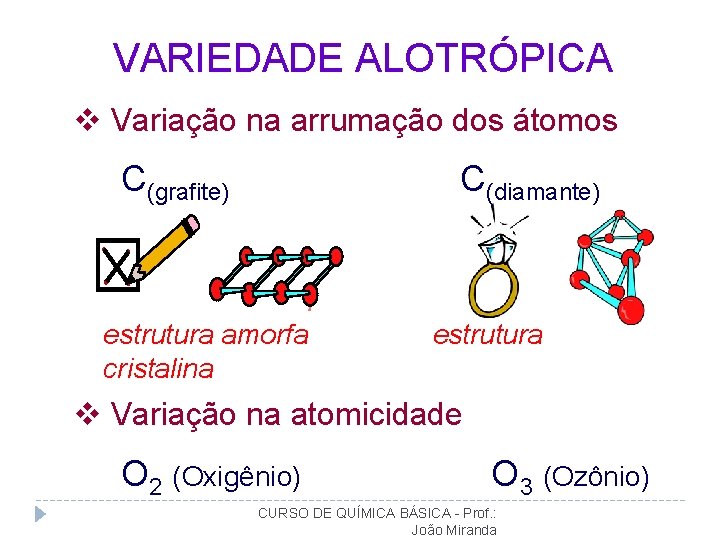
VARIEDADE ALOTRÓPICA v Variação na arrumação dos átomos C(grafite) C(diamante) estrutura amorfa cristalina estrutura v Variação na atomicidade O 2 (Oxigênio) O 3 (Ozônio) CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
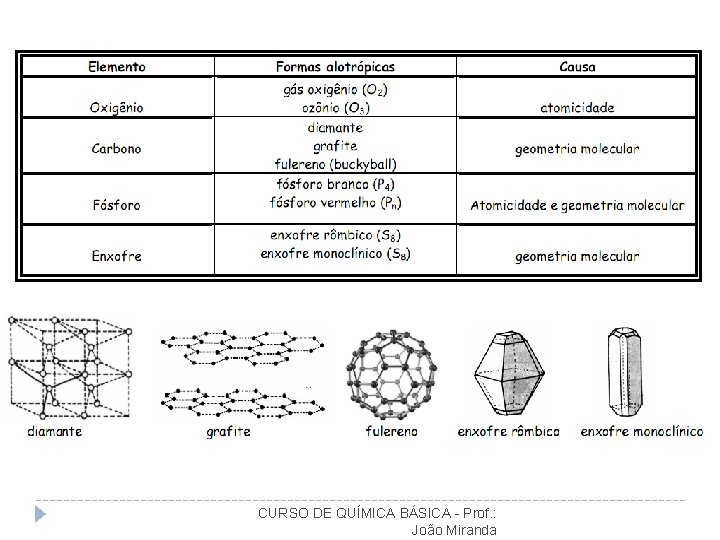
CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

FENÔMENO QUÍMICO Combustão do álcool etílico H 3 C- CH 2 - OH + 3 O 2 2 CO 2 + 3 H 2 O Reagentes Produtos v O fenômeno químico transforma a natureza íntima da matéria. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
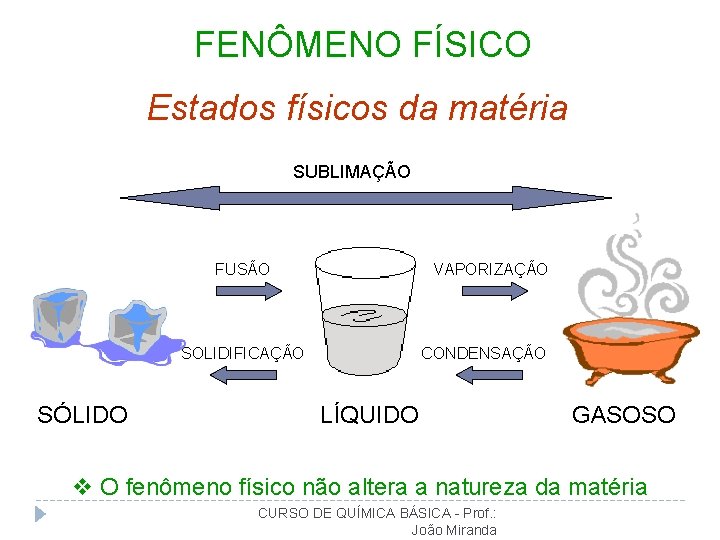
FENÔMENO FÍSICO Estados físicos da matéria SUBLIMAÇÃO FUSÃO VAPORIZAÇÃO SOLIDIFICAÇÃO SÓLIDO CONDENSAÇÃO LÍQUIDO GASOSO v O fenômeno físico não altera a natureza da matéria CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
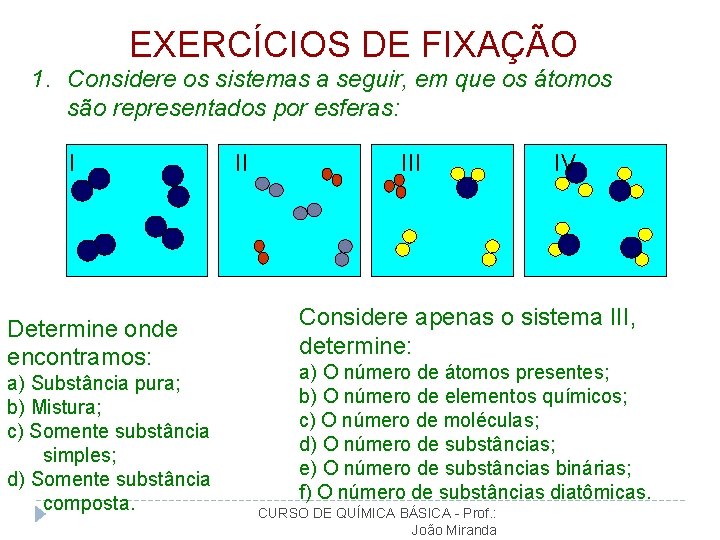
EXERCÍCIOS DE FIXAÇÃO 1. Considere os sistemas a seguir, em que os átomos são representados por esferas: I Determine onde encontramos: a) Substância pura; b) Mistura; c) Somente substância simples; d) Somente substância composta. II IV Considere apenas o sistema III, determine: a) O número de átomos presentes; b) O número de elementos químicos; c) O número de moléculas; d) O número de substâncias; e) O número de substâncias binárias; f) O número de substâncias diatômicas. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

2. Considere o sistema representado abaixo. Pode-se descrever o sistema em questão como constituido por: a) Três fases e um componente. b) Duas fases e dois componentes. c) Três fases e dois componentes. d) Três fases e três CURSO DE QUÍMICA BÁSICA - Prof. : componentes. João Miranda

3. Os diferentes tipos de matéria podem ser classificados em dois grupos: Substâncias puras e misturas. As substâncias puras podem ser simples e compostas. Considerando esse modo de classificação, pode-se afirmar: (01) O ar atmosférico é uma substância pura. (02) A água é uma substância simples. (04) O sangue é uma mistura. (08) Uma solução de açúcar é uma mistura (16) O oxigênio e o ozônio são substâncias distintas, embora constituídas por átomos de um mesmo elemento. (32) A matéria que contém três tipos de moléculas é uma substância composta. (64) A matéria que contém apenas um tipo de molécula é uma substância simples, mesmo que cada molécula seja formada por dois átomos diferentes. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

4. Observe os seguintes fatos: I – Uma pedra de naftalina deixada no armário. II – Uma vasilha com água deixada no freezer. III – Uma vasilha com água deixada no fogo. IV – O derretimento de um pedaço de chumbo quando aquecido. Nestes fatos estão relacionados corretamente os fenômenos: a)seguintes I – sublimação, II – solidificação, III – vaporização, IV – X fusão. b) I – sublimação, II – solidificação, III – fusão, IV – vaporização. c) I – fusão, II – sublimação, III –vaporização, IV – solidificação. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

5. Qual dos fenômenos a seguir não envolve reações químicas? a) Fusão de gelo. b) Digestão de alimentos. c) Combustão. d) Queima de vela. e) Explosão de dinamite. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
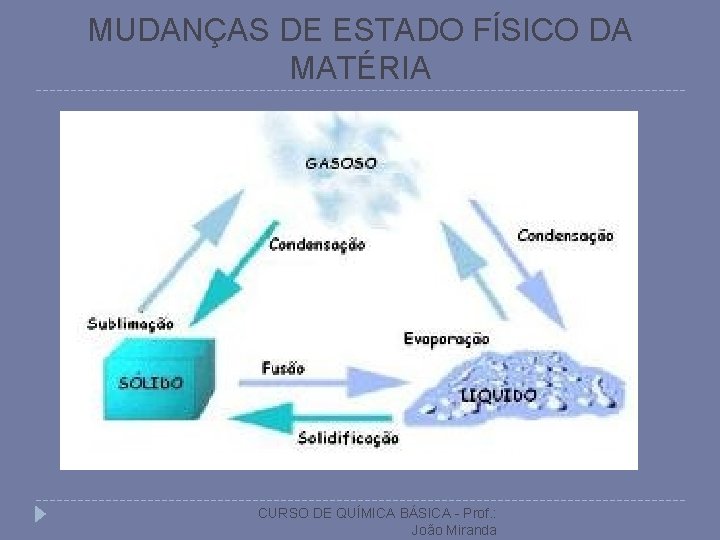
MUDANÇAS DE ESTADO FÍSICO DA MATÉRIA CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
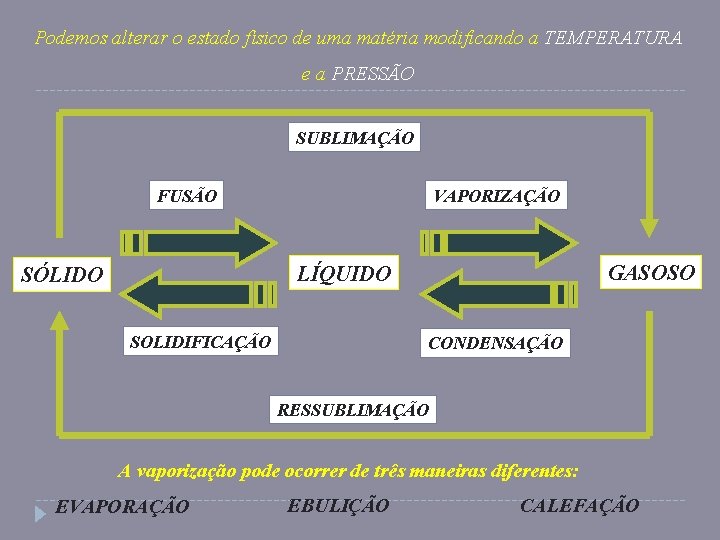
Podemos alterar o estado físico de uma matéria modificando a TEMPERATURA e a PRESSÃO SUBLIMAÇÃO FUSÃO VAPORIZAÇÃO GASOSO LÍQUIDO SÓLIDO SOLIDIFICAÇÃO CONDENSAÇÃO RESSUBLIMAÇÃO A vaporização pode ocorrer de três maneiras diferentes: EVAPORAÇÃO EBULIÇÃO CALEFAÇÃO
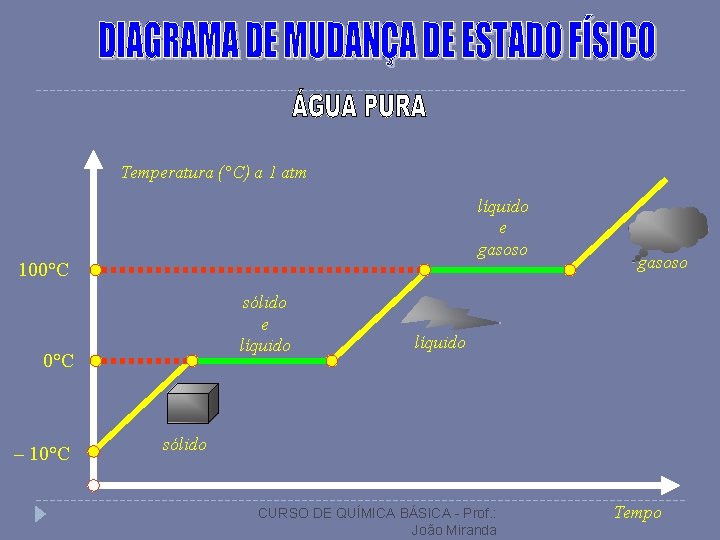
Temperatura (°C) a 1 atm líquido e gasoso 100°C sólido e líquido 0°C – 10°C gasoso líquido sólido CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Tempo
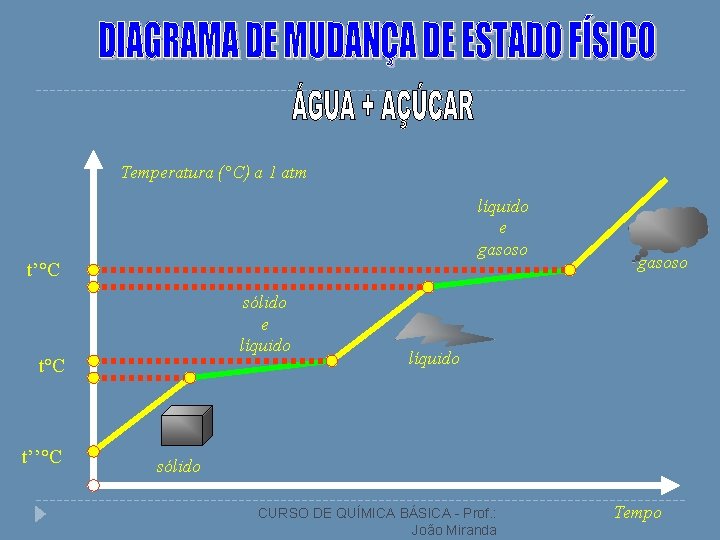
Temperatura (°C) a 1 atm líquido e gasoso t’°C sólido e líquido t°C t’’°C gasoso líquido sólido CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Tempo
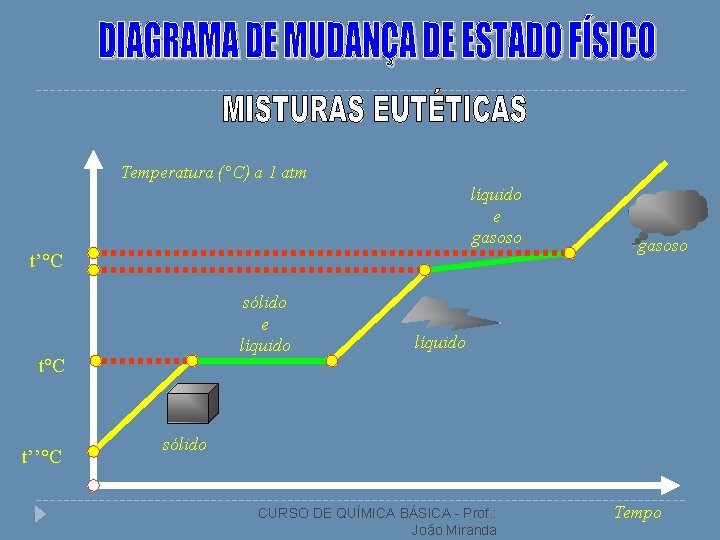
Temperatura (°C) a 1 atm líquido e gasoso t’°C sólido e líquido t°C t’’°C gasoso líquido sólido CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Tempo
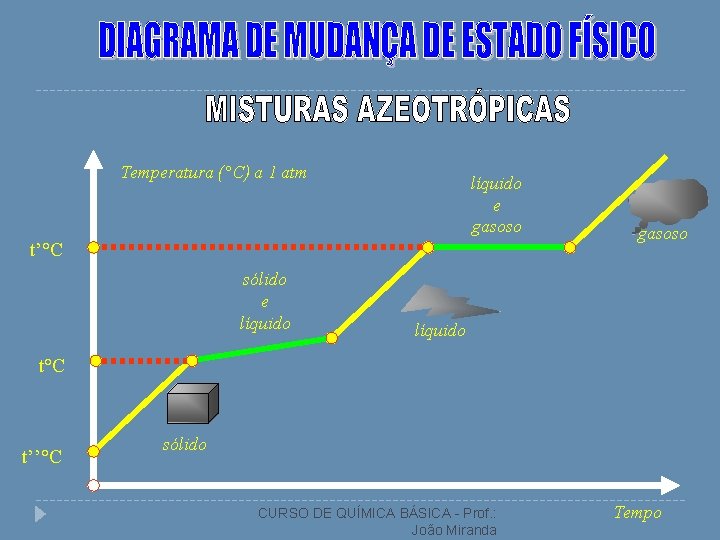
Temperatura (°C) a 1 atm líquido e gasoso t’°C sólido e líquido gasoso líquido t°C t’’°C sólido CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda Tempo

Densidade (massa específica) CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

Exemplo Se um corpo tem a massa de 20 g em um volume de 5 cm 3 , qual é a sua densidade ? Dados: m = 20 g V = 5 cm 3 = 5 m. L Logo: CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

A densidade do selênio é 4, 79 g/cm 3. Qual a massa, em kg, de 6, 5 cm 3 de selênio? Dados: d = 4, 79 g/cm 3 V = 6, 5 cm 3 logo: 4, 79. 6, 5 Então: CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
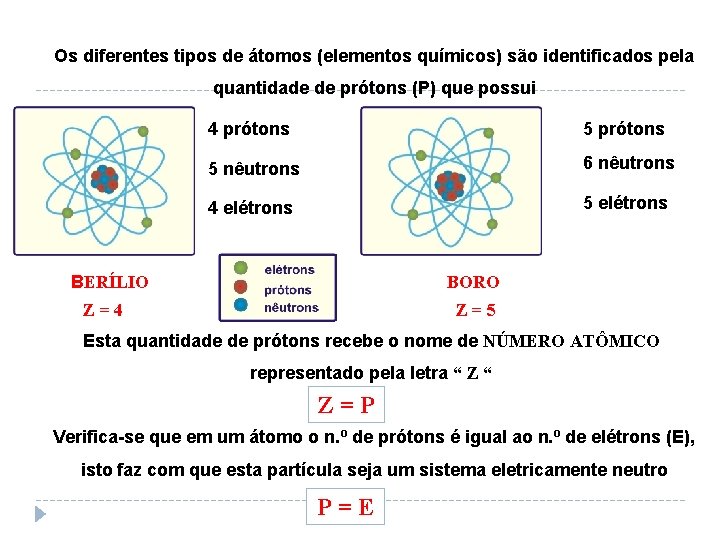
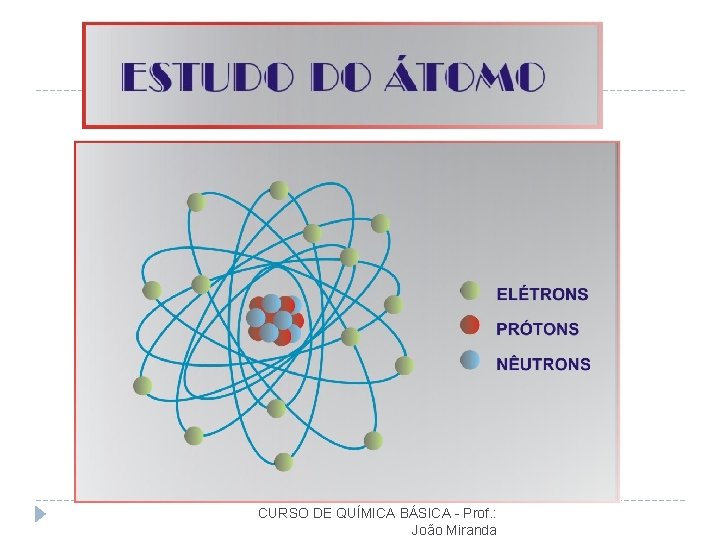
IDENTIFICANDO O ÁTOMO Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui 4 prótons 5 nêutrons 6 nêutrons 4 elétrons 5 elétrons BERÍLIO BORO Z=4 Z=5 Esta quantidade de prótons recebe o nome de NÚMERO ATÔMICO representado pela letra “ Z=P Verifica-se que em um átomo o n. º de prótons é igual ao n. º de elétrons (E), isto faz com que esta partícula seja um sistema eletricamente neutro P=E
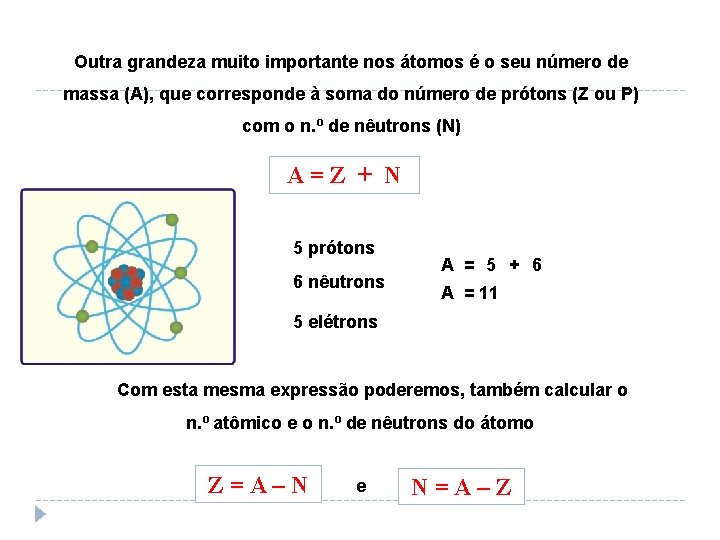
NÚMERO DE MASSA (A) Outra grandeza muito importante nos átomos é o seu número de massa (A), que corresponde à soma do número de prótons (Z ou P) com o n. º de nêutrons (N) A=Z + N 5 prótons 6 nêutrons A = 5 + 6 A = 11 5 elétrons Com esta mesma expressão poderemos, também calcular o n. º atômico e o n. º de nêutrons do átomo Z=A–N e N=A–Z

01) Isótopos radiativos são empregados no diagnóstico e tratamento de inúmeras doenças. Qual é a principal propriedade que caracteriza um elemento químico? a) número de massa b) número de prótons c) número de nêutrons d) energia de ionização e) diferença entre o número de prótons e de nêutrons

02) Um átomo que é constituído por 17 prótons, 18 nêutrons e 17 elétrons tem, respectivamente, número atômico e número de massa iguais a: a) 17 e 17. P = 17 Z = 17 P b) 17 e 18. N = 18 A = 17 Z + 18 N c) 18 e 17. E = 17 A = 35 d) 17 e 35. e) 35 e 17. 17 e 35

03) Um átomo de certo elemento químico tem número de massa igual a 144 e número atômico 70. Podemos afirmar que o número de nêutrons que no seu núcleo encontraremos é: a) 70. b) 74. c) 144. d) 210. e) 284.
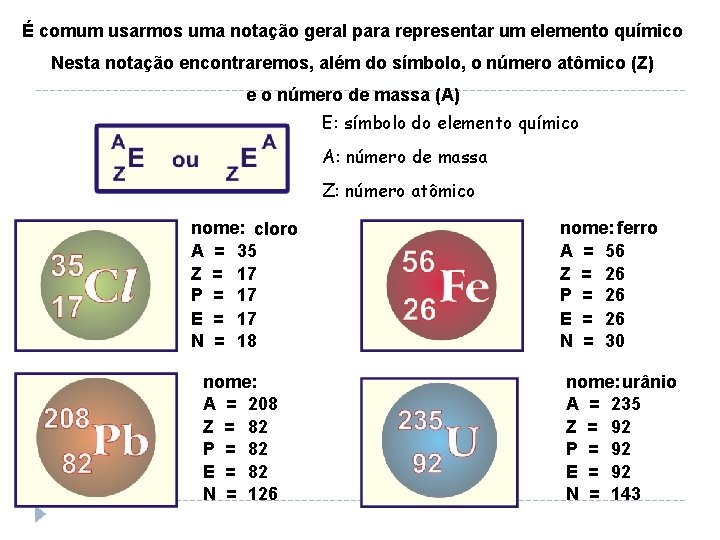
É comum usarmos uma notação geral para representar um elemento químico Nesta notação encontraremos, além do símbolo, o número atômico (Z) e o número de massa (A) E: símbolo do elemento químico A: número de massa Z: número atômico nome: cloro A = 35 Z = 17 P = 17 E = 17 N = 18 nome: chumbo A = 208 Z = 82 P = 82 E = 82 N = 126 nome: ferro A = 56 Z = 26 P = 26 E = 26 N = 30 nome: urânio A = 235 Z = 92 P = 92 E = 92 N = 143

04) Os números atômicos e de massa dos átomos A e B são dados em função de “x”. 8 x 5 x + 12 3 x + 4 A 4 x – 1 B Sabendo-se que o número de massa de A é igual ao número de massa de B, podemos concluir que: a) A e B pertencem ao mesmo elemento químico. b) B possui 16 nêutrons. c) o número atômico de A é 15. d) o número de nêutrons é igual ao número de prótons para o átomo A. e) o número de massa de B é 33.

Um átomo pode PERDER ou GANHAR ELÉTRONS para se tornar estável (detalhes em ligações químicas), nestes casos, será obtida uma estrutura com carga elétrica chamada ÍON

Quando o átomo PERDE elétrons o íon terá CARGA POSITIVA e será chamado de CÁTION 56 26 Fe 3+ O átomo de ferro PERDEU 3 ELÉTRONS para produzi-lo

Quando o átomo GANHA elétrons o íon terá CARGA NEGATIVA e será chamado de NION 16 8 O 2– O átomo de oxigênio GANHOU 2 ELÉTRONS para produzi-lo

05) Os íon representados a seguir apresentam o mesmo(a): a) massa. b) raio atômico. c) carga nuclear. d) número de elétrons. e) energia de ionização.

06) As afirmações referem-se ao número de partículas constituintes de espécies atômicas: 01) Dois átomos neutros com o mesmo número atômico têm o mesmo número de elétrons 02) Um ânion bivalente com 52 elétrons e número de massa 116 tem 64 nêutrons 04) Um átomo neutro com 31 elétrons tem número atômico igual a 31 08) Um átomo, neutro, ao perder três elétrons, mantém inalterado seu número atômico 16) Um cátion trivalente com 47 elétrons e 62 nêutrons tem número de massa igual a 112

Comparando-se dois ou mais átomos, podemos observar algumas semelhanças entre eles A depender da semelhança, teremos para esta relação uma denominação especial
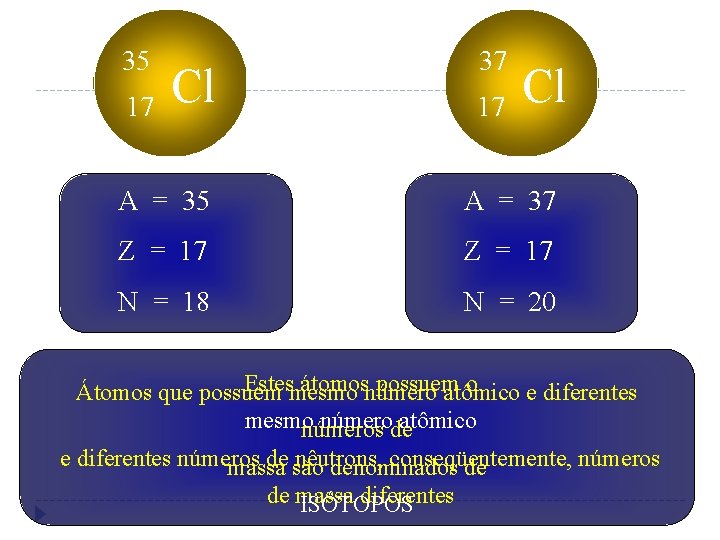
35 17 37 Cl 17 Cl A = 35 A = 37 Z = 17 N = 18 N = 20 Estesmesmo átomosnúmero possuem o Átomos que possuem atômico e diferentes mesmo númerode atômico números e diferentes números de são nêutrons, conseqüentemente, números massa denominados de de massa diferentes ISÓTOPOS
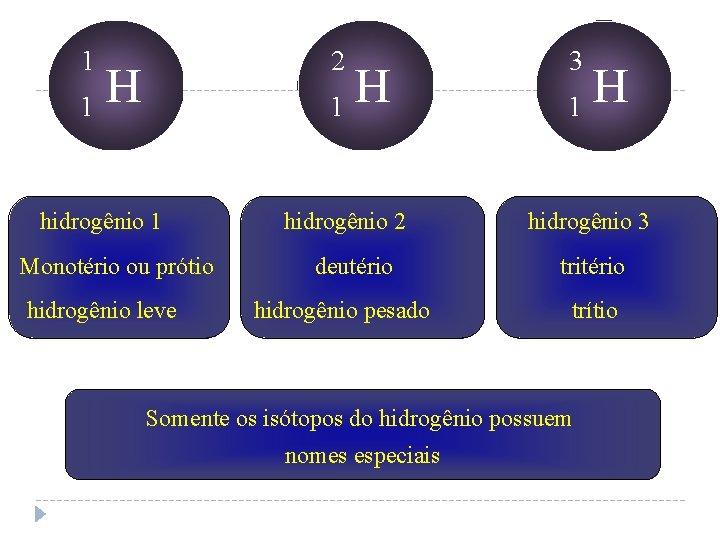
1 1 2 H 1 hidrogênio 1 Monotério ou prótio hidrogênio leve H hidrogênio 2 deutério hidrogênio pesado 3 1 hidrogênio 3 tritério trítio Somente os isótopos do hidrogênio possuem nomes especiais H

Os demais isótopos são identificados pelo nome do elemento químico seguido do seu respectivo número de massa 12 C 6 carbono 12 13 C 6 carbono 13 14 6 C carbono 14
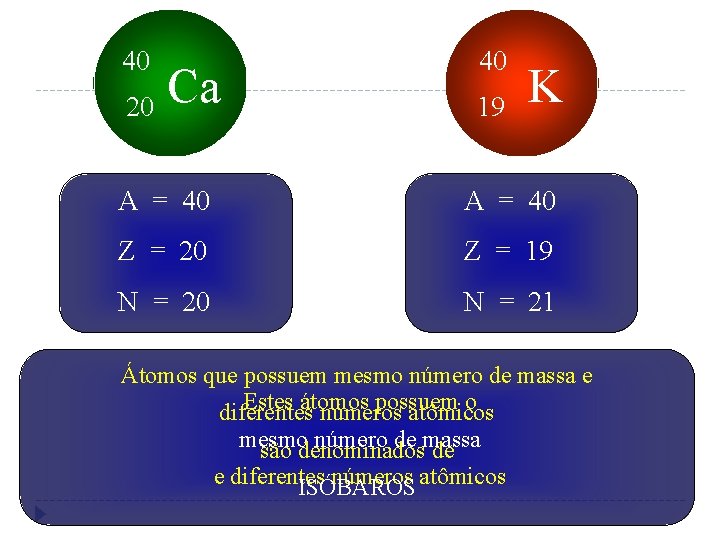
40 20 Ca 40 19 K A = 40 Z = 20 Z = 19 N = 20 N = 21 Átomos que possuem mesmo número de massa e Estes átomos possuem o diferentes números atômicos mesmo número de massa são denominados de e diferentes números atômicos ISÓBAROS
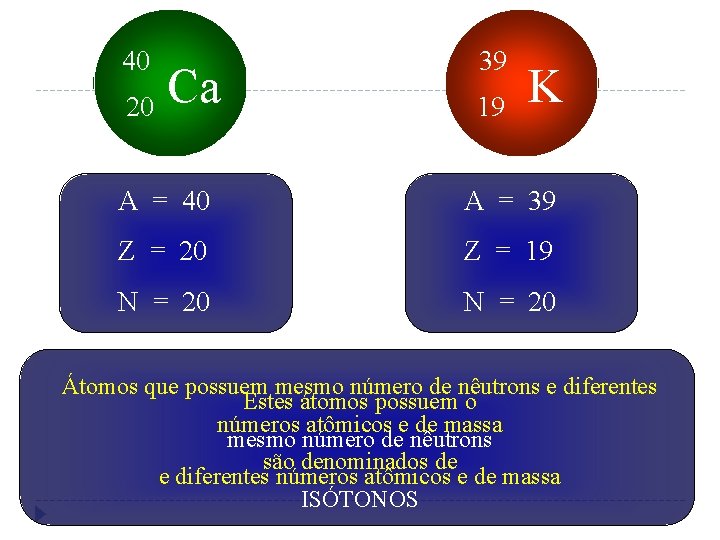
40 20 Ca 39 19 K A = 40 A = 39 Z = 20 Z = 19 N = 20 Átomos que possuem mesmo número de nêutrons e diferentes Estes átomos possuem o números atômicos e de massa mesmo número de nêutrons são denominados de e diferentes números atômicos e de massa ISÓTONOS
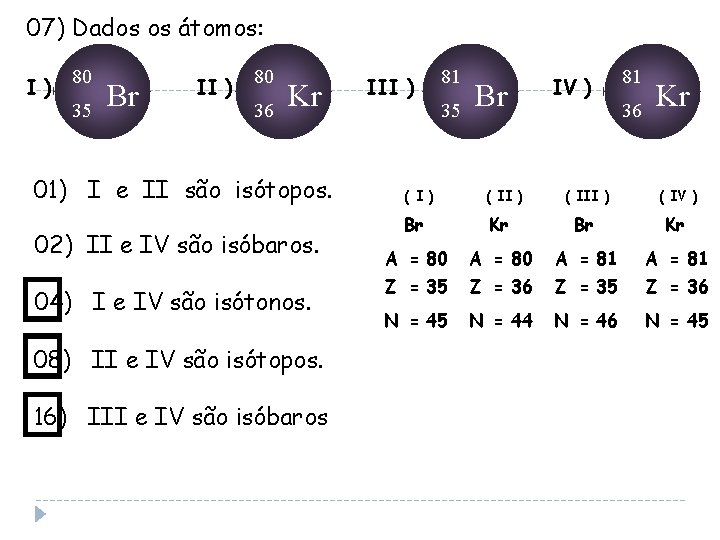
07) Dados os átomos: I ) 80 35 Br II ) 80 36 Kr 01) I e II são isótopos. 02) II e IV são isóbaros. 04) I e IV são isótonos. 08) II e IV são isótopos. 16) III e IV são isóbaros III ) 81 35 Br ( I ) ( II ) Br IV ) 81 36 Kr ( III ) ( IV ) Kr Br Kr A = 80 A = 81 Z = 35 Z = 36 N = 45 N = 44 N = 46 N = 45

08) O elemento químico B possui 20 nêutrons, é isótopo do elemento químico A, que possui 18 prótons, e isóbaro do elemento químico C, que tem 16 nêutrons. Com base nessas informações, pode-se afirmar que os elementos A, B e C apresentam, respectivamente, números atômicos iguais a: a) 16, 16 e 20. b) 16, 18 e 20. c) 16, 20 e 21. d) 18, 16 e 22. e) 18, 18 e 22.

Em torno do núcleo do átomo temos uma região denominada de ELETROSFERA A eletrosfera é dividida em 7 partes chamadas CAMADAS ELETRÔNICAS ou NÍVEIS DE ENERGIA
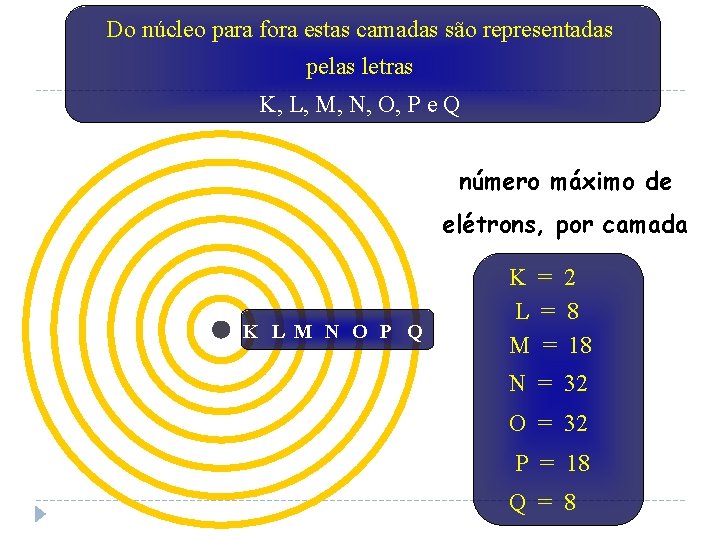
Do núcleo para fora estas camadas são representadas pelas letras K, L, M, N, O, P e Q número máximo de elétrons, por camada K L M N O P Q K = 2 L = 8 M = 18 N = 32 O = 32 P = 18 Q = 8
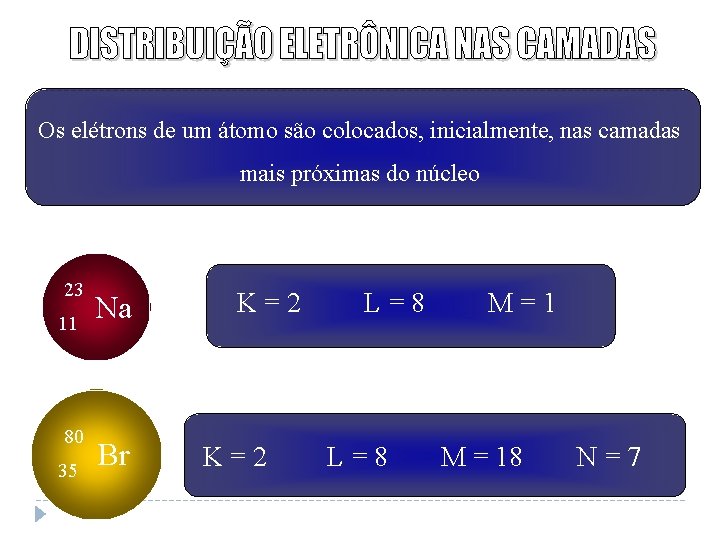
Os elétrons de um átomo são colocados, inicialmente, nas camadas mais próximas do núcleo 23 11 80 35 Na Br K=2 L=8 M=1 M = 18 N=7

Verifica-se que a última camada de um átomo não pode ter mais de 8 elétrons Quando isto ocorrer, devemos colocar na mesma camada, 8 ou 18 elétrons (aquele que for imediatamente inferior ao valor cancelado) e, o restante na camada seguinte 40 20 Ca K=2 L=8 M = 810 N=2

01) Um átomo tem número de massa 31 e 16 nêutrons. Qual o número de elétrons no seu nível mais externo? a) 2. b) 4. A = 31 N = 16 c) 5. Z = 31 – 16 Z = 15 d) 3. e) 8. Z=A–N K = 2 L = 8 M = 5

Pesquisando o átomo, Sommerfeld chegou à conclusão que os elétrons de um mesmo nível não estão igualmente distanciados do núcleo porque as trajetórias, além de circulares, como propunha Bohr, também podem ser elípticas Esses subgrupos de elétrons estão em regiões chamadas de subníveis e podem ser de até 4 tipos s p d f

subnível “ s “, que contém até 2 elétrons subnível “ p “, que contém até 6 elétrons subnível “ d “, que contém até 10 elétrons subnível “ f “, que contém até 14 elétrons Os subníveis em cada nível são: K 1 s 2 L 2 s 2 2 p 6 M 3 s 2 3 p 6 3 d 10 N 4 s 2 4 p 6 4 d 10 4 f 14 O 5 s 2 5 p 6 5 d 10 5 f 14 P 6 s 2 6 p 6 6 d 10 Q 7 s 2 7 p 6
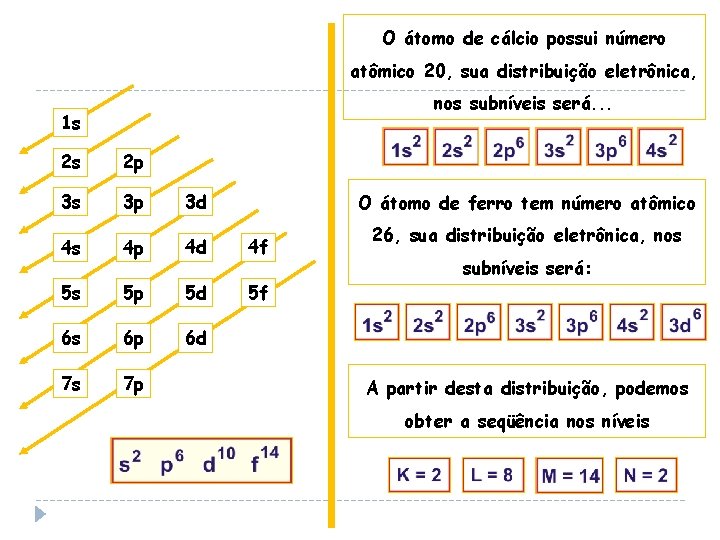
O átomo de cálcio possui número atômico 20, sua distribuição eletrônica, nos subníveis será. . . 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 6 s 6 p 6 d 7 s 7 p O átomo de ferro tem número atômico 26, sua distribuição eletrônica, nos subníveis será: A partir desta distribuição, podemos obter a seqüência nos níveis
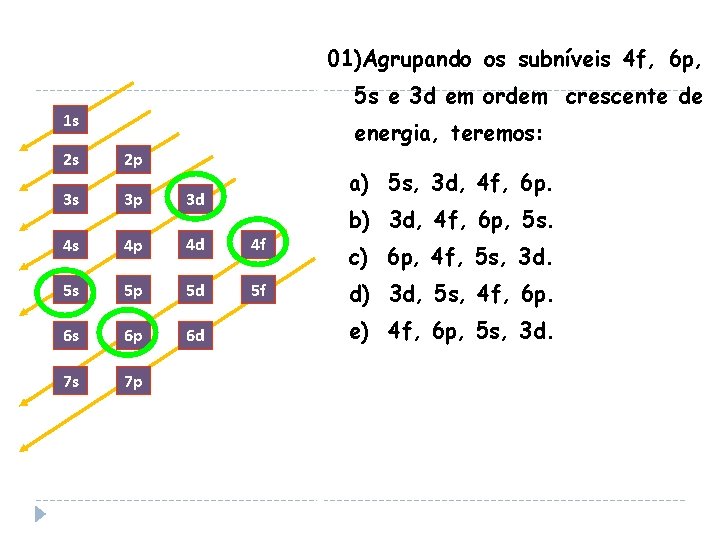
01)Agrupando os subníveis 4 f, 6 p, 5 s e 3 d em ordem crescente de 1 s energia, teremos: 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 6 s 6 p 6 d 7 s 7 p a) 5 s, 3 d, 4 f, 6 p. b) 3 d, 4 f, 6 p, 5 s. c) 6 p, 4 f, 5 s, 3 d. d) 3 d, 5 s, 4 f, 6 p. e) 4 f, 6 p, 5 s, 3 d.
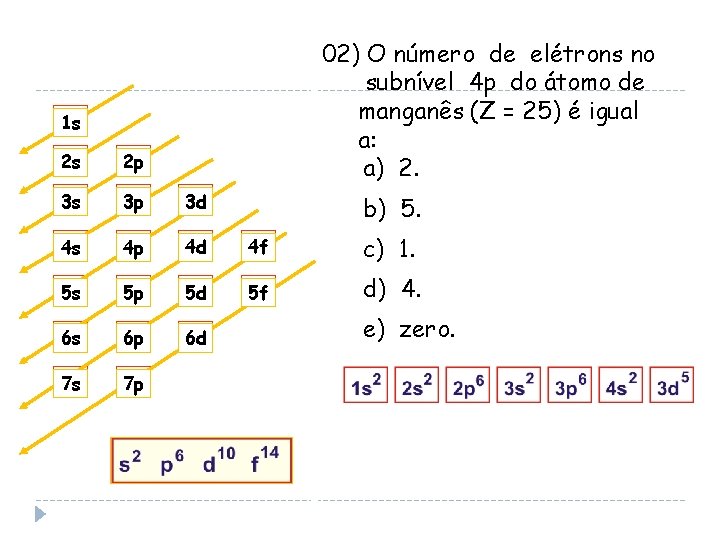
02) O número de elétrons no subnível 4 p do átomo de manganês (Z = 25) é igual a: a) 2. 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 4 f c) 1. 5 s 5 p 5 d 5 f 5 f d) 4. 6 s 6 p 6 d 7 s 7 p b) 5. e) zero.

Para os CÁTIONS devemos distribuir os elétrons como se eles fossem neutros e, em seguida, da última camada retirar os elétrons perdidos 26 1 s 2 2 p 6 Fe 3 s 2+ 2 3 p 6 4 s 2 3 d 6
LIGAÇÕES QUÍMICAS CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

Regra do Octeto: Elemento estável com 8 e- na camada de valência Teoria das Ligações Químicas Ligações Iônicas Ligações Covalente

Doação permanente de elétron Ligações Iônicas

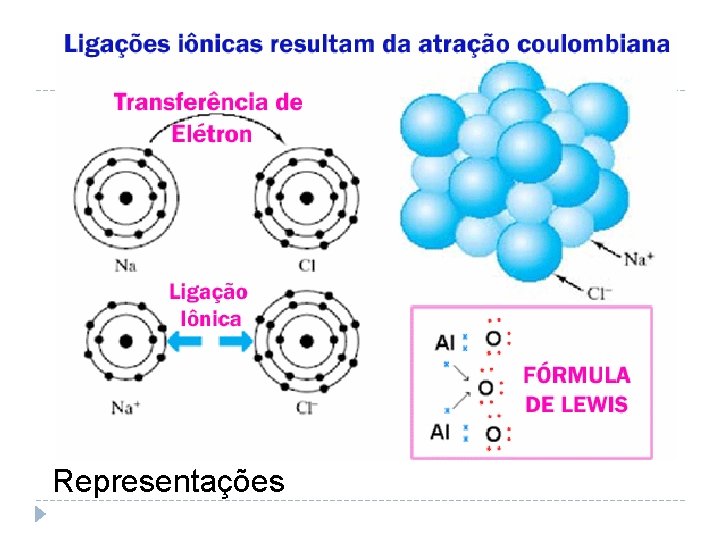
Representações

Compartilhamento eletrônico; - Ocorre o preenchimento dos orbitais incompletos Ligações Covalentes

Nas ligações Covalentes ocorre uma fusão entre orbitais moleculares que apresentam apenas 1 e- , formando outro orbital completo com 2 e-. Teoria dos Orbitais Moleculares

Compartilhamento de 1 par eletrônico, de um átomo estável para um átomo instável. 2 elétrons de um octeto completo Obs. : neste caso os elétrons formam uma espécie de núvem eletrônica, estabilizando os dois átomos. Ligações Covalentes do tipo COORDENADA (antigamente chamada de Coorednada Dativa)

Molécula de monóxido de carbono. Gás inerte, produzido por combustões incompletas. Representação Neste caso, o oxigênio está com o octeto completo. Como ele apresenta pares livres de elétrons, forma coordenanda para o carbono

RESUMO Ligações Iônicas: Ocorre entre metais e não metais, respectivamente, elementos com excesso de elétrons e necessidade de elétrons. Só ocorre com íons Metais = Cátions (+) Não metais = nions (-) Ligações Covalentes: Ocorre entre não metais com Hidrogênio; Ocorre entre não metais com não metais; Ocorre entre não metais com semi-metais; Ligações Metálicas: Entre metais CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

Mol Quantidade de Matéria n. Unidade de massa (padrão) n. U. M. A. ou “U” – Unidade de massa atômica n. Massa atômica n. Nº. Avogadro n. Massa Molar (mol) n. Massa do Gás em Volume n. Cálculos de Quantidade de matéria Mol - Quantidade de materia
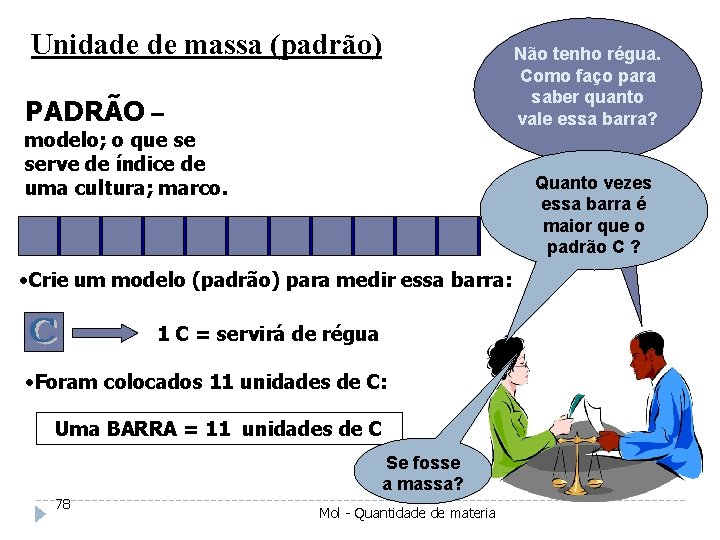
Unidade de massa (padrão) Não tenho régua. Como faço para saber quanto vale essa barra? PADRÃO – modelo; o que se serve de índice de uma cultura; marco. Quanto vezes essa barra é maior que o padrão C ? • Crie um modelo (padrão) para medir essa barra: 1 C = servirá de régua • Foram colocados 11 unidades de C: Uma BARRA = 11 unidades de C Se fosse a massa? 78 Mol - Quantidade de materia
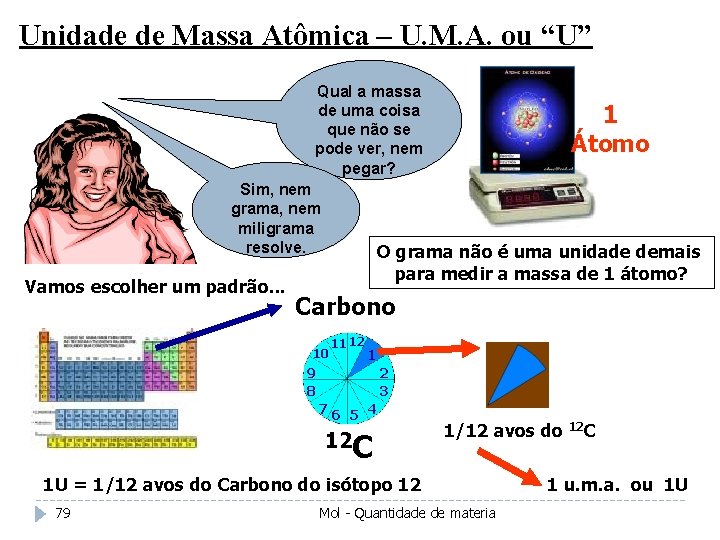
Unidade de Massa Atômica – U. M. A. ou “U” Qual a massa de uma coisa que não se pode ver, nem pegar? Sim, nem grama, nem miligrama resolve. Vamos escolher um padrão. . . 1 Átomo O grama não é uma unidade demais para medir a massa de 1 átomo? Carbono 10 11 12 1 9 8 2 3 76 5 4 12 C 1/12 avos do 12 C 1 U = 1/12 avos do Carbono do isótopo 12 79 Mol - Quantidade de materia 1 u. m. a. ou 1 U
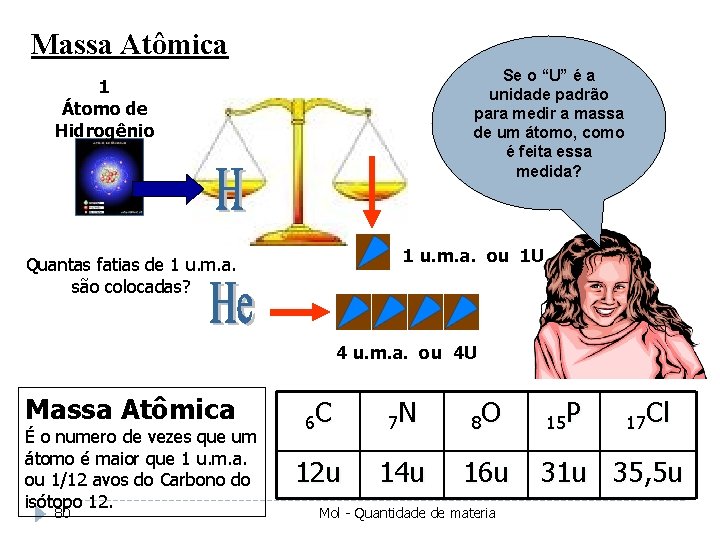
Massa Atômica Se o “U” é a unidade padrão para medir a massa de um átomo, como é feita essa medida? 1 Átomo de Hidrogênio 1 u. m. a. ou 1 U Quantas fatias de 1 u. m. a. são colocadas? 4 u. m. a. ou 4 U Massa Atômica É o numero de vezes que um átomo é maior que 1 u. m. a. ou 1/12 avos do Carbono do isótopo 12. 80 6 C 7 N 8 O 12 u 14 u 16 u Mol - Quantidade de materia 15 P 17 Cl 31 u 35, 5 u
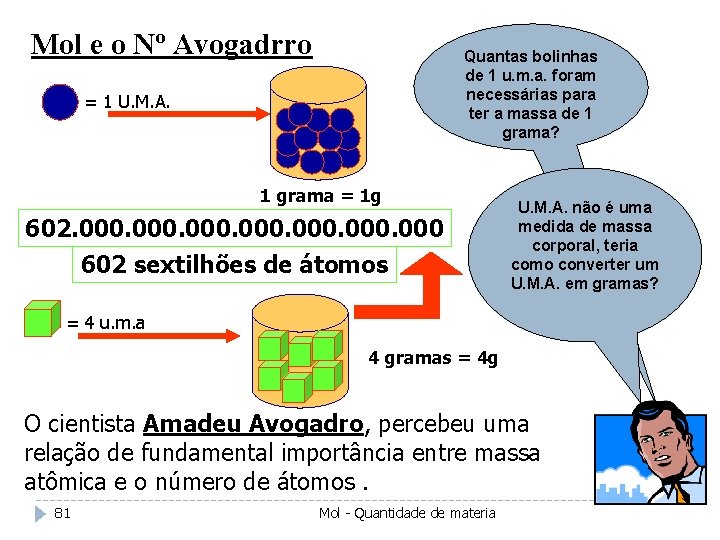
Mol e o Nº Avogadrro Quantas bolinhas de 1 u. m. a. foram necessárias para ter a massa de 1 grama? = 1 U. M. A. 1 grama = 1 g 602. 000 602 sextilhões de átomos U. M. A. não é uma medida de massa corporal, teria como converter um U. M. A. em gramas? = 4 u. m. a 4 gramas = 4 g O cientista Amadeu Avogadro, percebeu uma relação de fundamental importância entre massa atômica e o número de átomos. 81 Mol - Quantidade de materia
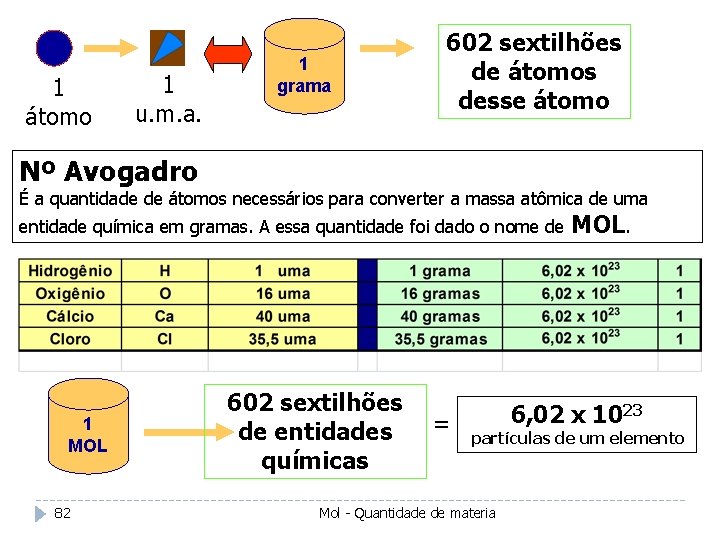
1 átomo 1 u. m. a. 1 grama 602 sextilhões de átomos desse átomo Nº Avogadro É a quantidade de átomos necessários para converter a massa atômica de uma entidade química em gramas. A essa quantidade foi dado o nome de 1 MOL 82 602 sextilhões de entidades químicas = MOL. 6, 02 x 1023 partículas de um elemento Mol - Quantidade de materia
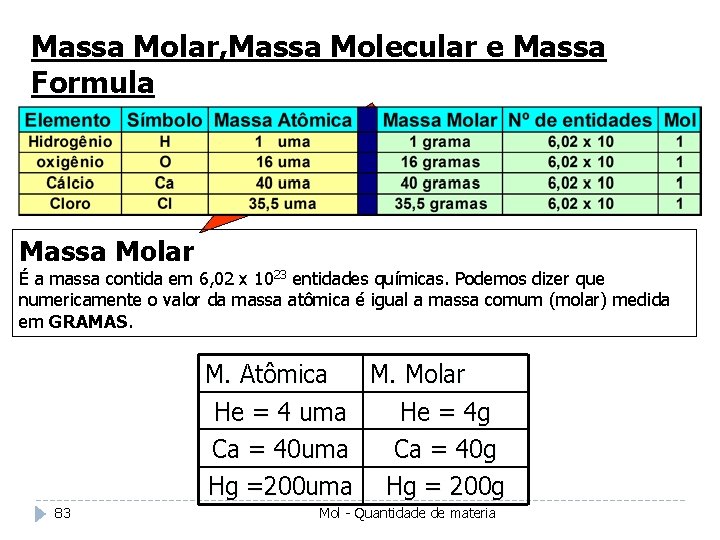
Massa Molar, Massa Molecular e Massa Formula Massa Molar É a massa contida em 6, 02 x 1023 entidades químicas. Podemos dizer que numericamente o valor da massa atômica é igual a massa comum (molar) medida em GRAMAS. M. Atômica M. Molar He = 4 uma He = 4 g Ca = 40 uma Ca = 40 g Hg =200 uma Hg = 200 g 83 Mol - Quantidade de materia
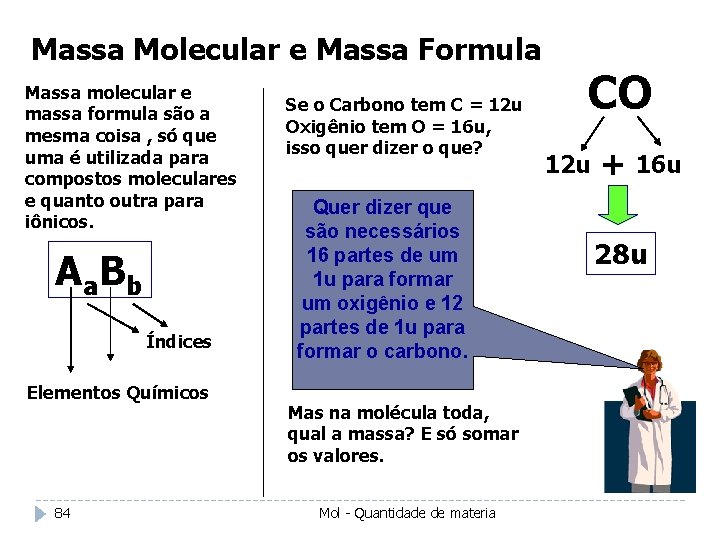
Massa Molecular e Massa Formula Massa molecular e massa formula são a mesma coisa , só que uma é utilizada para compostos moleculares e quanto outra para iônicos. A a Bb Índices Elementos Químicos 84 Se o Carbono tem C = 12 u Oxigênio tem O = 16 u, isso quer dizer o que? Quer dizer que são necessários 16 partes de um 1 u para formar um oxigênio e 12 partes de 1 u para formar o carbono. Mas na molécula toda, qual a massa? E só somar os valores. Mol - Quantidade de materia CO 12 u + 16 u 28 u
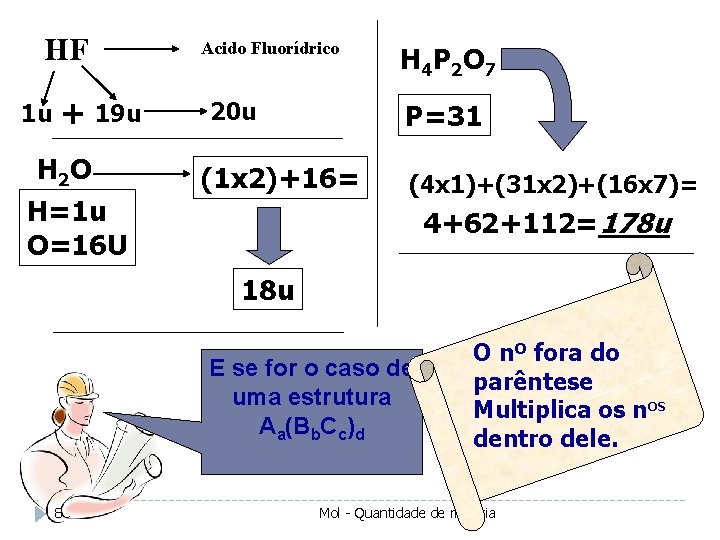
HF 1 u + 19 u H 2 O H=1 u O=16 U Acido Fluorídrico 20 u H 4 P 2 O 7 P=31 (1 x 2)+16= (4 x 1)+(31 x 2)+(16 x 7)= 4+62+112=178 u 18 u E se for o caso de uma estrutura Aa(Bb. Cc)d 85 O nº fora do parêntese Multiplica os nos dentro dele. Mol - Quantidade de materia
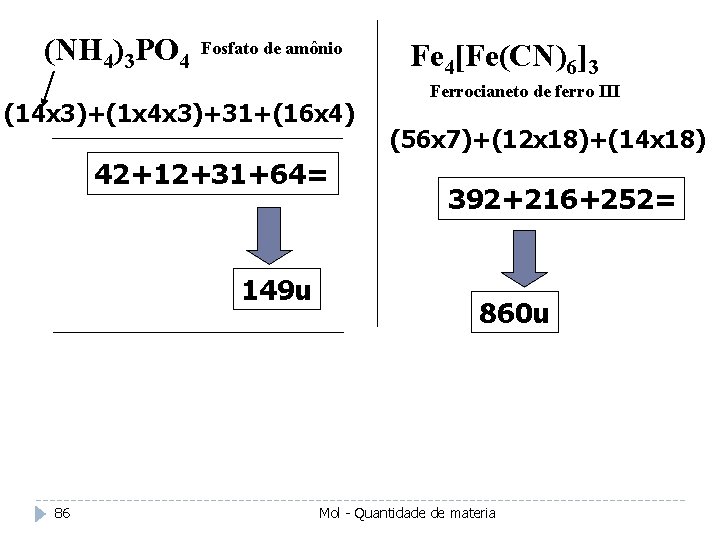
(NH 4)3 PO 4 Fosfato de amônio (14 x 3)+(1 x 4 x 3)+31+(16 x 4) 42+12+31+64= 149 u 86 Fe 4[Fe(CN)6]3 Ferrocianeto de ferro III (56 x 7)+(12 x 18)+(14 x 18) 392+216+252= 860 u Mol - Quantidade de materia
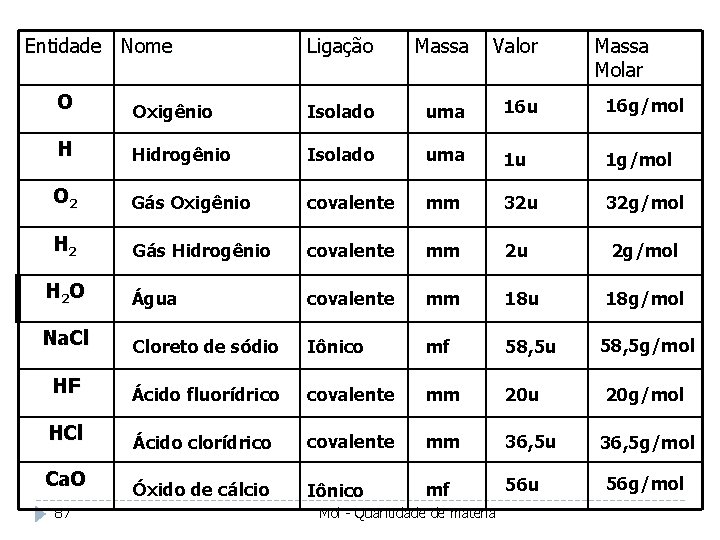
Entidade Nome Ligação Massa Valor Massa Molar O Oxigênio Isolado uma 16 u 16 g/mol H Hidrogênio Isolado uma 1 u 1 g/mol O 2 Gás Oxigênio covalente mm 32 u 32 g/mol H 2 Gás Hidrogênio covalente mm 2 u 2 g/mol H 2 O Água covalente mm 18 u Na. Cl Cloreto de sódio Iônico mf 58, 5 u HF Ácido fluorídrico covalente mm 20 u HCl Ácido clorídrico covalente mm 36, 5 u Ca. O Óxido de cálcio Iônico mf 56 u 87 Mol - Quantidade de materia 18 g/mol 58, 5 g/mol 20 g/mol 36, 5 g/mol 56 g/mol

Massa de gás em volume Por convenção, a pressão atmosférica ao nível do mar recebe o nome de PRESSAO NORMAL e vale uma atmosfera (1 atm) ou 760 mm. Hg (760 milímetros de mercúrio) ou 760 torr (760 Torricelli), e toda essa informação deve ser dada em CNTP, ou CONDIÇOES NORMAIS DE TEMPERATURA E PRESSÃO. Que determina a temperatura normal de 0°C. 1 mol de moléculas de qualquer gás, nas CNTP, ocupa aproximadamente 22, 4 L ou 22. 400 m. L ou 22. 400 cm 3 88 Mol - Quantidade de materia

Resumo Geral para iniciação dos cálculos Estequiométricos Massa Mol Massa do elemento 1 Ms 89 = Mol = Partículas Volume 6, 02 x 1023 22, 4 L P Mol - Quantidade de materia = V

Exercício 5 - Assinale a alternativa que contém a espécie de "menor" massa molecular: a) ácido acético → CH 3 COOH b) ácido iodídrico → HI c) ácido sulfúrico → H 2 SO 4 d) ácido fosfórico → H 3 PO 4 e) ácido fosforoso → H 3 PO 3 Dados: H = 1 u; C = 12 u; O = 16 u; P = 31 u; S = 32 u; I = 127 u a) C = 12 x 2 = 24 H=1 x 4= 4 O = 16 x 2 = 32 Total = 60 U. M. M. b) 128 U. M. M. c) 98 U. M. M d) 98 U. M. M. e) 82 U. M. M. CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

6 – Qual a quantidade de mols existentes em 1, 5× 1024 moléculas de ácido fosfórico (H 3 PO 4)? 6, 0 x 1023 moléculas 1 mol H 3 PO 4 1, 5× 1024 moléculas X X = 2, 5 mols 7 - (UEL) A amostra de 2, 0 mols de carbono tem massa, aproximadamente: 1 mol C 2 mols C 12 u. m. a 12 g 24 g CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

10 - Na natureza, de cada 5 átomos de boro, 1 tem massa atômica igual a 10 u. m. a (unidade de massa atômica) e 4 têm massa atômica igual a 11 u. m. a. Com base nesses dados, a massa atômica do boro, expressa em u. m. a, é igual a: a) 10 b) 10, 5 c) 10, 8 d) 11 e) 11, 5 5 átomos B 100% 1 átomos B 20% 10 B 20% 11 B 80% Massa Atômica Ponderada (map) map = (10 B x 20%) + (11 B x 80%) 100 map = (10 x 20) + (11 x 80) 100 map = 200 + 880 100 CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda = map = 10, 8 u. m. a.
CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
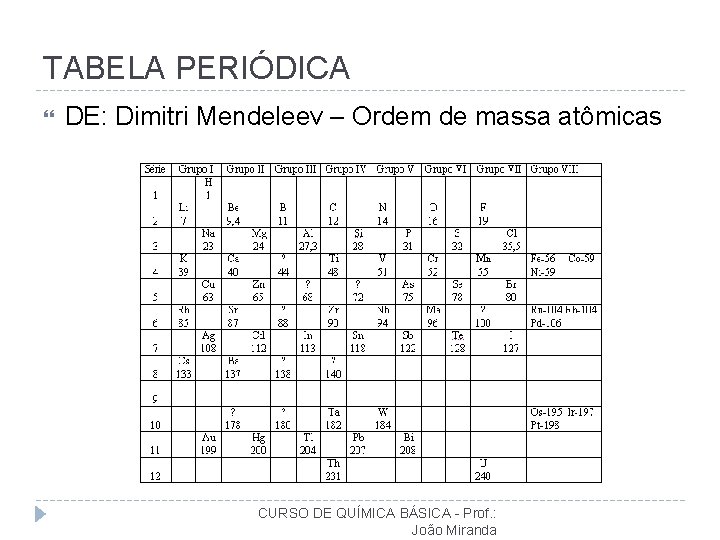
TABELA PERIÓDICA DE: Dimitri Mendeleev – Ordem de massa atômicas CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
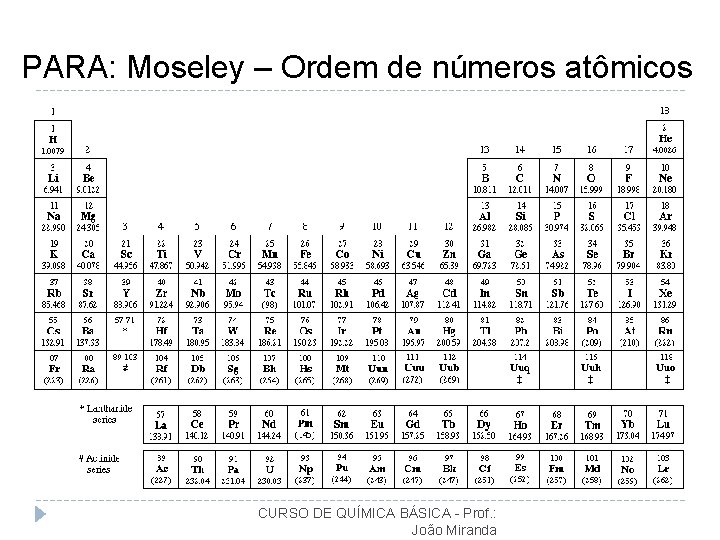
PARA: Moseley – Ordem de números atômicos CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

BEM-VINDOS AO REINO PERIÓDICO. Esta é uma terra de fantasia, mas está mais próxima da realidade do que parece. Este é o reino dos elementos químicos, as substâncias a partir das quais tudo é tangível é feito. Não é um país muito grande pois consiste de um pouco mais de centenas de regiões, mas ainda assim é responsável por tudo que constitui nosso mundo. ATKINS, P. W. 1996

Lei Periódica "As propriedades físicas e químicas dos elementos, são funções periódicas de seus números atômicos". Na tabela, os elementos estão arranjados horizontalmente, em seqüência numérica, de acordo com seus números atômicos, resultando o aparecimento de sete linhas horizontais (ou períodos). Funções da Tabela Periódica: -Organizar os elementos químicos conhecidos; -Prever a descoberta de novos elementos químicos naturais ou sintéticos; -Ordenar elementos por características físico-químicas; -Caracterizar propriedades que variam de elemento para elemento; CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

Elementos Químicos Os elementos químicos são representados por letras maiúsculas ou uma letra maiúscula seguida de uma letra minúscula. Os Símbolos são de origem latina: Português Latim Símbolo Sódio Natrium Na Potássio Kalium K Enxofre Sulphur S Fósforo Phosphurus P Ouro Aurum Au

Organização da Tabela Periódica Períodos e séries: São as filas horizontais da tabela periódica. São em número de 7 e indicam o número de níveis ou camadas preenchidas com elétrons. K L M N O P Q 1 2 3 4 5 6 7 P Q CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

Famílias ou Grupos São as colunas verticais da Tabela Periódica. Em um Grupo ou Família, encontram-se elementos com propriedades químicas semelhantes. Para os Elementos Representativos, o nº do Grupo representa o nº de elétrons da última camada (camada de valência). 18 K 1 2 L M N O P Q 13 14 1516 17 3 4 5 6 7 8 9 101112 1 2 3 4 5 6 7
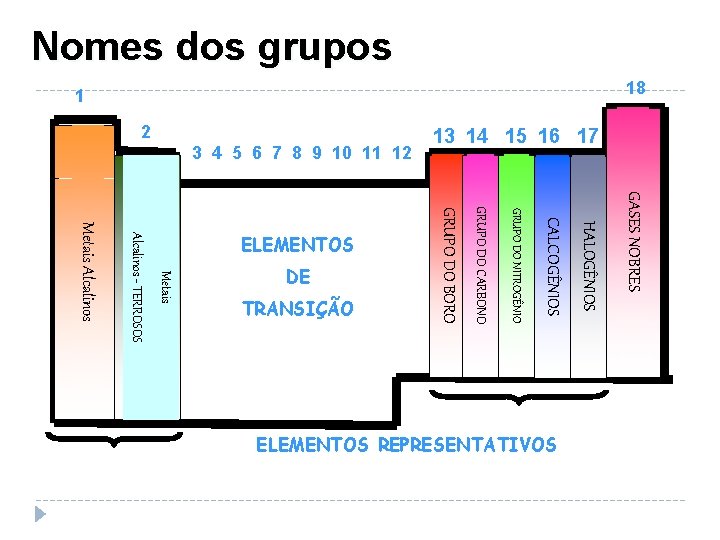
Nomes dos grupos 18 1 3 4 5 6 7 8 9 10 11 12 GASES NOBRES Metais Alcalinos ELEMENTOS REPRESENTATIVOS HALOGÊNIOS CALCOGÊNIOS GRUPO DO NITROGÊNIO GRUPO DO CARBONO GRUPO DO BORO TRANSIÇÃO Metais DE Alcalinos - TERROSOS ELEMENTOS 13 14 15 16 17 2
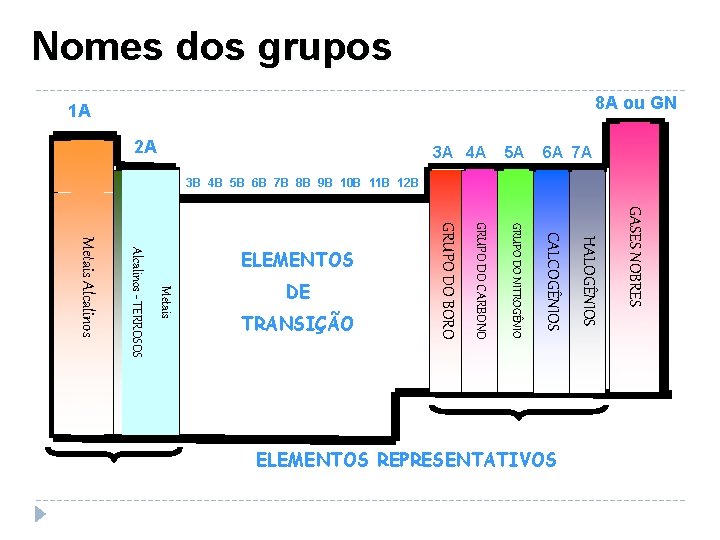
Nomes dos grupos 8 A ou GN 1 A GASES NOBRES GRUPO DO NITROGÊNIO CALCOGÊNIOS TRANSIÇÃO Metais DE Alcalinos - TERROSOS ELEMENTOS Metais Alcalinos ELEMENTOS REPRESENTATIVOS HALOGÊNIOS 6 A 7 A GRUPO DO BORO 5 A GRUPO DO CARBONO 3 B 4 B 5 B 6 B 7 B 8 B 9 B 10 B 11 B 12 B 3 A 4 A 2 A
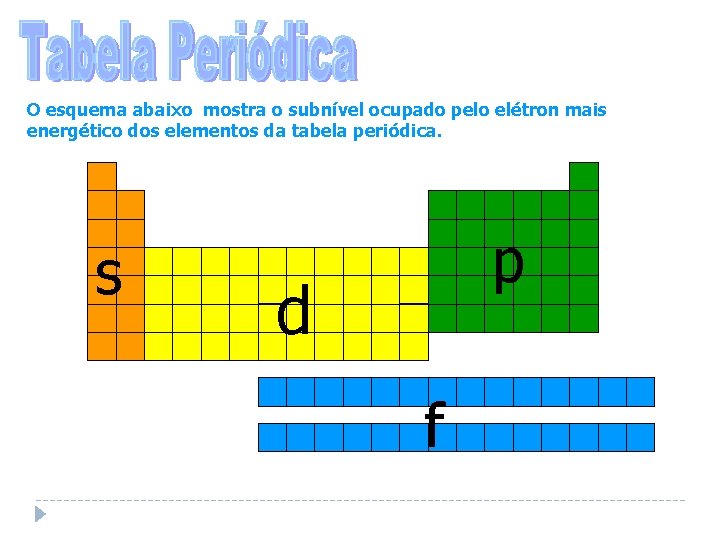
O esquema abaixo mostra o subnível ocupado pelo elétron mais energético dos elementos da tabela periódica. s p d f
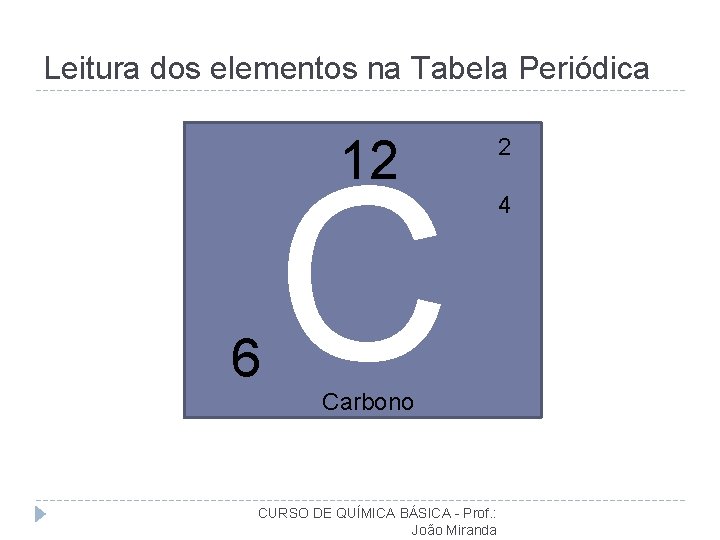
Leitura dos elementos na Tabela Periódica 12 6 C Carbono CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda 2 4
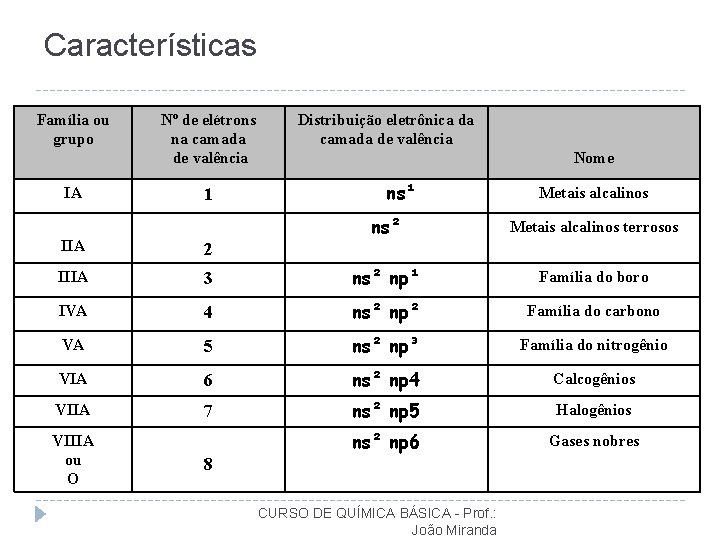
Características Família ou grupo IA Nº de elétrons na camada de valência 1 Distribuição eletrônica da camada de valência Nome ns¹ Metais alcalinos ns² Metais alcalinos terrosos IIA 2 IIIA 3 ns² np¹ Família do boro IVA 4 ns² np² Família do carbono VA 5 ns² np³ Família do nitrogênio VIA 6 ns² np 4 Calcogênios VIIA 7 ns² np 5 Halogênios ns² np 6 Gases nobres VIIIA ou O 8 CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda
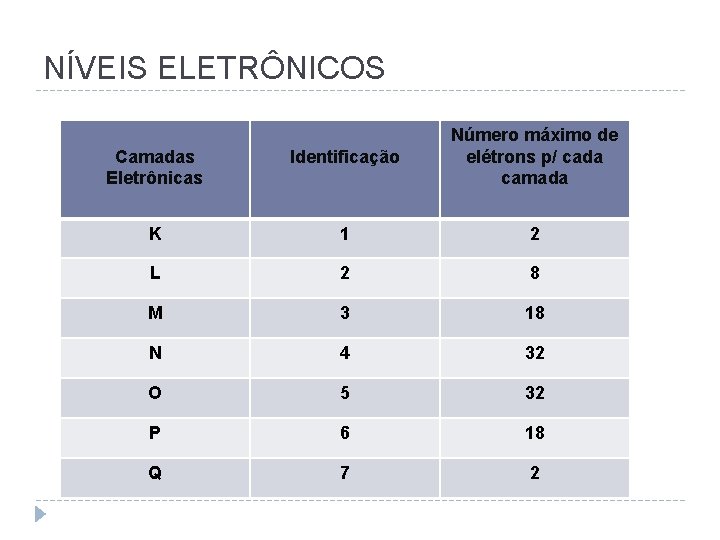
NÍVEIS ELETRÔNICOS Camadas Eletrônicas Identificação Número máximo de elétrons p/ cada camada K 1 2 L 2 8 M 3 18 N 4 32 O 5 32 P 6 18 Q 7 2
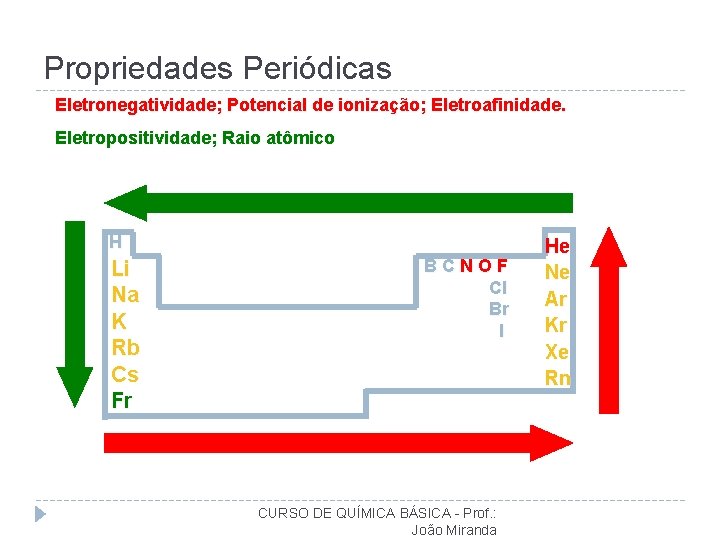
Propriedades Periódicas Eletronegatividade; Potencial de ionização; Eletroafinidade. Eletropositividade; Raio atômico H Li Na K Rb Cs Fr BCNOF Cl Br I CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda He Ne Ar Kr Xe Rn

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

CURSO DE QUÍMICA BÁSICA - Prof. : João Miranda

Liga’s Hit II Ligações são sensacionais; Ligações ocorrem nos orbitais; Regra do octeto de Lewis; Oito elétrons, igual a um gás; Cátions, ânions, Cátions e nions = metais nãometais; Ligações são sensacionais; Ligações ocorrem. CURSO nos. DEorbitais; QUÍMICA BÁSICA - Prof. : João Miranda

Liga’s HIT 1 Eu já sei o que é uma liga; Aprendi as Ligações; (Refrão) Um metal e outro metal formam uma liga metálica; Um metal e um não metal formam ligação iônica; Não metal e hidrogênio, não metal e semi-metal, aí as covalentes; (Refrão) As Ligações
- Slides: 114