CURSO DE ATUALIZAO EM HEMOGLOBINRIA PAROXSTICA NOCTURNA HPN

CURSO DE ATUALIZAÇÃO EM HEMOGLOBINÚRIA PAROXÍSTICA NOCTURNA (HPN) Fisiopatologia da HPN Com a colaboração de:
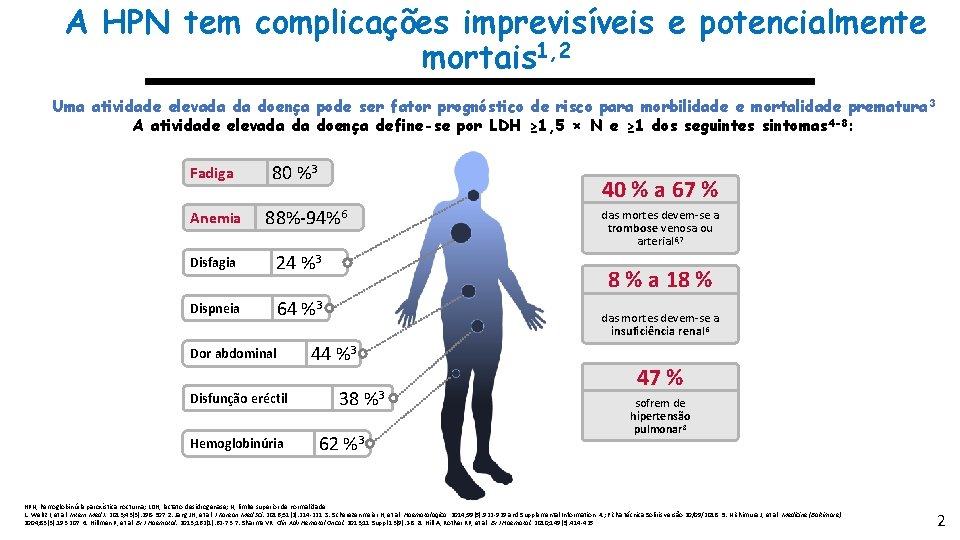
A HPN tem complicações imprevisíveis e potencialmente mortais 1, 2 Uma atividade elevada da doença pode ser fator prognóstico de risco para morbilidade e mortalidade prematura 3 A atividade elevada da doença define-se por LDH ≥ 1, 5 × N e ≥ 1 dos seguintes sintomas 4 -8: Fadiga Anemia 80 %3 40 % a 67 % 88%-94%6 Disfagia 24 %3 Dispneia 64 %3 Dor abdominal Disfunção eréctil Hemoglobinúria das mortes devem-se a trombose venosa ou arterial 6, 7 8 % a 18 % das mortes devem-se a insuficiência renal 6 44 %3 38 %3 62 %3 47 % sofrem de hipertensão pulmonar 8 HPN, hemoglobinúria paroxística nocturna; LDH, lactato desidrogenase; N, limite superior de normalidade. 1. Weitz I, et al. Intern Med J. 2013; 43(3): 298 -307. 2. Jang JH, et al. J Korean Med Sci. 2016; 31(2): 214 -221. 3. Scherezenmeier H, et al. Haematologica. 2014; 99(5): 922 -929 and Supplemental Information. 4. ; Ficha técnica Soliris versão 20/09/2018. 5. Nishimura J, et al. Medicine (Baltimore). 2004; 83(3): 193 -207. 6. Hillmen P, et al. Br J Haematol. 2013; 162(1): 62 -73. 7. Sharma VR. Clin Adv Hematol Oncol. 2013; 11 Suppl 13(9): 2 -8. 8. Hill A, Rother RP, et al. Br J Haematol. 2010; 149(3): 414 -425. 2
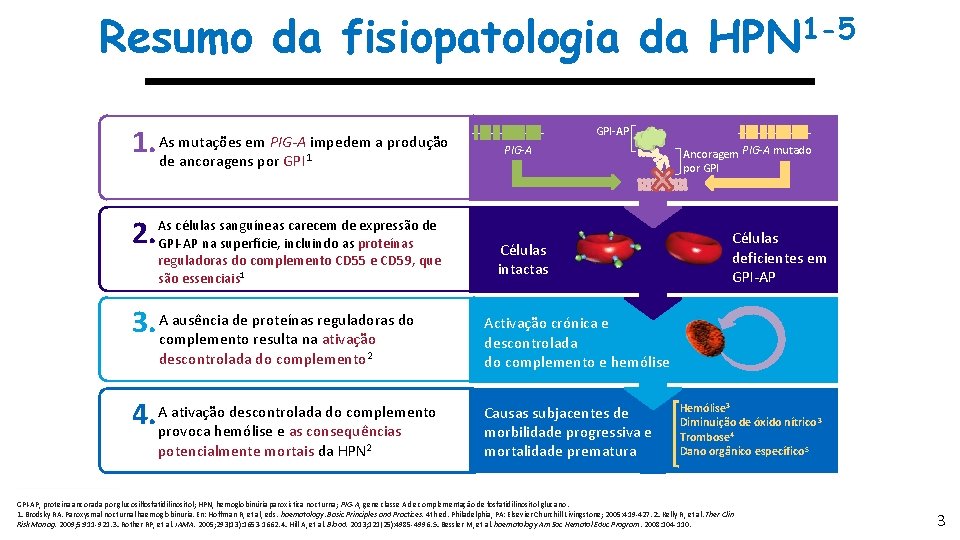
Resumo da fisiopatologia da HPN 1 -5 1. As mutações em PIG-A impedem a produção de ancoragens por GPI 1 2. As células sanguíneas carecem de expressão de GPI-AP na superfície, incluindo as proteínas reguladoras do complemento CD 55 e CD 59, que são essenciais 1 3. A ausência de proteínas reguladoras do complemento resulta na ativação 4. GPI-AP PIG-A Células intactas descontrolada do complemento 2 Activação crónica e descontrolada do complemento e hemólise A ativação descontrolada do complemento provoca hemólise e as consequências potencialmente mortais da HPN 2 Causas subjacentes de morbilidade progressiva e mortalidade prematura Ancoragem PIG-A mutado por GPI Células deficientes em GPI-AP Hemólise 3 Diminuição de óxido nítrico 3 Trombose 4 Dano orgânico específico 5 GPI-AP, proteína ancorada por glucosilfosfatidilinositol; HPN, hemoglobinúria paroxística nocturna; PIG-A, gene classe A de complementação de fosfatidilinositol glucano. 1. Brodsky RA. Paroxysmal nocturnal haemoglobinuria. En: Hoffman R, et al, eds. haematology: Basic Principles and Practices. 4 th ed. Philadelphia, PA: Elsevier Churchill Livingstone; 2005: 419 -427. 2. Kelly R, et al. Ther Clin Risk Manag. 2009; 5: 911 -921. 3. Rother RP, et al. JAMA. 2005; 293(13): 1653 -1662. 4. Hill A, et al. Blood. 2013; 121(25): 4985 -4996. 5. Bessler M, et al. haematology Am Soc Hematol Educ Program. 2008: 104 -110. 3
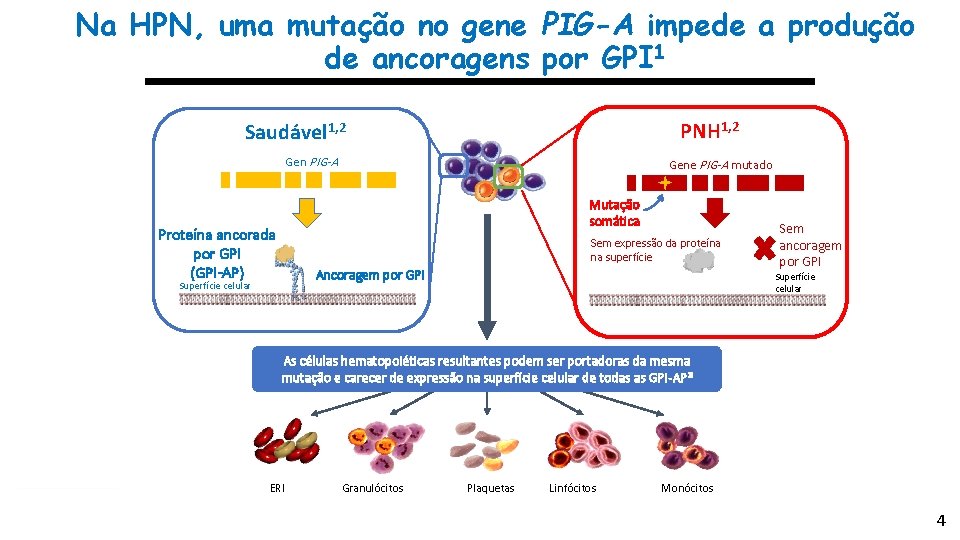
Na HPN, uma mutação no gene PIG-A impede a produção de ancoragens por GPI 1 Saudável 1, 2 CMH PNH 1, 2 Gen PIG-A Gene PIG-A mutado Mutação somática Proteína ancorada por GPI (GPI-AP) Sem expressão da proteína na superfície Ancoragem por GPI Superfície celular Sem ancoragem por GPI Superfície celular As células hematopoiéticas resultantes podem ser portadoras da mesma mutação e carecer de expressão na superfície celular de todas as GPI-AP 3 ERI Granulócitos Plaquetas Linfócitos Monócitos 4
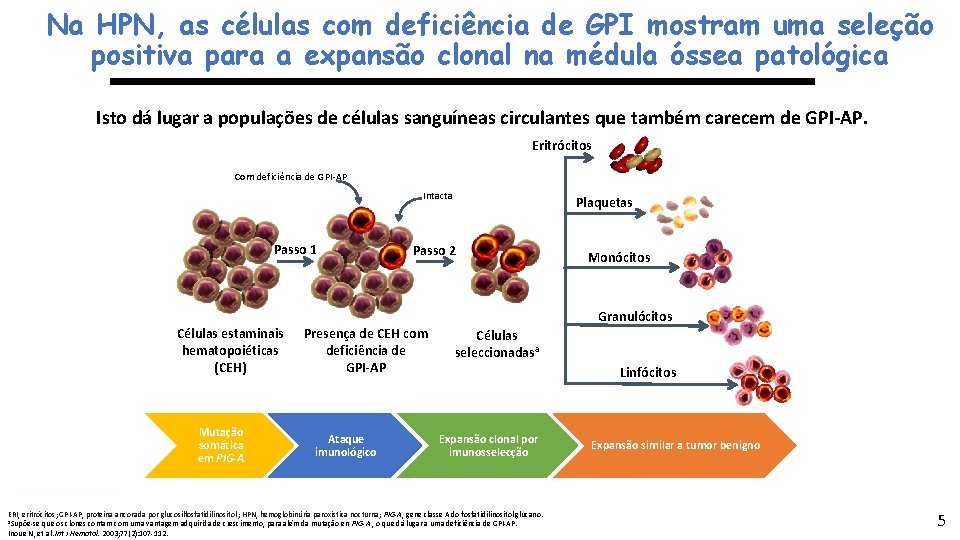
Na HPN, as células com deficiência de GPI mostram uma seleção positiva para a expansão clonal na médula óssea patológica Isto dá lugar a populações de células sanguíneas circulantes que também carecem de GPI-AP. Eritrócitos Com deficiência de GPI-AP Intacta Passo 1 Plaquetas Passo 2 Monócitos Granulócitos Células estaminais hematopoiéticas (CEH) Mutação somática em PIG-A Presença de CEH com deficiência de GPI-AP Ataque imunológico Células seleccionadasa Linfócitos Expansão clonal por imunosselecção ERI, eritrócitos; GPI-AP, proteína ancorada por glucosilfosfatidilinositol; HPN, hemoglobinúria paroxística nocturna; PIG-A, gene classe A do fosfatidilinositol glucano. a. Supõe-se que os clones contam com uma vantagem adquirida de crescimento, para além da mutação en PIG-A , o que dá lugar a uma deficiência de GPI-AP. Inoue N, et al. Int J Hematol. 2003; 77(2): 107 -112. Expansão similar a tumor benigno 5
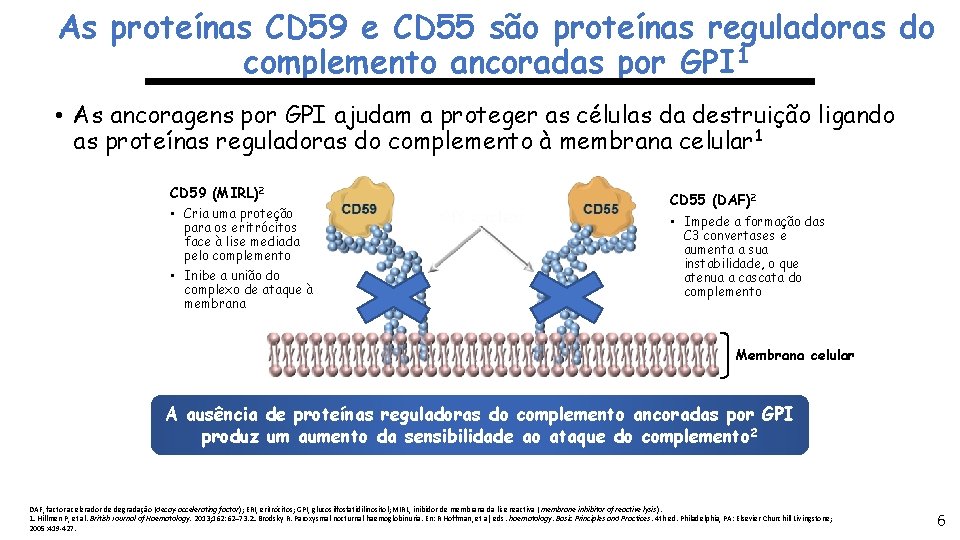
As proteínas CD 59 e CD 55 são proteínas reguladoras do complemento ancoradas por GPI 1 • As ancoragens por GPI ajudam a proteger as células da destruição ligando as proteínas reguladoras do complemento à membrana celular 1 CD 59 (MIRL)2 • Cria uma proteção para os eritrócitos face à lise mediada pelo complemento • Inibe a união do complexo de ataque à membrana CD 55 (DAF)2 • Impede a formação das C 3 convertases e aumenta a sua instabilidade, o que atenua a cascata do complemento Membrana celular A ausência de proteínas reguladoras do complemento ancoradas por GPI produz um aumento da sensibilidade ao ataque do complemento 2 DAF, factor acelerador de degradação (decay-accelerating factor); ERI, eritrócitos; GPI, glucosilfosfatidilinositol; MIRL, inibidor de membrana da lise reactiva ( membrane inhibitor of reactive lysis). 1. Hillmen P, et al. British Journal of Haematology. 2013; 162: 62– 73. 2. Brodsky R. Paroxysmal nocturnal haemoglobinuria. En: R Hoffman, et al, eds. haematology: Basic Principles and Practices. 4 th ed. Philadelphia, PA: Elsevier Churchill Livingstone; 2005: 419 -427. 6

O sistema do complemento é um componente essencial do sistema imunitário protetor natural 1 O complemento é um sistema de mais de 30 proteínas plasmáticas que deteta e elimina as ameaças rapidamente 1 • O sistema do complemento tem quatro funções principais 1. Opsonização (recobrimento) de micróbios, marcando-os para a fagocitose 2 2. Depuração dos imunocomplexos 1 3. Geração da resposta inflamatória 2 4. Formação do complexo de ataque à membrana (CAM) e lise celular 2 O sistema do complemento está sempre ativo e as proteínas reguladoras do complemento (como CD 55 e CD 59) são necessárias para evitar que a ativação descontrolada do complemento cause dano nos tecidos do hospedeiro 1 1. Murphy KP. Janeway's Immunobiology. 8 th ed. New York, NY: Garland Science, Taylor & Francis Group LLC; 2012: 37 -73. 2. Abbas AK, et al. Basic Immunology: Functions and Disorders of the Immune System. 5 th ed. St Louis, MO: Elsevier; 2016: 169 -190. Proteínas reguladoras do complemento Ativação do complemento 7
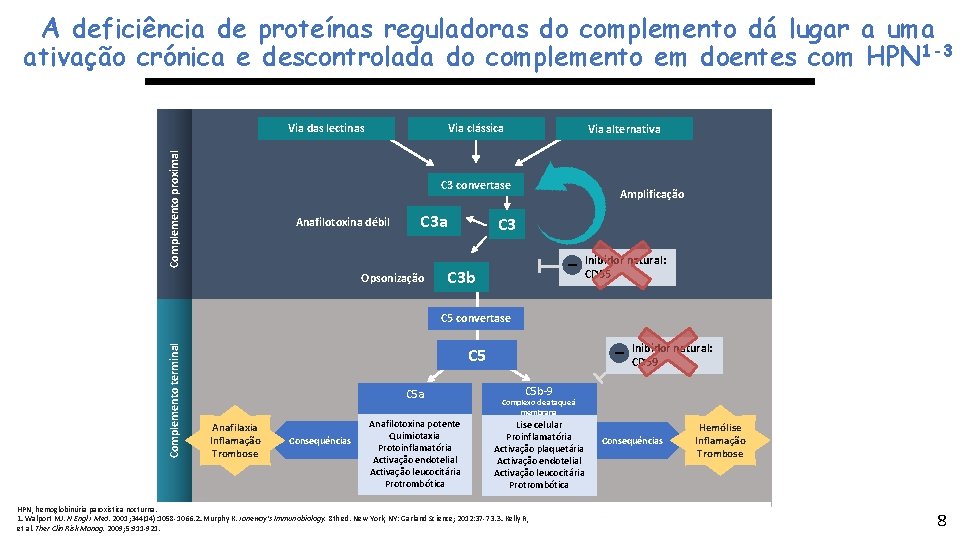
A deficiência de proteínas reguladoras do complemento dá lugar a uma ativação crónica e descontrolada do complemento em doentes com HPN 1 -3 Complemento proximal Via das lectinas Via clássica Via alternativa C 3 convertase Anafilotoxina débil C 3 a Opsonização Amplificação C 3 _ C 3 b Inibidor natural: CD 55 Complemento terminal C 5 convertase _ C 5 a Anafilaxia Inflamação Trombose Consequências Anafilotoxina potente Quimiotaxia Protoinflamatória Activação endotelial Activação leucocitária Protrombótica Inibidor natural: CD 59 C 5 b-9 Complexo de ataque à membrana Lise celular Proinflamatória Activação plaquetária Activação endotelial Activação leucocitária Protrombótica HPN, hemoglobinúria paroxística nocturna. 1. Walport MJ. N Engl J Med. 2001; 344(14): 1058 -1066. 2. Murphy K. Janeway's Immunobiology. 8 th ed. New York, NY: Garland Science; 2012: 37 -73. 3. Kelly R, et al. Ther Clin Risk Manag. 2009; 5: 911 -921. Consequências Hemólise Inflamação Trombose 8
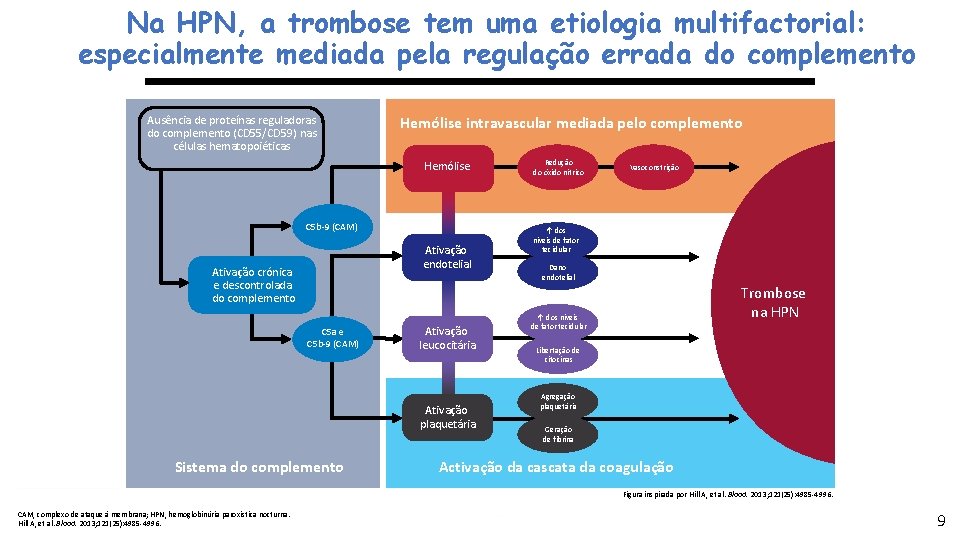
Na HPN, a trombose tem uma etiologia multifactorial: especialmente mediada pela regulação errada do complemento Ausência de proteínas reguladoras do complemento (CD 55/CD 59) nas células hematopoiéticas Hemólise intravascular mediada pelo complemento Hemólise C 5 b-9 (CAM) Ativação endotelial Ativação crónica e descontrolada do complemento C 5 a e C 5 b-9 (CAM) Ativação leucocitária Ativação plaquetária Sistema do complemento Redução do óxido nítrico Vasoconstrição ↑ dos níveis de fator tecidular Dano endotelial Trombose na HPN ↑ dos níveis de fator tecidular Libertação de citocinas Agregação plaquetária Geração de fibrina Activação da cascata da coagulação Figura inspirada por Hill A, et al. Blood. 2013; 121(25): 4985 -4996. CAM, complexo de ataque à membrana; HPN, hemoglobinúria paroxística nocturna. Hill A, et al. Blood. 2013; 121(25): 4985 -4996. 9
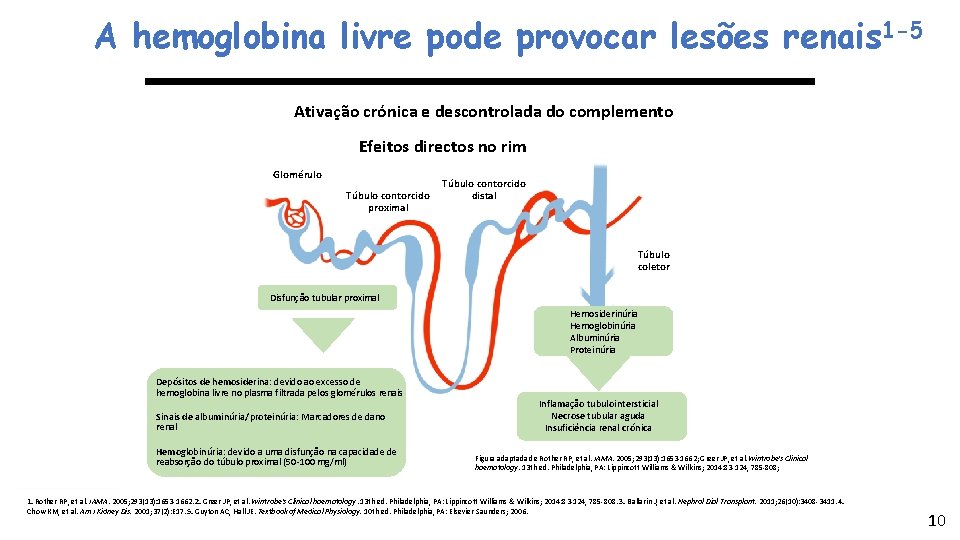
A hemoglobina livre pode provocar lesões renais 1 -5 Ativação crónica e descontrolada do complemento Efeitos directos no rim Glomérulo Túbulo contorcido proximal Túbulo contorcido distal Túbulo coletor Disfunção tubular proximal Hemosiderinúria Hemoglobinúria Albuminúria Proteinúria Depósitos de hemosiderina: devido ao excesso de hemoglobina livre no plasma filtrada pelos glomérulos renais Sinais de albuminúria/proteinúria: Marcadores de dano renal Hemoglobinúria: devido a uma disfunção na capacidade de reabsorção do túbulo proximal (50 -100 mg/ml) Inflamação tubulointersticial Necrose tubular aguda Insuficiência renal crónica Figura adaptada de Rother RP, et al. JAMA. 2005; 293(13): 1653 -1662; Greer JP, et al. Wintrobe's Clinical haematology. 13 th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2014: 83 -124, 785 -808; 1. Rother RP, et al. JAMA. 2005; 293(13): 1653 -1662. 2. Greer JP, et al. Wintrobe's Clinical haematology. 13 th ed. Philadelphia, PA: Lippincott Williams & Wilkins; 2014: 83 -124, 785 -808. 3. Ballarin J, et al. Nephrol Dial Transplant. 2011; 26(10): 3408 -3411. 4. Chow KM, et al. Am J Kidney Dis. 2001; 37(2): E 17. 5. Guyton AC, Hall JE. Textbook of Medical Physiology. 10 th ed. Philadelphia, PA: Elsevier Saunders; 2006. 10
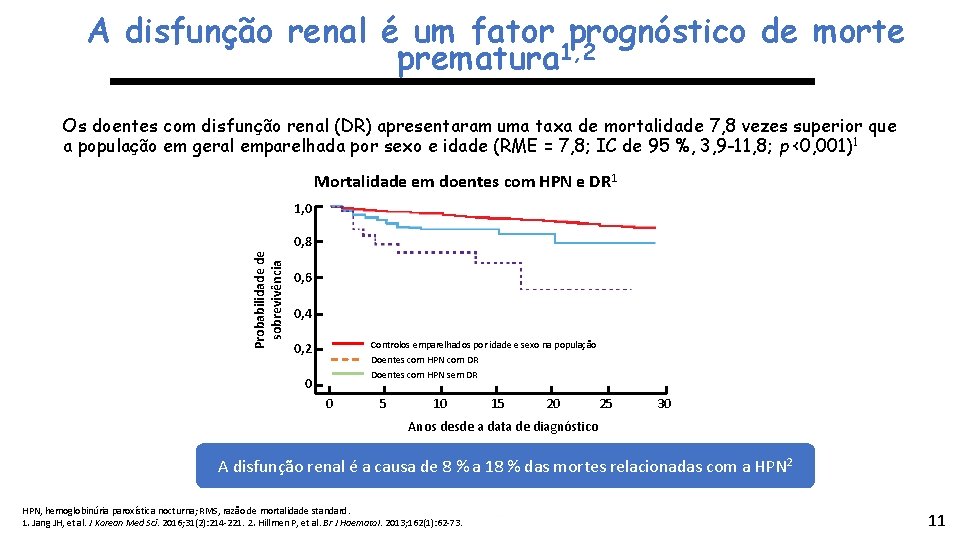
A disfunção renal é um fator prognóstico de morte prematura 1, 2 Os doentes com disfunção renal (DR) apresentaram uma taxa de mortalidade 7, 8 vezes superior que a população em geral emparelhada por sexo e idade (RME = 7, 8; IC de 95 %, 3, 9 -11, 8; p <0, 001)1 Mortalidade em doentes com HPN e DR 1 Probabilidade de sobrevivência 1, 0 0, 8 0, 6 0, 4 Controlos emparelhados por idade e sexo na população Doentes com HPN com DR 0, 2 Doentes com HPN sem DR 0 0 5 10 15 20 25 30 Anos desde a data de diagnóstico A disfunção renal é a causa de 8 % a 18 % das mortes relacionadas com a HPN 2 HPN, hemoglobinúria paroxística nocturna; RMS, razão de mortalidade standard. 1. Jang JH, et al. J Korean Med Sci. 2016; 31(2): 214 -221. 2. Hillmen P, et al. Br J Haematol. 2013; 162(1): 62 -73. 11
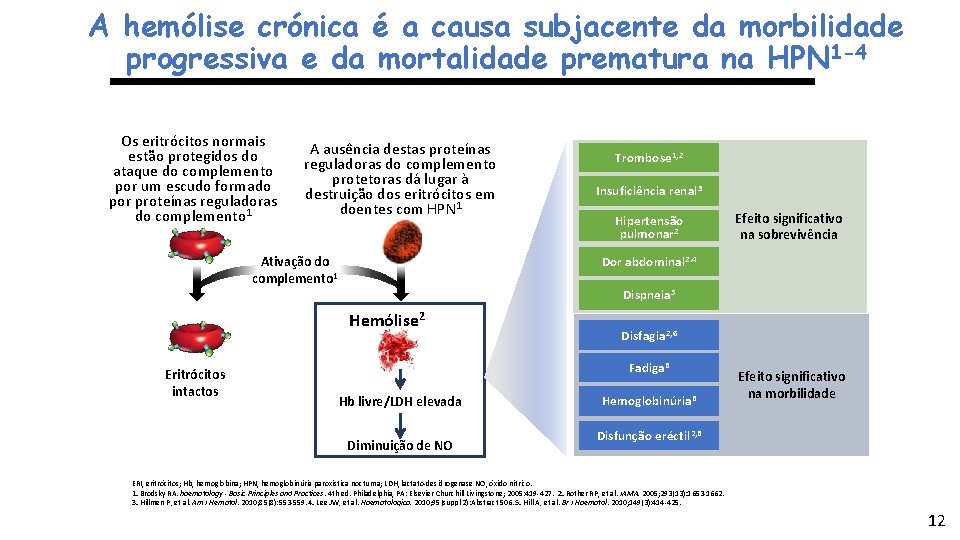
A hemólise crónica é a causa subjacente da morbilidade progressiva e da mortalidade prematura na HPN 1 -4 Os eritrócitos normais estão protegidos do ataque do complemento por um escudo formado por proteínas reguladoras do complemento 1 A ausência destas proteínas reguladoras do complemento protetoras dá lugar à destruição dos eritrócitos em doentes com HPN 1 Ativação do complemento 1 Insuficiência renal 3 Hipertensão pulmonar 2 Efeito significativo na sobrevivência Dor abdominal 2. 4 Dispneia 5 Hemólise 2 Eritrócitos intactos Trombose 1, 2 Disfagia 2, 6 Fadiga 6 Hb livre/LDH elevada Diminuição de NO Hemoglobinúria 6 Efeito significativo na morbilidade Disfunção eréctil 2, 6 ERI, eritrócitos; Hb, hemoglobina; HPN, hemoglobinúria paroxística nocturna; LDH, lactato-desidrogenase NO, óxido nítrico. 1. Brodsky RA. haematology - Basic Principles and Practices. 4 th ed. Philadelphia, PA: Elsevier Churchill Livingstone; 2005: 419 -427. 2. Rother RP, et al. JAMA. 2005; 293(13): 1653 -1662. 3. Hillmen P, et al. Am J Hematol. 2010; 85(8): 553 -559. 4. Lee JW, et al. Haematologica. 2010; 95(suppl 2): Abstract 506. 5. Hill A, et al. Br J Haematol. 2010; 149(3): 414 -425. 6. Hill A, et al. Br J Haematol. 2007; 137(3): 181 -192. 12
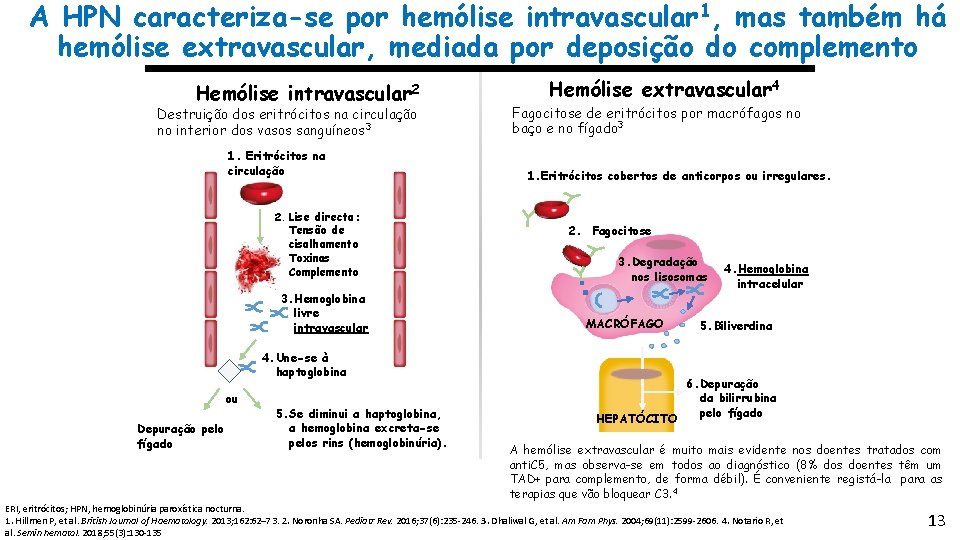
A HPN caracteriza-se por hemólise intravascular 1, mas também há hemólise extravascular, mediada por deposição do complemento Hemólise intravascular 2 Destruição dos eritrócitos na circulação no interior dos vasos sanguíneos 3 1. Eritrócitos na circulação 2. Lise directa: Tensão de cisalhamento Toxinas Complemento 3. Hemoglobina livre intravascular Hemólise extravascular 4 Fagocitose de eritrócitos por macrófagos no baço e no fígado 3 1. Eritrócitos cobertos de anticorpos ou irregulares. 2. Fagocitose 3. Degradação nos lisosomas MACRÓFAGO 4. Une-se à haptoglobina ou Depuração pelo fígado 5. Se diminui a haptoglobina, a hemoglobina excreta-se pelos rins (hemoglobinúria). HEPATÓCITO 4. Hemoglobina intracelular 5. Biliverdina 6. Depuração da bilirrubina pelo fígado A hemólise extravascular é muito mais evidente nos doentes tratados com anti. C 5, mas observa-se em todos ao diagnóstico (8% dos doentes têm um TAD+ para complemento, de forma débil). É conveniente registá-la para as terapias que vão bloquear C 3. 4 ERI, eritrócitos; HPN, hemoglobinúria paroxística nocturna. 1. Hillmen P, et al. British Journal of Haematology. 2013; 162: 62– 73. 2. Noronha SA. Pediatr Rev. 2016; 37(6): 235 -246. 3. Dhaliwal G, et al. Am Fam Phys. 2004; 69(11): 2599 -2606. 4. Notario R, et al. Semin hematol. 2018; 55(3): 130 -135 13
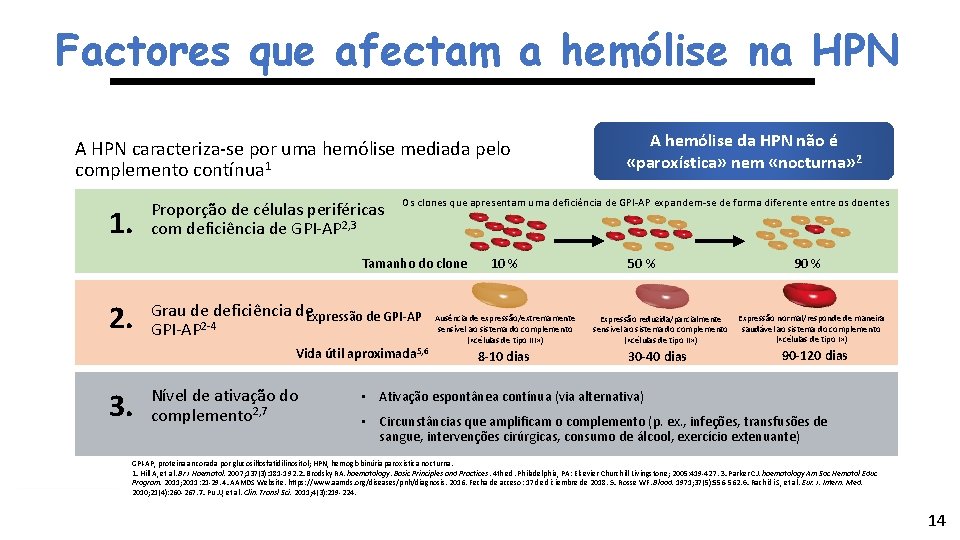
Factores que afectam a hemólise na HPN A HPN caracteriza-se por uma hemólise mediada pelo complemento contínua 1 1. Proporção de células periféricas com deficiência de GPI-AP 2, 3 Os clones que apresentam uma deficiência de GPI-AP expandem-se de forma diferente entre os doentes Tamanho do clone 2. Grau de deficiência de Expressão de GPI-AP 2 -4 Vida útil aproximada 5, 6 3. Nível de ativação do complemento 2, 7 A hemólise da HPN não é «paroxística» nem «nocturna» 2 10 % Ausência de expressão/extremamente sensível ao sistema do complemento ( «células de tipo III» ) 8 -10 dias 50 % 90 % Expressão normal/responde de maneira Expressão reduzida/parcialmente sensivel ao sistema do complemento saudável ao sistema do complemento ( «células de tipo I» ) ( «células de tipo II» ) 30 -40 dias 90 -120 dias • Ativação espontânea contínua (via alternativa) • Circunstâncias que amplificam o complemento (p. ex. , infeções, transfusões de sangue, intervenções cirúrgicas, consumo de álcool, exercício extenuante) GPI-AP, proteína ancorada por glucosilfosfatidilinositol; HPN, hemoglobinúria paroxística nocturna. 1. Hill A, et al. Br J Haematol. 2007; 137(3): 181 -192. 2. Brodsky RA. haematology: Basic Principles and Practices. 4 th ed. Philadelphia, PA: Elsevier Churchill Livingstone; 2005: 419 -427. 3. Parker CJ. haematology Am Soc Hematol Educ Program. 2011; 2011: 21 -29. 4. AAMDS Website. https: //www. aamds. org/diseases/pnh/diagnosis. 2016. Fecha de acceso: 17 de diciembre de 2018. 5. Rosse WF. Blood. 1971; 37(5): 556 -562. 6. Rachidi S, et al. Eur. J. Intern. Med. 2010; 21(4): 260 -267. 7. Pu JJ, et al. Clin. Transl Sci. 2011; 4(3): 219 -224. 14

CONCLUSÕES -A HPN é o resultado de uma mutação somática no gene PIG-A que impede a síntese de ancoragens por GPI, o que provoca uma carência das proteínas inibidoras do complemento CD 55 e CD 59 na superfície das células afectadas 1 -Normalmente, o CD 55 inibe a cascata do complemento nas etapas críticas das convertases de C 3 e C 5, enquanto o CD 59 bloqueia a formação do CAM na superfície celular 2 -As células com deficiência de proteínas ancoradas por GPI sobrevivem preferencialmente ao ataque imunológico no contexto de uma disfunção medular 3, 4 -O baixo número ou ausência de proteínas inibidoras do complemento CD 55 e CD 59 na superfície das células afetadas causa uma ativação descontrolada do complemento 1 -A ativação descontrolada do complemento provoca hemólise intravascular crónica, que liberta hemoglobina livre 1, 5 -A hemoglobina livre sequestra e reduz o óxido nítrico endógeno, o que dá lugar a muitas das complicações clínicas potencialmente mortais da HPN 5 CAM; complexo de ataque à membrana; GPI, glucosilfosfatidilinositol; HPN, hemoglobinúria paroxística nocturna; PIG-A, gene de classe A de complementação do fosfatidilinositol glucano. 1. Brodsky RA. haematology - Basic Principles and Practices. 4 th ed. Philadelphia, PA: Elsevier Churchill Livingstone; 2005: 419 -427. 2. Kelly R, et al. Ther Clin Risk Manag. 2009; 5: 911 -921. 3. Hill A, et al. Br J Haematol. 2007; 137(3): 181 -192. 4. Hill A, et al. Nat Rev Dis Primers. 2017; 3(17028): 1 -14. 5. Rother RP, et al. JAMA. 2005; 293(13): 1653 -1662. 15
- Slides: 15