Curso conceito A Reviso de orgnica Vtor Diniz










- Slides: 37

Curso conceito A Revisão de orgânica Vítor Diniz

Hidrocarbonetos: subdivisão e nomenclatura �Subdivisões dos hidrocarbonetos Para facilitar o estudo e a nomenclatura dos hidrocarbonetos, eles são divididos em subgrupos ou classes, conforme tabela a seguir:

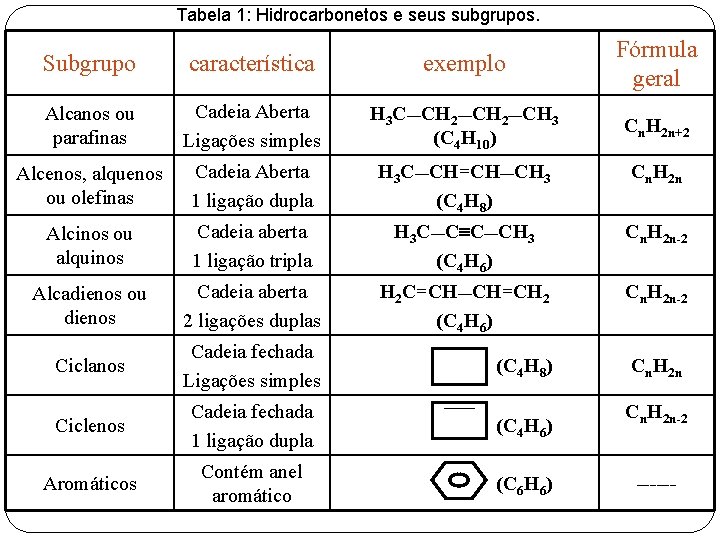
Tabela 1: Hidrocarbonetos e seus subgrupos. Subgrupo característica exemplo Fórmula geral Alcanos ou parafinas Cadeia Aberta Ligações simples H 3 C—CH 2—CH 3 (C 4 H 10) Cn. H 2 n+2 Alcenos, alquenos ou olefinas Cadeia Aberta 1 ligação dupla H 3 C—CH=CH—CH 3 (C 4 H 8) Cn. H 2 n Alcinos ou alquinos Cadeia aberta 1 ligação tripla H 3 C—C C—CH 3 (C 4 H 6) Cn. H 2 n-2 Alcadienos ou dienos Cadeia aberta 2 ligações duplas H 2 C=CH—CH=CH 2 (C 4 H 6) Cn. H 2 n-2 Ciclanos Cadeia fechada Ligações simples (C 4 H 8) Cn. H 2 n Ciclenos Cadeia fechada 1 ligação dupla (C 4 H 6) Aromáticos Contém anel aromático (C 6 H 6) Cn. H 2 n-2 ------

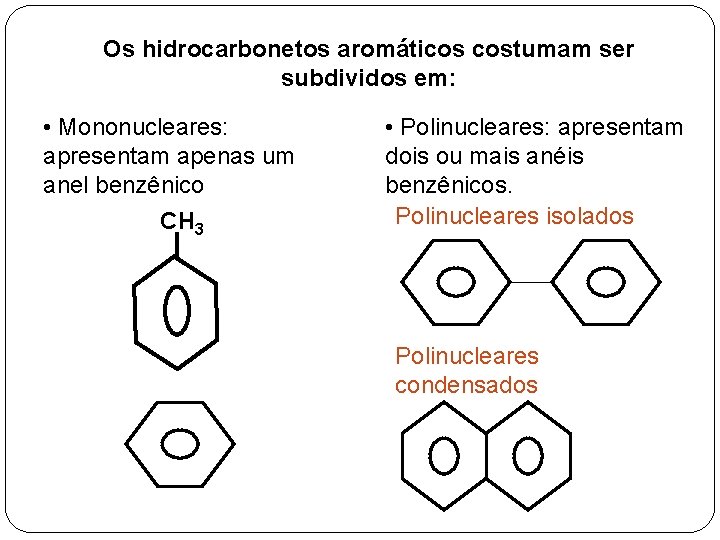
Os hidrocarbonetos aromáticos costumam ser subdividos em: • Mononucleares: apresentam apenas um anel benzênico CH 3 • Polinucleares: apresentam dois ou mais anéis benzênicos. Polinucleares isolados Polinucleares condensados

Nomenclatura de Hidrocarbonetos de cadeia não-ramificada Os químicos elaboraram um método lógico para dar nome aos compostos orgânicos, pois é impossível decorar tantos nomes diferentes. A nomenclatura de compostos orgânicos segue as regras elaboradas pela IUPAC (União Internacional de Química Pura e Aplicada). Segundo essas regras, o nome de um composto orgânico é formado unindo três fragmentos: PREFIXO + INFIXO + SUFIXO

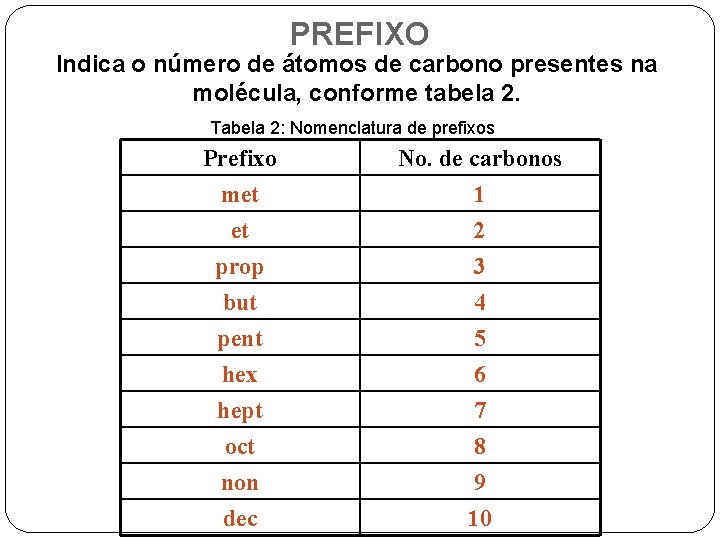
PREFIXO Indica o número de átomos de carbono presentes na molécula, conforme tabela 2. Tabela 2: Nomenclatura de prefixos Prefixo met et prop No. de carbonos 1 2 3 but pent hex hept oct non 4 5 6 7 8 9 dec 10

INFIXO Indica o tipo de ligação entre os átomos de carbono, conforme tabela 3 Tabela 3: Nomenclatura de infixos Infixo Tipo de ligação an Ligação simples en Ligação dupla in Ligação tripla dien 2 ligações duplas

SUFIXO Indica o grupo de substâncias orgânicas ou função orgânica a que o composto pertence. Tabela 4: Nomenclatura para sufixos Sufixo Indica que o composto é um o Hidrocarboneto ol al Álcool Aldeído ona oico Cetona Ácido carboxílico

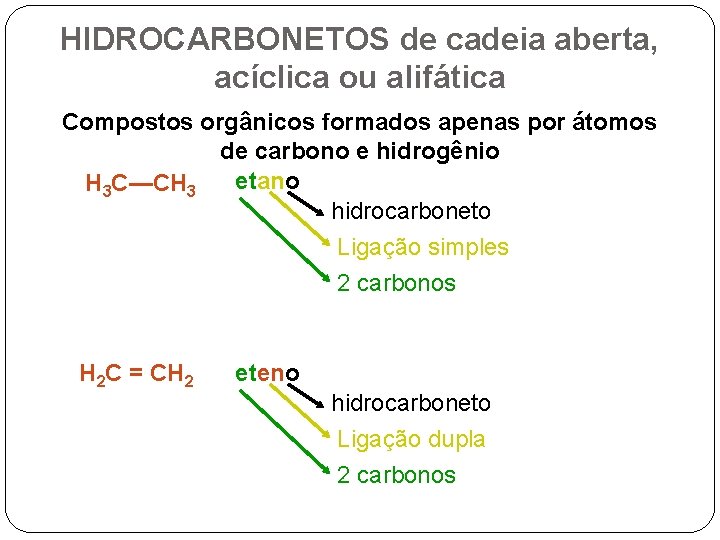
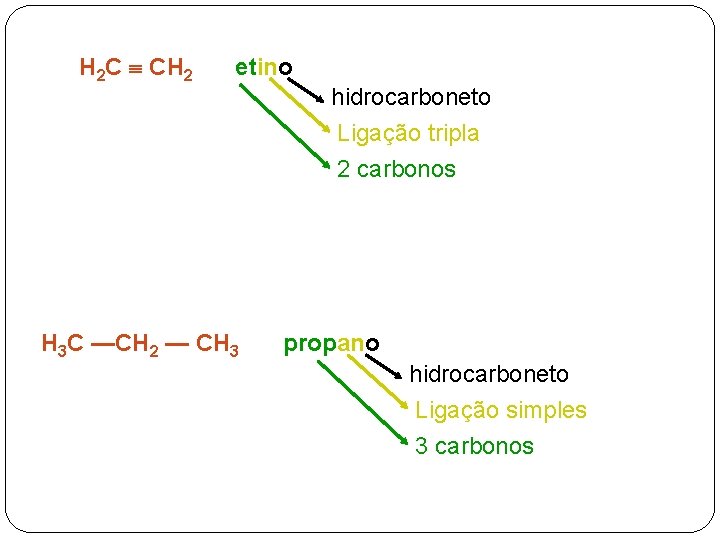
HIDROCARBONETOS de cadeia aberta, acíclica ou alifática Compostos orgânicos formados apenas por átomos de carbono e hidrogênio etano H 3 C—CH 3 hidrocarboneto Ligação simples 2 carbonos H 2 C = CH 2 eteno hidrocarboneto Ligação dupla 2 carbonos

H 2 C CH 2 etino hidrocarboneto Ligação tripla 2 carbonos H 3 C —CH 2 — CH 3 propano hidrocarboneto Ligação simples 3 carbonos

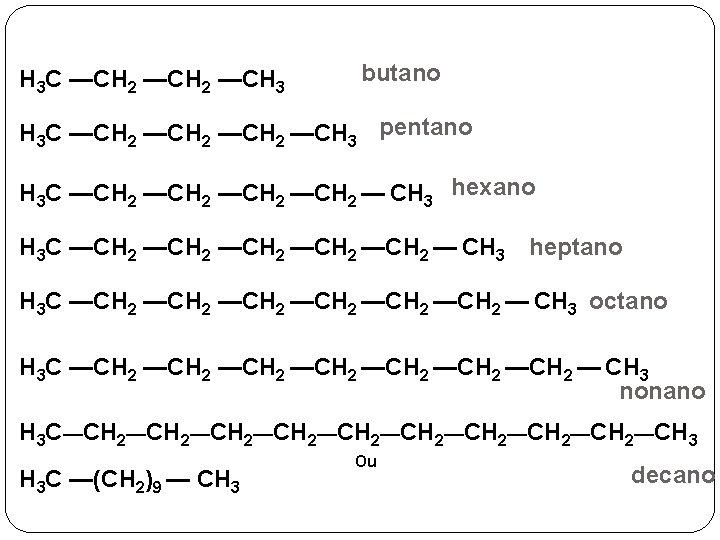
H 3 C —CH 2 —CH 3 butano H 3 C —CH 2 —CH 3 pentano H 3 C —CH 2 — CH 3 hexano H 3 C —CH 2 —CH 2 — CH 3 heptano H 3 C —CH 2 —CH 2 — CH 3 octano H 3 C —CH 2 —CH 2 — CH 3 nonano H 3 C—CH 2—CH 2—CH 2—CH 3 H 3 C —(CH 2)9 — CH 3 Ou decano

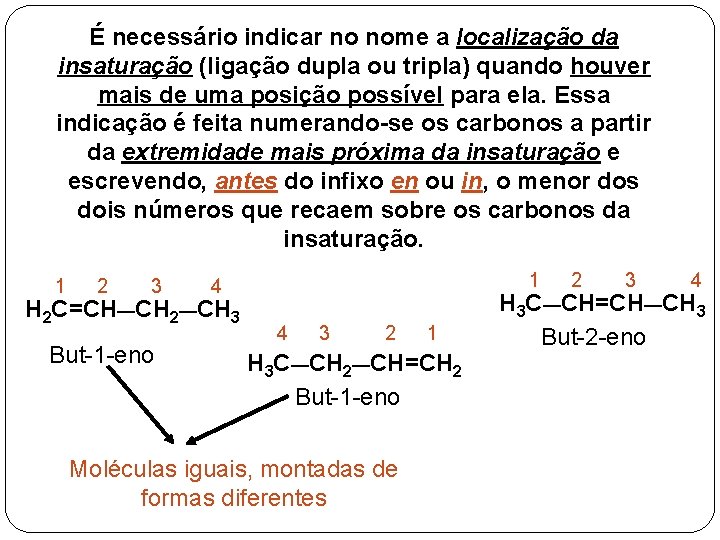
É necessário indicar no nome a localização da insaturação (ligação dupla ou tripla) quando houver mais de uma posição possível para ela. Essa indicação é feita numerando-se os carbonos a partir da extremidade mais próxima da insaturação e escrevendo, antes do infixo en ou in, o menor dos dois números que recaem sobre os carbonos da insaturação. 1 2 3 H 2 C=CH—CH 2—CH 3 But-1 -eno 1 4 4 3 2 1 H 3 C—CH 2—CH=CH 2 But-1 -eno Moléculas iguais, montadas de formas diferentes 2 3 4 H 3 C—CH=CH—CH 3 But-2 -eno

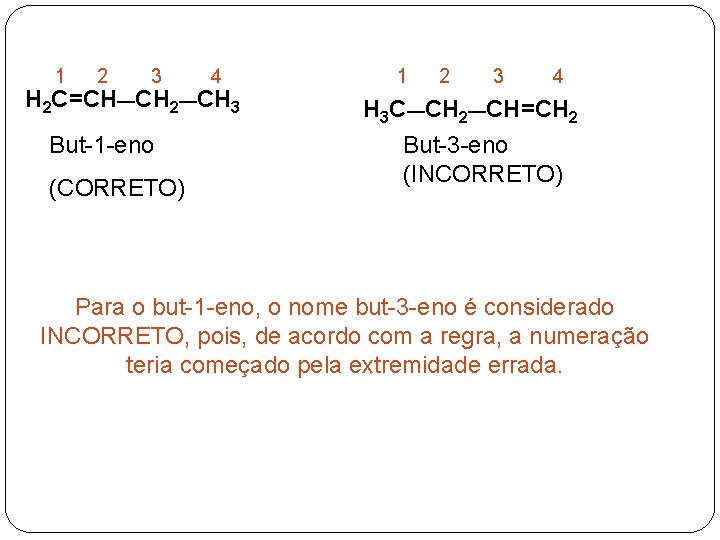
1 2 3 4 H 2 C=CH—CH 2—CH 3 But-1 -eno (CORRETO) 1 2 3 4 H 3 C—CH 2—CH=CH 2 But-3 -eno (INCORRETO) Para o but-1 -eno, o nome but-3 -eno é considerado INCORRETO, pois, de acordo com a regra, a numeração teria começado pela extremidade errada.

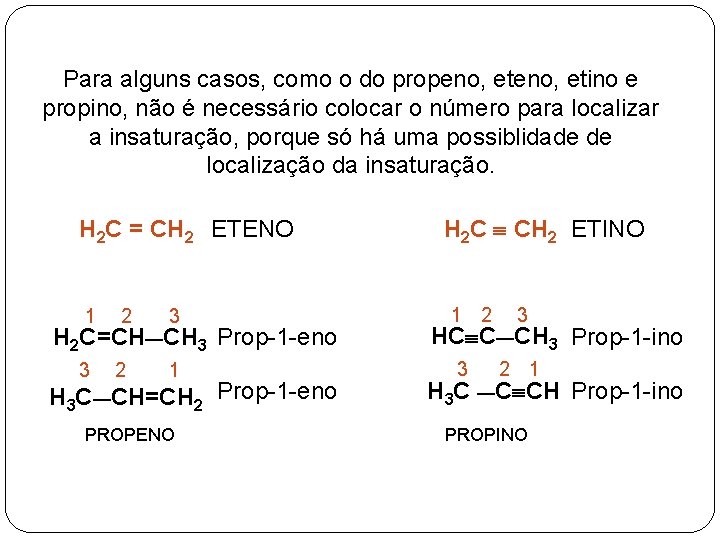
Para alguns casos, como o do propeno, etino e propino, não é necessário colocar o número para localizar a insaturação, porque só há uma possiblidade de localização da insaturação. H 2 C = CH 2 ETENO 1 2 3 3 2 1 H 2 C=CH—CH 3 Prop-1 -eno H 3 C—CH=CH 2 Prop-1 -eno PROPENO H 2 C CH 2 ETINO 1 2 3 HC C—CH 3 Prop-1 -ino 3 2 1 H 3 C —C CH Prop-1 -ino PROPINO

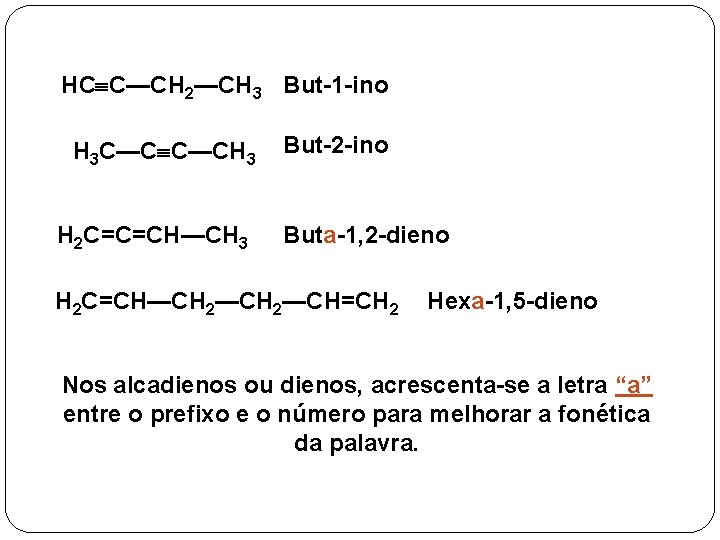
HC C—CH 2—CH 3 But-1 -ino H 3 C—C C—CH 3 H 2 C=C=CH—CH 3 But-2 -ino Buta-1, 2 -dieno H 2 C=CH—CH 2—CH=CH 2 Hexa-1, 5 -dieno Nos alcadienos ou dienos, acrescenta-se a letra “a” entre o prefixo e o número para melhorar a fonética da palavra.

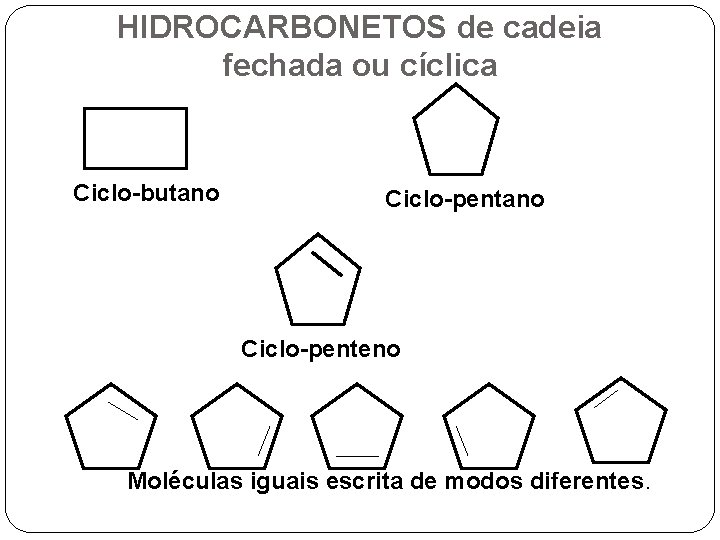
HIDROCARBONETOS de cadeia fechada ou cíclica Ciclo-butano Ciclo-penteno Moléculas iguais escrita de modos diferentes.

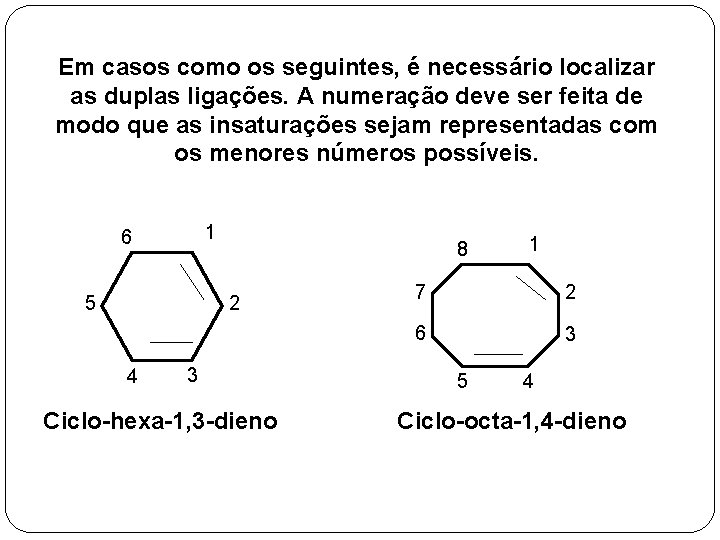
Em casos como os seguintes, é necessário localizar as duplas ligações. A numeração deve ser feita de modo que as insaturações sejam representadas com os menores números possíveis. 1 6 5 8 2 4 3 Ciclo-hexa-1, 3 -dieno 1 7 2 6 3 5 4 Ciclo-octa-1, 4 -dieno

Uma visão geral das reações orgânicas Tópicos 1. Rupturas de ligações 2. Classificação dos reagentes 3. Mecanismos de reações orgânicas 4. Classificação das reações orgânicas 5. Diagrama de energia e estado de transição 6. Reações de oxi-redução de orgânicos

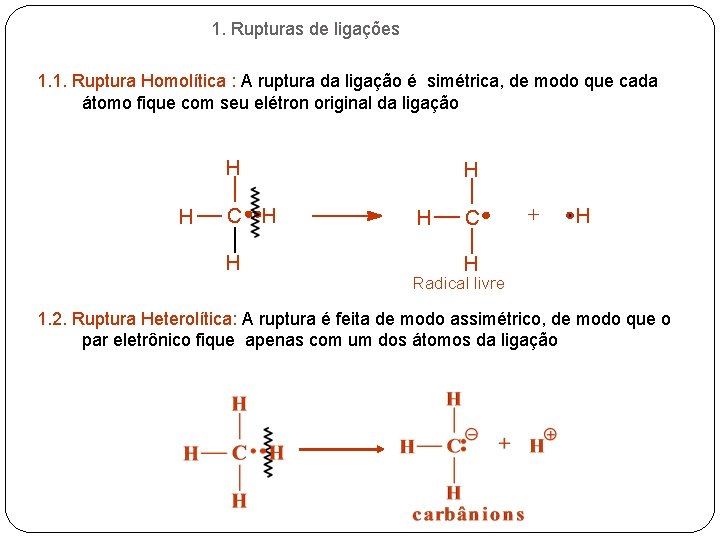
1. Rupturas de ligações 1. 1. Ruptura Homolítica : A ruptura da ligação é simétrica, de modo que cada átomo fique com seu elétron original da ligação H H C + H H Radical livre 1. 2. Ruptura Heterolítica: A ruptura é feita de modo assimétrico, de modo que o par eletrônico fique apenas com um dos átomos da ligação

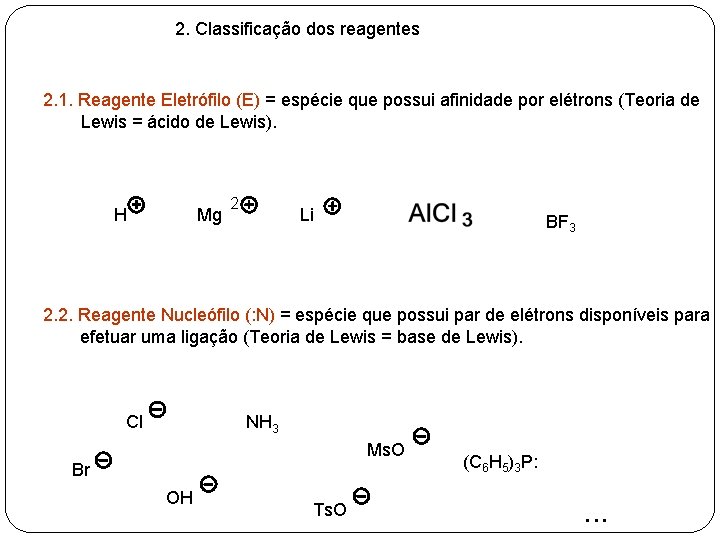
2. Classificação dos reagentes 2. 1. Reagente Eletrófilo (E) = espécie que possui afinidade por elétrons (Teoria de Lewis = ácido de Lewis). H Mg 2 Li BF 3 2. 2. Reagente Nucleófilo (: N) = espécie que possui par de elétrons disponíveis para efetuar uma ligação (Teoria de Lewis = base de Lewis). Cl NH 3 Ms. O Br OH Ts. O (C 6 H 5)3 P: . . .

3. Mecanismos de reações orgânicas É a descrição das várias etapas pelas quais uma reação passa, como a ruptura das ligações, os ataques eletrofílicos e nucleofílicos ao reagente orgânico, a formação de novas ligações e de compostos intermediários

3. 1. Mecanismo via radicais Características dos radicais • Ocorrem em moléculas apolares ou com baixa diferença de eletronegatividade • São eletronicamente neutros • Muito reativos • As reações radicalares não são muito comuns quando comparado a reações polares

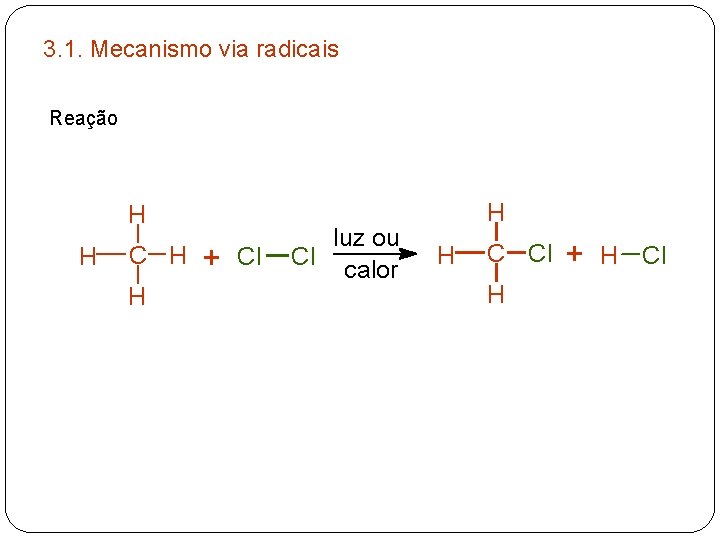
3. 1. Mecanismo via radicais Reação H H C H H + Cl luz ou Cl calor H H C Cl H + H Cl

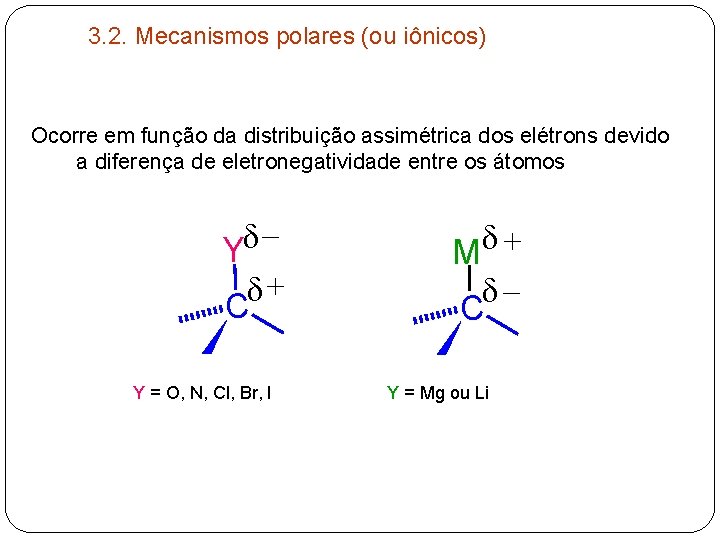
3. 2. Mecanismos polares (ou iônicos) Ocorre em função da distribuição assimétrica dos elétrons devido a diferença de eletronegatividade entre os átomos _ Yd d+ C Y = O, N, Cl, Br, I Md + _ d C Y = Mg ou Li

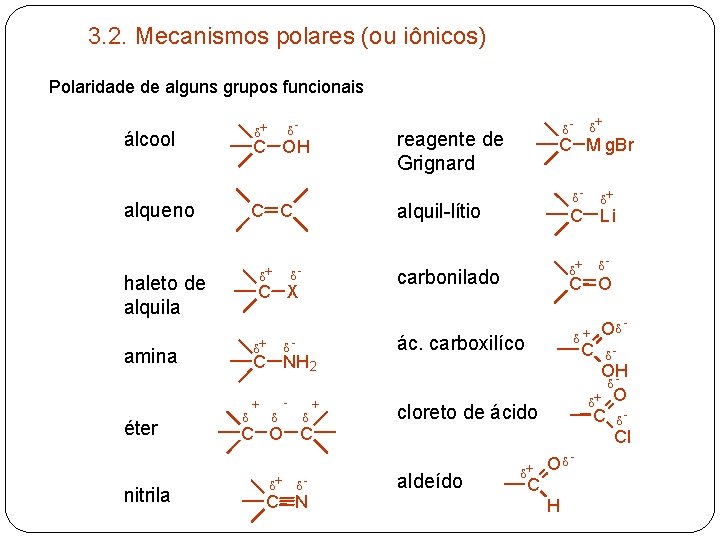
3. 2. Mecanismos polares (ou iônicos) Polaridade de alguns grupos funcionais d+ álcool d+ d amina d - C NH 2 d + d d d + d - C N d - C O d+ ác. carboxilíco C d+ Od d - - OH d d+ O C d. Cl cloreto de ácido aldeído d+ d+ C O C d+ - C Li carbonilado C X d+ C M g. Br alquil-lítio - d+ - d reagente de Grignard C C haleto de alquila nitrila - C OH alqueno éter d Od C H -

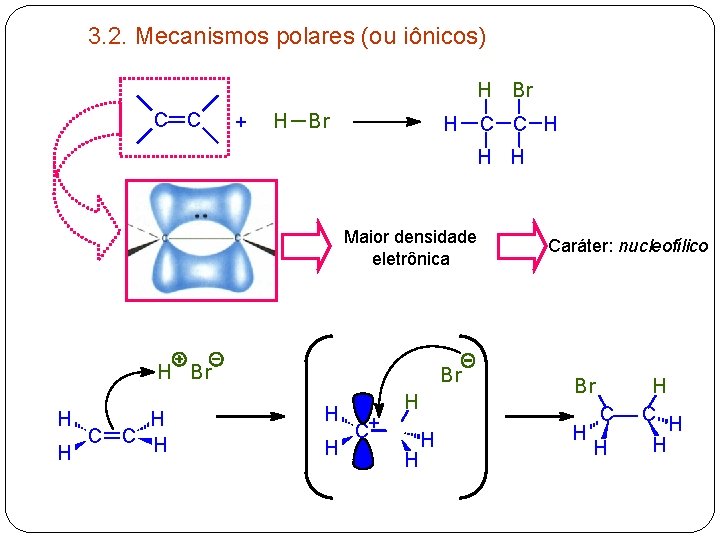
3. 2. Mecanismos polares (ou iônicos) H Br C C + H Br H C C H H H Maior densidade eletrônica H Br H H C C H H Br H H C+ H H H Caráter: nucleofílico Br H C H H

4. Classificação das reações orgânicas 4. 1. Reações de adição 4. 2. Reações de substituição 4. 3. Reações de eliminação 4. 4. Reações de rearranjo

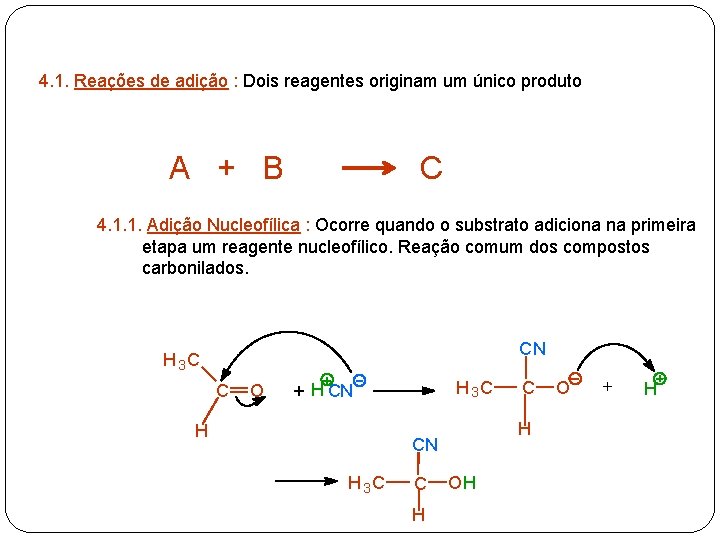
4. 1. Reações de adição : Dois reagentes originam um único produto A + B C 4. 1. 1. Adição Nucleofílica : Ocorre quando o substrato adiciona na primeira etapa um reagente nucleofílico. Reação comum dos compostos carbonilados. CN H 3 C C O H 3 C + H CN H 3 C C H C OH O + H

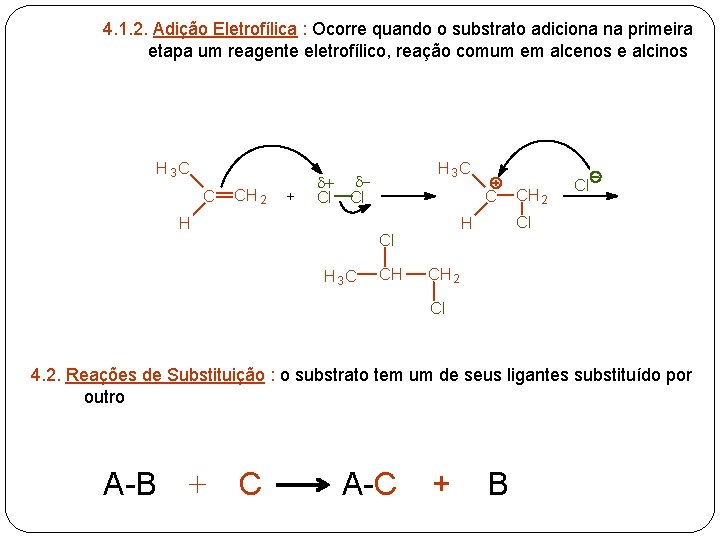
4. 1. 2. Adição Eletrofílica : Ocorre quando o substrato adiciona na primeira etapa um reagente eletrofílico, reação comum em alcenos e alcinos H 3 C C CH 2 + d+ Cl H 3 C d. Cl H C H 3 C CH Cl Cl H Cl CH 2 Cl 4. 2. Reações de Substituição : o substrato tem um de seus ligantes substituído por outro A-B + C A-C + B

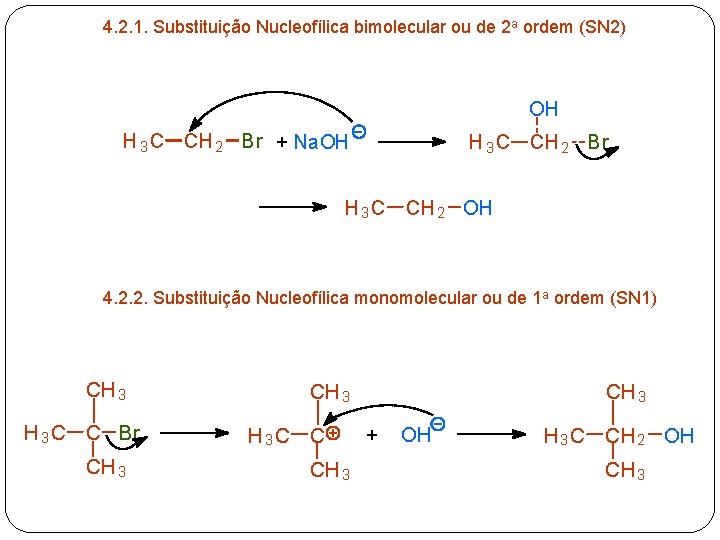
4. 2. 1. Substituição Nucleofílica bimolecular ou de 2 a ordem (SN 2) OH H 3 C CH 2 Br + Na. OH H 3 C CH 2 Br H 3 C CH 2 OH 4. 2. 2. Substituição Nucleofílica monomolecular ou de 1 a ordem (SN 1) CH 3 C C Br CH 3 H 3 C C CH 3 + OH H 3 C CH 2 OH CH 3

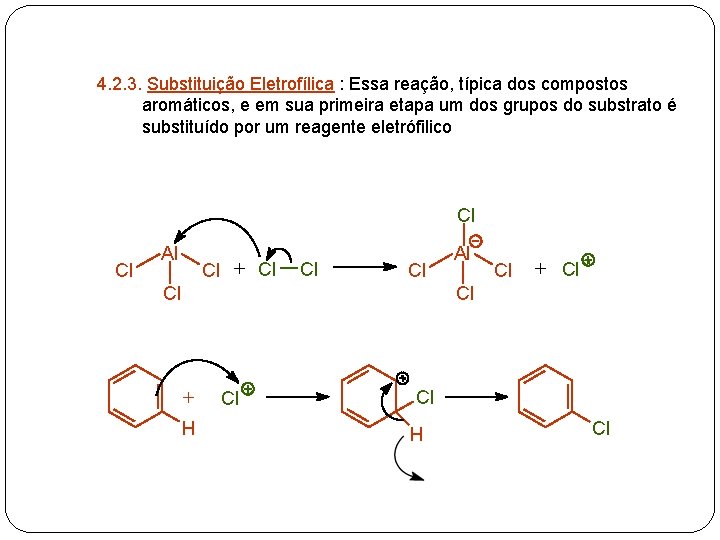
4. 2. 3. Substituição Eletrofílica : Essa reação, típica dos compostos aromáticos, e em sua primeira etapa um dos grupos do substrato é substituído por um reagente eletrófilico Cl Cl Al Cl + Cl Cl Cl + H Cl Cl H Cl

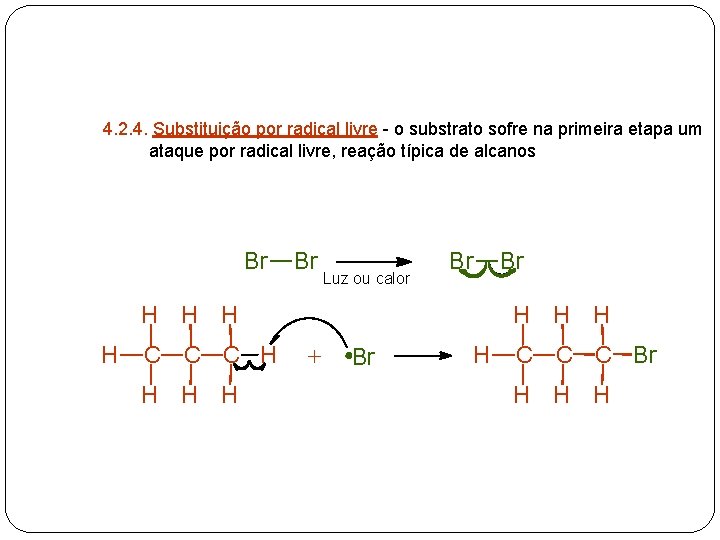
4. 2. 4. Substituição por radical livre - o substrato sofre na primeira etapa um ataque por radical livre, reação típica de alcanos Br H H C C C H H Br + Luz ou calor Br Br H H H C C C Br H H H

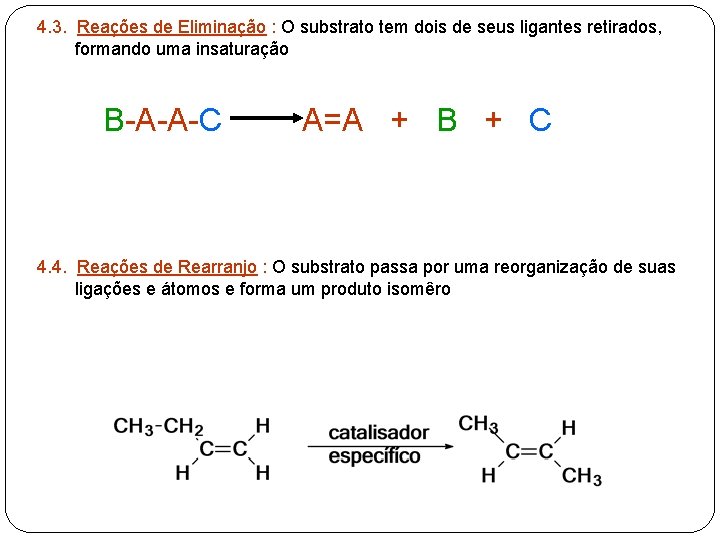
4. 3. Reações de Eliminação : O substrato tem dois de seus ligantes retirados, formando uma insaturação B-A-A-C A=A + B + C 4. 4. Reações de Rearranjo : O substrato passa por uma reorganização de suas ligações e átomos e forma um produto isomêro

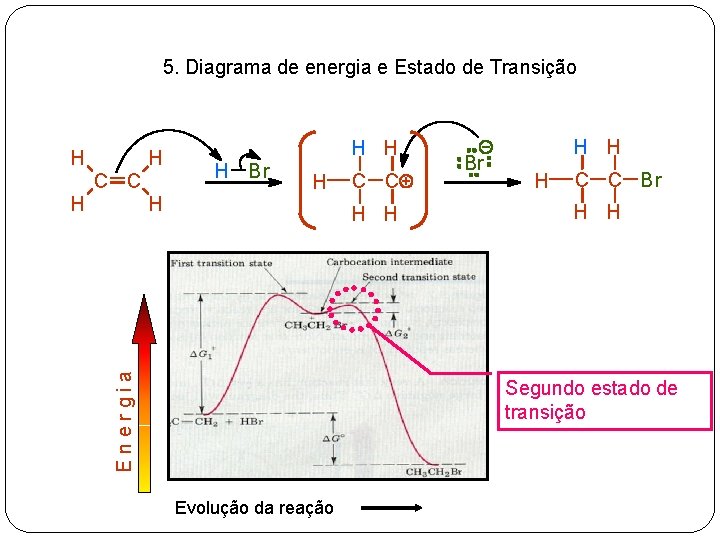
5. Diagrama de energia e Estado de Transição H H C C H H Br H C C H H Energia H H H Br H H H C C Br H H Segundo estado de transição Evolução da reação

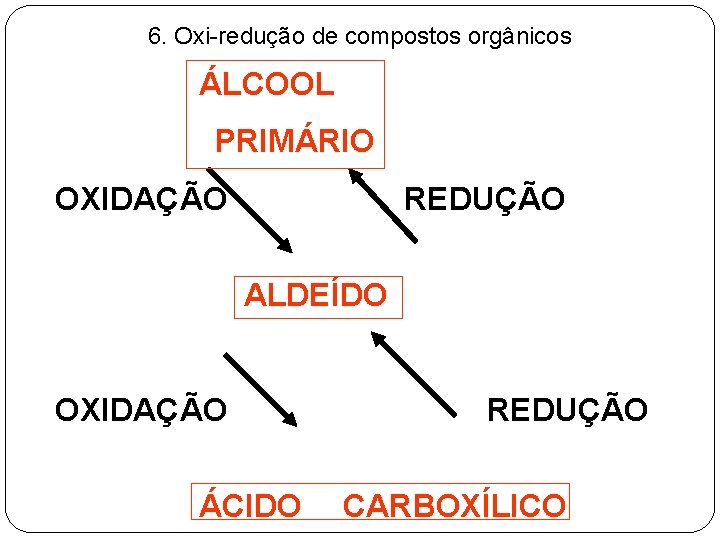
6. Oxi-redução de compostos orgânicos ÁLCOOL PRIMÁRIO OXIDAÇÃO REDUÇÃO ALDEÍDO OXIDAÇÃO ÁCIDO REDUÇÃO CARBOXÍLICO

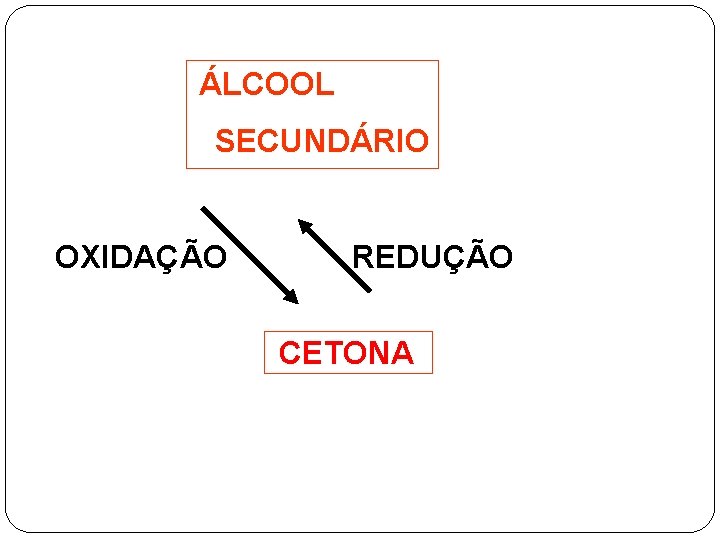
ÁLCOOL SECUNDÁRIO OXIDAÇÃO REDUÇÃO CETONA

Referências Bibliográficas Mc. Murry, J. Química orgânica, 4ª ed. Livros Técnicos e Científicos Editora S. A. , 1996. Mc. Murry, J. Organic chemistry, 3ª ed. Books/ Cole Publishing Company, 1992 Solomons, T. W. G. Organic Chemistry, John Wiley & Sons, Inc. , 1996.