Curs pentru specializarea BIOLOGIE anul I semestrul al

Curs pentru specializarea BIOLOGIE anul I – semestrul al II-lea Şef lucrări dr. ing. Alexa Irina-Claudia
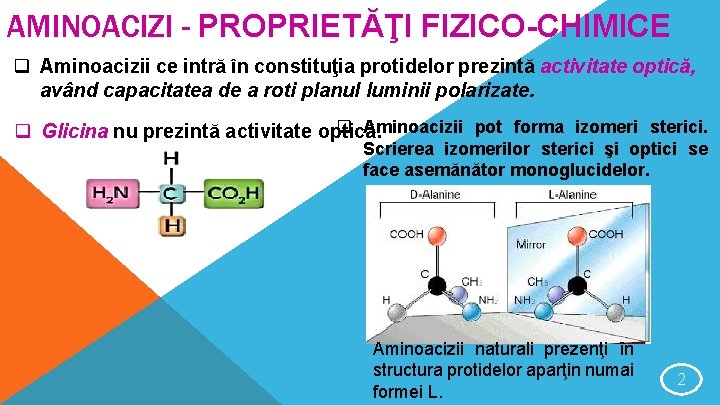
AMINOACIZI - PROPRIETĂŢI FIZICO-CHIMICE q Aminoacizii ce intră în constituţia protidelor prezintă activitate optică, având capacitatea de a roti planul luminii polarizate. q Aminoacizii pot forma izomeri sterici. q Glicina nu prezintă activitate optică. Scrierea izomerilor sterici şi optici se face asemănător monoglucidelor. Aminoacizii naturali prezenţi în structura protidelor aparţin numai formei L. 2
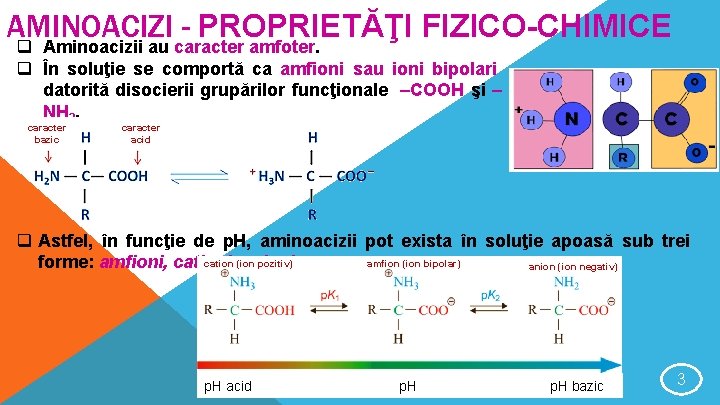
AMINOACIZI PROPRIETĂŢI FIZICO-CHIMICE q Aminoacizii au caracter amfoter. q În soluţie se comportă ca amfioni sau ioni bipolari datorită disocierii grupărilor funcţionale –COOH şi – NH 2. caracter bazic caracter acid q Astfel, în funcţie de p. H, aminoacizii pot exista în soluţie apoasă sub trei amfion (ion bipolar) cation (ion pozitiv) forme: amfioni, cationi, anioni. anion (ion negativ) p. H acid p. H bazic 3

AMINOACIZI - PROPRIETĂŢI CHIMICE q Proprietăţile chimice ale aminoacizilor sunt determinate de: - prezenţa grupării –COOH - prezenţa grupării –NH 2 - prezenţa altor grupări funcţionale (–OH, –SH) - prezenţa simultană a celor două grupări funcţionale – COOH şi –NH 2 REACŢIA DE CONDENSARE INTERMOLECULARĂ v Doi sau mai mulţi aminoacizi reacţionează între ei cu eliminare intermoleculară de apă între o grupare –COOH a unui aminoacid şi o grupare –NH 2 a altui aminoacid. v Legătura peptidică formată –CO-NH- stă la baza structurii peptidelor, 4 polipeptidelor şi proteinelor.
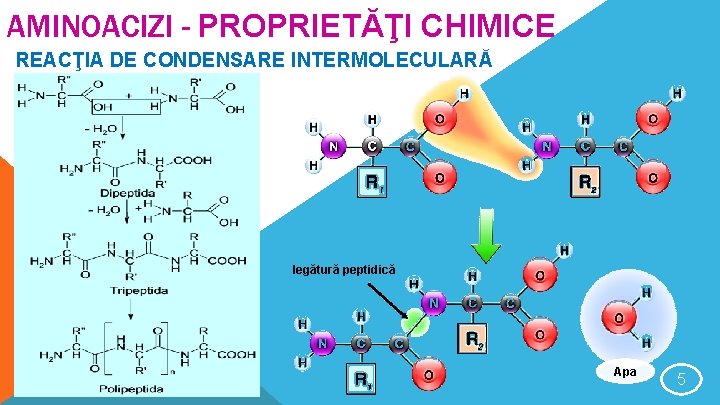
AMINOACIZI - PROPRIETĂŢI CHIMICE REACŢIA DE CONDENSARE INTERMOLECULARĂ legătură peptidică Apa 5
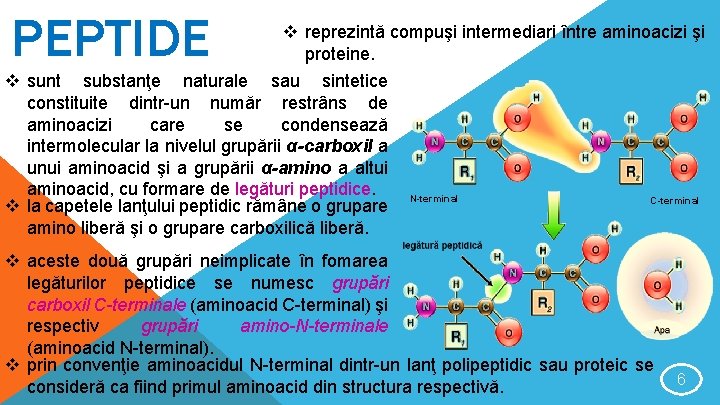
PEPTIDE v reprezintă compuşi intermediari între aminoacizi şi proteine. v sunt substanţe naturale sau sintetice constituite dintr-un număr restrâns de aminoacizi care se condensează intermolecular la nivelul grupării α-carboxil a unui aminoacid şi a grupării α-amino a altui aminoacid, cu formare de legături peptidice. N-terminal C-terminal v la capetele lanţului peptidic rămâne o grupare amino liberă şi o grupare carboxilică liberă. v aceste două grupări neimplicate în fomarea legăturilor peptidice se numesc grupări carboxil C-terminale (aminoacid C-terminal) şi respectiv grupări amino-N-terminale (aminoacid N-terminal). v prin convenţie aminoacidul N-terminal dintr-un lanţ polipeptidic sau proteic se consideră ca fiind primul aminoacid din structura respectivă. 6

PEPTIDE v Denumirea peptidelor se formează din numele radicalilor aminoacizilor constituenţi, cu excepţia aminoacidului care gruparea carboxilică liberă, ultimul din lanţul polipeptidic. v Denumirea radicalului se formează din numele aminoacidului înlocuind terminaţia cu sufixul il. v Exemplu: peptida formată din alanină, leucină, valină, glicocol şi arginină se va numi: alanil-leucil-valil-glicil-arginină. v Mai putem scrie şi folosind simbolurile aminoacizilor care au notaţie internaţională, formată din primele trei litere ale numelui acestuia. v Exemplu: H-Ala-Leu-Val-Gli-Arg-OH. În faţa litera H reprezintă gruparea –NH 2 liberă, iar la sfârşit OH reprezintă gruparea –COOH 7

PROTEINE v reprezintă substanţe complexe cu caracter macromolecular şi cu un înalt grad de organizare structurală, sunt alcătuite numai din aminoacizi, având mase moleculare de 1 x 103 – 1 x 105. v se caracterizează printr-o mare diversitate structurală determinată de: - numărul aminoacizilor constituenţi; - tipurile aminoacizilor constituenţi; - secvenţa aminoacizilor componenţi; - organizarea spaţială configuraţională a macromoleculei respective. 8
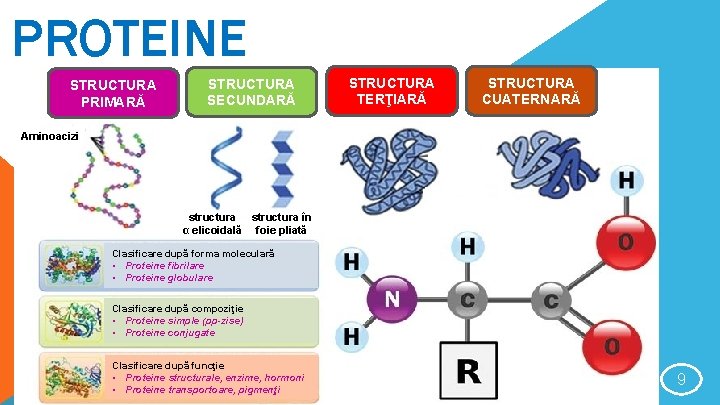
PROTEINE STRUCTURA PRIMARĂ STRUCTURA SECUNDARĂ STRUCTURA TERŢIARĂ STRUCTURA CUATERNARĂ Aminoacizi structura în α elicoidală foie pliată Clasificare după forma moleculară • Proteine fibrilare • Proteine globulare Clasificare după compoziţie • Proteine simple (pp-zise) • Proteine conjugate Clasificare după funcţie • Proteine structurale, enzime, hormoni • Proteine transportoare, pigmenţi 9
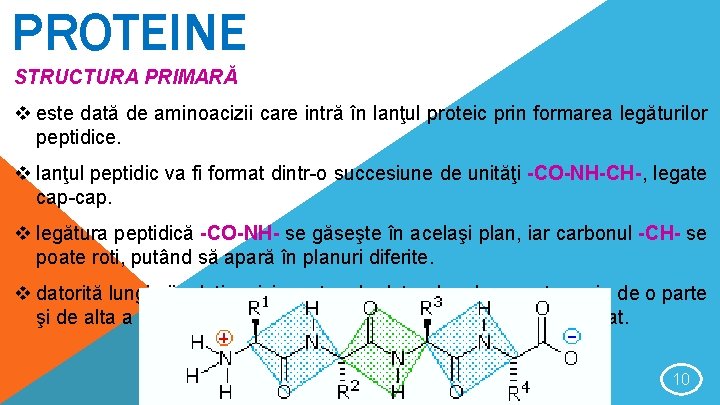
PROTEINE STRUCTURA PRIMARĂ v este dată de aminoacizii care intră în lanţul proteic prin formarea legăturilor peptidice. v lanţul peptidic va fi format dintr-o succesiune de unităţi -CO-NH-CH-, legate cap-cap. v legătura peptidică -CO-NH- se găseşte în acelaşi plan, iar carbonul -CH- se poate roti, putând să apară în planuri diferite. v datorită lungimii relativ mici a catenelor laterale, ele se pot aranja de o parte şi de alta a lanţului proteic, astfel că lanţul proteic nu este ramificat. 10
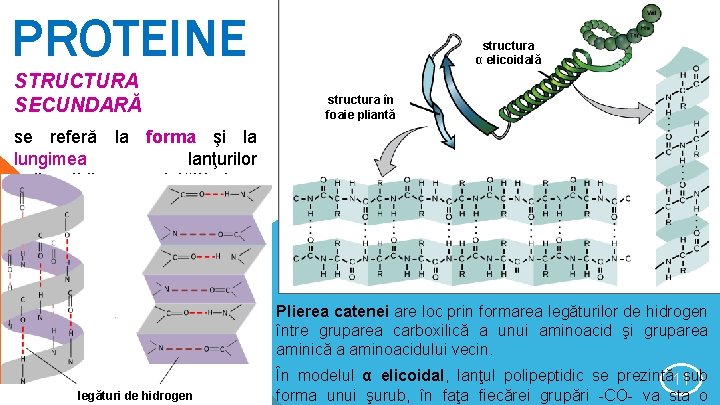
PROTEINE STRUCTURA SECUNDARĂ structura α elicoidală structura în foaie pliantă se referă la forma şi la lungimea lanţurilor polipeptidice, proprietăţi induse de legăturile de hidrogen. Plierea catenei are loc prin formarea legăturilor de hidrogen între gruparea carboxilică a unui aminoacid şi gruparea aminică a aminoacidului vecin. legături de hidrogen În modelul α elicoidal, lanţul polipeptidic se prezintă11 sub forma unui şurub, în faţa fiecărei grupări -CO- va sta o
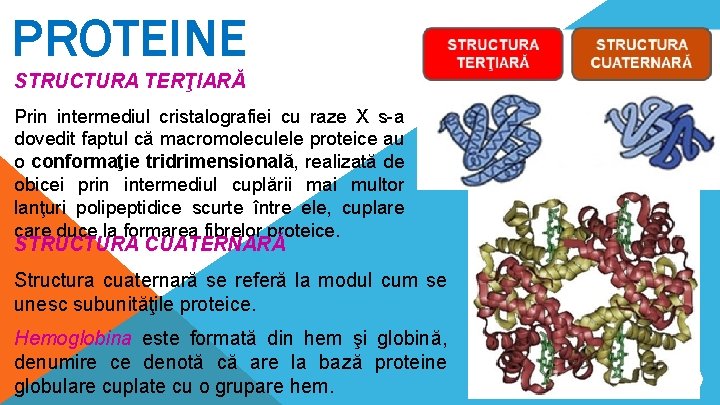
PROTEINE STRUCTURA TERŢIARĂ Prin intermediul cristalografiei cu raze X s-a dovedit faptul că macromoleculele proteice au o conformaţie tridrimensională, realizată de obicei prin intermediul cuplării mai multor lanţuri polipeptidice scurte între ele, cuplare care duce la formarea fibrelor proteice. STRUCTURA CUATERNARĂ Structura cuaternară se referă la modul cum se unesc subunităţile proteice. Hemoglobina este formată din hem şi globină, denumire ce denotă că are la bază proteine globulare cuplate cu o grupare hem. 12
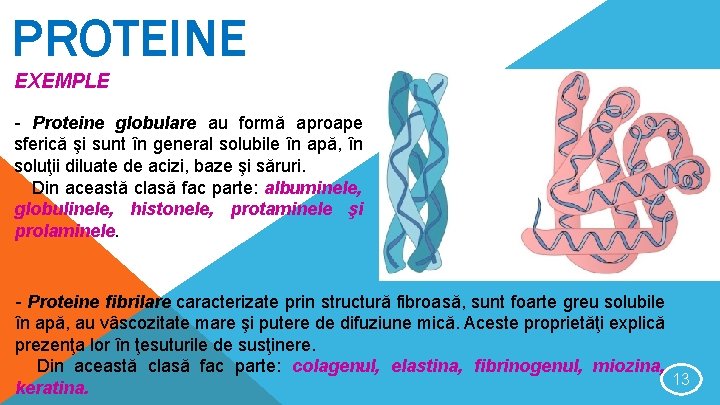
PROTEINE EXEMPLE - Proteine globulare au formă aproape sferică şi sunt în general solubile în apă, în soluţii diluate de acizi, baze şi săruri. Din această clasă fac parte: albuminele, globulinele, histonele, protaminele şi prolaminele. - Proteine fibrilare caracterizate prin structură fibroasă, sunt foarte greu solubile în apă, au vâscozitate mare şi putere de difuziune mică. Aceste proprietăţi explică prezenţa lor în ţesuturile de susţinere. Din această clasă fac parte: colagenul, elastina, fibrinogenul, miozina, 13 keratina.
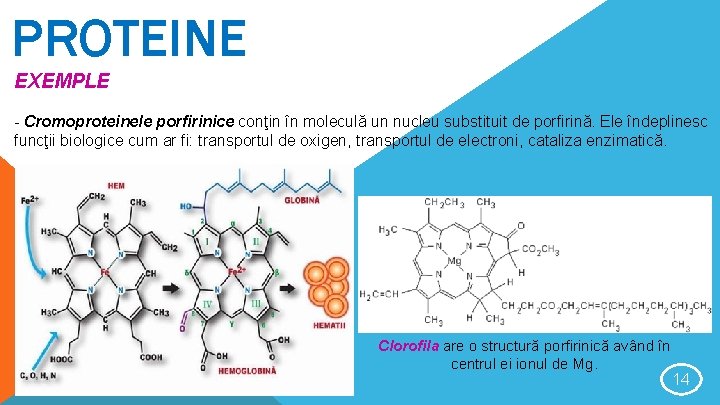
PROTEINE EXEMPLE - Cromoproteinele porfirinice conţin în moleculă un nucleu substituit de porfirină. Ele îndeplinesc funcţii biologice cum ar fi: transportul de oxigen, transportul de electroni, cataliza enzimatică. Clorofila are o structură porfirinică având în centrul ei ionul de Mg. 14
- Slides: 14