CUPRUL Profesor Ion Fevronia Scoala cu cls IVIII




















- Slides: 21

CUPRUL Profesor Ion Fevronia Scoala cu cls. I-VIII nr. 1 Voluntari

OBIECTE VECHI DIN CUPRU

COMORI ALE EPOCII BRONZULUI

CUPRUL

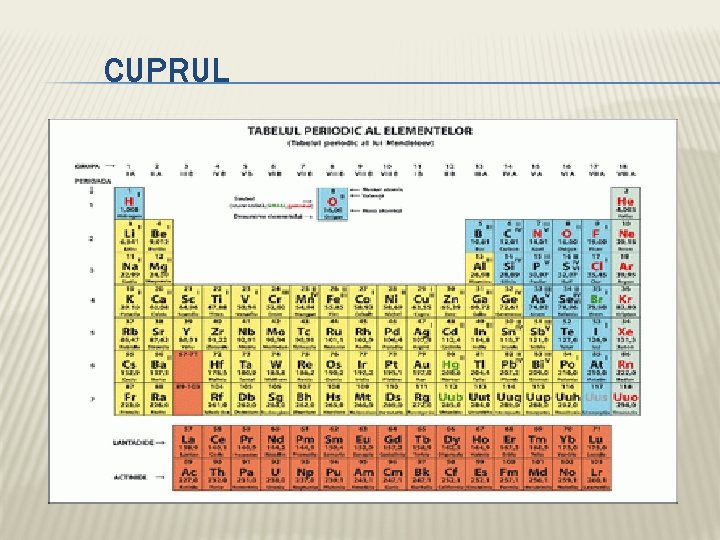
CUPRU - SRUCTURA Cu (A=64, Z=29) contine in nucleu: p+= 29; n 0= 35; e−= 29; K 2 L 8 M 18 N 1 => perioada 4; gr. I sec. Cu – 1 e- → Cu+ Ø Cu – 2 e- → Cu 2+ Valenţă variabilă: I si II; electrovalenţa +1; +2; Ø Metal cu caracter electropozitiv. Ø

STARE NATURALA Ø Ø Ø Cuprul a fost folosit de oameni din cele mai vechi timpuri, arheologii descoperind obiecte din acest metal datând din anul 8700 î. Hr. Foarte rar se găseşte în stare liberă. Este mult mai răspandit sub formă de combinaţii: - Cu 2 S (calcozina); Cu. S (covelina) - Cu. Fe. S 2 (calcopirita); - Cu 2 O (cupritul); Cu. O (tenorit) - Cu. CO 3 x. Cu(OH)2 (malachitul); - Cu. SO 4 x 5 H 2 O (calcanita)

CUPRU – STARE NATURALA - calcozina (Cu 2 S ) (Cu. S) - covelina

CUPRU – STARE NATURALA -calcopirita (Cu. Fe. S 2) -tenorit (Cu. O) - cuprit (Cu 2 O)

CUPRU – STARE NATURALA -malachit (Cu. SO 4 x 5 H 2 O) (Cu. CO 3 x. Cu(OH)2) -calcanita

ZACAMINTE DE CUPRU v Cele mai importante zăcăminte de cupru se găsesc în Munţii Anzi (Chile şi Peru); v In ţara noastră se găsesc zăcăminte de cupru la Baia de Aramă, Roşia Poieni, Lacul Ursului, Moldova Nouă, etc. . v Cuprul se găseşte şi în diferite plante şi animale (crustacee, moluşte). v În organismul uman se găseşte în ficat şi rinichi (~100 -200 mg).

MINA GRASBERG - INDONEZIA

PROPRIETATI FIZICE Ø Ø Ø Ø Ø - solid de culoare roşiatică (în foiţe foarte subţiri apare în transparenţă albastru-verzui); - luciu specific; - moale, are duritatea 3; densitate – 8, 96 g/cm 3 ; - maleabil şi ductil; - foarte tenace - un fir de cupru cu diametrul de 2 mm poate susţine o greutate de 140 kg; - foarte bun conducător de căldură şi electricitate; - formează uşor aliaje (alamă, bronz , aliaje pentru monede, etc) - punct de topire ridicat. - insolubil in apa

PROPRIETATI CHIMICE Ø Ø Ø - reactivitate chimică redusă; - în aer umed, bogat în dioxid de carbon, se acoperă cu un strat de carbonat bazic, albastruverzui, cunoscut sub denumirea de cocleală (toxic). - la temperatură ridicata este atacat de oxigen, halogeni şi sulf. 2 Cu + O 2 → 2 Cu. O (negru) 4 Cu + O 2 → 2 Cu 2 O (roşu) Cu + Cl 2 → Cu. Cl 2 Cu + S → Cu. S

PROPRIETATI CHIMICE reactioneaza cu oxiacizii concentrati, in doua etape, in ambele cazuri degajandu-se gaze toxice q Cu+ H 2 SO 4 → Cu. O+SO 2+ H 2 O (etapa 1) Cu. O+ H 2 SO 4 → Cu. SO 4+ H 2 O (etapa 2) Cu+ 2 H 2 SO 4 → Cu. SO 4+ 2 H 2 O+ SO 2↑ q 3 Cu+ 2 HNO 3 → 3 Cu. O+ 2 NO↑+ H 2 O (etapa 1) Cu. O+ 2 HNO 3 → Cu(NO 3)2+ H 2 O (etapa 2) Ø

PROPRIETATI CHIMICE Cu este situat in seria de activitate chimica dupa H, deci nu poate reactiona cu H 2 O si HCl Ø Cu reactioneaza cu o solutie de azotat de argint, rezultand Ag care se depune pe sarma de cupru Cu+ 2 Ag. NO 3 → Cu(NO 3)2+ 2 Ag ↓ Cu poate scoate din compuşi metalele mai puţin active decat el Ø

CONCLUZII Cuprul poate reactiona cu: ü Oxigenul din aer (ardere) ü Nemetale (clor si sulf) ü Oxiacizii concentrati (H 2 SO 4 si HNO 3) ü Scoate din compusi metalele mai putin active decat el (Au, Ag, Hg) Cuprul nu reactioneaza cu HCl sau H 2 O.

FIZIOLOGIE v v Cuprul este un oligoelement esenţial , răspîndit în majoritatea ţesuturilordin organism. Se apreciază că în corpul unui adult se găsesc 100 -150 mg Cu. Necesarul zilnic pentru un adult este de 2, 5 mg. . Pentru copii necesarul se stabileşte în funcţie de greutatea corporală: 0, 05 mg Cu/1 kg corp. Sursele alimentare bogate în cupru sunt: carnea (ficat, rinichi), crustaceele, moluştele , legumele verzi (frunze) şi legumele uscate. Dintre fructe, cuprul se află în special în nuci, struguri şi migdale. În cazul aporturilor insuficiente de cupru , în special la copii, se declanşează anemii determinate de lipsa ferului în hemoglobină (la fixarea căruia participă).

TOXICITATE � � In stare metalică nu este otrăvitor; combinaţiile lui sunt toxice când sunt luate în doze mari (din această cauză vasele din cupru se cositoresc); La persoanele care lucrează în mine sau în procesul de prelucrare a minereurilor de cupru pot apare intoxicaţii care se manifestă prin colici abdominali, senzaţie de greaţă, diaree, vomă, anemie. Combinaţiile Cu (II) au acţiune iritantă locală, toxică la nivelul muşchilor striaţi şi a miocardului producând paralizia şi stop cardiac. Totodată unele combinaţii ale Cu (II) produc anemie hemolitică, toxicitatea manifestându-se la nivelul ficatului şi al rinichilor. Afectarea metabolismului cuprului conduce la manifestări grave, două maladii fiind reprezentative : maladia lui Menkes şi maladia lui Wilson.

UTILIZARI q q q Cuprul si aliajele sale au aplicaţii în toate ramurile industriilor moderne ca urmare a calităţilor deosebite pe care le au: conductibilitate termică şi electrică ridicată, maleabilitate, ductilitate, rezistenţă la rupere şi coroziune. Datorita marii sale conductibilităţi electrice, este întrebuinţat în industria electrotehnică pentru fabricarea de cabluri electrice, colectoare ale motoarelor şi dinamuri electrice, capete de contacte, placi de circuite imprimate, etc. . Datorită conductibilităţii sale termice este utilizat pentru fabricarea de schimbătoare de căldură, cazane, radiatoare, serpentine, ţevi pentru fierbătoare, etc. .

UTILIZARI

UTILIZARI q q Pentru marea sa maleabilitate, este folosit la fabricarea de vase şi căldări, aparate pentru cercetări ştiinţifice, vase de bucătărie, ceasornice, muniţii, statui, monezi, medalii, acoperişuri pentru clădiri, etc. . In industria metalurgică: aliaje (alame, bronzuri, aliaje pentru monede şi medalii), recipiente industriale, etc. . In industria chimică : catalizator de hidrogenare şi de descompunere; coloranţi pentru vopseluri sau artificii; Cuprul care o puritate de peste 99%, este folosit la fabricarea conductelor de gaz şi apă, a materialelor pentru acoperişuri, a ustensilelor şi a unor obiecte ornamentale.