CUPRUL PROFESOR ELENA COSMA COALA GENERAL NR 1





























- Slides: 31

CUPRUL PROFESOR ELENA COSMA ŞCOALA GENERALĂ NR. 1 BISTRIŢA

CUPRUL �Numele elementului vine de la Cipru aes Cyprium (latină) = metal din Cipru �Insula Cipru era cunoscută din antichitate ca “insula cu o mie de mine” de unde, începând cu anul 1500 î. Hr. , grecii şi, apoi, romanii au extras cuprul. �Cuprul se mai numeşte şi aramă

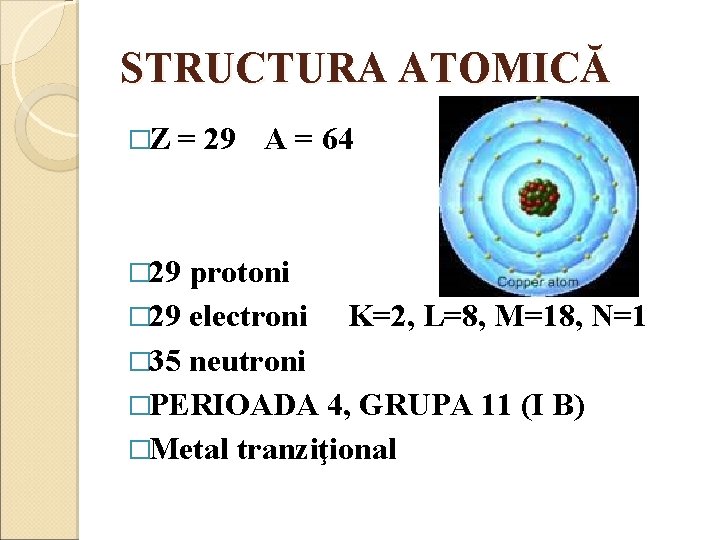
STRUCTURA ATOMICĂ �Z = 29 A = 64 � 29 protoni � 29 electroni K=2, L=8, M=18, N=1 � 35 neutroni �PERIOADA 4, GRUPA 11 (I B) �Metal tranziţional

STARE NATURALĂ Cu �Liber – se găseşte destul de rar în stare nativă.

STARE NATURALĂ Cu �În combinaţii �– oxid ◦ Cu 2 O cuprit �- sulfuri ◦ Cu. Fe. S 2 calcopirita ◦ Cu 2 S calcozina �- carbonaţi ◦ 2 Cu. CO 3∙Cu(OH)2 azurit ◦ Cu. CO 3∙Cu(OH)2 malachit

STARE NATURALĂ Cu Cupritul

STARE NATURALĂ Cu Calcopirita

STARE NATURALĂ Cu Calcozina

STARE NATURALĂ Cu Azuritul

STARE NATURALĂ Cu Malachitul

PROPRIETĂŢI FIZICE �solid; �roşiatic (arămiu); �cu duritate mică (3); �metal greu (densitate 8, 96 g/cm 3); �bun conductor de căldură şi electricitate fiind al II-lea după argint; �prezintă punct de topire ridicat (1083ºC); �ductil şi maleabil (foiţa subţire este albastruverzuie);

PROPRIETĂŢI FIZICE �formează uşor aliaje cu Zn, Sn, Ni aliaje ◦ alama Cu-Zn ◦ bronz Cu-Sn

PROPRIETĂŢI FIZICE aliaje ◦ constantanul Cu-Ni-Mn ◦ nichelina Cu- Ni-Zn

PROPRIETĂŢI CHIMICE �Este un metal cu reactivitate mică. �În aer uscat, la temperatura obişnuită, este stabil, dar în mediu umed şi în prezenţa dioxidului de carbon, se acoperă cu un strat verde de carbonat bazic de cupru Cu. CO 3∙Cu(OH)2 cunoscut sub numele de cocleală şi care este foarte toxic. �Din acest motiv vasele din cupru se acoperă cu un strat de staniu, operaţie numită cositorire.

COCLEALA

PROPRIETĂŢI CHIMICE �Încălzit în aer sau oxigen la 300ºC, cuprul se combină cu oxigenul şi formează oxidul de Cu(II) negru, iar la temperatură mai înaltă se formează oxidul de Cu(I) roşu

PROPRIETĂŢI CHIMICE �Cuprul, ca şi alte metale care au valenţă variabilă, îşi manifestă valenţa maximă când reacţionează cu clorul obţinându-se clorura de cupru(II) care colorează flacăra în verde.

PROPRIETĂŢI CHIMICE �Cuprul reacţionează cu sulful obţinându-se sulfura de cupru(II), neagră. �De altfel, numele sulfului în limba latină este “sulphurium” care vine din limba sanscrită unde “sulvari” înseamnă “inamicul cuprului”, deoarece cuprul încălzit cu sulf se înnegreşte.

PROPRIETĂŢI CHIMICE �Având reactivitate mică, nu poate dezlocui hidrogenul din acizi. �Cu acidul clorhidric nu reacţionează �Cu acidul sulfuric concentrat, la cald, formează sulfat de Cu(II), dioxid de sulf şi apă

PROPRIETĂŢI CHIMICE �Cu acidul azotic concentrat reacţionează şi la rece formând azotat de Cu(II), monoxid de azot şi apă �Monoxidul de azot – gaz incolor -se oxidează mai departe la dioxid de azot (hipoazotidă) gaz brun roşcat

PROPRIETĂŢI CHIMICE �Cu este înlocuit în săruri de metalele mai reactive decât el �Cu poate înlocui în săruri pe metalele Hg, Ag, Pt, Au (metale cu reactivitate mai mică decât a lui) �Metalul dezlocuit se depune pe cupru

ACŢIUNEA FIZIOLOGICĂ �Cuprul este indispensabil organismului. �Organismul uman adult conţine 100 -200 mg de Cu, depozitat în ficat şi rinichi. �Necesarul zilnic este de 2 mg, absorbţia făcându-se la nivelul intestinului. �Are rol esenţial în biosinteza hemoglobinei şi în procesele de oxidare la nivel celular, făcând parte din structura multor enzime.

ACŢIUNEA FIZIOLOGICĂ �Cuprul din organismul nostru ne face părul să strălucească, ne protejează de artrită, dureri articulare, dureri de plămâni. �Dar, cum de acţionează atât de favorabil? Deoarece este esenţial în procesul de sinteza a colagenului, în folosirea fierului în hemoglobină şi în metabolismul vitaminei C, în fixarea calciului, în secreţia tiroidiană. �Are şi un rol imunitar.

ACŢIUNEA FIZIOLOGICĂ �Suplimentarea dozei se poate face prin consumul de surse naturale de cupru, precum: ciocolata, nucile, fasolea, mazărea, fructele de mare, vinul roşu, ciupercile etc.

METALURGIA CUPRULUI Turnarea alamei Turnătorie de cupru

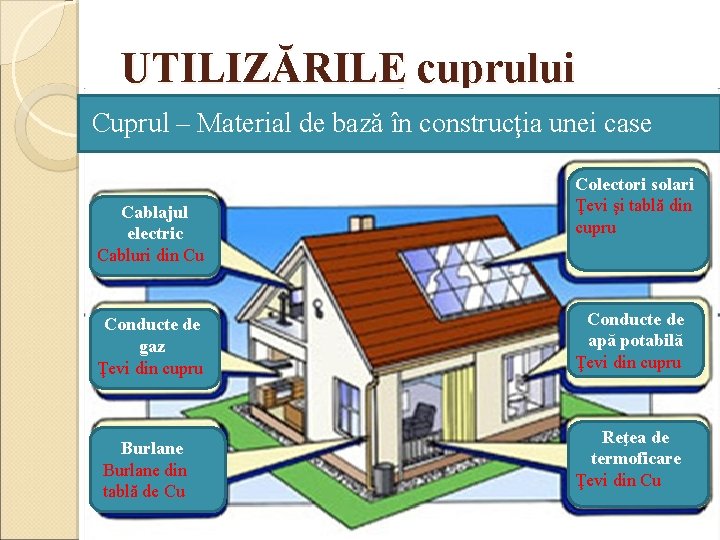
UTILIZĂRILE cuprului Cuprul – Material de bază în construcţia unei case Cablajul electric Cabluri din Cu Conducte de gaz Ţevi din cupru Burlane din tablă de Cu Colectori solari Ţevi şi tablă din cupru Conducte de apă potabilă Ţevi din cupru Reţea de termoficare Ţevi din Cu

UTILIZĂRILE cuprului

UTILIZĂRILE bronzului

UTILIZĂRILE alamei

UTILIZĂRILE altor aliaje

BIBLIOGRAFIE �Constantinescu, Rodica şi Râpă, Marilena – CHIMIE - Manual pt. clasa a. VIII-a, Ed. SIGMA, Bucureşti, 2000 �Gheorghiu, Cornelia şi Panait, Claudia – Chimia - Manual pentru clasa a VIII-a, EDP, Bucureşti, 1980 �Fătu, Sanda; Stroe, Felicia; Stroe, Constantin – CHIMIE – Manual pentru şcoala profesională, Ed. ALL EDUCATIONAL, Bucureşti, 2001 � Wikipedia. org