CUC THIT K BI GING IN T E

CUỘC THIẾT KẾ BÀI GIẢNG ĐIỆN TỬ E - LEARNING HÓA HỌC 8 Giáo viên thực hiện: Nguyễn Tuấn Phong Email: thanphongchi@gmail. com Số điện thoại : 01675782109 Trường PTDTBT - THCS Keo Lôm – Huyện Điện Biên Đông

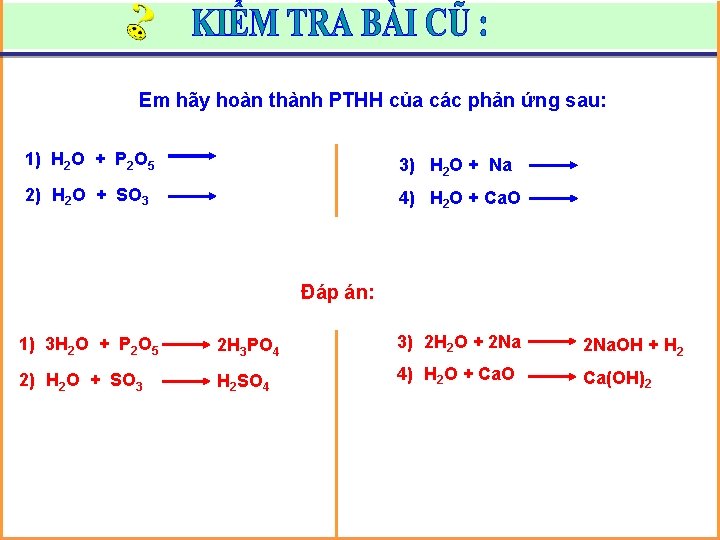
Em hãy hoàn thành PTHH của các phản ứng sau: 1) H 2 O + P 2 O 5 3) H 2 O + Na 2) H 2 O + SO 3 4) H 2 O + Ca. O Đáp án: 1) 3 H 2 O + P 2 O 5 2 H 3 PO 4 3) 2 H 2 O + 2 Na. OH + H 2 2) H 2 O + SO 3 H 2 SO 4 4) H 2 O + Ca. O Ca(OH)2


Tiết 5556: - Bài AXIT 37: AXIT - BAZƠ - MUỐI Tiết - BAZƠ - MUỐI I. Axit 1. Khái niệm - Ví dụ: HCl; H 2 SO 4; H 3 PO 4 Lấy ví dụ mô t sô axit mà em biết ?

Tiết 5556: - Bài AXIT 37: AXIT - BAZƠ - MUỐI Tiết - BAZƠ - MUỐI I. Axit 1. Khái niệm - Ví dụ: HCl; H 2 SO 4; H 3 PO 4 Xác định đặc điểm giống nhau về thành phần phân tử của các axit: - Kết luận: phân tử axit gồm có một hay nhiều nguyên tử H liên kết với gốc axit, các nguyên tử H này có thể thay thế bằng các nguyên tử kim loại. H 2 SO 4 HCl H 3 PO 4 ? CÓ NGUYÊN TỬ H giống nhau (1 hoặc nhiều) Liên kết với nhau CÓ GỐC AXIT - Nhận xét: +) phân tử axit gồm có một hay nhiều nguyên tử H liên kết với gốc axit Cho phương trình hóa học sau: Zn + 2 HCl Fe + Zn. Cl 2 + H 2 SO 4 Fe. SO 4 + H 2 Các nguyên tử H trong axit có thể thay thế bằng các nguyên tử kim loại không?
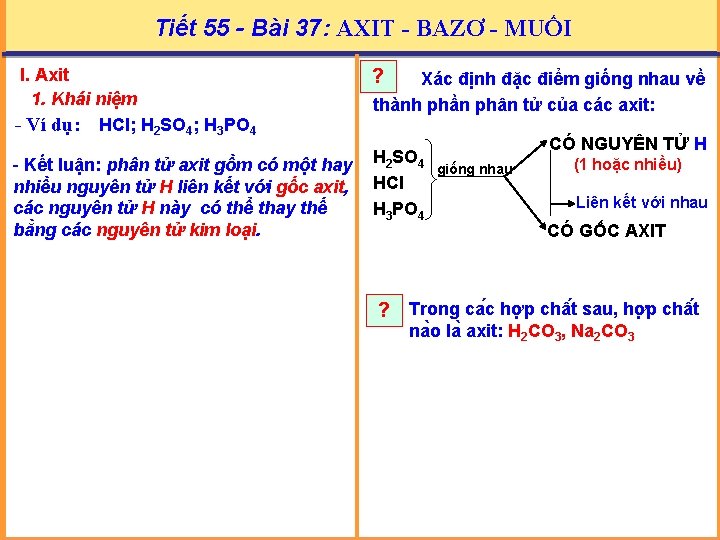
Tiết 5556: - Bài AXIT 37: AXIT - BAZƠ - MUỐI Tiết - BAZƠ - MUỐI I. Axit 1. Khái niệm - Ví dụ: HCl; H 2 SO 4; H 3 PO 4 ? - Kết luận: phân tử axit gồm có một hay nhiều nguyên tử H liên kết với gốc axit, các nguyên tử H này có thể thay thế bằng các nguyên tử kim loại. H 2 SO 4 HCl H 3 PO 4 Xác định đặc điểm giống nhau về thành phần phân tử của các axit: CÓ NGUYÊN TỬ H giống nhau (1 hoặc nhiều) Liên kết với nhau CÓ GỐC AXIT ? Trong ca c hơ p châ t sau, hơ p châ t na o la axit: H 2 CO 3, Na 2 CO 3
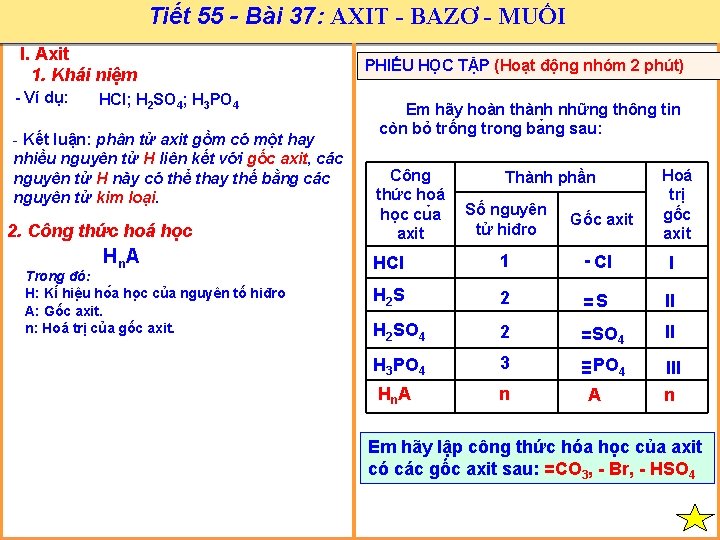
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm - Ví dụ: HCl; H 2 SO 4; H 3 PO 4 - Kết luận: phân tử axit gồm có một hay nhiều nguyên tử H liên kết với gốc axit, các nguyên tử H này có thể thay thế bằng các nguyên tử kim loại. 2. Công thức hoá học Hn A Trong đó: H: Ki hiê u ho a ho c của nguyên tố hiđro A: Gốc axit. n: Hoá trị của gốc axit. PHIẾU HỌC TẬP (Hoạt động nhóm 2 phút) Em hãy hoàn thành những thông tin còn bỏ trống trong ba ng sau: Công thức hoá học cu a axit Thành phần Hoá trị gốc axit Số nguyên tử hiđro Gốc axit HCl 1 - Cl I H 2 S 2 =S II H 2 SO 4 2 = SO 4 II H 3 PO 4 3 ≡ PO 4 III Hn. A n Em hãy lập công thức hóa học của axit có các gốc axit sau: =CO 3, - Br, - HSO 4

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm - Ví dụ: HCl ; H 2 SO 4 ; H 3 PO 4 - Kết luận: phân tử axit chứa một hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn A Trong đó: H: Ki hiê u ho a ho c của nguyên tố hiđro A: Gốc axit. n: Hoá trị của gốc axi. 3. Phân loại Dựa vào thành phần phân tử, axit chia làm 2 loại: - Axit không có oxi: HCl; H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3; H 3 PO 4 Các axit ở dãy 1 và dãy 2 có điểm gì khác nhau? Vậy dựa vào đâu để người ta phân loại axit? Dãy 1: HCl; H 2 S; Dãy 2: H 3 PO 4; H 2 SO 4 ; H 2 SO 3; HNO 3
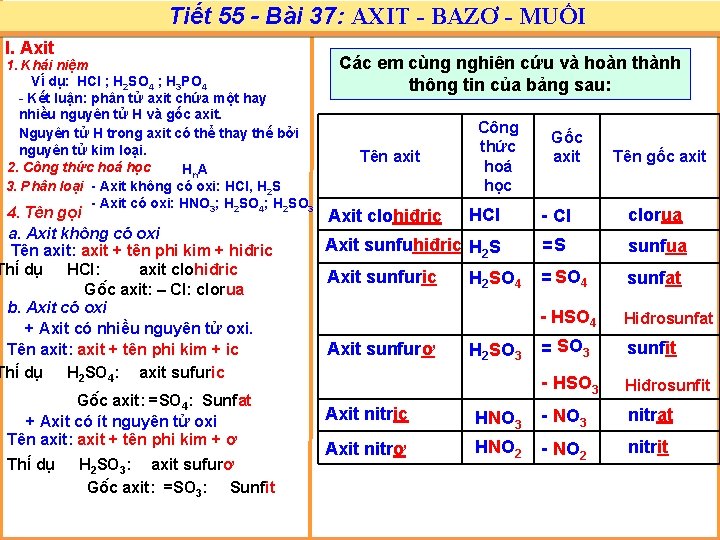
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm Vi du : HCl ; H 2 SO 4 ; H 3 PO 4 - Kết luận: phân tử axit chứa một hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a. Axit không có oxi Tên axit: axit + tên phi kim + hiđric Thi du HCl: axit clohiđric Gô c axit: – Cl: clorua b. Axit có oxi + Axit có nhiều nguyên tử oxi. Tên axit: axit + tên phi kim + ic Thi du H 2 SO 4: axit sufuric Gô c axit: =SO 4: Sunfat + Axit có ít nguyên tử oxi Tên axit: axit + tên phi kim + ơ Thi du H 2 SO 3: axit sufurơ Gô c axit: =SO 3: Sunfit Các em cùng nghiên cứu và hoàn thành thông tin của bảng sau: Tên axit Công thức hoá học Gốc axit Tên gốc axit HCl - Cl clorua Axit sunfuhiđric H 2 S =S sunfua Axit sunfuric = SO 4 sunfat - HSO 4 Hiđrosunfat = SO 3 sunfit - HSO 3 Hiđrosunfit Axit clohiđric Axit sunfurơ H 2 SO 4 H 2 SO 3 Axit nitric HNO 3 - NO 3 nitrat Axit nitrơ HNO 2 - NO 2 nitrit

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 Em hãy kể tên một số chất là bazơ mà em biết.
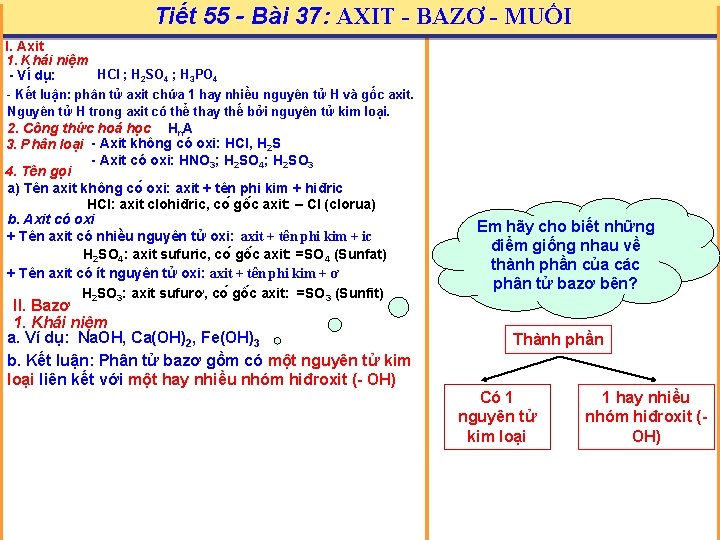
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) Em hãy cho biết những điểm giống nhau về thành phần của các phân tử bazơ bên? Thành phần Có 1 nguyên tử kim loại 1 hay nhiều nhóm hiđroxit (OH)

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) ? Trong các hợp chất sau, hợp chất nào là bazơ? Mg(OH)2, Mg. CO 3, H 2 CO 3

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) 2. Công thức hoá học M(OH)n Trong đó: M: Ki hiê u ho a ho c chung của kim loại. - OH: Nhóm hiđroxit. n: Hoá trị của kim loại, hay số nhóm hiđroxit. Em hãy cho biết hóa trị kim loại và số nhóm - OH của các bazơ bên? Nếu gọi M là kim loại có hóa trị là n thì công thức của bazơ là gì?

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) 2. Công thức hoá học M(OH)n Trong đó: M: Ki hiê u ho a ho c chung của kim loại. - OH: Nhóm hiđroxit. n: Hoá trị của kim loại, hay số nhóm hiđroxit. Em hãy lập công thức hóa học của bazơ ứng với các kim loại sau: K, Zn, Al
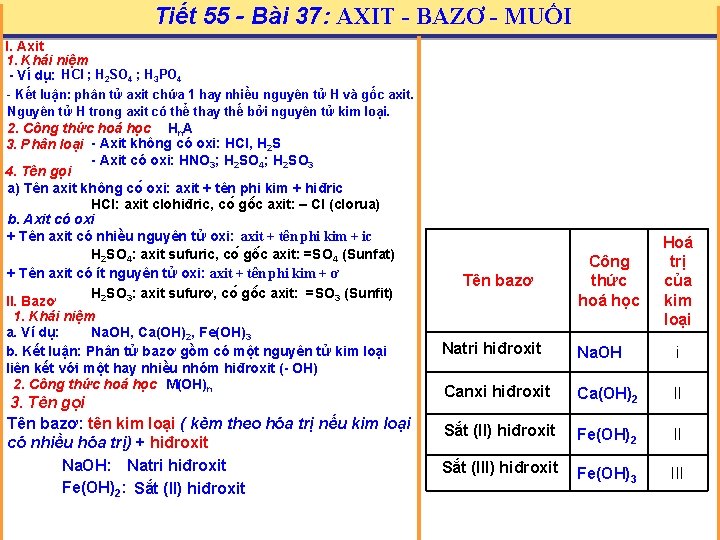
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm - Vi du : HCl ; H 2 SO 4 ; H 3 PO 4 - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) 2. Công thức hoá học M(OH)n 3. Tên gọi Tên bazơ: tên kim loại ( kèm theo hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit Na. OH: Natri hiđroxit Fe(OH)2: Sắt (II) hiđroxit Tên bazơ Công thức hoá học Hoá trị của kim loại Natri hiđroxit Na. OH i Canxi hiđroxit Ca(OH)2 II Sắt (II) hiđroxit Fe(OH)2 II Sắt (III) hiđroxit Fe(OH)3 III

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) 2. Công thức hoá học M(OH)a 3. Tên gọi Tên bazơ: tên kim loại ( kèm theo hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit Fe(OH)2: Sắt (II) hiđroxit Natri hiđroxit Na. OH: 4. Phân loại Gọi tên các bazơ sau: Al(OH)3, Cu(OH)2
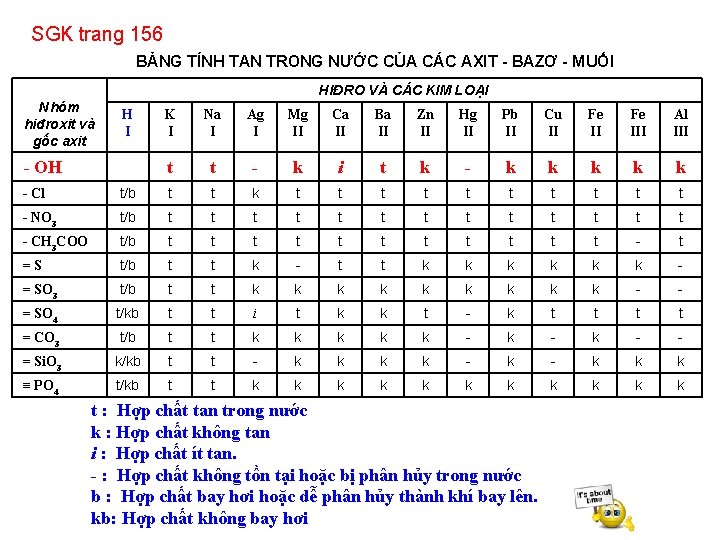
SGK trang 156 BẢNG TÍNH TAN TRONG NƯỚC CỦA CÁC AXIT - BAZƠ - MUỐI HIĐRO VÀ CÁC KIM LOẠI Nhóm hiđroxit và gốc axit H I - OH K I Na I Ag I Mg II Ca II Ba II Zn II Hg II Pb II Cu II Fe III Al III t t - k i t k - k k k - Cl t/b t t k t t t t t - NO 3 t/b t t t t - CH 3 COO t/b t t t - t =S t/b t t k - t t k k k - = SO 3 t/b t t k k k k k - - = SO 4 t/kb t t i t k k t - k t t = CO 3 t/b t t k k k - k - - = Si. O 3 k/kb t t - k k k ≡ PO 4 t/kb t t k k k t : Hợp chất tan trong nước k : Hợp chất không tan i : Hợp chất ít tan. - : Hợp chất không tồn tại hoặc bị phân hủy trong nước b : Hợp chất bay hơi hoặc dễ phân hủy thành khí bay lên. kb: Hợp chất không bay hơi

Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI I. Axit 1. Khái niệm HCl ; H 2 SO 4 ; H 3 PO 4 - Vi du : - Kết luận: phân tử axit chứa 1 hay nhiều nguyên tử H và gốc axit. Nguyên tử H trong axit có thể thay thế bởi nguyên tử kim loại. 2. Công thức hoá học Hn. A 3. Phân loại - Axit không có oxi: HCl, H 2 S - Axit có oxi: HNO 3; H 2 SO 4; H 2 SO 3 4. Tên gọi a) Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric, co gô c axit: – Cl (clorua) b. Axit có oxi + Tên axit có nhiều nguyên tử oxi: axit + tên phi kim + ic H 2 SO 4: axit sufuric, co gô c axit: =SO 4 (Sunfat) + Tên axit có ít nguyên tử oxi: axit + tên phi kim + ơ H 2 SO 3: axit sufurơ, co gô c axit: =SO 3 (Sunfit) II. Bazơ 1. Khái niệm a. Ví dụ: Na. OH, Ca(OH)2, Fe(OH)3 b. Kết luận: Phân tử bazơ gồm có một nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (- OH) 2. Công thức hoá học M (OH)a 3. Tên gọi Tên bazơ: tên kim loại( kèm theo hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit Fe(OH)2: Sắt (II) hiđroxit Natri hiđroxit Na. OH: 4. Phân loại Dựa vào tính tan trong nước bazơ được chia làm hai loại: - bazơ tan được trong nước (kiềm) Ví dụ: Na. OH, KOH, Ca(OH)2, Ba(OH)2 - bazơ không tan được trong nước: Ví dụ: Cu(OH)2, Mg(OH)2, Fe(OH)3 …
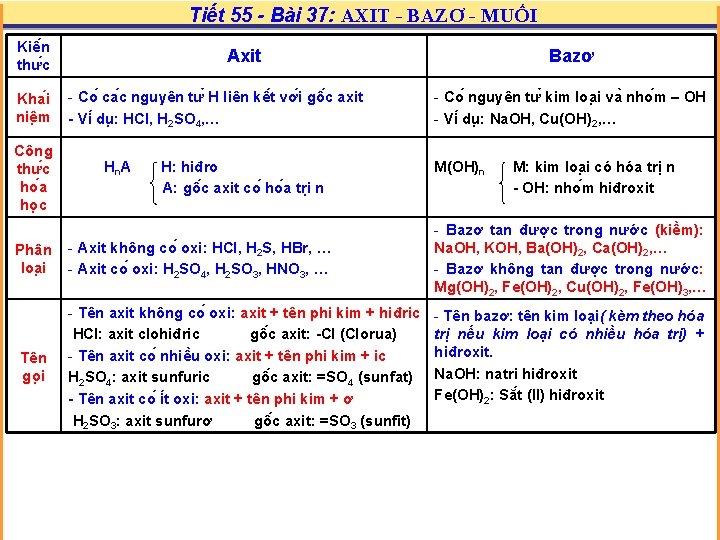
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI Kiê n thư c Kha i niê m Công thư c ho a ho c Phân loa i Tên go i Axit - Co ca c nguyên tư H liên kê t vơ i gô c axit - Vi du : HCl, H 2 SO 4, … Hn. A H: hiđro A: gô c axit co ho a tri n - Axit không co oxi: HCl, H 2 S, HBr, … - Axit co oxi: H 2 SO 4, H 2 SO 3, HNO 3, … - Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric gô c axit: -Cl (Clorua) - Tên axit co nhiê u oxi: axit + tên phi kim + ic H 2 SO 4: axit sunfuric gô c axit: =SO 4 (sunfat) - Tên axit co i t oxi: axit + tên phi kim + ơ H 2 SO 3: axit sunfurơ gô c axit: =SO 3 (sunfit) Bazơ - Co nguyên tư kim loa i va nho m – OH - Vi du : Na. OH, Cu(OH)2, … M(OH)n M: kim loa i có hóa trị n - OH: nho m hiđroxit - Bazơ tan được trong nước (kiềm): Na. OH, KOH, Ba(OH)2, Ca(OH)2, … - Bazơ không tan được trong nước: Mg(OH)2, Fe(OH)2, Cu(OH)2, Fe(OH)3, … - Tên bazơ: tên kim loại( kèm theo hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit. Na. OH: natri hiđroxit Fe(OH)2: Să t (II) hiđroxit
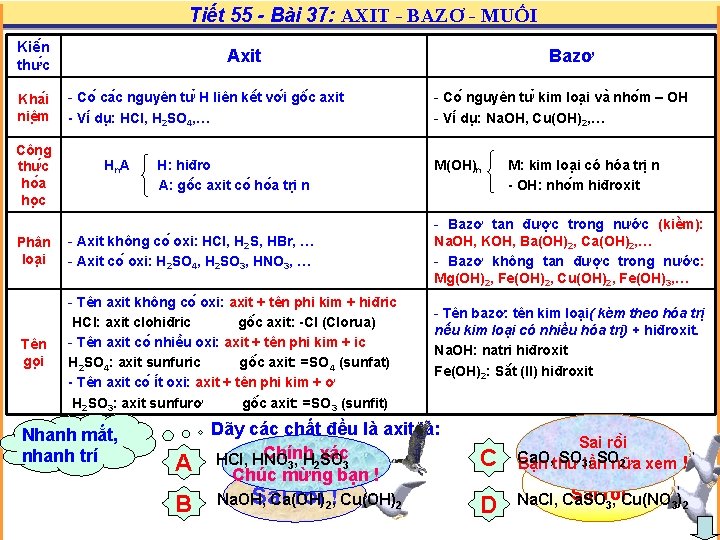
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI Kiê n thư c Kha i niê m Công thư c ho a ho c Phân loa i Tên go i Axit - Co ca c nguyên tư H liên kê t vơ i gô c axit - Vi du : HCl, H 2 SO 4, … Hn. A H: hiđro A: gô c axit co ho a tri n - Axit không co oxi: HCl, H 2 S, HBr, … - Axit co oxi: H 2 SO 4, H 2 SO 3, HNO 3, … - Tên axit không co oxi: axit + tên phi kim + hiđric HCl: axit clohiđric gô c axit: -Cl (Clorua) - Tên axit co nhiê u oxi: axit + tên phi kim + ic H 2 SO 4: axit sunfuric gô c axit: =SO 4 (sunfat) - Tên axit co i t oxi: axit + tên phi kim + ơ H 2 SO 3: axit sunfurơ gô c axit: =SO 3 (sunfit) Nhanh mắt, nhanh trí A B Bazơ - Co nguyên tư kim loa i va nho m – OH - Vi du : Na. OH, Cu(OH)2, … M(OH)n - Bazơ tan được trong nước (kiềm): Na. OH, KOH, Ba(OH)2, Ca(OH)2, … - Bazơ không tan được trong nước: Mg(OH)2, Fe(OH)2, Cu(OH)2, Fe(OH)3, … - Tên bazơ: tên kim loại( kèm theo hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit. Na. OH: natri hiđroxit Fe(OH)2: Să t (II) hiđroxit Dãy các chất đều là axit là: Chính xác HCl, HNO 3, H 2 SO 3 Chúc mừng bạn ! Sai rồi 2!, Cu(OH)2 Na. OH, Ca(OH) M: kim loa i có hóa trị n - OH: nho m hiđroxit C D Sai rô i Ca. O, SO 2 Bạn thử 3 lần nữa xem ! Ồ ! Tiếc quá. Sai rô i Na. Cl, Ca. SO 3, Cu(NO 3)2
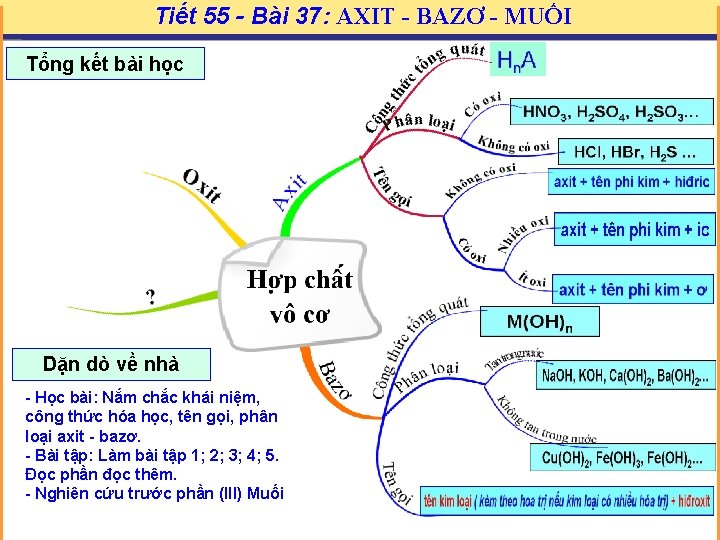
Tiết 55 - Bài 37: AXIT - BAZƠ - MUỐI Tổng kết bài học Dặn dò về nhà - Học bài: Nắm chắc khái niệm, công thức hóa học, tên gọi, phân loại axit - bazơ. - Bài tập: Làm bài tập 1; 2; 3; 4; 5. Đọc phần đọc thêm. - Nghiên cứu trước phần (III) Muối

- Slides: 23