CROMATOGRAFA EN COLUMNA Licda Carol de Santisteban Anlisis

CROMATOGRAFíA EN COLUMNA Licda. Carol de Santisteban Análisis Instrumental Departamento de Fisicoquímica Escuela de Química USAC

TIPOS, SEGÚN FM • C. de líquidos • C. de gases • C. de fluidos supercríticos

C. De líquidos • Todos los tipos de fases estacionarias y móviles. • Diferentes posibilidades de mecanismos de separación, según tipo de fase estacionaria. • Características esenciales de solventes: ◦ índice de polaridad (reparto) ◦ fuerza eluyente (adsorción)

Mecanismos de separación • • • C. de adsorción C. de reparto C. de afinidad C. de intercambio iónico C. de exclusión molecular

Selección • • Fase estacionaria de acuerdo a interacciones posibles según naturaleza del analito ◦ ◦ Van der Waals reparto fase reversa Polar reparto fase normal Medianamente polar adsorción Iónico intercambio iónico ◦ ◦ Biomoléculas: Distribución de tamaños exclusión molecular Distribución de cargas intercambio iónico, otras Actividad biológica afinidad Fase móvil de acuerdo a fase estacionaria e interacciones deseadas

CROMATOGRAFÍA DE ADSORCIÓN

FASES ESTACIONARIAS • Fase estacionaria adsorbente • Carbonato de calcio, Tswett • Sílica, alúmina las más utilizadas actualmente • Sílica > alúmina (capacidad de carga, variedad, reacciones indeseadas) • Forma, porosidad, superficie,
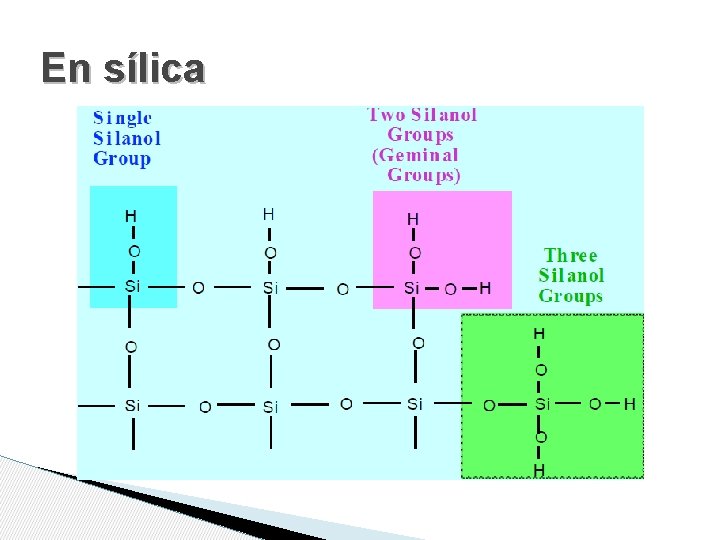
En sílica
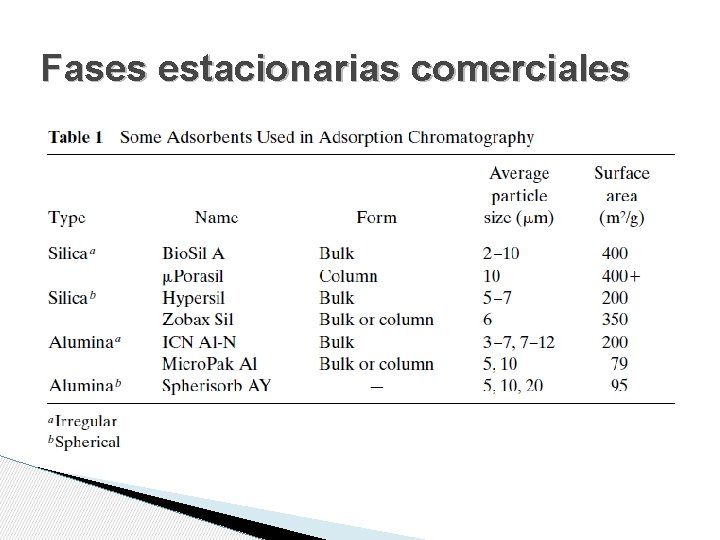
Fases estacionarias comerciales
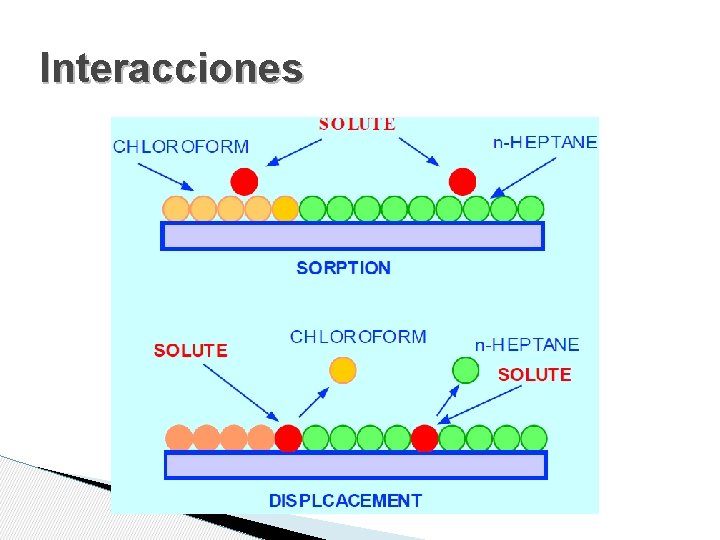
Interacciones

FASES MÓVILES • Dada una FS la FM controla k’ y α • Fuerza eluyente ◦ Energía de adsorción del disolvente (en la FS) por unidad de área (de FM) • A mayor valor de ε 0 mayor fuerza mayor polaridad • Mezcla de solventes valores intermedios de fuerza eluyente, pero la relación no es lineal

Variación de k’ y α • Variación de retención ◦ Cambio de proporciones ◦ Cambio de fuerza eluyente • Variación de selectividad ◦ Cambio de solventes ◦ Conservación de fuerza eluyente • Pruebas preliminares en capa fina
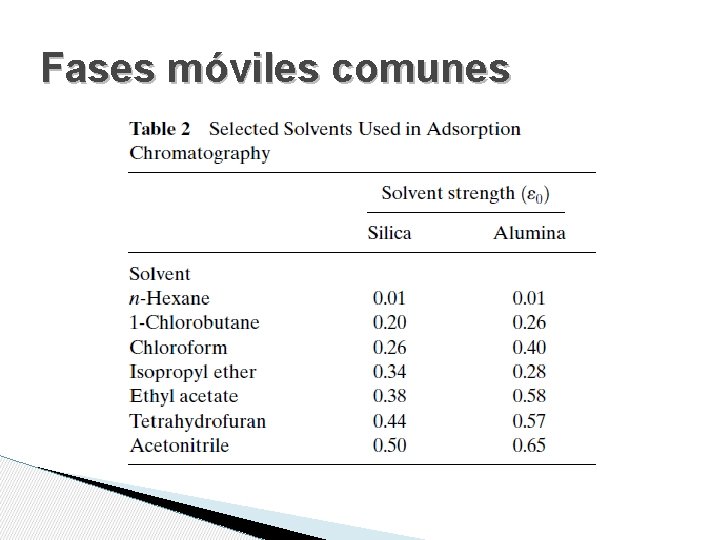
Fases móviles comunes

RETENCIÓN • Alcanos < olefinas < aromáticos < haluros, sulfuros < éteres < nitroderivados < ésteres – aldehídos – cetonas < alcoholes – aminas < sulfonas < sulfóxidos < amidas < ácidos carboxílicos

MECANISMO • Desplazamiento • Competición entre moléculas de FM y analito por adsorberse sobre los sitios activos de FS

APLICACIONES • • Apolares a medianamente polares Peso molecular < 5000 Poco solubles en agua Generalmente complementario a reparto Amplio rango de aplicación Bueno para separar isómeros Todas las ramas de investigación

CROMATOGRAFÍA DE REPARTO

C. De reparto • Desarrollada como alternativa a c. de adsorción (fácil, reproducible; mejor resolución y vida útil que adsorción • Más utilizada actualmente (fases enlazadas, HPLC) • Modalidades líquido-líquido y fase enlazada • Fase normal o fase reversa

FASES ESTACIONARIAS • Película de fase estacionaria líquida o pseudolíquida unida a soporte • Idealmente el soporte no interacciona • Unión de FS física (c. líquido-líquido) o química (c. de fase enlazada) • Sangrado de columna
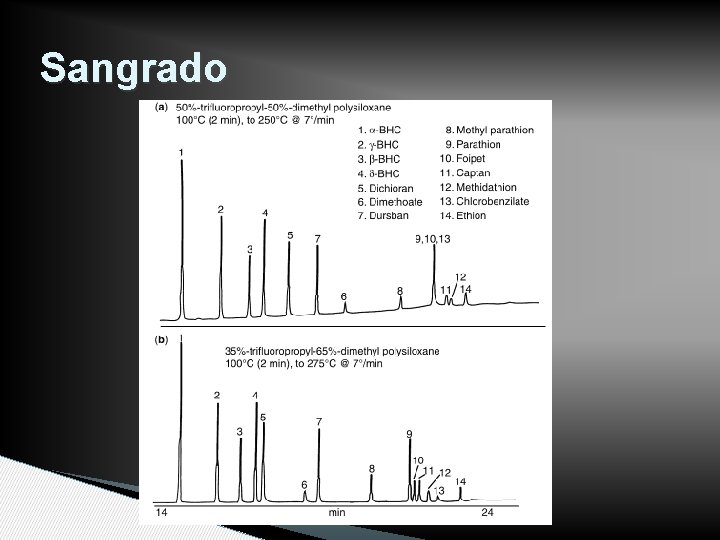
Sangrado

Fases líquidas • Preparación por varios métodos. ◦ ◦ Evaporación de solvente Recubrimiento directo Precipitación Recubrimiento dinámico • Para fase normal: agua, formamida, glicerol, polialcoholes • Para fase reversa: escualano, octanol, hidrocarburos grandes

Fases enlazadas • Unión con enlace covalente de cadena orgánica (grupo funcional) al soporte • Funcionalización de la cadena, longitud de la cadena, grado de recubrimiento del soporte • Polaridad, capacidad, retención.

Fases enlazadas

Fases enlazadas

FASES MÓVILES • De acuerdo a la polaridad de analito y fase estacionaria • Influye sobre la estructura de la fase estacionaria • Sus variaciones influyen en la resolución • Índice de polaridad (sol. En dioxano, nitrometano y etanol)
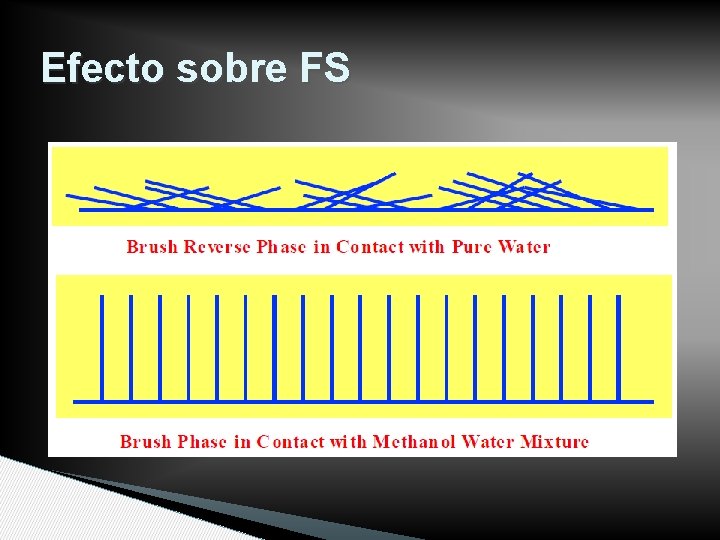
Efecto sobre FS
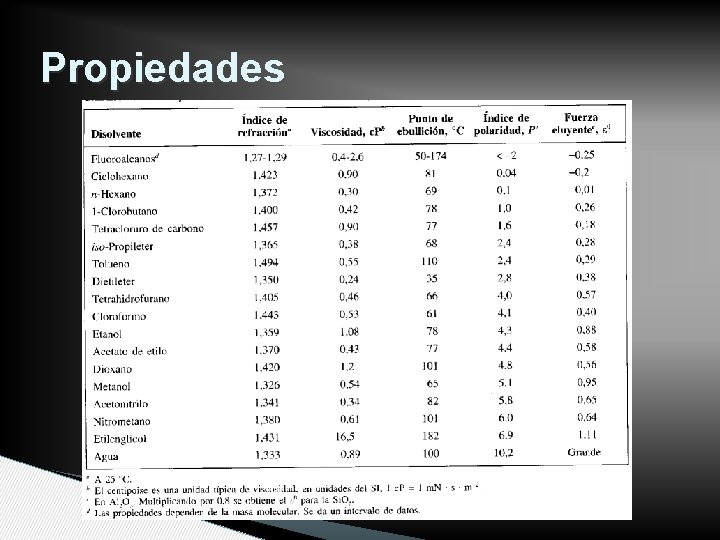
Propiedades

MECANISMO • Basado en polaridad • Polaridad analitos: Hidrocarburos < éteres < ésteres < cetonas < aldehídos < amidas < aminas < alcoholes •
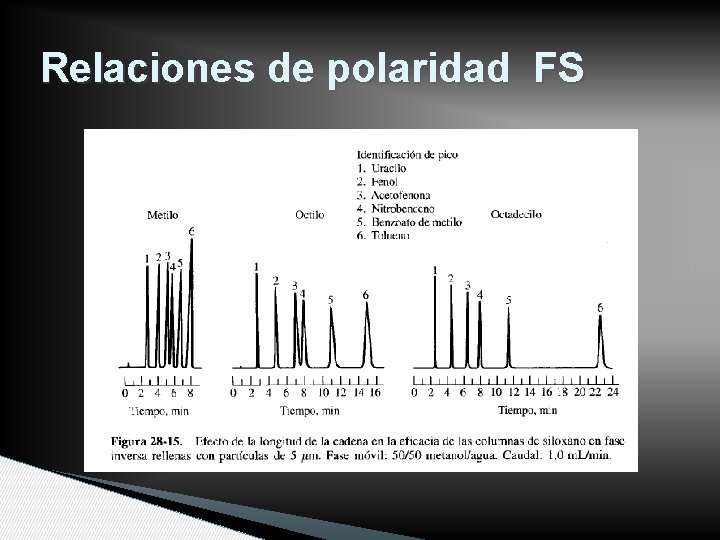
Relaciones de polaridad FS
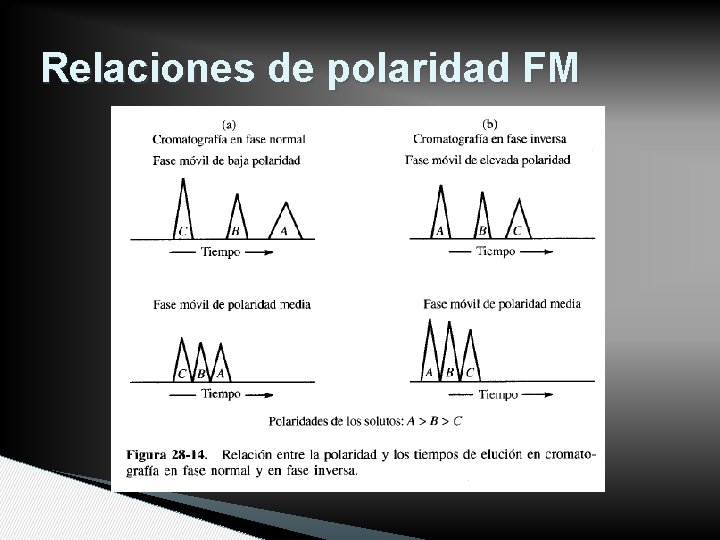
Relaciones de polaridad FM
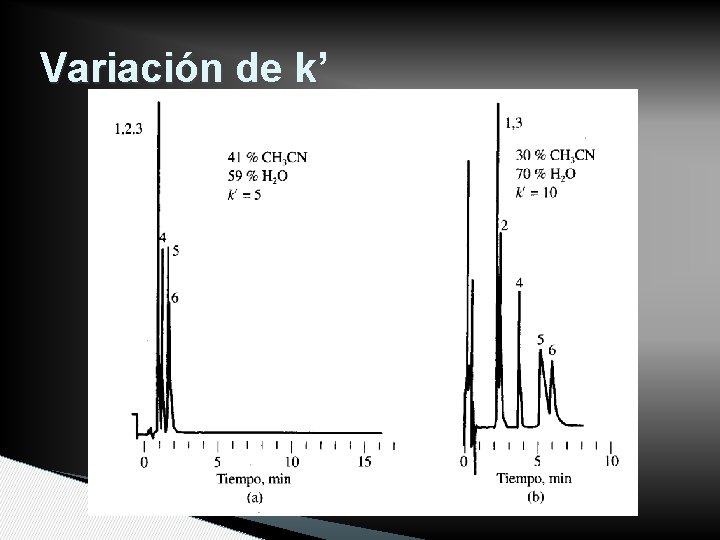
Variación de k’
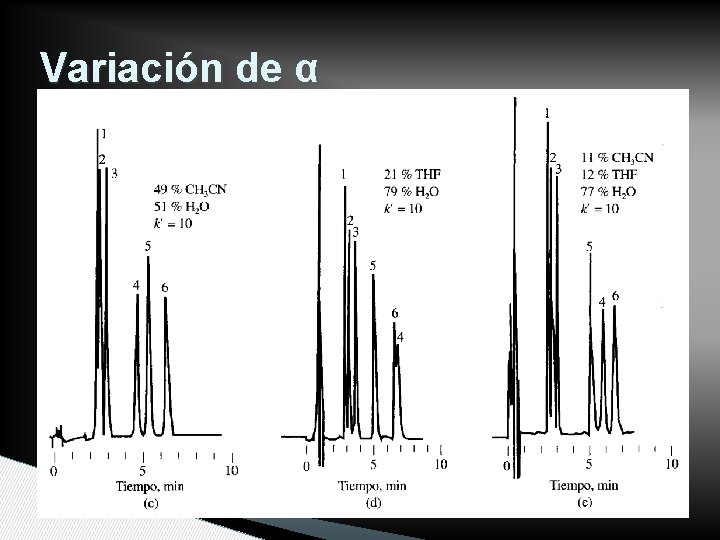
Variación de α

APLICACIONES • Tradicionalmente, analitos polares de bajo a medio peso molecular • En general, mayoría de analitos, con la técnica adecuada

Aplicaciones
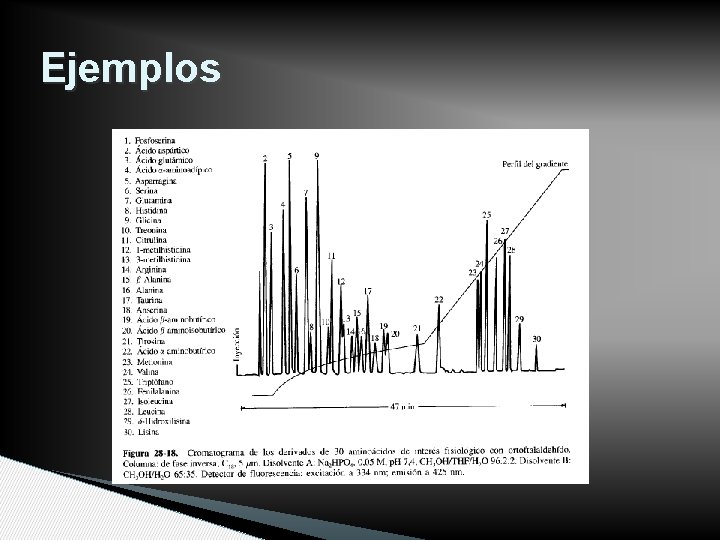
Ejemplos

CASOS ESPECIALES • Derivatización • C. de pares iónicos • C. con fases quirales
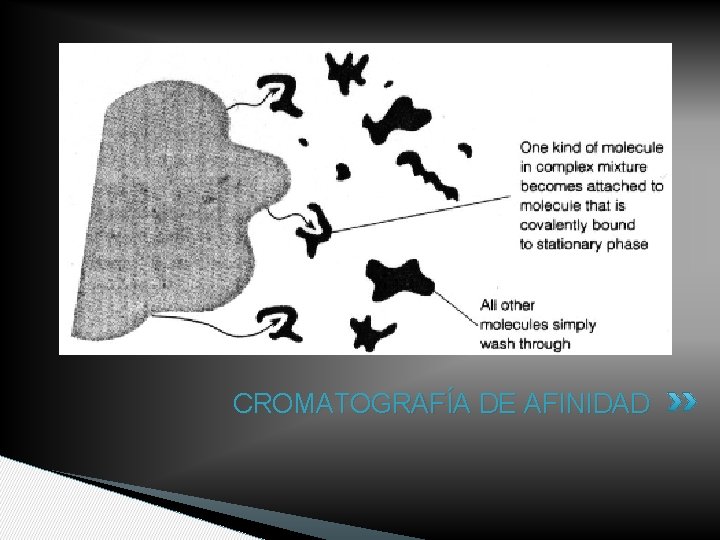
CROMATOGRAFÍA DE AFINIDAD

C. De afinidad • Mecanismo de retención basado en interacciones ESPECÍFICAS reversibles, propias de los sistemas biológicos (interacción antígeno-anticuerpo, enzima sustrato) • Modelo llave-cerradura

FASES ESTACIONARIAS • Fase estacionaria: inmobilización al soporte (unión química) de uno de los componentes de un par (ligando de afinidad) • Ligandos generales y ligandos de alta especificidad • Ligandos de origen natural o sintético

FASES ESTACIONARIAS • Soporte: baja retención de analitos en general, fácil modificación (unión de ligandos), estable a condiciones de análisis • Bajo rendimiento: material no rígido, de partícula grande (geles orgánicos) • Alto rendimiento: rígido, partícula pequeña (sílica, vidrio, poliestireno)

C. De afinidad

FASES MÓVILES • Elución por fases • Inyección del analito, en presencia de FM con las condiciones adecuadas para la unión ligando- analito (composición, p. H, fuerza iónica). Fase móvil débil • Elución del analito en presencia de FM que los desplaza o promueve la disociación del complejo ligando-analito. Fase móvil fuerte

Tipos de elución • Elución inespecífica • Elución bioespecífica ◦ Elución bioespecífica en fase normal ◦ Elución bioespecífica en fase reversa • OJO En este tipo de cromatografía fase normal y fase reversa NO se refieren a polaridad

Tipos de elución • Normal: El buffer de elución contiene un agente que compite con el ligando por unirse con el soluto. • Reversa: El buffer de elución contiene un agente que compite con el soluto por unirse con el ligando. • La elución no específica, debilita el enlace.
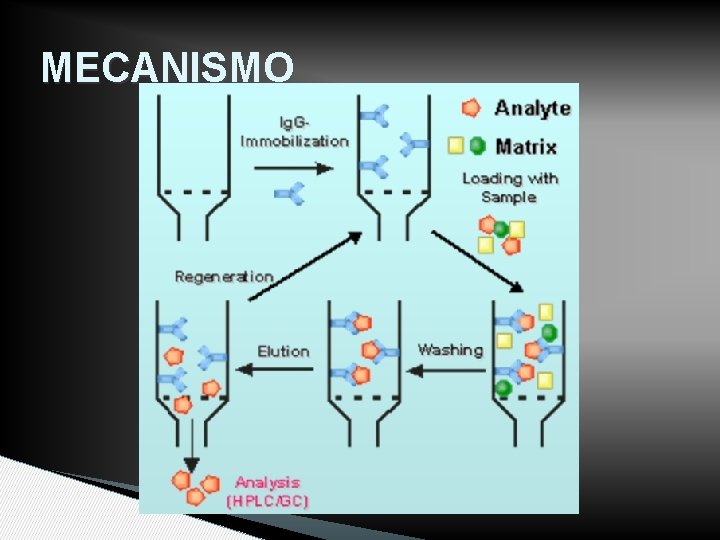
MECANISMO
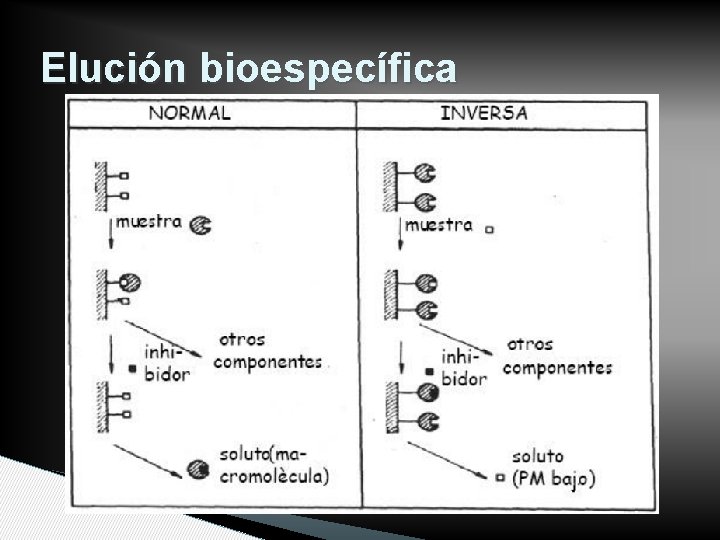
Elución bioespecífica

APLICACIONES • Biomoléculas • Moléculas con efecto biológico • Células
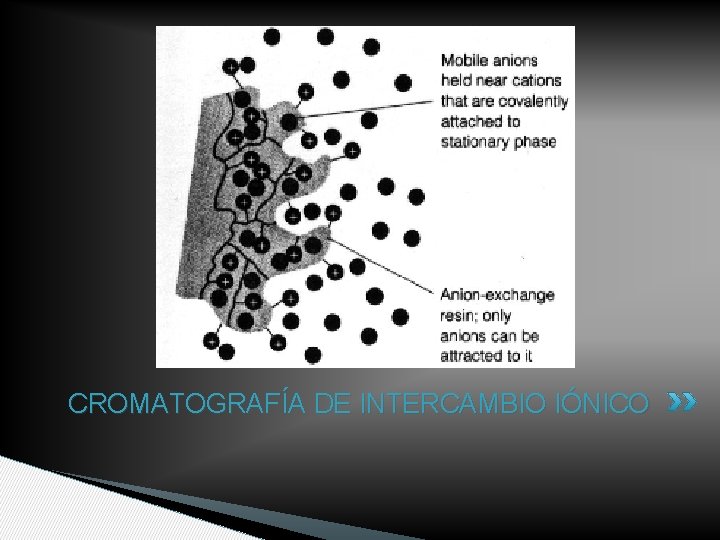
CROMATOGRAFÍA DE INTERCAMBIO IÓNICO

C. De intercambio iónico • Basado en los equilibrios de intercambio entre los distintos iones de una solución sobre la fase estacionaria • Competición entre iones de FM y de analito por adsorberse sobre los sitios activos de FS

FASES ESTACIONARIAS • Sólido de elevada masa molecular, insoluble en FM, superficie con grupos funcionales ionizables • Naturales (arcillas, zeolitas) o sintéticos (resinas)
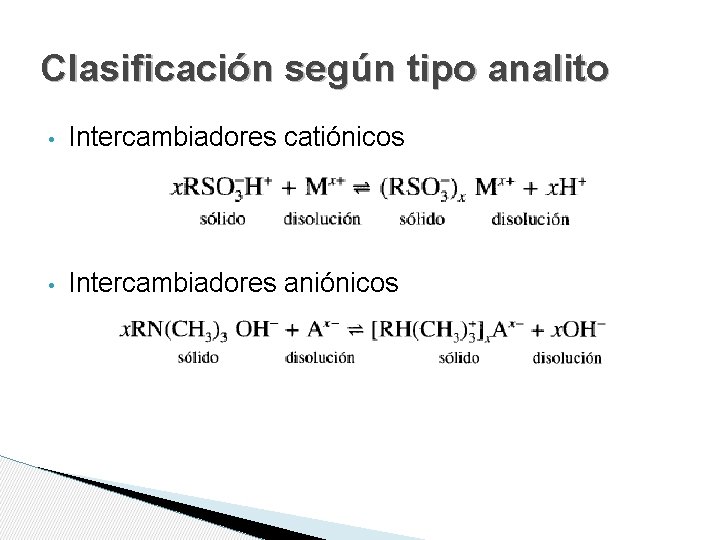
Clasificación según tipo analito • Intercambiadores catiónicos • Intercambiadores aniónicos

Clasificación según forma • • Fases estacionarias porosas: Copolímero estireno-divinilbenceno como soporte, superficie modificada con grupos ionizables Fases estacionarias peliculares: Partículas esféricas no porosas de soporte (vidrio, polímero, sílica) con película de resina de intercambio

FASES MÓVILES • Soluciones acuosas con o sin modificadores orgánicos (metanol) • Contienen sustancias iónicas (buffer) • p. H controla ionización de FS retención/elución • Fuerza iónica controla competición contra analito controla elución controla

MECANISMO • http: //www. wiley. com/college/fob/quiz 05/55. html

Retención • Polivalentes más que monovalentes • Para grupos con la misma carga, las diferencias de retención se dan por tamaño del ión hidratado y otras propiedades

APLICACIONES • Analitos iónicos, bajo a medio peso molecular • Orgánicos e inorgánicos • Fármacos, metabolitos, alimentos
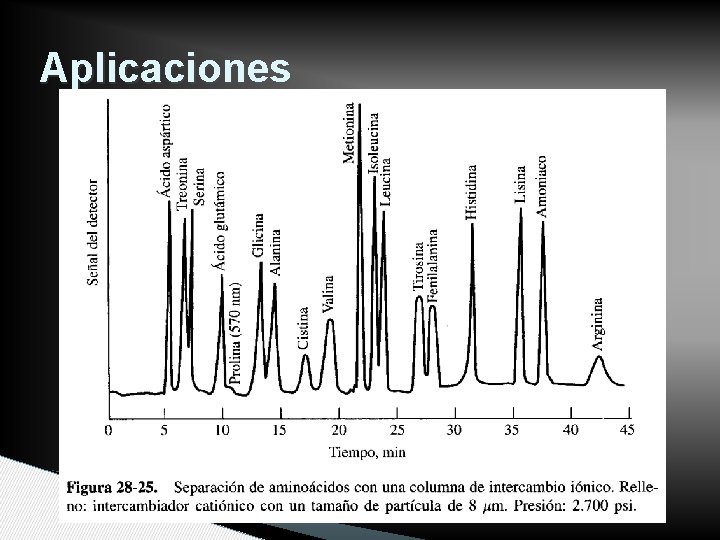
Aplicaciones

CROMATOGRAFÍA DE EXCLUSIÓN MOLECULAR

C. De exclusión molecular • Exclusión por tamaño • Basado en la capacidad de penetración de los analitos en los poros de la FE de acuerdo con su tamaño (y en menor medida con su forma)

FASES ESTACIONARIAS • Red de poros uniforme, a manera de tamiz • Poca interacción con el analito (evitando otros mecanismos de retención) • Partículas de sílica o poliméricas • Polímeros orgánicos o inorgánicos Geles hidrofóbicos o hidrofílicos •

Propiedades FS • Tamaño promedio de poro impone límites a la separación (porosidad o grado de enrecruzamiento). • Límite de exclusión: Peso molecular por encima del cual no se retienen las moléculas • Límite de penetración: Peso molecular por debajo del cual hay libre penetración
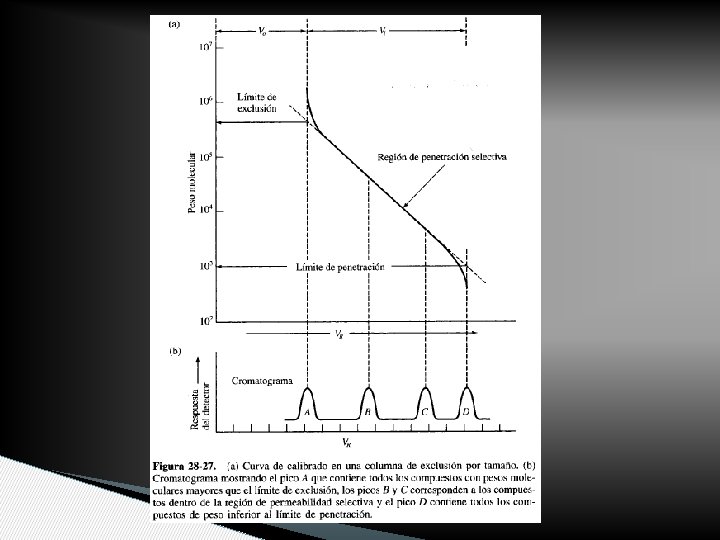

FASES MÓVILES • Capaz de disolver completamente los analitos • En este tipo de c. NO existe fase normal y reversa: • Filtración sobre gel: rellenos hidrofílicos y solventes acuosos • Penetrabilidad sobre gel: rellenos hidrofóbicos y solventes orgánicos no polares

MECANISMO • • http: //www. wiley. com/college/fob/quiz 05/56. html

APLICACIONES • Moléculas grandes, amplio rango de polaridad • Biomoléculas • Polímeros

Aplicaciones de la C. líquida

MUCHAS GRACIAS POR SU ATENCIÓN Fin
- Slides: 67