Cp nht iu tr vim gan C TS








![Pangenotypic Regimens: SOF/VEL với 12 tuần ASTRAL-1[1]*: 100 98 ASTRAL-3†[2]: SOF/VEL với 12 tuần Pangenotypic Regimens: SOF/VEL với 12 tuần ASTRAL-1[1]*: 100 98 ASTRAL-3†[2]: SOF/VEL với 12 tuần](https://slidetodoc.com/presentation_image_h2/b4963a98ffc62c1daa156c6d5477eda6/image-20.jpg)
![Pangenotypic Regimens: GLE/PIB với 8 tuần ở bệnh nhân không xơ gan ENDURANCE 1[1]*: Pangenotypic Regimens: GLE/PIB với 8 tuần ở bệnh nhân không xơ gan ENDURANCE 1[1]*:](https://slidetodoc.com/presentation_image_h2/b4963a98ffc62c1daa156c6d5477eda6/image-21.jpg)










- Slides: 36

Cập nhật điều trị viêm gan C TS. BS Nguyễn Văn Dũng Trung tâm Bệnh Nhiệt đới – Bệnh viện Bạch Mai

Dịch tễ học HCV • Ước tính tỷ lệ nhiễm HCV toàn cầu trong năm 2015: 1. 0% (95% ui 0. 8– 1. 1)1 • Tương ứng với 71. 1 triệu (62. 5– 79. 4) nhiễm vi rút 1, 2 • ~399, 000 tử vong mỗi năm, chủ yếu do xơ gan và HCC 2 Tỷ lệ nhiễm HCV và nhiễm mới HCV, theo khu vực WHO, 20152 HCV incidence rate per 100, 000: Best estimate (uncertainty level) 31. 0 (22. 5– 54. 4) 6. 4 (5. 9– 7. 0) New HCV infections (x 1, 000): Best estimate (uncertainty level) 309 (222– 544) 63 (59– 69) Eastern Mediterranean 62. 5 (55. 6– 65. 2) 409 (363– 426) European 61. 8 (50. 3– 66. 0) 565 (460– 603) South-East Asia 14. 8 (12. 5– 26. 9) 287 (243– 524) Western Pacific 6. 0 (5. 6– 6. 6) 111 (104– 124) 23. 7 (21. 3– 28. 7) 1, 751 (1, 572– 2, 120) WHO region African Americas Global Map key 1. Polaris Observatory HCV Collaborators. Lancet Gastroenterol Hepatol 2017; 2: 161– 76; 2. World Health Organization. Global Hepatitis Report 2017. Available at: http: //apps. who. int/iris/bitstream/handle/10665/255016/9789241565455 -eng. pdf? sequence=1 ; EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

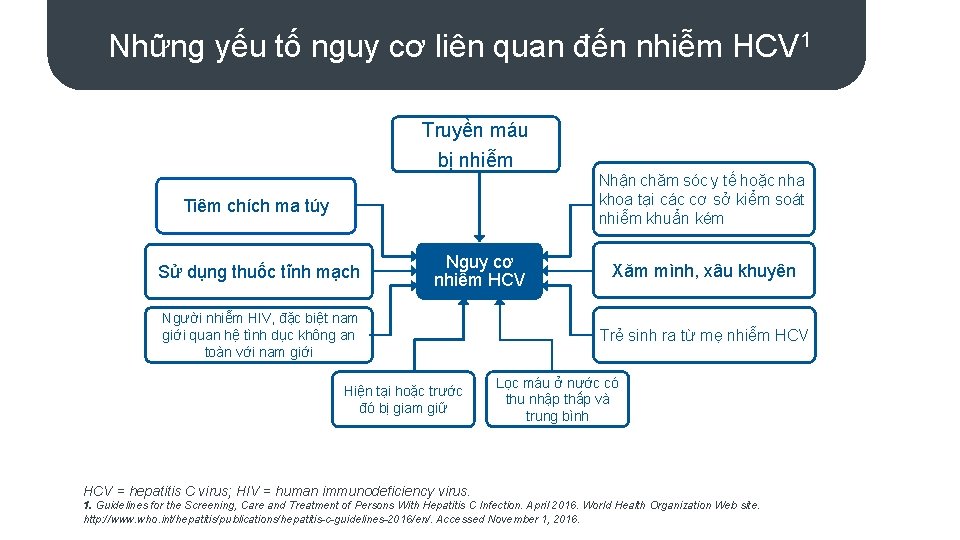
Những yếu tố nguy cơ liên quan đến nhiễm HCV 1 Truyền máu bị nhiễm Nhận chăm sóc y tế hoặc nha khoa tại các cơ sở kiểm soát nhiễm khuẩn kém Tiêm chích ma túy Sử dụng thuốc tĩnh mạch Nguy cơ nhiễm HCV Người nhiễm HIV, đặc biệt nam giới quan hệ tình dục không an toàn với nam giới Hiện tại hoặc trước đó bị giam giữ Xăm mình, xâu khuyên Trẻ sinh ra từ mẹ nhiễm HCV Lọc máu ở nước có thu nhập thấp và trung bình HCV = hepatitis C virus; HIV = human immunodeficiency virus. 1. Guidelines for the Screening, Care and Treatment of Persons With Hepatitis C Infection. April 2016. World Health Organization Web site. http: //www. who. int/hepatitis/publications/hepatitis-c-guidelines-2016/en/. Accessed November 1, 2016.

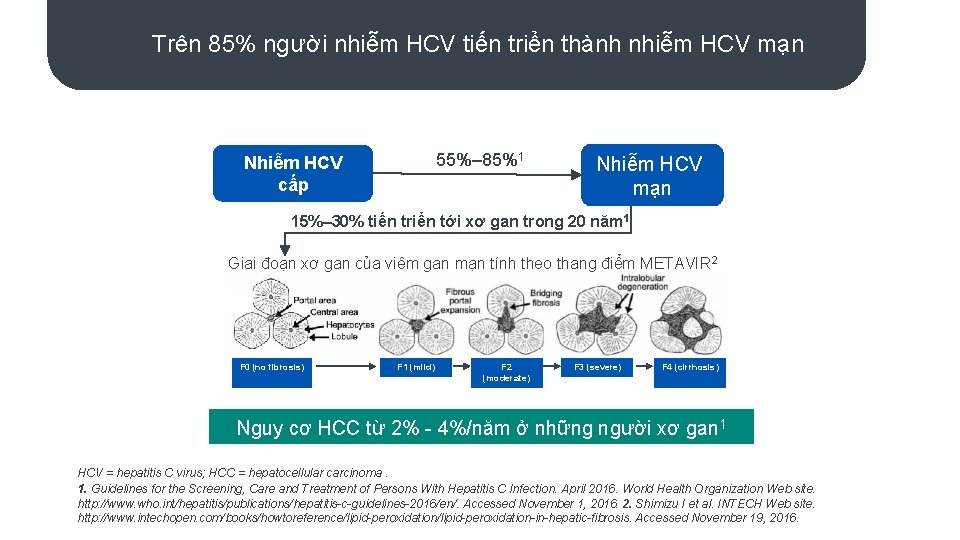
Trên 85% người nhiễm HCV tiến triển thành nhiễm HCV mạn 55%– 85%1 Nhiễm HCV cấp Nhiễm HCV mạn 15%– 30% tiến triển tới xơ gan trong 20 năm 1 Giai đoạn xơ gan của viêm gan mạn tính theo thang điểm METAVIR 2 F 0 (no fibrosis) F 1 (mild) F 2 (moderate) F 3 (severe) F 4 (cirrhosis) Nguy cơ HCC từ 2% - 4%/năm ở những người xơ gan 1 HCV = hepatitis C virus; HCC = hepatocellular carcinoma. 1. Guidelines for the Screening, Care and Treatment of Persons With Hepatitis C Infection. April 2016. World Health Organization Web site. http: //www. who. int/hepatitis/publications/hepatitis-c-guidelines-2016/en/. Accessed November 1, 2016. 2. Shimizu I et al. INTECH Web site. http: //www. intechopen. com/books/howtoreference/lipid-peroxidation-in-hepatic-fibrosis. Accessed November 19, 2016.

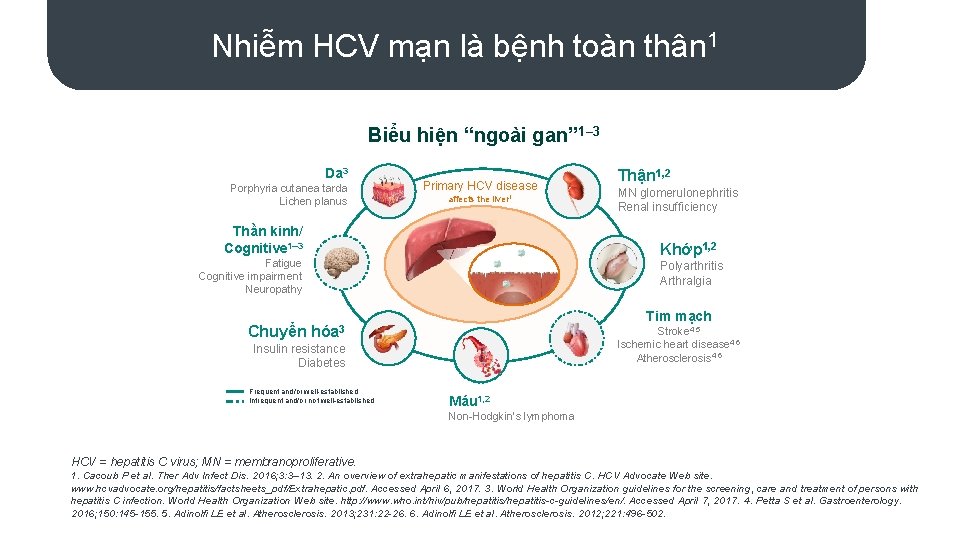
Nhiễm HCV mạn là bệnh toàn thân 1 Biểu hiện “ngoài gan” 1– 3 Da 3 Porphyria cutanea tarda Lichen planus Primary HCV disease affects the liver 1 Thần kinh/ Cognitive 1– 3 MN glomerulonephritis Renal insufficiency Khớp 1, 2 Fatigue Cognitive impairment Neuropathy Chuyển Thận 1, 2 Polyarthritis Arthralgia Tim mạch hóa 3 Stroke 4, 5 Ischemic heart disease 4, 6 Atherosclerosis 4, 6 Insulin resistance Diabetes Frequent and/or well-established Infrequent and/or not well-established Máu 1, 2 Non-Hodgkin’s lymphoma HCV = hepatitis C virus; MN = membranoproliferative. 1. Cacoub P et al. Ther Adv Infect Dis. 2016; 3: 3– 13. 2. An overview of extrahepatic manifestations of hepatitis C. HCV Advocate Web site. www. hcvadvocate. org/hepatitis/factsheets_pdf/Extrahepatic. pdf. Accessed April 6, 2017. 3. World Health Organization guidelines for the screening, care and treatment of persons with hepatitis C infection. World Health Organization Web site. http: //www. who. int/hiv/pub/hepatitis-c-guidelines/en/. Accessed April 7, 2017. 4. Petta S et al. Gastroenterology. 2016; 150: 145 -155. 5. Adinolfi LE et al. Atherosclerosis. 2013; 231: 22 -26. 6. Adinolfi LE et al. Atherosclerosis. 2012; 221: 496 -502.

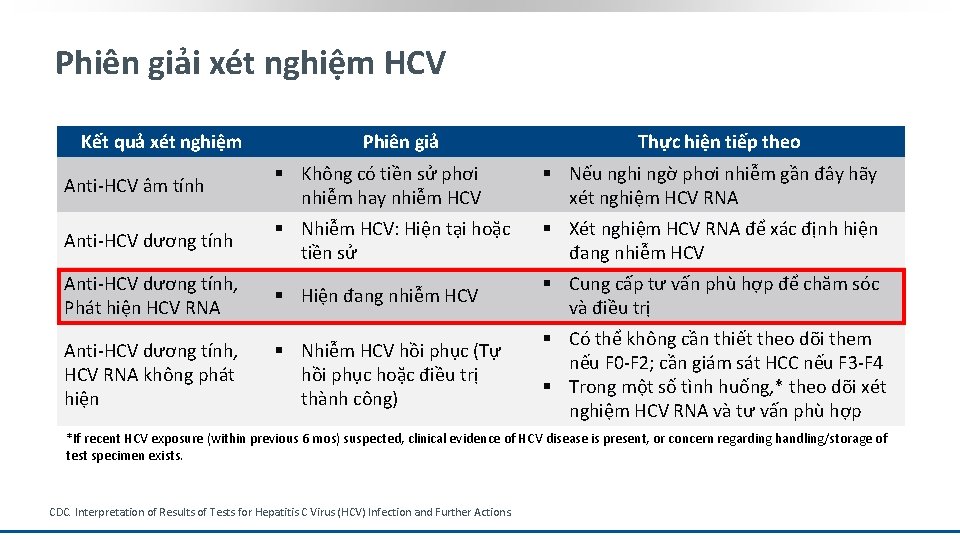
Phiên giải xét nghiệm HCV Kết quả xét nghiệm Phiên giả Thực hiện tiếp theo Anti-HCV âm tính § Không có tiền sử phơi nhiễm hay nhiễm HCV § Nếu nghi ngờ phơi nhiễm gần đây hãy xét nghiệm HCV RNA Anti-HCV dương tính § Nhiễm HCV: Hiện tại hoặc tiền sử § Xét nghiệm HCV RNA để xác định hiện đang nhiễm HCV Anti-HCV dương tính, Phát hiện HCV RNA § Hiện đang nhiễm HCV § Cung cấp tư vấn phù hợp để chăm sóc và điều trị Anti-HCV dương tính, HCV RNA không phát hiện § Nhiễm HCV hồi phục (Tự hồi phục hoặc điều trị thành công) § Có thể không cần thiết theo dõi them nếu F 0 -F 2; cần giám sát HCC nếu F 3 -F 4 § Trong một số tình huống, * theo dõi xét nghiệm HCV RNA và tư vấn phù hợp *If recent HCV exposure (within previous 6 mos) suspected, clinical evidence of HCV disease is present, or concern regarding handling/storage of test specimen exists. CDC. Interpretation of Results of Tests for Hepatitis C Virus (HCV) Infection and Further Actions.

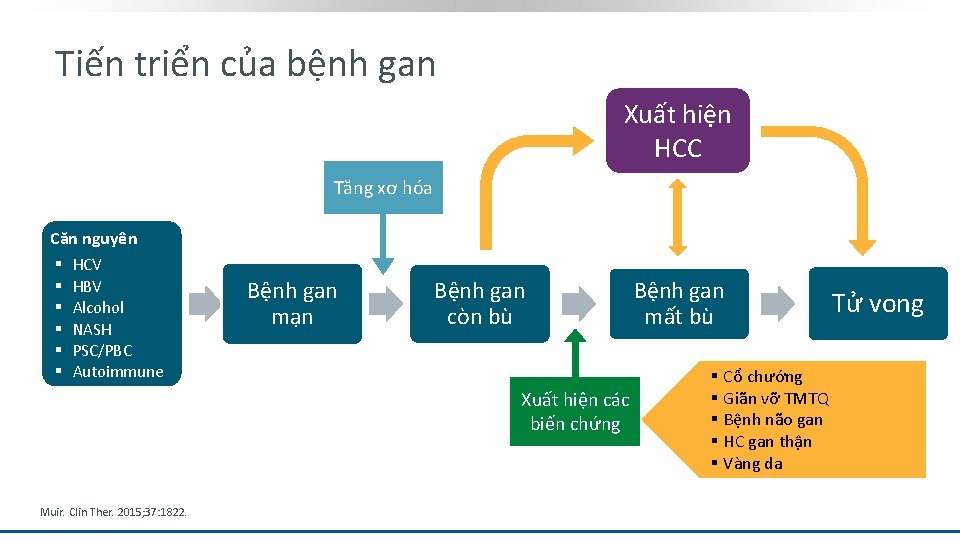
Tiến triển của bệnh gan Xuất hiện HCC Tăng xơ hóa Căn nguyên § HCV § HBV § Alcohol § NASH § PSC/PBC § Autoimmune Bệnh gan mạn Bệnh gan còn bù Xuất hiện các biến chứng Muir. Clin Ther. 2015; 37: 1822. Bệnh gan mất bù § Cổ chướng § Giãn vỡ TMTQ § Bệnh não gan § HC gan thận § Vàng da Tử vong

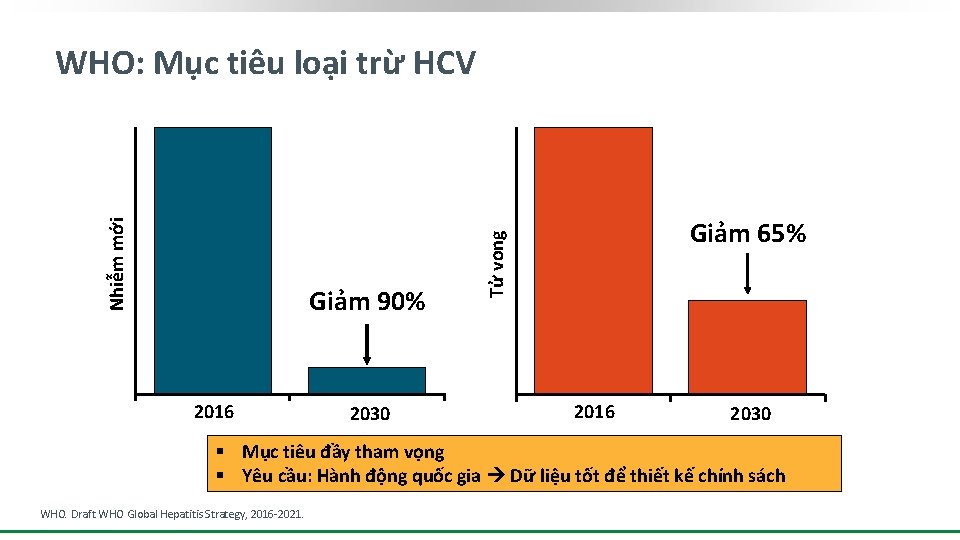
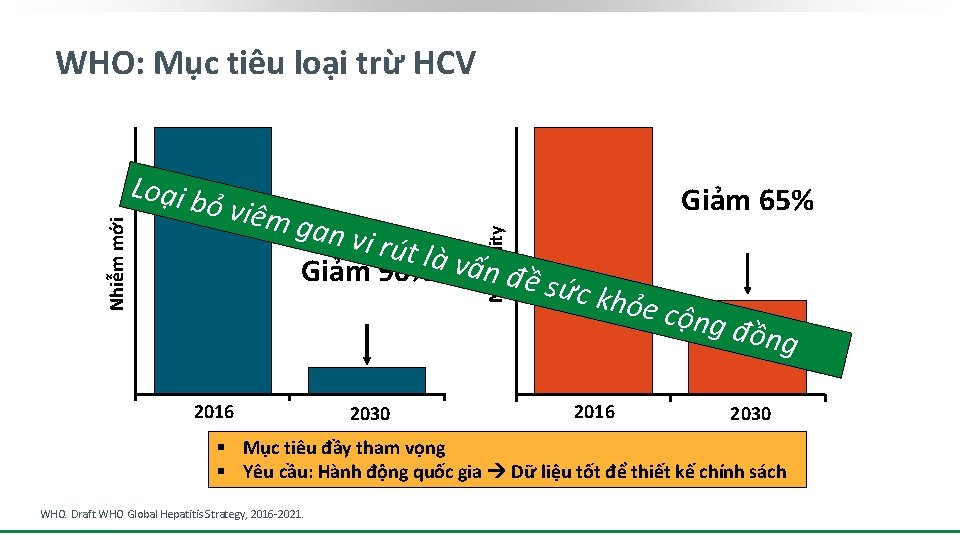
Giảm 90% 2016 2030 Giảm 65% Tử vong Nhiễm mới WHO: Mục tiêu loại trừ HCV 2016 2030 § Mục tiêu đầy tham vọng § Yêu cầu: Hành động quốc gia Dữ liệu tốt để thiết kế chính sách WHO. Draft WHO Global Hepatitis Strategy, 2016 -2021.

Loại b ỏ viêm Giảm 65% gan v i rút là Giảm 90% vấn đề s Mortality Nhiễm mới WHO: Mục tiêu loại trừ HCV ức kh ỏe cộn g đồn g 2016 2030 § Mục tiêu đầy tham vọng § Yêu cầu: Hành động quốc gia Dữ liệu tốt để thiết kế chính sách WHO. Draft WHO Global Hepatitis Strategy, 2016 -2021.

Mục tiêu điều trị • Mục tiêu – điều trị khỏi nhiễm HCV để: – Ngăn ngừa các biến chứng liên quan đến gan và các bệnh ngoài gan, bao gồm: • Hoại tử gan, xơ hóa, xơ gan mất bù, HCC, biểu hiện ngoài gan nặng và tử vong – Cải thiện chất lượng cuộc sống và xóa bỏ sự kỳ thị – Ngăn ngừa sự lây truyền HCV EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Chỉ định điều trị: Ai nên điều trị? Tất cả BN nhiễm HCV phải được xem xét điều trị, bao gồm BN chưa từng điều trị và BN thất bại điều trị BN cần được điều trị không chậm chễ • Xơ hóa đáng kể hoặc xơ gan (METAVIR score ≥F 2): bao gồm xơ gan còn bù (Child–Pugh A) và xơ gan mất bù (Child–Pugh B or C) • Các biểu hiện lâm sàng ngoài gan rõ ràng† • HCV tái phát sau ghép gan • BN có nguy cơ bệnh gan tiến triển nhanh do bệnh kèm theo‡ • Những người có nguy cơ lây truyền HCV – PWID – MSM với hành vi tình dục có nguy cơ cao – Phụ nữ trong tuổi sinh đẻ muốn có thai – Bệnh nhân chạy thận nhân tạo – Cá nhân bị giam giữ (Incarcerated individuals) • Những BN xơ gan mất bù và chỉ định ghép gan (MELD score ≥ 18– 20), ghép trước và điều trị sau ghép • Thời gian đợi >6 tháng, điều trị trước khi ghép (clinical benefit not well established) • Điều trị không được khuyến cáo ở những BN có tuổi thọ hạn chế do bệnh đi kèm không liên quan đến gan *Individuals who failed to achieve SVR after prior treatment; †Symptomatic vasculitis associated with HCV-related mixed cryoglobulinaemia, HCV immune complexrelated nephropathy and non-Hodgkin B-cell lymphoma; ‡Non-liver solid organ or stem cell transplant recipients, HBV coinfection, diabetes EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Nhiễm HCV cấp: Điều trị hay trì hoãn? § Nguy cơ của trì hoãn ‒ Nguy cơ lây truyền § Rào cản của điều trị ngay nhiễm HCV cấp ‒ Hướng dẫn không xác nhận điều trị ngay ‒ Thuốc DAAs không chấp nhận điều trị HCV cấp Khuyến cáo điều trị nhiễm HCV cấp Nếu bác sĩ và bệnh nhân quyết định rằng chậm điều trị là chấp nhận được, việc theo dõi chuyển đảo huyết thanh được khuyến cáo trong tối thiểu 6 tháng. Khi quyết định điều trị sau 6 tháng, điều trị thực hiện như viêm gan C mạn. Nếu quyết định điều trị trong giai đoạn nhiễm HCV cấp, theo dõi HCV-RNA trong ít nhất 12 -15 tuần trước khi bắt đầu điều trị để có thời gian tự thanh thải. AASLD-IDSA. HCV guidance. 2018.

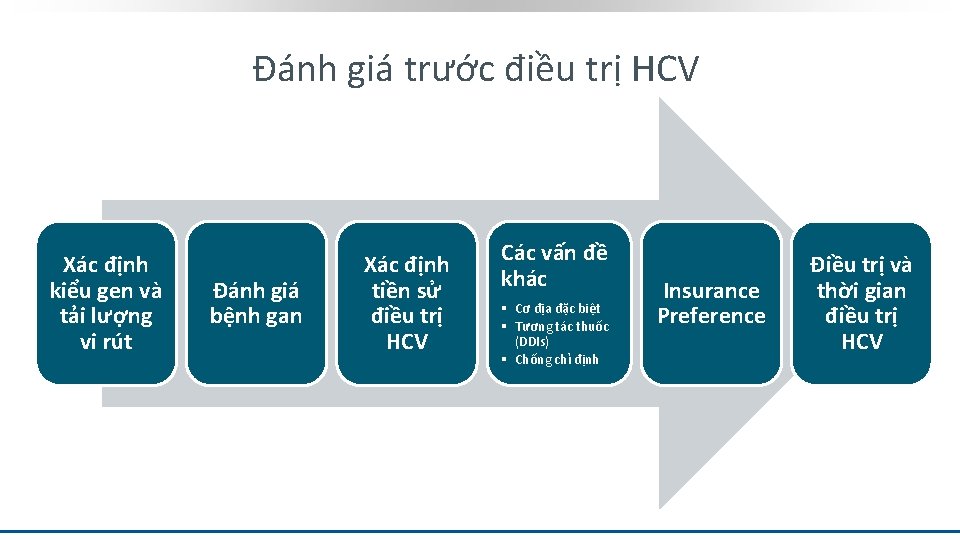
Đánh giá trước điều trị HCV Xác định kiểu gen và tải lượng vi rút Đánh giá bệnh gan Xác định tiền sử điều trị HCV Các vấn đề khác § Cơ địa đặc biệt § Tương tác thuốc (DDIs) § Chống chỉ định Insurance Preference Điều trị và thời gian điều trị HCV

EASL HCV Guidelines: Đánh giá trước điều trị § Đánh giá mức độ nặng của bệnh gan § Đánh giá và thực hiện các biện pháp điều trị thích hợp với các bệnh đi kèm tác động vào tiến triển của bệnh gan § Xác định BN bị xơ gan ‒ Xơ gan đòi hỏi phải điều chỉnh phác đồ điều trị và theo dõi HCC sau điều trị ‒ Bệnh nhân bị xơ hóa tiến triển (METAVIR F 3) cũng cần theo dõi HCC sau điều trị EASL. HCV Guidelines. 2018. § Đánh giá ban đầu giai đoạn xơ hóa nên sử dung phương pháp không xâm lấn ‒ Sử dụng sinh thiết gan với những trường hợp không chắc chắn hoặc các nguyên nhân khác có thể § Đánh giá chức năng thận (ie, creatinine/ e. GFR) § Xác định các biểu hiện ngoài gan của HCV nếu xuất hiện § Tiêm vac xin HBV, HAV cho những người chưa được bảo vệ

Cân nhắc điều trị HCV § Kiểu gen/tải lượng vi rút § Tiền sử điều trị ‒ Chưa điều trị ‒ Điều trị trước đó ‒ Thất bại điều trị trước đó ‒ Kháng thuốc § Thuốc hiện tại § Tiền sử bệnh (Medical history) ‒ CTM, CN gan, cơ bản § Giai đoạn bệnh gan ‒ Xơ hóa và xơ gan ‒ Xơ gan còn bù, mất bù § Cơ địa đặc biệt ‒ Đồng nhiễm HIV ‒ Tương tác thuốc (Drug–drug interactions) ‒ Bệnh thận mạn (Chronic kidney disease) ‒ Tiền sử uống các thảo dược ‒ Ghép tạng

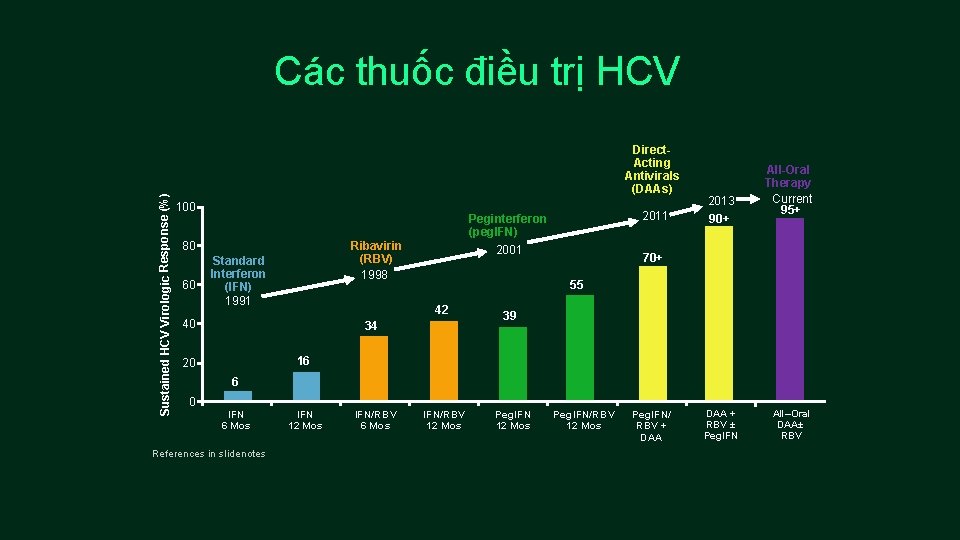
Sustained HCV Virologic Response (%) Các thuốc điều trị HCV Direct. Acting Antivirals (DAAs) 100 80 60 2011 Peginterferon (peg. IFN) Ribavirin (RBV) 1998 Standard Interferon (IFN) 1991 2001 70+ 55 42 40 2013 90+ All-Oral Therapy Current 95+ 34 39 16 20 6 0 IFN 6 Mos References in slidenotes IFN 12 Mos IFN/RBV 6 Mos IFN/RBV 12 Mos Peg. IFN/ RBV + DAA + RBV ± Peg. IFN All–Oral DAA± RBV

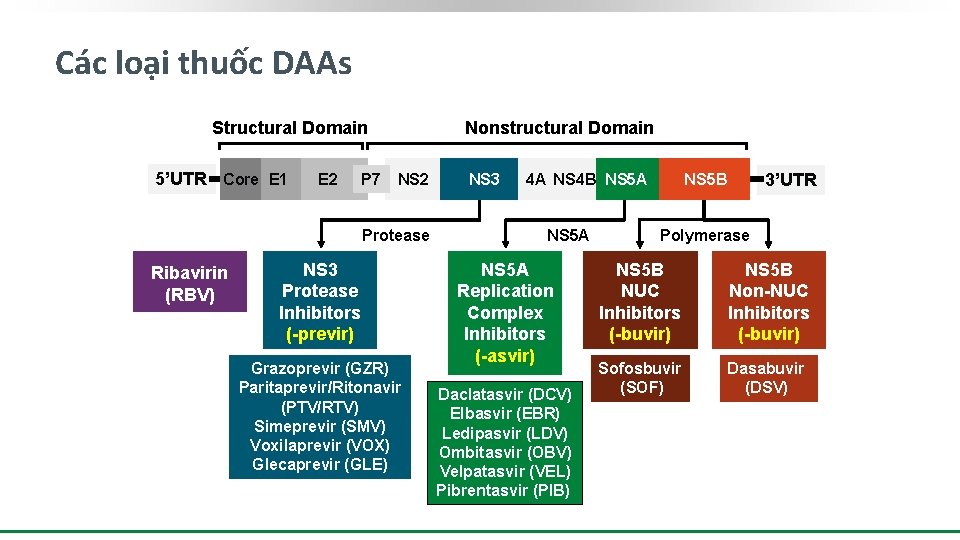
Các loại thuốc DAAs Structural Domain 5’UTR Core E 1 E 2 P 7 Nonstructural Domain NS 2 Protease Ribavirin (RBV) NS 3 Protease Inhibitors (-previr) Grazoprevir (GZR) Paritaprevir/Ritonavir (PTV/RTV) Simeprevir (SMV) Voxilaprevir (VOX) Glecaprevir (GLE) NS 3 4 A NS 4 B NS 5 A Replication Complex Inhibitors (-asvir) Daclatasvir (DCV) Elbasvir (EBR) Ledipasvir (LDV) Ombitasvir (OBV) Velpatasvir (VEL) Pibrentasvir (PIB) 3’UTR NS 5 B Polymerase NS 5 B NUC Inhibitors (-buvir) NS 5 B Non-NUC Inhibitors (-buvir) Sofosbuvir (SOF) Dasabuvir (DSV)

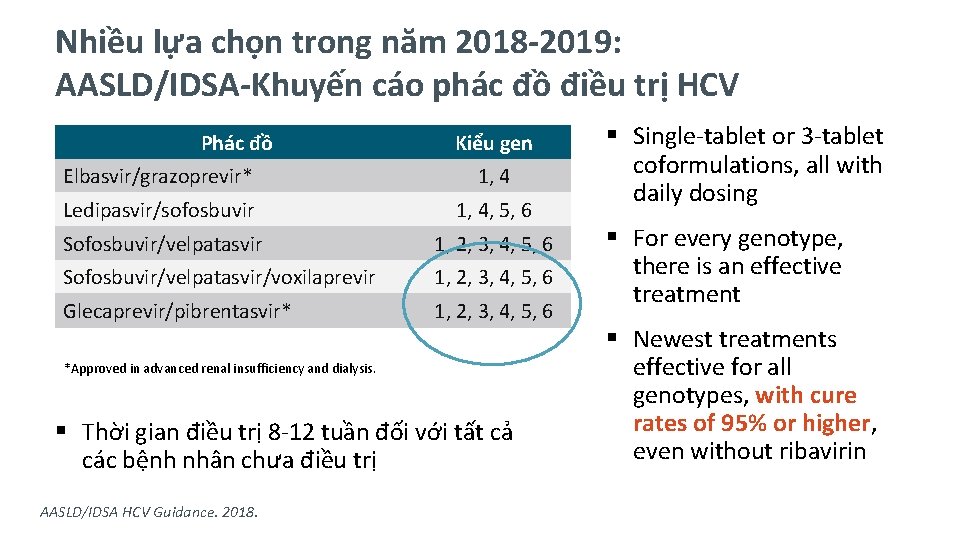
Nhiều lựa chọn trong năm 2018 -2019: AASLD/IDSA-Khuyến cáo phác đồ điều trị HCV Phác đồ Kiểu gen Elbasvir/grazoprevir* 1, 4 Ledipasvir/sofosbuvir 1, 4, 5, 6 Sofosbuvir/velpatasvir 1, 2, 3, 4, 5, 6 Sofosbuvir/velpatasvir/voxilaprevir 1, 2, 3, 4, 5, 6 Glecaprevir/pibrentasvir* 1, 2, 3, 4, 5, 6 *Approved in advanced renal insufficiency and dialysis. § Thời gian điều trị 8 -12 tuần đối với tất cả các bệnh nhân chưa điều trị AASLD/IDSA HCV Guidance. 2018. § Single-tablet or 3 -tablet coformulations, all with daily dosing § For every genotype, there is an effective treatment § Newest treatments effective for all genotypes, with cure rates of 95% or higher, even without ribavirin

Rất nhiều lựa chọn… Làm thế nào để bạn chọn đúng? § Tất cả đều tác dụng tốt! § Tỷ lệ SVR > 95% trong tất cả các thử nghiệm lâm sàng và nghiên cứu thực tế § An toàn/Dung nạp tuyệt vời § Đối với hầu hết bệnh nhân, bất kỳ lựa chọn nào đều tốt
![Pangenotypic Regimens SOFVEL với 12 tuần ASTRAL11 100 98 ASTRAL32 SOFVEL với 12 tuần Pangenotypic Regimens: SOF/VEL với 12 tuần ASTRAL-1[1]*: 100 98 ASTRAL-3†[2]: SOF/VEL với 12 tuần](https://slidetodoc.com/presentation_image_h2/b4963a98ffc62c1daa156c6d5477eda6/image-20.jpg)
Pangenotypic Regimens: SOF/VEL với 12 tuần ASTRAL-1[1]*: 100 98 ASTRAL-3†[2]: SOF/VEL với 12 tuần in GT 3 SOF/VEL với 12 tuần in GT 1, 2, 4, 5, 6 99 100 97 100 80 40 20 n/N = 0 1 relapse 2 lost to f/u 1 withdrew consent SVR 12 (%) 80 60 97 1 relapse 1 death 206/ 210 117/ 118 104/ 104 116/ 116 34/ 35 41/ 41 1 a 1 b 2 4 5 6 60 40 20 n/N = 0 HCV Genotype *Graph includes treatment-naive and treatment-experienced patients, with and without cirrhosis. †Graph includes treatment-naive and treatment-experienced patients. 1. Feld. NEJM. 2015; 373: 2599. 2. Foster. NEJM. 2015; 373: 2608. 191/ 197 Không xơ gan (F 0 -F 3)
![Pangenotypic Regimens GLEPIB với 8 tuần ở bệnh nhân không xơ gan ENDURANCE 11 Pangenotypic Regimens: GLE/PIB với 8 tuần ở bệnh nhân không xơ gan ENDURANCE 1[1]*:](https://slidetodoc.com/presentation_image_h2/b4963a98ffc62c1daa156c6d5477eda6/image-21.jpg)
Pangenotypic Regimens: GLE/PIB với 8 tuần ở bệnh nhân không xơ gan ENDURANCE 1[1]*: GT 1 100 99. 1 SURVEYOR 2, Part 4[2]*: GT 2, 4, 5, 6 98 93 100 ENDURANCE-3[1]: GT 3 90 100 60 40 20 n/N = 0 99 75 80 SVR 12 (%) 80 95 1 breakthrough (GT 1 a) 2 relapses 332/ 335 142/ 145 43/ 46 1 2 4 2/2 5 HCV Genotype *Includes treatment-naive and treatment-experienced patients. 1. Zeuzem. NEJM. 2018; 378: 354. 2. Asselah. Clin Gastro Hepatol. 2018; 16: 417. 9/10 6 60 40 20 n/N = 0 1 breakthrough 5 relapse 2 lost to f/u All 4 developed Y 93 H 149/ 157 135/ 137 12/ 16 Overall No A 30 K With A 30 K

Bệnh nhân mắc bệnh gan nặng • Do hiệu quả, dễ sử dụng, an toàn và dung nạp, phác đồ điều trị không có IFN là lựa chọn duy nhất ở BN xơ gan mất bù (Child–Pugh B or C) không có HCC đợi ghép gan Recommendations Chỉ định điều trị • MELD score <18– 20: điều trị trước khi ghép gan • MELD score ≥ 18– 20: – Ghép đầu tiên mà không cần điều trị thuốc kháng vi rút và điều trị nhiễm HCV sau khi ghép – Điều trị trước khi ghép nếu thời gian chờ đợi vượt quá 6 tháng (depending on the local situation) Điều trị (MELD score <18– 20) • SOF/LDV (GT 1, 4, 5 và 6) or SOF/VEL (tất cả genotyp) + RBV* for 12 tuần • Chống chỉ định với phác đồ chứa ức chế protease • Chống chỉ định/dung nạp kém với RBV: SOF/LDV (GT 1, 4, 5, 6) or SOF/VEL (tất cả genotyp) for 24 tuần *Daily weight-based RBV (1, 000 mg or 1, 200 mg in patients <75 kg or ≥ 75 kg, respectively); start RBV at a dose of 600 mg daily and adjust dose depending on tolerance EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Bệnh nhân mắc bệnh gan nặng Recommendations Tái phát sau ghép gan • Tất cả bệnh nhân tái phát sau ghép gan nên được xem xét điều trị • Điều trị nên được bắt đầu sớm sau khi ghép (≥ 3 tháng) • Phác đồ điều trị bao gồm: – – SOF/VEL trong 12 tuần (tất cả genotyp) SOF/LDV trong 12 tuần (GT 1, 4, 5, 6) GLE/PIB trong 12 tuần (e. GFR ≤ 30 m. L/min/1. 73 m 2; tất cả genotyp)* SOF/LDV or SOF/LDV + RBV trong 24 tuần (xơ gan mất bù)† HCC với chỉ định ghép gan • Ghép gan phải được coi là mục tiêu điều trị chính • Đưa ra quyết định theo từng trường hợp thông qua thảo luận nhóm (MDT) • Điều trị HCV có thể được bắt đầu trước hoặc trì hoãn cho đến khi ghép tùy thuộc vào hoàn cảnh HCC không có chỉ định ghép gan • Điều trị HCV nên được thực hiện nhưng HCC nên được theo dõi sau khi đạt SVR • Sử dụng các phác đồ DAA tườn tự bệnh nhân xơ gan mất bù không có HCC chờ ghép gan *Monitor immunosuppressant drug levels and dose adjust; †Daily weight-based RBV (1, 000 mg or 1, 200 mg in patients <75 kg or ≥ 75 kg, respectively); start RBV at a dose of 600 mg daily and adjust dose depending on tolerance EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

HCV là nguyên nhân và biến chứng của CKD 1 Lây nhiễm HCV có thể là kết quả điều trị CKD 1– 5: • Truyền máua • Lây nhiễm qua ghép thận • Lây nhiễm tại đơn vị lọc máu HCV là 1 yếu tố nguy cơ độc lập của CKD 2, 6 • HCV là nguyên nhân đáng kể gây bệnh thận đặc biệt MN glomerulonephritis 1, 7 • Nhiễm HCV liên quan đến 80% trường hợp viêm mạch máu liên quan đến phức hợp cryoglobulin và MN glomerulonephritis 7 HCV = hepatitis C virus; CKD = chronic kidney disease; MN = membranoproliferative. a. In the absence of effective screening of blood donors for HCV. 1. Fabrizi F et al. New J Sci. 2014; doi. org/10. 1155/2014/180203. 2. KDIGO 2017 Draft clinical practice guidelines for the prevention, diagnosis, evaluation, and treatment of hepatitis C in chronic kidney disease. Kidney Disease: Improving Global Outcomes Web site. ww. kdigo. org/clinical_practice_guidelines/Hep%20 C/KDIGO%202017%20 Hep%20 C%20 GL%20 Public%20 Review%20 Draft%20 FINAL. pdf. Accessed March 3, 2017. 3. Fabrizi F et al. Int J Artif Organs. 2015; 38: 471– 480. 4. Guidelines for the screening, care and treatment of persons with hepatitis C infection. World Health Organization Web site. http: //www. who. int/hiv/pub/hepatitis-c-guidelines/en/. Accessed April 7, 2017. 5. Jadoul M et al. Blood Purif. 2017; 43: 206– 209. 6. Chen Y et al. Kidney Int. 2013; 85: 1200– 1207. 7. Cacoub P et al. Ther Adv Infect Dis. 2016; 3: 3– 13.

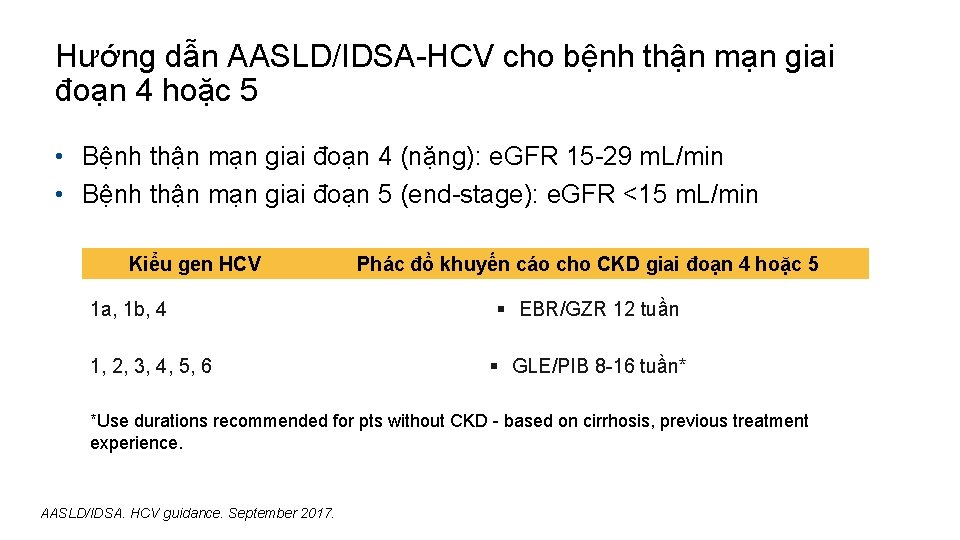
Hướng dẫn AASLD/IDSA-HCV cho bệnh thận mạn giai đoạn 4 hoặc 5 • Bệnh thận mạn giai đoạn 4 (nặng): e. GFR 15 -29 m. L/min • Bệnh thận mạn giai đoạn 5 (end-stage): e. GFR <15 m. L/min Kiểu gen HCV 1 a, 1 b, 4 1, 2, 3, 4, 5, 6 Phác đồ khuyến cáo cho CKD giai đoạn 4 hoặc 5 § EBR/GZR 12 tuần § GLE/PIB 8 -16 tuần* *Use durations recommended for pts without CKD - based on cirrhosis, previous treatment experience. AASLD/IDSA. HCV guidance. September 2017.

Tái hoạt HBV: Nguy cơ gì với bệnh nhân HBs. Ag dương tính? § 17 nghiên cứu gồm 1621 BN: 242 BN HBs. Ag (+) § Tái hoạt HBV thường ở BN HBs. Ag (+) : 24% § Viêm gan liên quan đến tái hoạt HBV: 9%, 3 BN suy gan ‒ Nguy cơ thấp nếu HBV DNA âm tính (RR: 0. 17) Mucke. Lancet Gastro Hepatol. 2018; 3: 172.

Tái hoạt HBV: Nguy cơ gì với BN HBc. Ab dương tính? § 17 nghiên cứu gồm 1621 BN: 1379 BN chỉ có HBc. Ab dương tính § Không có BN viêm gan liên quan đến tái hoạt HBV! Mucke. Lancet Gastro Hepatol. 2018; 3: 172.

Tiếp tục sàng lọc HCV sau điều trị § Cần theo dõi và sàng lọc HCV nếu: ‒ Bệnh nhân có nguy cơ nhiễm HCV liên tục ‒ Bệnh nhân TCMT ‒ Nguy cơ lây nhiễm cao quan hệ tình dục ‒ HIV đồng nhiễm MSM ‒ Không giải thích được rối loạn chức năng gan § Yêu cầu định lượng HCV RNA ‒ Bệnh nhân duy trì anti-HCV dương tính sau SVR 12 AASLD/IDSA HCV Guidance. 2018.

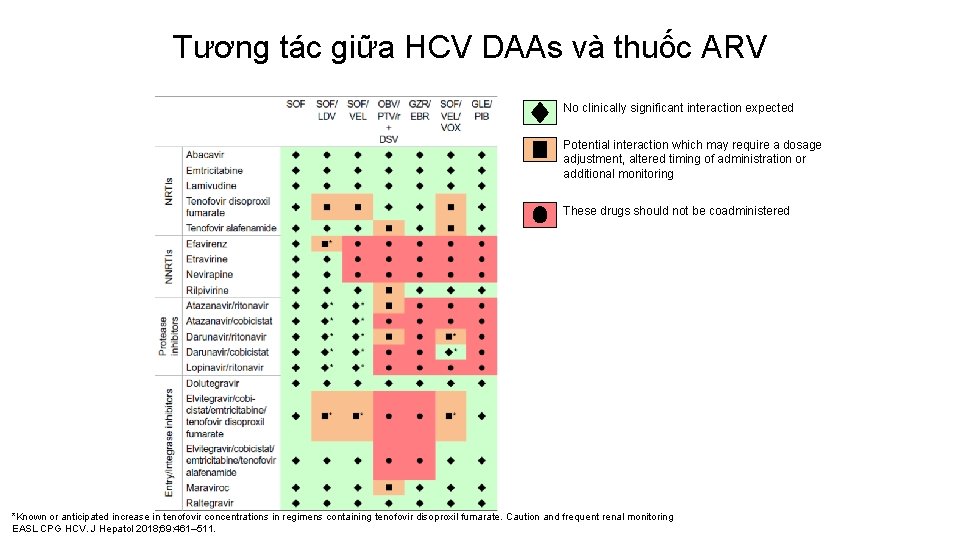
Tương tác giữa HCV DAAs và thuốc ARV No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered *Known or anticipated increase in tenofovir concentrations in regimens containing tenofovir disoproxil fumarate. Caution and frequent renal monitoring EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

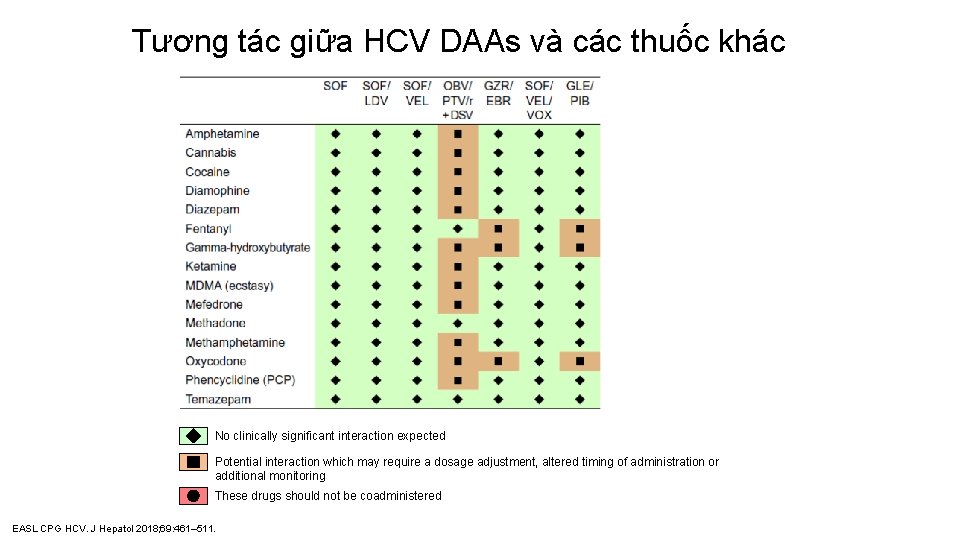
Tương tác giữa HCV DAAs và các thuốc khác No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Tương tác giữa HCV DAAs và thuốc hạ mỡ máu No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Tương tác giữa HCV DAAs và thuốc tác động hệ thần kinh trung ương No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Tương tác giữa HCV DAAs và các thuốc tim mạch No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

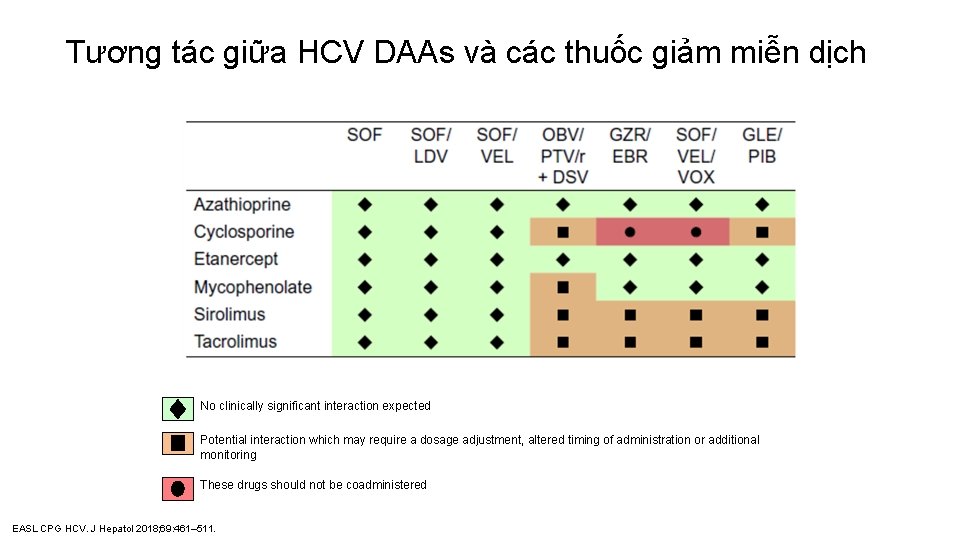
Tương tác giữa HCV DAAs và các thuốc giảm miễn dịch No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

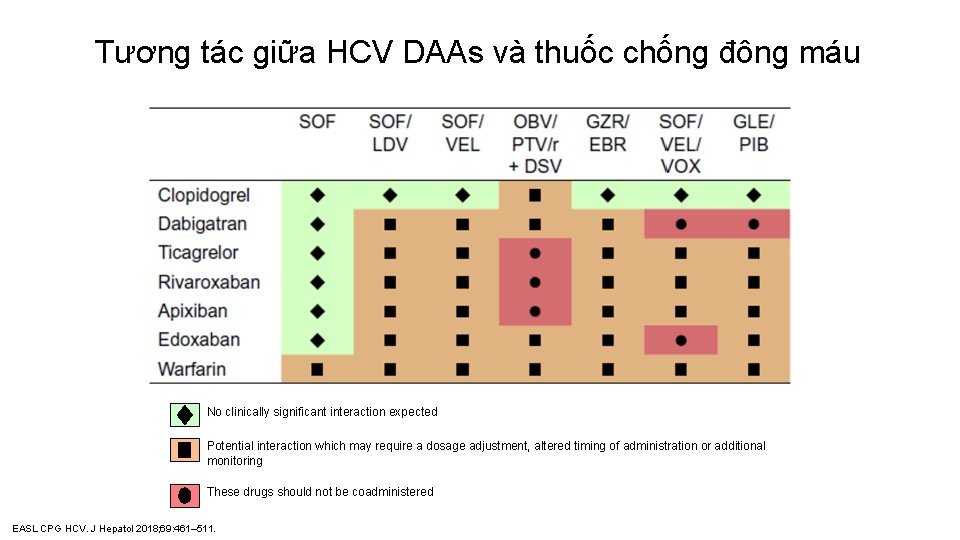
Tương tác giữa HCV DAAs và thuốc chống đông máu No clinically significant interaction expected Potential interaction which may require a dosage adjustment, altered timing of administration or additional monitoring These drugs should not be coadministered EASL CPG HCV. J Hepatol 2018; 69: 461– 511.

Trân trọng cám ơn quý Thầy cô và đồng nghiệp