Cours Master 1 Biologie Molculaire de la Cellule

Cours Master 1 Biologie Moléculaire de la Cellule le 4 décembre 2009 Cellules souches et thérapie cellulair Professeur Claude Desnuelle, Chef du Pôle Neurosciences CHU de Nice Responsable enseignement Biologie Cellulaire, Faculté de Médecine de Nice, UMR CNRS 6543

Statut de cellule souche: définitions • Cellule Souche: capable de s’autorenouveler et de donner naissance à au moins une lignée cellulaire différenciée • Totipotente: donne toutes lignées cellulaires (ex: oeuf fertilisé) • Pluripotente: donne la quasi-totalité des lignées cellulaires (ex: blastocyste, cellule ES) • Multipotente: donne plusieurs lignées cellulaires (ex: cellule hématopoïétique) • Progéniteur: donne un petit nombre de lignées (ex: cellule satellite musculaire) • Caractérisation: phénotypique et/ou fonctionnelle

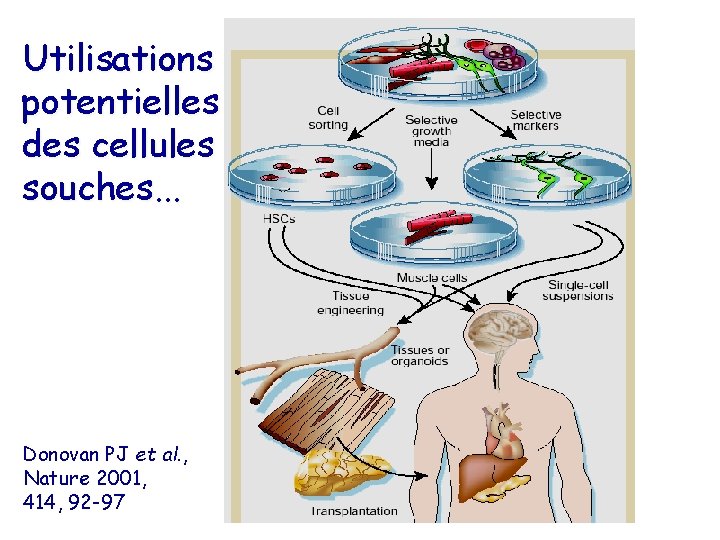
Utilisations potentielles des cellules souches. . . Donovan PJ et al. , Nature 2001, 414, 92 -97
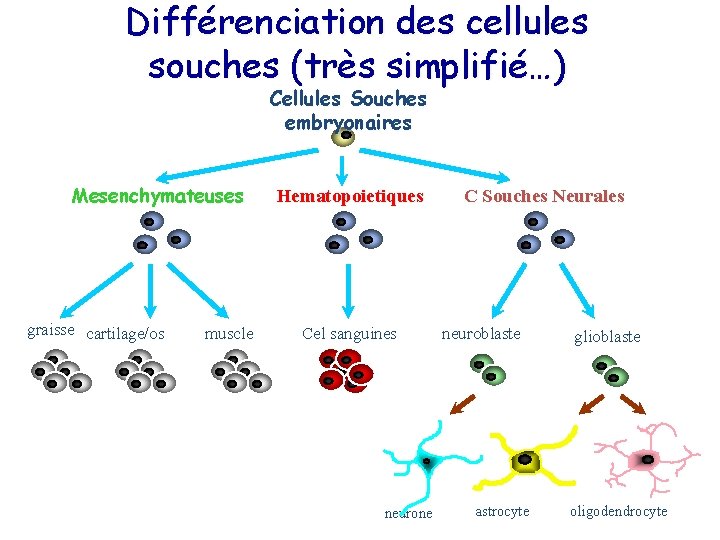
Différenciation des cellules souches (très simplifié…) Cellules Souches embryonaires Mesenchymateuses graisse cartilage/os muscle Hematopoietiques Cel sanguines neurone C Souches Neurales neuroblaste astrocyte glioblaste oligodendrocyte
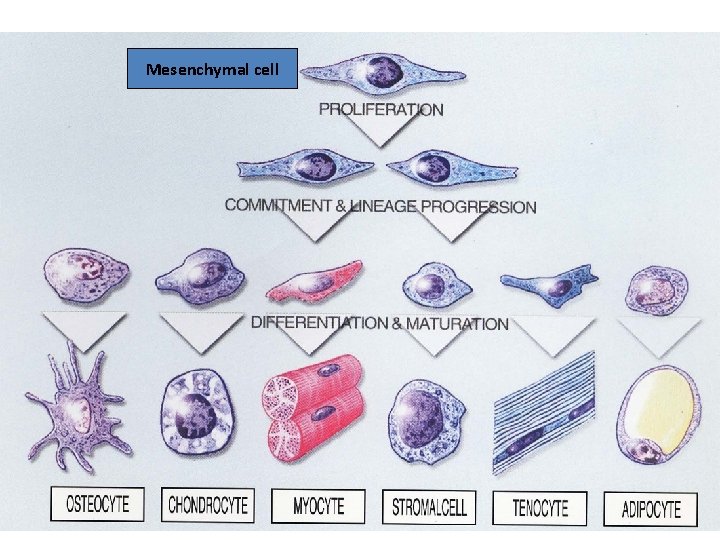
Mesenchymal cell

Utilisations thérapeutiques des cellules souches adultes • Usage clinique établi – Moelle osseuse (autologue, hétérologue), peau (autologue, hétérologue), cartilage • Essais précliniques et cliniques – Système nerveux central (Parkinson, Huntington), coeur (infarctus), pancréas (diabète), muscle (dystrophies), os, organoïdes (sécrétion), cœur • Stade expérimental – Système nerveux périphérique (myéline), coeur (néo-angiogénèse, repopulation), ingénierie tissulaire, foie, rétine, sphincters. . .

Cellules souches adultes: la chute de certains dogmes 1) Présence de cellules souches dans des tissus hautement différenciés 2) Potentiel inattendu de certains précurseurs tissulaires 3) Migration, attraction, et commande de réparation à distance 4) Réparation par substitution tissulaire

1 - Présence de cellules souches en tissus différenciés • Neurones – Uchida et al. , Direct isolation of human central nervous system cells, PNAS 97, 14720, 2000 • Cellules canalaires – Ramiya et al. , Reversal of insulin-dependent diabetes using islets generated in vitro from pancreatic stem cells, Nature Medicine 6, 278, 2000 • Cellules souches de peau et follicule pileux – Oshima et al. , Morphogenesis and renewal of hair follicles from adult multipotent stem cells, Cell 104, 233, 2001 • Adipocytes – Zuk et al. , Multilineage cells from human adipose tissue: implications for cell-based therapies, Tissue Engineering 7, 211, 2001

2 - Hétérogénéité des cellules souches et non-spécificité tissulaire Moelle osseuse: – Prockop, Marrow stromal cells as stem cells for nonhematopoietic tissues, Science 276, 71, 1997 – Johnstone et al. , In vitro chondrogenesis of bone-marrow-derived mesenchymal progenitor cells, Exp Cell Res 238, 265, 1998 – Toma et al. , Human mesenchymal stem cells differentiate to a cardiomyocyte phenotype in the adult murine heart, Circulation 105, 93, 2002 – Orlic et al. , Bone marrow cells regenerate infarcted myocardium, Nature 410, 701, 2001 – Lagasse et al. , Purified hematopoietic stem cells can differentiate into hepatocytes in vivo, Nat Med 6, 1229, 2000 – Woodbury et al. , Adult rat and human bone marrow stromal cells differentiate into neurons, J Neurosci Res 61, 364, 2000

2 - Hétérogénéité des cellules souches et non-spécificité tissulaire Muscle Williams JT et al. , Cells isolated from adult human skeletal muscle capable of differentiating into multiple mesodermal phenotypes, Am Surg 65, 22, 1999 Jackson et al. , Hematopoietic potential of stem cells isolated from murine skeletal muscle, PNAS 96, 14482, 1999 Neurons Bjornson et al. , Turning brain into blood: a hematopoietic fate adopted by adult neural stem cells in vivo, Science 283, 534, 1999 Galli et al. , Skeletal myogenic potential of human and mouse neural stem cells, Nature Neuroscience 3, 986, 2000 Connective tissue Young et al. , Mesenchymal stem cells reside within the connective tissues of many organs, Dev Dyn 202, 137, 1995

3 - Migration des cellules souches, réparation « commandée à distance » Coeur Orlic et al. , Mobilized bone marrow cells repair the infarcted heart, improving function and survival, PNAS 98, 10344, 2001 Kocher et al. , Neovascularization of ischemic myocardium by human bone-marrow-derived angioblasts prevents cardiomyocytes apoptosis, reduces remodeling and improves cardiac function, Nat Med 7, 430, 2001 Quaini et al. , Chimerism of the transplanted heart, New England J Medecine 346, 5, 2002 Jackson, Regeneration of ischemic cardiac muscle and vascular endothelium by adult stem cells, J Clin Invest 107, 1395, 2001 Os Horwitz et al. , Transplantability and therapeutic effects of bone marrow-derived mesenchymal cells in children with osteogenesis imperfecta, Nat Med 5, 309, 1999

3 - Migration des cellules souches, réparation « commandée à distance » Muscle Ferrari et al. , Muscle regeneration by bone marrow-derived myogenic progenitors, Science 279, 1528, 1998 Gussoni et al. , Dystrophin expression in the mdx mouse restored by stem cell transplantation, Nature 401, 1999 Labarge et al. , Biological progression from adult bone marrow to mononucleate muscle stem cell to multinucleate muscle fiber in response to injury, Cell 111, 589 -601, 2002 Colonisations multiples Liechty et al. , Human mesenchymal stem cells engraft and demonstrate sitespecific differentiation after in utero transplantation in sheep, Nat Med 6, 1282, 2000 Foie Lagasse et al. , Purified hematopoietic stem cells can differentiate into hepatocytes in vivo. Nature Medicine 6, 1229 - 1234, 2000
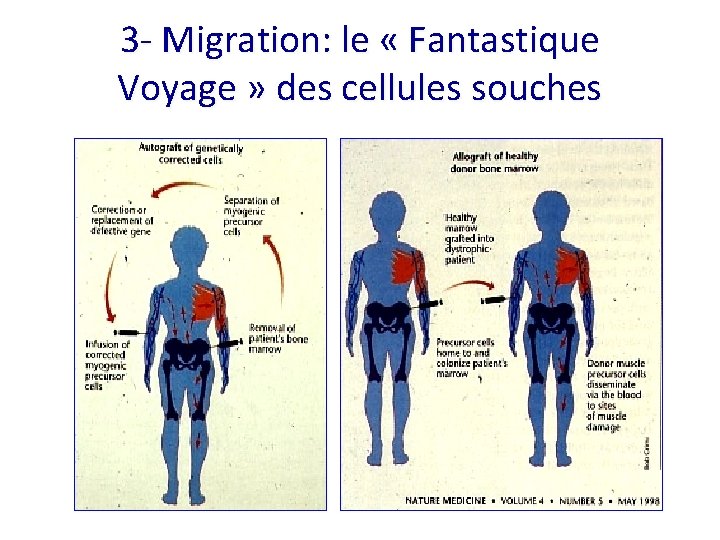
3 - Migration: le « Fantastique Voyage » des cellules souches
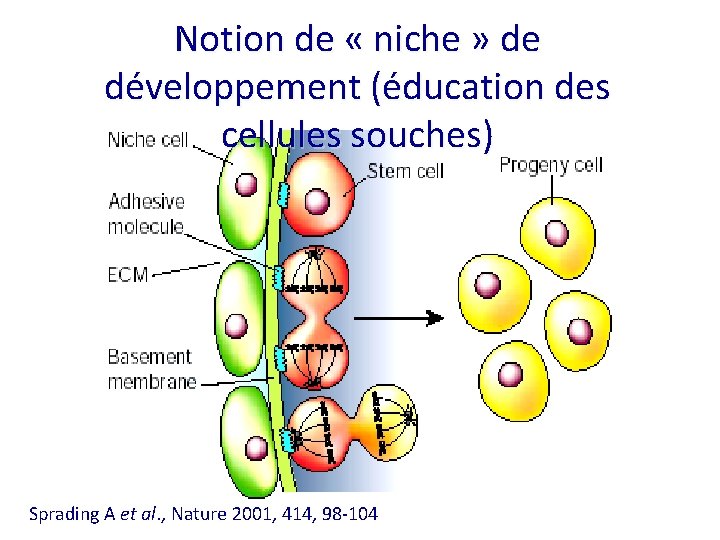
Notion de « niche » de développement (éducation des cellules souches) Sprading A et al. , Nature 2001, 414, 98 -104

Devenir des cellules souches: différents mécanismes discutés Wagers AJ & Weissman I, Cell 2004, 116, 639 -648

Exemples de types de cellules souches identifiées par marqueurs Moelle osseuse Cellules mononuclées Sang Tissus variés: nerveux, musculaire, hépatique, Cellules médullaire, mésenchymateuses pancréatique… CD 34 -, CD 45 -, c-kit-, CEP Cellules mésenchymateus CD 90+, CD 166+ CD 34+, CD 31+, du tissu cardiaque Cellules. CD 105+, hématopoïétiques Cellules CD 34+, c-kit+, CD 133+, Lin- c-kit+, CD 133+, VEGFR 2+, VEmésenchymateuses Cellules monocytiques cadherin+, Tiedu tissu adipeux CD 14+, CD 45+, CD 34 -, CD 133 -, 2+ CD 34+, CD 13, CD 14 low, VE-cadherin. CS sang de cordon. CD 45 low Progéniteurs vasculaires CD 34+, Side population CD 34+, Sca-1+, Ckit+ CD 34 -, c-Kit+, Sca-1+, Hoechst. Somatic stem cells. Cellules associées aux (CD 13+, CD 44+, CD 29+, -MAPCS CD 45 -, CD 14 -) vaisseaux (péricytes, mésangioblastes, CD 34 -, VE-cadherin-, AC 133+, CD 146+): moelle, VEGFR 2+, muscle… Side-populations: tissu EPCs squelettique, CD 34+, CD 31+, c-kit+, médullaire, cardiaque… CD 133+, VEGFR 2+, VE-
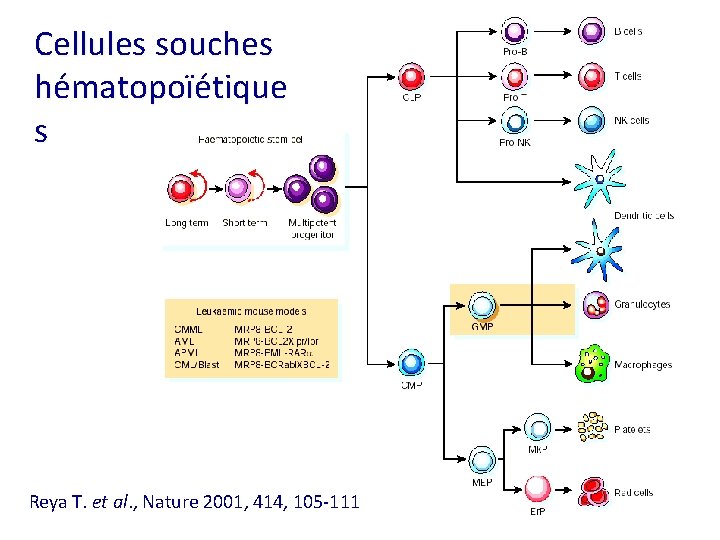
Cellules souches hématopoïétique s Reya T. et al. , Nature 2001, 414, 105 -111

Potentiels de la moelle osseuse • Non fractionnée: mélange • Mésenchyme: progéniteurs vasculaires, adipocytes, ostéoblastes. . . • Cellules mésenchymateuses: - Population native - Cellules traitées (5 -azacytidine) • Fractions hématopoïétiques (34+, 133+…) • Cellules SP multipotentes (Side Population) • Multipotent Adult Progenitor Cells (MAPCs) INSERM-Institut de Myologie
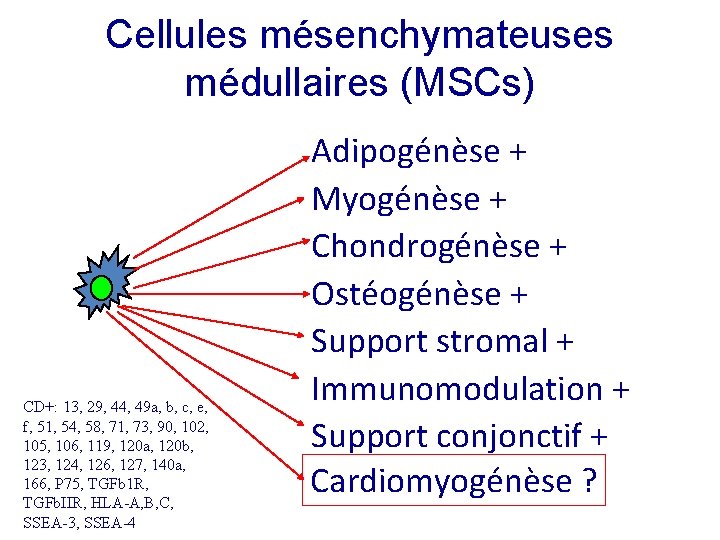
Cellules mésenchymateuses médullaires (MSCs) CD+: 13, 29, 44, 49 a, b, c, e, f, 51, 54, 58, 71, 73, 90, 102, 105, 106, 119, 120 a, 120 b, 123, 124, 126, 127, 140 a, 166, P 75, TGFb 1 R, TGFb. IIR, HLA-A, B, C, SSEA-3, SSEA-4 Adipogénèse + Myogénèse + Chondrogénèse + Ostéogénèse + Support stromal + Immunomodulation + Support conjonctif + Cardiomyogénèse ?
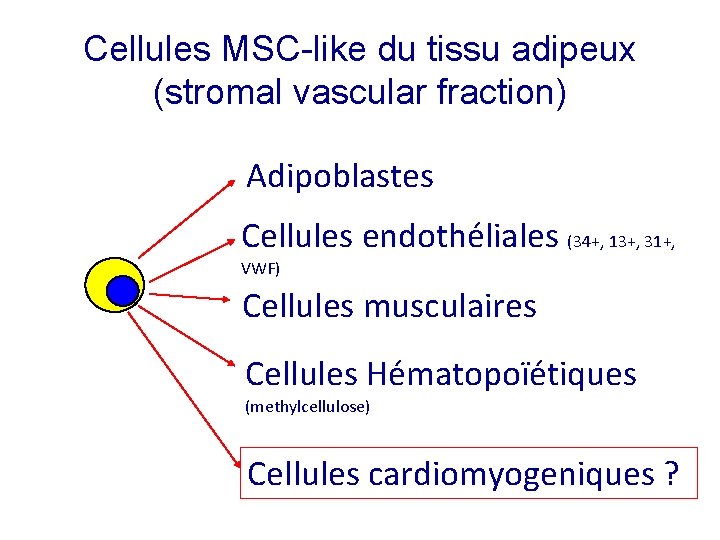
Cellules MSC-like du tissu adipeux (stromal vascular fraction) Adipoblastes Cellules endothéliales (34+, 13+, 31+, VWF) Cellules musculaires Cellules Hématopoïétiques (methylcellulose) Cellules cardiomyogeniques ?
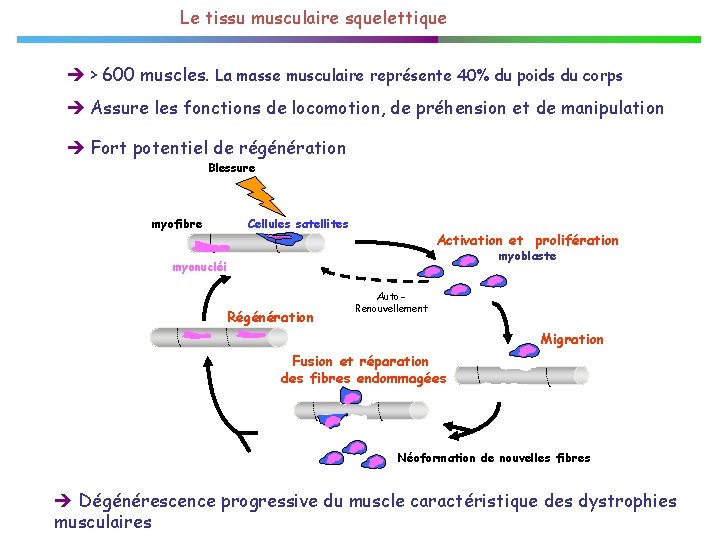
Le tissu musculaire squelettique > 600 muscles. La masse musculaire représente 40% du poids du corps Assure les fonctions de locomotion, de préhension et de manipulation Fort potentiel de régénération Blessure myofibre Cellules satellites Activation et prolifération myoblaste myonucléi Régénération Auto. Renouvellement Migration Fusion et réparation des fibres endommagées Néoformation de nouvelles fibres Dégénérescence progressive du muscle caractéristique des dystrophies musculaires
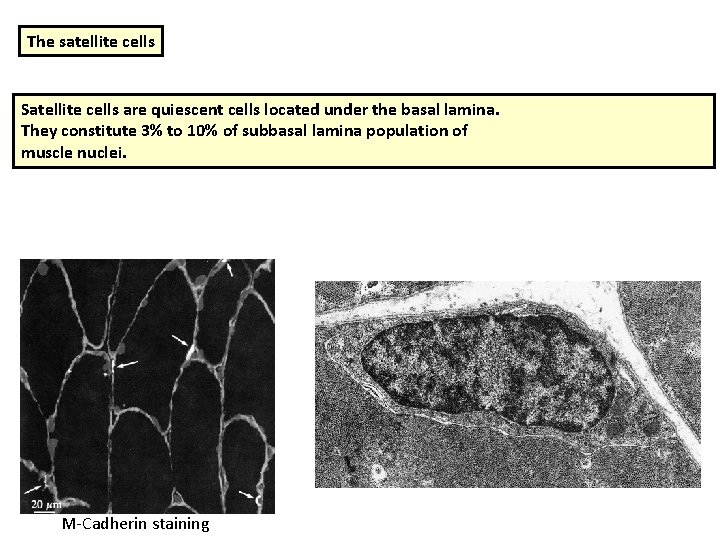
The satellite cells Satellite cells are quiescent cells located under the basal lamina. They constitute 3% to 10% of subbasal lamina population of muscle nuclei. M-Cadherin staining

The satellite cells Proliferation of satellite cells is evoked not only by acute muscle injury but also by overuse. Satellite cells are able to form myofibers through a process equivalent to embryonic myogenesis. They represent the major source of myogenic cells in adult mamalian muscle : mononucleate myoblasts have a key role in regeneration In dystrophic muscle, multiple rounds of regeneration give rise to satellite cells with a decreased proliferation ability, and reduced telomere length when compared to satellite cells from young and healthy muscle
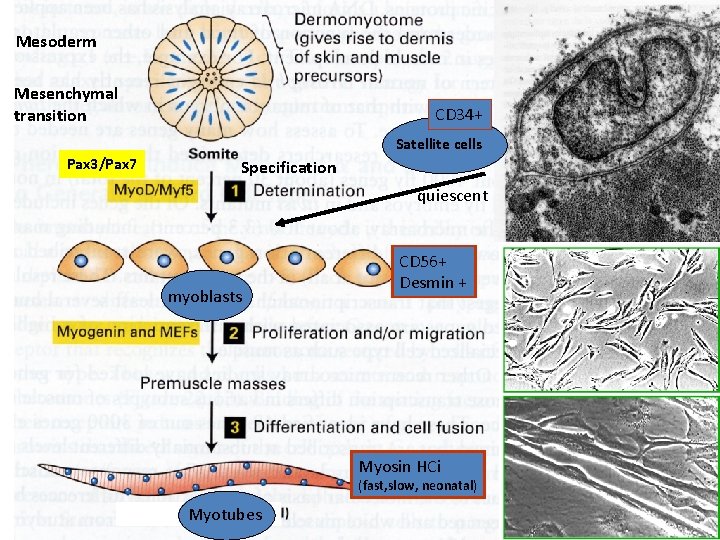
Mesoderm Mesenchymal transition CD 34+ Satellite cells Pax 3/Pax 7 Specification quiescent myoblasts CD 56+ Desmin + Myosin HCi (fast, slow, neonatal) 30 Novembre 2009 Myotubes
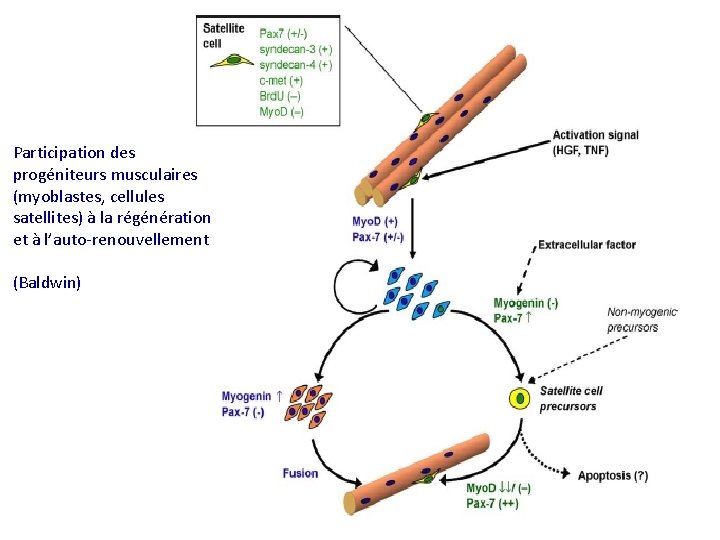
Participation des progéniteurs musculaires (myoblastes, cellules satellites) à la régénération et à l’auto-renouvellement (Baldwin)
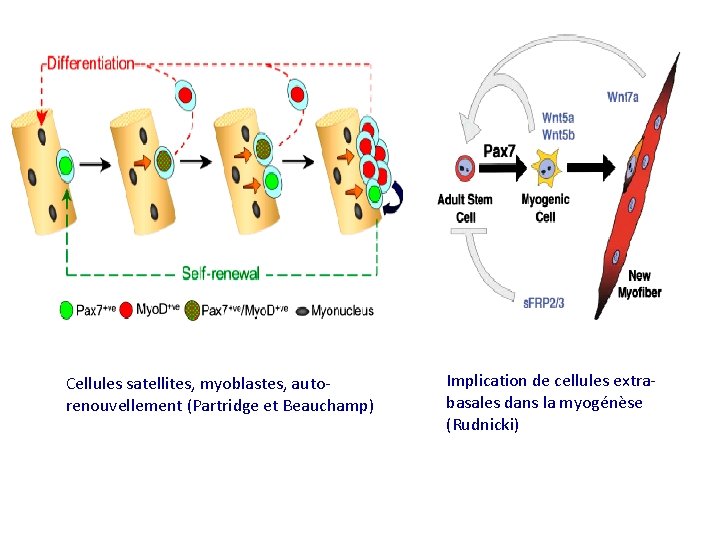
Cellules satellites, myoblastes, autorenouvellement (Partridge et Beauchamp) Implication de cellules extrabasales dans la myogénèse (Rudnicki)
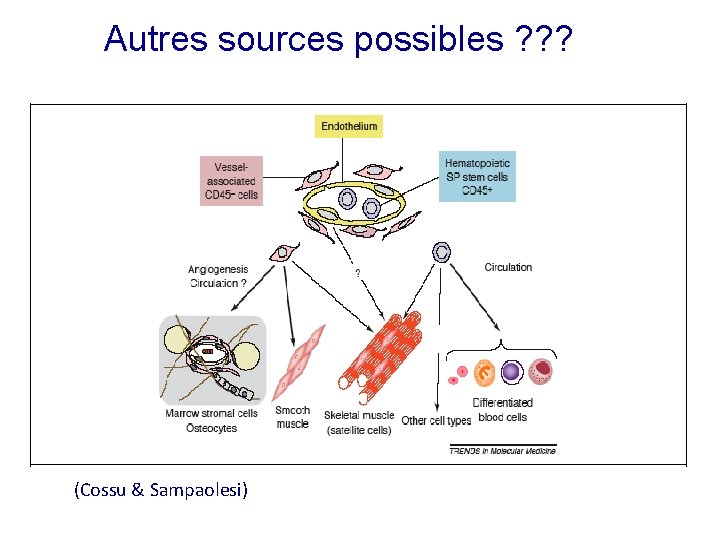
Autres sources possibles ? ? ? (Cossu & Sampaolesi)

Cellules souches cardiaques ? • The post-natal heart contains a myocardial stem cell population. Hierlihy et al. , FEBS letters 530, 239 -243, 2002 • Cardiac progenitor cells from adult myocardium: homing, differentiation, and fusion after infarction. H. Oh et al. , PNAS Oct 2003, 100, 12313 -12318. • Isl 1 identifies a cardiac progenitor population that proliferates prior to differentiation and contributes to a majority of cells to the heart. C-L Cai et al. , Developmental Cell 5, 877 -889, 2003. • Postnatal isl 1+ cardioblasts enter fully differentiated cardiomyocyte lineages. Laugwitz KL et al. , Nature 2005; 433: 647 -53.

Utilisations thérapeutiques de cellules souches / validations • Indication thérapeutique focalisée • Effet recherché (structure, sécrétion, contraction…) • Type cellulaire • Voie d’administration • Effets toxiques, prévention, traitement • Mesure de l’effet (implantation, efficacité) • Extension à grande échelle
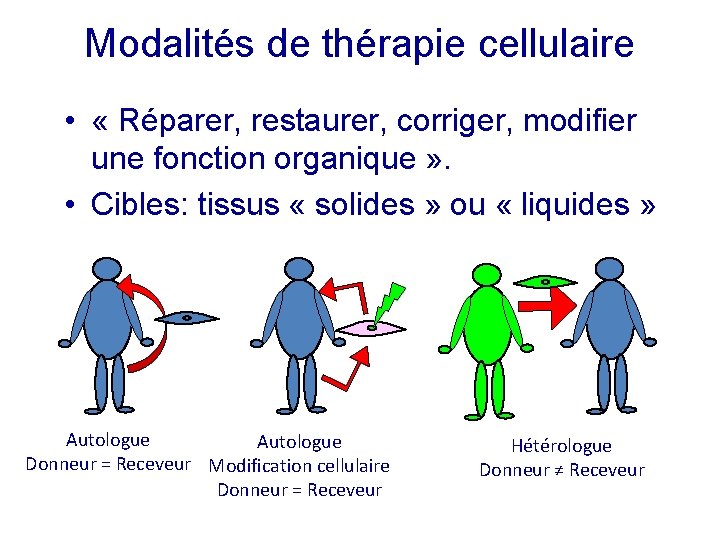
Modalités de thérapie cellulaire • « Réparer, restaurer, corriger, modifier une fonction organique » . • Cibles: tissus « solides » ou « liquides » Autologue Donneur = Receveur Modification cellulaire Donneur = Receveur Hétérologue Donneur ≠ Receveur

Thérapie cellulaire autologue • S’il est possible de transférer des cellules d’un territoire à l’autre • Avantage: Pas de rejet immunologique • Inconvénient: gène « morbide » conservé • Exemples: DMOP, DMFSH, Infarctus, sphincters, greffes de peau
Thérapie cellulaire autologue avec modification • S’il est possible d’amplifier les cellules. Si une correction est faisable, identifiée • Avantage: cellules du donneur Correction génique • Inconvénients: manipulations temporaire ou de gènes; production, sécurité, définitive utilisation clinique Sécrétion d’un produit • Exemples: épidermolyse thérapeutique bulleuse, myosites, enfantsbulles, DMD Amélioration des propriétés biologiques

Thérapie cellulaire hétérologue • Si les cellules du receveur ne sont pas accessibles, modifiables, fonctionnelles • Avantage: génôme non morbide, capacités régénératives • Inconvénients: immunogénicité, sécurité virale • Exemples: DMD, greffes de moelle…

Essais en développement. . . • • Cartilage Cerveau Cœur Foie Hématopoïèse Immunité Muscle squelettique • • Os Pancréas Peau Rétine Tendons Vaisseaux. . .

Messages • • Cellules souches existent Caractérisations incomplètes Filiations, réseaux mal connus ou identifiés Propriétés biologiques encore mal connues (mobilisation, activation, prolifération, interactions cellulaires, migration, différenciation, . . . ) • Utilisation thérapeutique dépendra de capacité de production, du contrôle de différenciation, d’administration, d’intégration • Essais encourageants. Ne soigneront pas toutes les maladies……. .
- Slides: 37