Cours dHmatocytologie DUT ABB 4 automatisation de lHmogramme

Cours d'Hémato-cytologie DUT ABB 4 - automatisation de l'Hémogramme Auteur : Bruno Flamand, IUT de Dijon

CYTOLOGIE HEMATOLOGIQUE L’HEMOGRAMME englobe: -les numérations des éléments figurés -le dosage de l’Hémoglobine -la mesure de l’Hématocrite -le calculs des constantes érythrocytaires et plaquettaires -l’établissement de la formule leucocytaire Prélèvement: sang veineux sur EDTA (ou citrate de Na), éventuellement sang capillaire L’Hémogramme est automatisé complètement ou partiellement dans les laboratoires

• Numérations: GR, GB, Plaquettes. • Valeurs et constantes: -érythrocytaires: -Taux Hémoglobine sanguin Hb -Hématocrite Ht -Volume Globulaire Moyen VGM -Concentration Corpusculaire Moyenne en Hb CCMH -Taux Corpusculaire Moyen en Hb TCMH -Indice de Distribution des Rouges IDR -plaquettaires: -Thrombocrite THT -Volume Plaquettaire Moyen VPM Indice de Distribution Plaquettaire IDP

• Formule leucocytaire: répartition des différentes sous-populations de leucocytes: PN, PE, PB, L, M -FL manuelle par lecture microscopique de frottis coloré au MGG (100 à 200 leucocytes répertoriés), si anomalie de FL automatisée -FL automatisée (5000 à 10000 leucocytes répertoriés) Les résultats sont rendus en valeur relative % et en valeur absolue par mm 3, mais l’interprétation n’est valable que sur les valeurs absolues L’Hémogramme: NFS Numération Formule (leucocytaire) Sanguine • GR, Hb, Hte, VGM, TCMH, IDR: orientation du diagnostic des anémies • Plaquettes: diagnostic des pb d’hémostase primaire • GB, FL: diagnostic des pb infectieux, inflammatoires, leucémiques
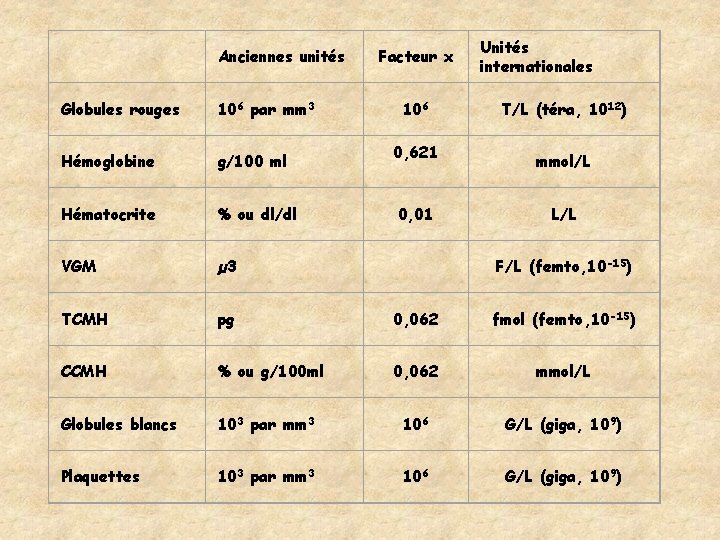
Anciennes unités Facteur x 106 Unités internationales Globules rouges 106 par mm 3 Hémoglobine g/100 ml Hématocrite % ou dl/dl VGM µ 3 TCMH pg 0, 062 fmol (femto, 10 -15) CCMH % ou g/100 ml 0, 062 mmol/L Globules blancs 103 par mm 3 106 G/L (giga, 109) Plaquettes 103 par mm 3 106 G/L (giga, 109) 0, 621 0, 01 T/L (téra, 1012) mmol/L L/L F/L (femto, 10 -15)
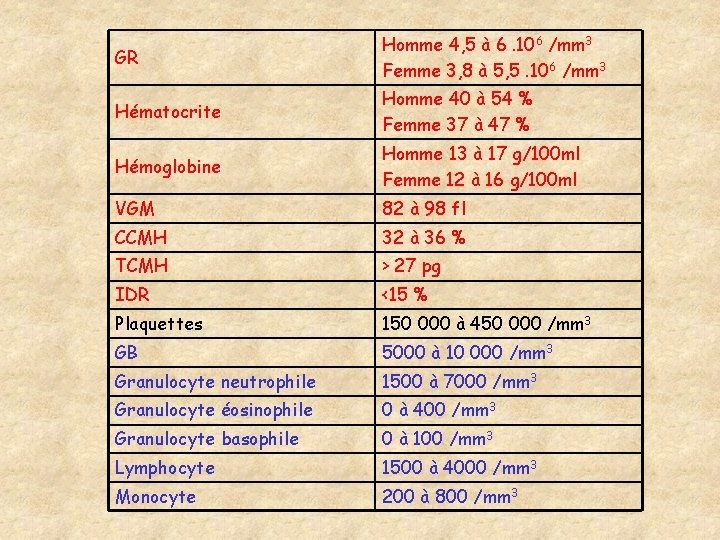
GR Homme 4, 5 à 6. 106 /mm 3 Femme 3, 8 à 5, 5. 106 /mm 3 Hématocrite Homme 40 à 54 % Femme 37 à 47 % Hémoglobine Homme 13 à 17 g/100 ml Femme 12 à 16 g/100 ml VGM 82 à 98 fl CCMH 32 à 36 % TCMH > 27 pg IDR <15 % Plaquettes 150 000 à 450 000 /mm 3 GB 5000 à 10 000 /mm 3 Granulocyte neutrophile 1500 à 7000 /mm 3 Granulocyte éosinophile 0 à 400 /mm 3 Granulocyte basophile 0 à 100 /mm 3 Lymphocyte 1500 à 4000 /mm 3 Monocyte 200 à 800 /mm 3
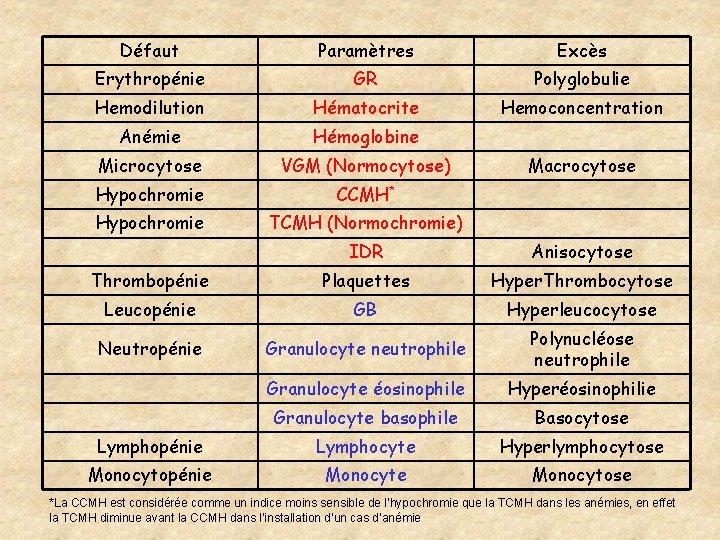
Défaut Paramètres Excès Erythropénie GR Polyglobulie Hemodilution Hématocrite Hemoconcentration Anémie Hémoglobine Microcytose VGM (Normocytose) Hypochromie CCMH* Hypochromie TCMH (Normochromie) Macrocytose IDR Anisocytose Thrombopénie Plaquettes Hyper. Thrombocytose Leucopénie GB Hyperleucocytose Neutropénie Granulocyte neutrophile Polynucléose neutrophile Granulocyte éosinophile Hyperéosinophilie Granulocyte basophile Basocytose Lymphopénie Lymphocyte Hyperlymphocytose Monocytopénie Monocytose *La CCMH est considérée comme un indice moins sensible de l’hypochromie que la TCMH dans les anémies, en effet la TCMH diminue avant la CCMH dans l’installation d’un cas d’anémie

Automatisation de l'hémogramme La chronologie par étapes Semi Automates GB Plt VGM GR Hb Hte 1954 Numération Formule 3 pop. Formule 5 populations 7 par. 8 par. - Plt (+ Plt) 1972 18 par. 22 par. (NFS) (HD) 1980 1990 + Rétic. 1994 + Etaleur/Colorateur 2000
Pentra 60 Horiba-ABX Pentra 120 Retic Horiba-ABX Sysmex XT ACT 5 DIFF Beckman Coulter CELL-DYN 3700 Abbot Laboratories CELL-DYN SMS Abbot Laboratories Coulter HMX Beckman Coulter

LH 1500 Series Automation Beckman Coulter CELL-DYN Work. Cell Abbott Laboratories

LA NUMERATION DES TROIS LIGNEES GR, GB, PLT Deux principes très différents: • La Variation d’impédance Principe Coulter du nom des inventeurs (Wallace and Joe Coulter- 1953), Méthode de référence, la plus répandue. Utilisée pour les numérations, et la formule leucocytaire approchée. • La mesure optique Associe les principes de bases de la Cytométrie en Flux (1977): -focalisation hydrodynamique -diffraction lumineuse recueillie à différents angles /incidence Utilisée surtout pour la numération des GB associée à la FL, cependant quelques automates utilisent la mesure optique pour les numérations des 3 lignées GR, GB, PLT (Bayer automate ADVIA 120, Sysmex automate XT 2000)
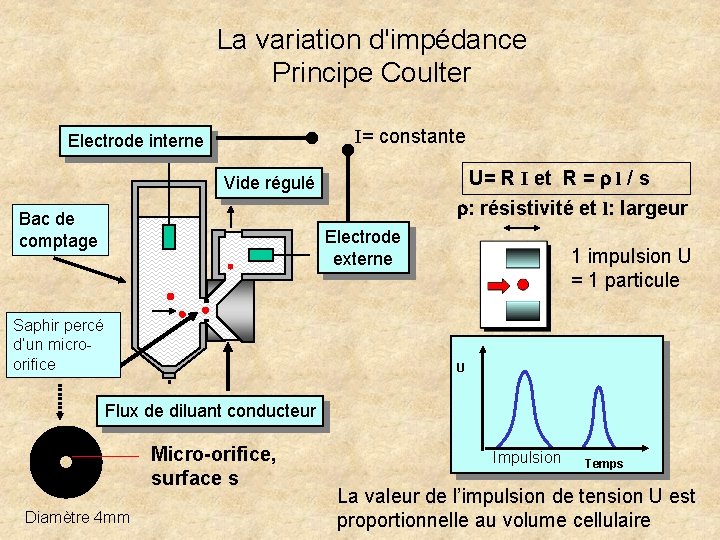
La variation d'impédance Principe Coulter I= constante Electrode interne U= R I et R = r l / s r: résistivité et l: largeur Vide régulé Bac de comptage Electrode externe Saphir percé d’un microorifice 1 impulsion U = 1 particule U Flux de diluant conducteur Micro-orifice, surface s Diamètre 4 mm Impulsion Temps La valeur de l’impulsion de tension U est proportionnelle au volume cellulaire
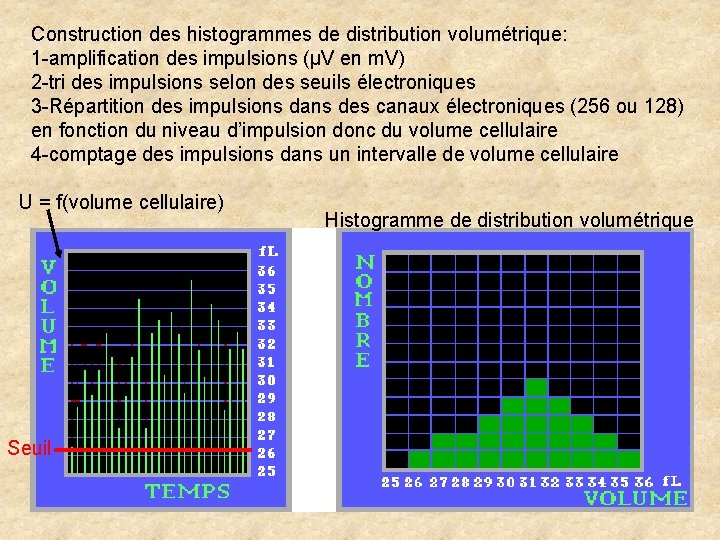
Construction des histogrammes de distribution volumétrique: 1 -amplification des impulsions (µV en m. V) 2 -tri des impulsions selon des seuils électroniques 3 -Répartition des impulsions dans des canaux électroniques (256 ou 128) en fonction du niveau d’impulsion donc du volume cellulaire 4 -comptage des impulsions dans un intervalle de volume cellulaire U = f(volume cellulaire) Seuil Histogramme de distribution volumétrique

Numération des Globules Rouges et des Plaquettes Bac de comptage des GR/PLT • Comptage et mesure du volume à partir d'une suspension cellulaire diluée en solution isotonique: taux de dilution élevé (1/10 000 à 1/20 000 ), ce qui permet de rendre négligeable une interférence des GB • • Un seul bac de comptage: Toute particule d'un volume supérieur à 25 fl (et inférieur à 250 fl) est comptée comme un GR Toute particule d’un volume supérieur à 2 fl (et inférieur à 25 fl) est comptée comme une PLT Chaque particule est placée dans un histogramme de distribution volumétrique • •

Numération des Globules Rouges Histogramme des GR VGM Mise en évidence de fragments de cytoplasme ou de grandes plaquettes par l'analyse de l'histogramme à partir de 24 fl. La trainée peut correspondre aux : –Passages en coïncidence –Agrégats cellulaires –Cellules agées –Globules blancs
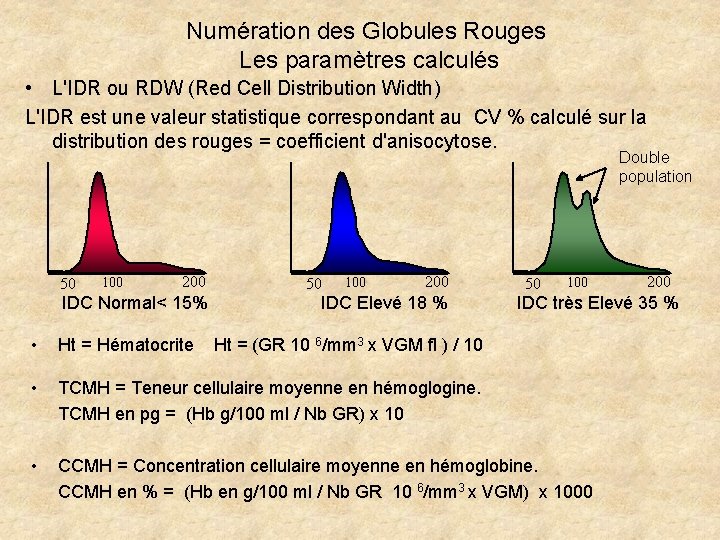
Numération des Globules Rouges Les paramètres calculés • L'IDR ou RDW (Red Cell Distribution Width) L'IDR est une valeur statistique correspondant au CV % calculé sur la distribution des rouges = coefficient d'anisocytose. Double population 50 100 200 IDC Normal< 15% 50 100 200 IDC Elevé 18 % 50 100 200 IDC très Elevé 35 % • Ht = Hématocrite Ht = (GR 10 6/mm 3 x VGM fl ) / 10 • TCMH = Teneur cellulaire moyenne en hémoglogine. TCMH en pg = (Hb g/100 ml / Nb GR) x 10 • CCMH = Concentration cellulaire moyenne en hémoglobine. CCMH en % = (Hb en g/100 ml / Nb GR 10 6/mm 3 x VGM) x 1000
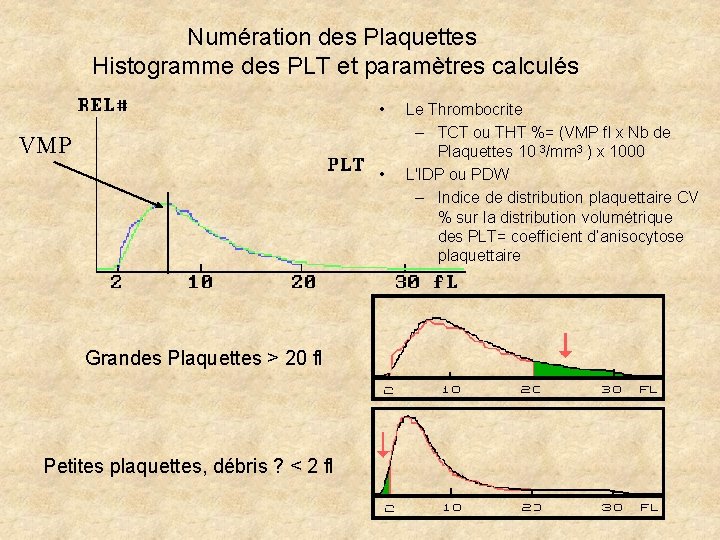
Numération des Plaquettes Histogramme des PLT et paramètres calculés • VMP • Grandes Plaquettes > 20 fl Petites plaquettes, débris ? < 2 fl Le Thrombocrite – TCT ou THT %= (VMP fl x Nb de Plaquettes 10 3/mm 3 ) x 1000 L'IDP ou PDW – Indice de distribution plaquettaire CV % sur la distribution volumétrique des PLT= coefficient d’anisocytose plaquettaire
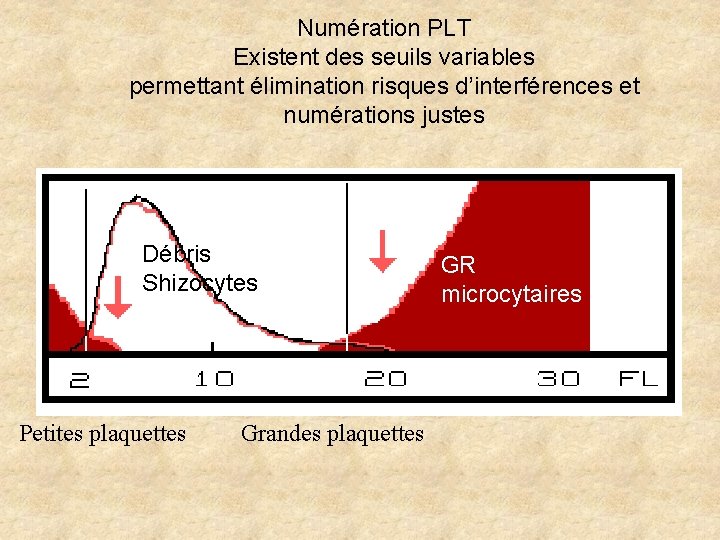
Numération PLT Existent des seuils variables permettant élimination risques d’interférences et numérations justes Débris Shizocytes Petites plaquettes Grandes plaquettes GR microcytaires

Numération des globules blancs Bac de comptage des GB • Comptage à partir d'une suspension cellulaire diluée en liquide hémolytique: taux de dilution faible, (1/200 à 1/300) • Un bac de comptage réservé • Toute particule d'un volume supérieur à 35 fl est comptée comme un globule blanc. • Les globules rouges sont lysés (ammonium quaternaire, ferri cyanure, cyanure de K+), permet la libération de Hb Cyan. Met. Hb • Une partie de la dilution des leucocytes passe dans une cuve spectrophotométrique pour la mesure à 540 nm Source lumineuse LED Photo-détecteur Filtre Cuve de mesure

Correction de passage en coïncidence Doublet ou triplet cellulaires • Le résultat de numération est assujeti à une correction dite "correction de coïncidence". • Occasionnellement deux ou trois cellules peuvent traverser l'orifice de comptage en même temps. U Temps • Une impulsion de grande amplitude est générée. • La fréquence de ces passages en coïncidence est statistiquement prévisible en fonction du nombre de cellules. Cette correction est réalisée automatiquement par les analyseurs.

LA FORMULE LEUCOCYTAIRE automatisée TROIS POPULATIONS ou CINQ POPULATIONS (5 Diff) • La formule leucocytaire 3 populations ou formule approchée, (GRA / Lympho / Mono): pour la majorité des automates, elle est réalisée par analyse par variation d’impédance des volumes cellulaires des globules blancs, après lyse des GR, et action différentielle d’une lyse ménagée sur les GB, lyse qui modifie leur volume. Cette FL approchée n’a pas de valeur légale, et très peu de valeur fonctionnelle, un automate de ce type décharge l’automate principal du passage de sangs de patients sans anomalie • La FL complète ou 5 populations, permet en associant plusieurs principes technologiques, l’analyse des GN, GE, GB, M, L, et le repérage facilité de populations anormales du sang (lymphocytes atypiques, cellules immatures précurseurs, érythroblastes…)

Il est des circonstances où il faut effectuer obligatoirement une formule au microscope, et ne pas se contenter de la formule de l’automate: • FL du nouveau-né • Premier examen d’un malade avec nettes anomalies de numération • Variations brutales et inexpliquées par rapports aux NF antérieures • Incohérence avec le contexte clinique ou thérapeutique • Alarmes de l’automate pour lesquelles il n’y a pas d’explication évidente au vu du dossier et/ou des examens antérieurs • Alarmes de l’automate pour distribution cellulaires inhabituelles sur les graphes
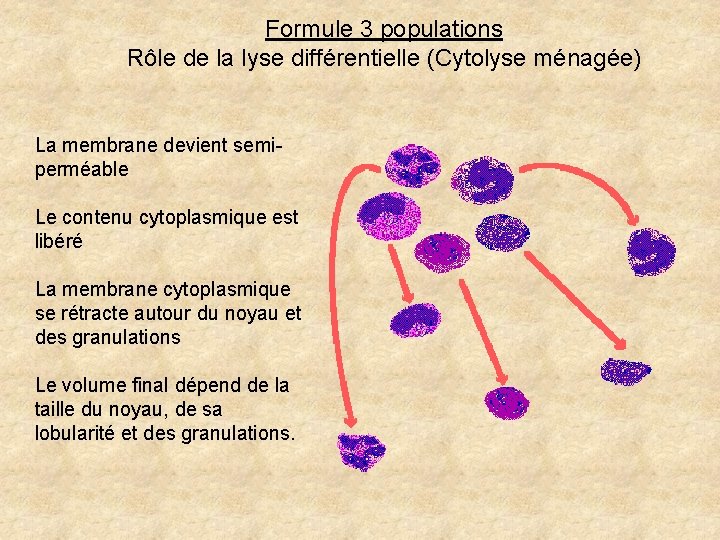
Formule 3 populations Rôle de la lyse différentielle (Cytolyse ménagée) La membrane devient semiperméable Le contenu cytoplasmique est libéré La membrane cytoplasmique se rétracte autour du noyau et des granulations Le volume final dépend de la taille du noyau, de sa lobularité et des granulations.
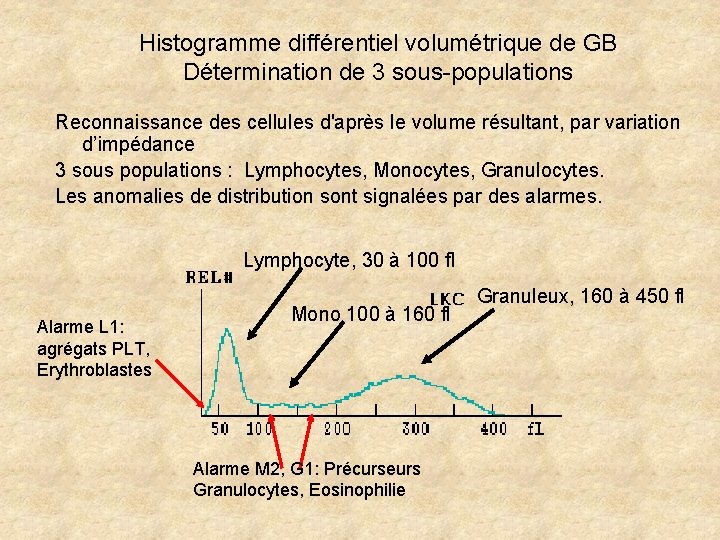
Histogramme différentiel volumétrique de GB Détermination de 3 sous-populations Reconnaissance des cellules d'après le volume résultant, par variation d’impédance 3 sous populations : Lymphocytes, Monocytes, Granulocytes. Les anomalies de distribution sont signalées par des alarmes. Lymphocyte, 30 à 100 fl Alarme L 1: agrégats PLT, Erythroblastes Mono 100 à 160 fl Alarme M 2, G 1: Précurseurs Granulocytes, Eosinophilie Granuleux, 160 à 450 fl

Formule Leucocytaire 5 populations • Analyse automatisée individuelle des caractéristiques cellulaires naturelles ou modifiées d’un seul leucocyte PERFORMANCE • Analyse sur un nombre élevé de leucocytes (5000 à 10000): PRECISION de la FL automatisée par rapport à FL microscopique • Circulation des GB , après hémolyse des GR, individuellement, séparés, dans un système liquide de flux laminaire: Focalisation Hydrodynamique ou gainage cellulaire, principe de base de la technologie de Cyto. Métrie en Flux (CMF) • Apparition successive des GB indivualisés dans un ensemble de mesure, permettant une analyse optique simultanée de plusieurs paramètres naturels (volume cellulaire, présence de granulation, hétérogénéité du noyau) ou modifiés (coloration, fluorescence) de la cellule. (CFM = FACS « Fluorescence Activated Cell Sorter » )

Hydrofocalisation Flux de gainage Flux échantillon FOCALISATION HYDRODYNAMIQUE Flux de gainage Flux échantillon - Suspension cellulaire exposée à une surpression (1 bar) injectée au centre d'une veine liquide d'entraînement (liquide de gainage) circulant à une vitesse différente - Sortie de la suspension cellulaire par un rétrécissement d'un micro-orifice 50 µm à 300 µm - Absence de mélange "Suspension cellulaire/ liquide de gainage" car densité du liquide de gainage > densité du liquide suspension cellulaire - Ecoulement laminaire des cellules: 500 à 5000 cellules/sec, 25 à 36 km/H, séparation ≥ 1 mm, orientation des cellules selon leur plus grand axe dans le flux, et déformation cellulaire uniforme en fonction de la cellule
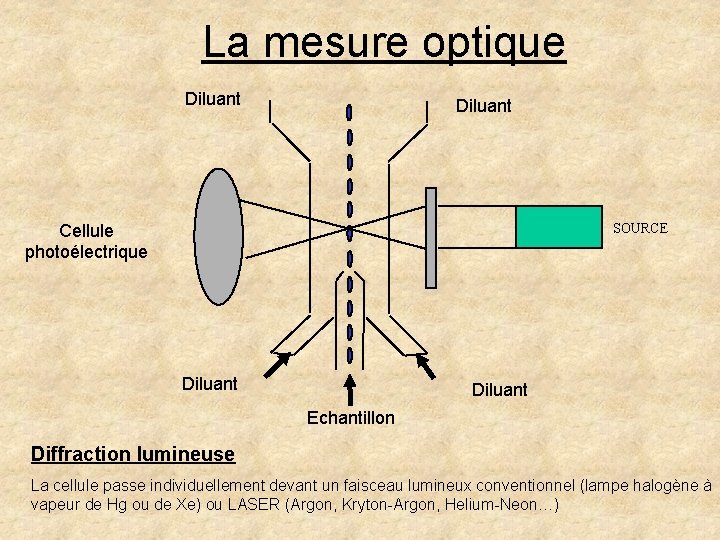
La mesure optique Diluant Cellule photoélectrique SOURCE Diluant Echantillon Diffraction lumineuse La cellule passe individuellement devant un faisceau lumineux conventionnel (lampe halogène à vapeur de Hg ou de Xe) ou LASER (Argon, Kryton-Argon, Helium-Neon…)

Diffraction lumineuse Intensité de la lumière diffractée peut être corrélée à des caractéristiques morphologiques cellulaires: - Intensité de la lumière diffractée par la cellule, recueillie dans l'axe de la lumière incidente, dite "diffraction aux petits angles" (2 à 6°), (FALS Forward Angle Light Scatter, ou FSC Forward Scatter Channel), est en relation proportionnelle avec la taille cellulaire , la forme cellulaire, et l’indice de réfraction cellulaire - Intensité de la lumière diffractée par la cellule, recueillie de 8° à 90° de l'axe de la lumière incidente, "diffraction aux grands angles", (RALS Right Angle Light Scatter, ou SSC Side Scatter Channel), est relation proportionnelle avec l'hétérogénéité du contenu cellulaire, présence/absence et taille de granulation cytoplasmique, forme et taille du noyau, rapport N/C, densité chromatinienne du noyau, ce Paramètre est appelé « Granularité » Détection aux petits angles : Taille Détection aux grands angles: « Granularité »

Formule 5 Populations : critères de reconnaissance Les automates associent divers principes technologiques permettant l’accès à divers critères de reconnaissance l l l Variation Impédance (= Volume cellulaire) Principe Coulter pour le volume, ou mesure optique pour la taille Diffraction lumineuse (= taille cellulaire et Granularité) Diffraction de la lumière par la cellule (différents angles) Cytochimie sélective Coloration d’un élément de la cellule, par simple affinité (ex: coloration des granulations éosinophiles) ou par activité enzymatique chromogène sélective (ex: peroxydase des granulations) Conductivité (opacité) Courant Radio Haute Fréquence (RF) Structure de la cellule par un conduction courant haute fréquence Cytolyse Lyse sélective de populations. Ex: tous les GB sauf PB. (évidemment dans tous les cas de FL complète automatisée, la lyse de GR est obligatoire

Détermination de la formule 5 populations Chaque société sur ses automates combine plusieurs technologies et donc plusieurs critères de reconnaissance l Impédance + Conductivité HF + Diffraction lumineuse Beckman. Coulter Automates MAXM, Hm. X, Gen. S, LH 500, LH 750 l Impédance + Cytolyse + Cytochimie (Actvité peroxydasique) Bayer. Diagnostics Automates Advia 120, Technicon H 2, H 3 l Impédance + Cytolyse + Cytochimie (Coloration des granulations. Eo. ) Horiba. Abx Automates Pentra 60, Pentra 80, Pentra 120 Bayer. Diagnostics Automates Advia 70 Beckman. Coulter Automates ACT 5 Diffraction lumineuse + Cytochimie (Eosino) + Cytolyse Sysmex SF 3000, XE 2100 l l Diffraction lumineuse multi-angulaire sans cytolyse Abbott. Diagnostics Automates CELL-DYN 3200, 3700, 4000
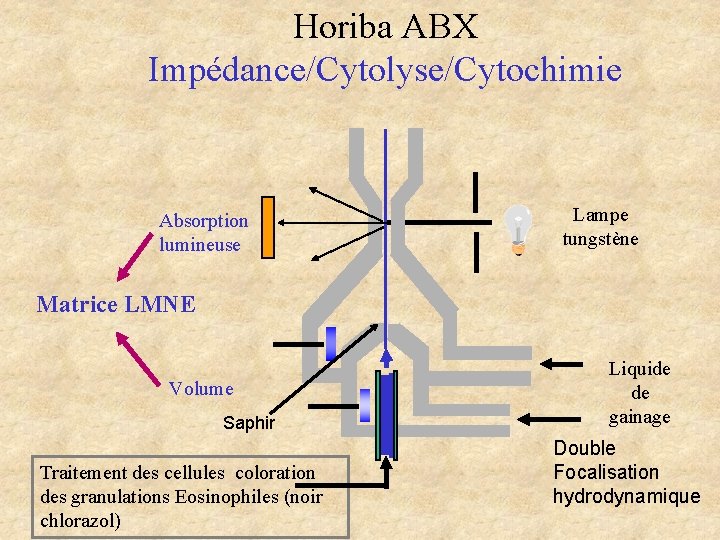
Horiba ABX Impédance/Cytolyse/Cytochimie Absorption lumineuse Lampe tungstène Matrice LMNE Volume Saphir Traitement des cellules coloration des granulations Eosinophiles (noir chlorazol) Liquide de gainage Double Focalisation hydrodynamique
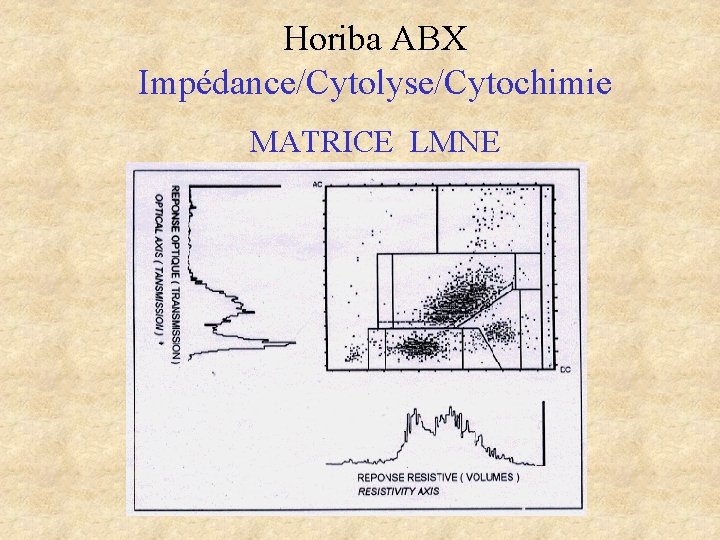
Horiba ABX Impédance/Cytolyse/Cytochimie MATRICE LMNE
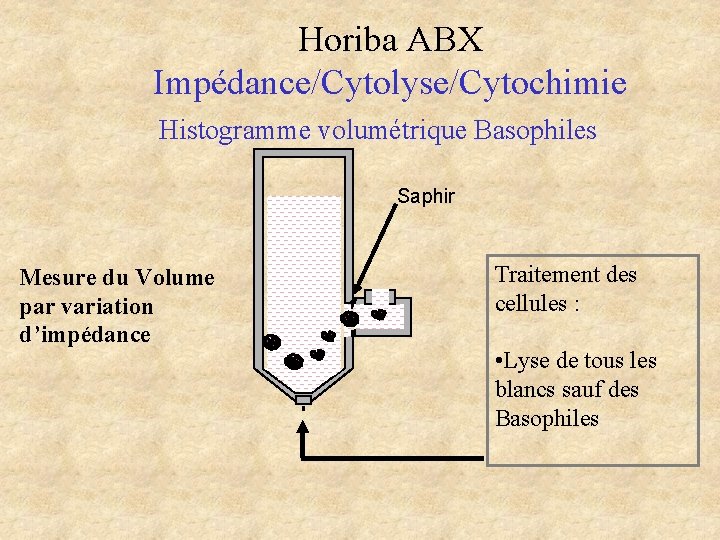
Horiba ABX Impédance/Cytolyse/Cytochimie Histogramme volumétrique Basophiles Saphir Mesure du Volume par variation d’impédance Traitement des cellules : • Lyse de tous les blancs sauf des Basophiles

Horiba ABX Impédance/Cytolyse/Cytochimie Matrice LMNE Absorbance Eo. . . Ne. . . Ly Ly. A . GCI . . . . . Bruit de fond . Nombre . . . GCI. . . . . Mo+Ba Volume Basophiles Noyaux GB Volume Histogramme Basophiles
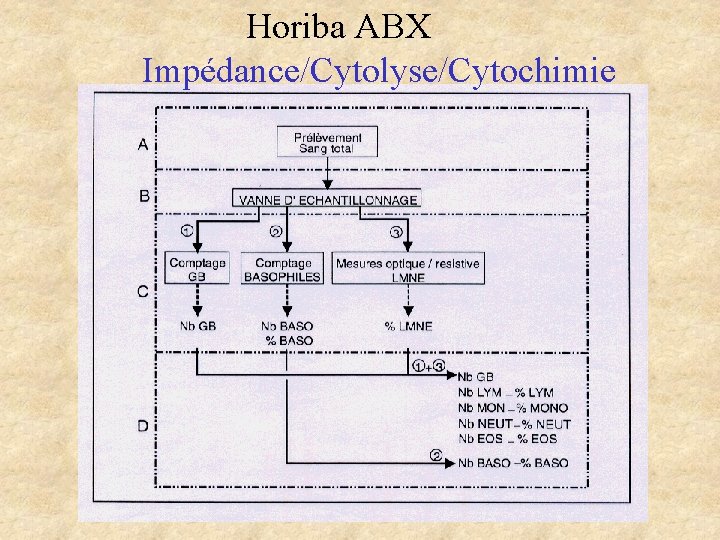
Horiba ABX Impédance/Cytolyse/Cytochimie

Exemple d’hémogramme complet sur Pentra Horiba ABX
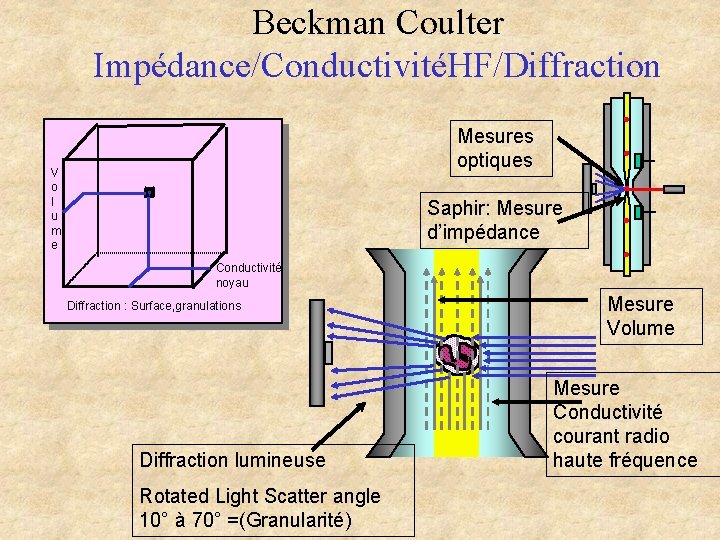
Beckman Coulter Impédance/ConductivitéHF/Diffraction Mesures optiques V o l u m e Saphir: Mesure d’impédance Conductivité noyau Diffraction : Surface, granulations Diffraction lumineuse Rotated Light Scatter angle 10° à 70° =(Granularité) Mesure Volume Mesure Conductivité courant radio haute fréquence

Beckman Coulter Impédance/Conductivité/Diffraction PE M M GRA L Diffraction M L PN Conductivité PB L Soustraction des coordonnées « Diffraction » des PN, PE, du nuage GRA, pour « révéler PB »
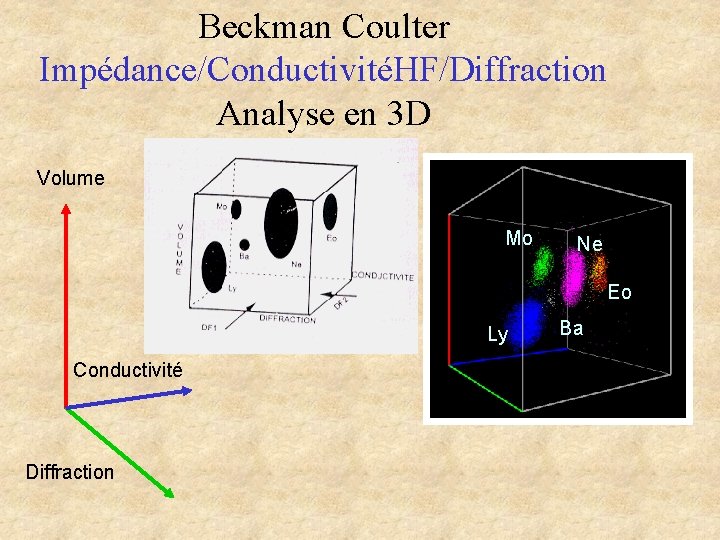
Beckman Coulter Impédance/ConductivitéHF/Diffraction Analyse en 3 D Volume Mo Ne Eo Ly Conductivité Diffraction Ba
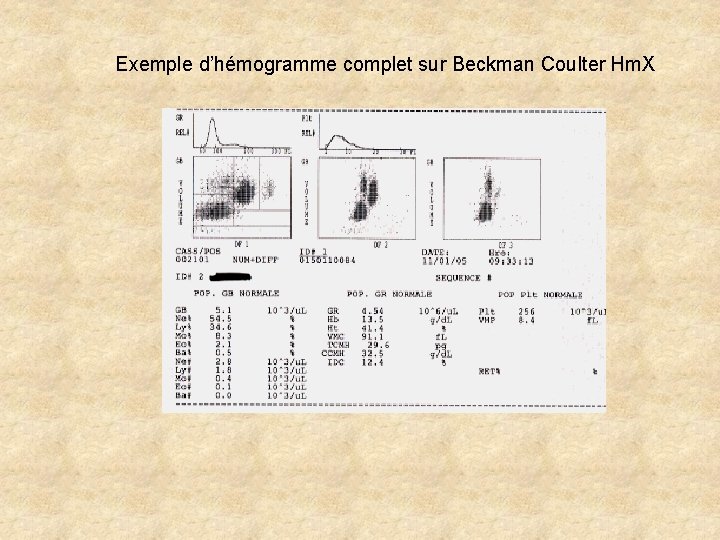
Exemple d’hémogramme complet sur Beckman Coulter Hm. X
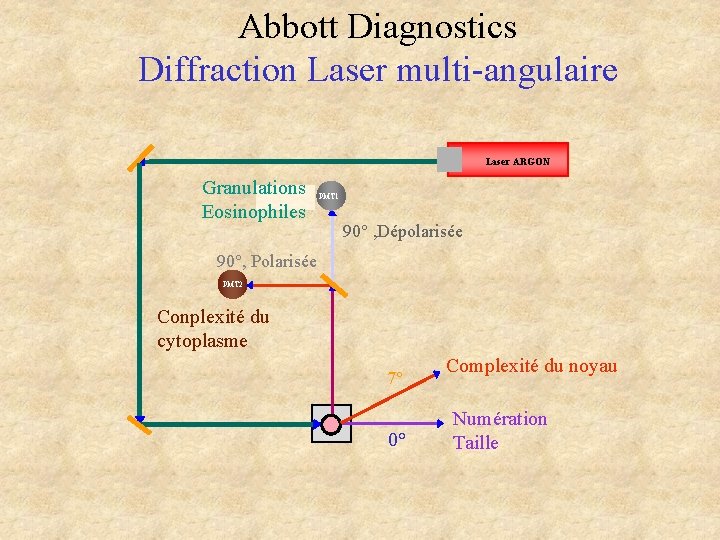
Abbott Diagnostics Diffraction Laser multi-angulaire Laser ARGON Granulations Eosinophiles PMT 1 90° , Dépolarisée 90°, Polarisée PMT 2 Conplexité du cytoplasme 7° 0° Complexité du noyau Numération Taille
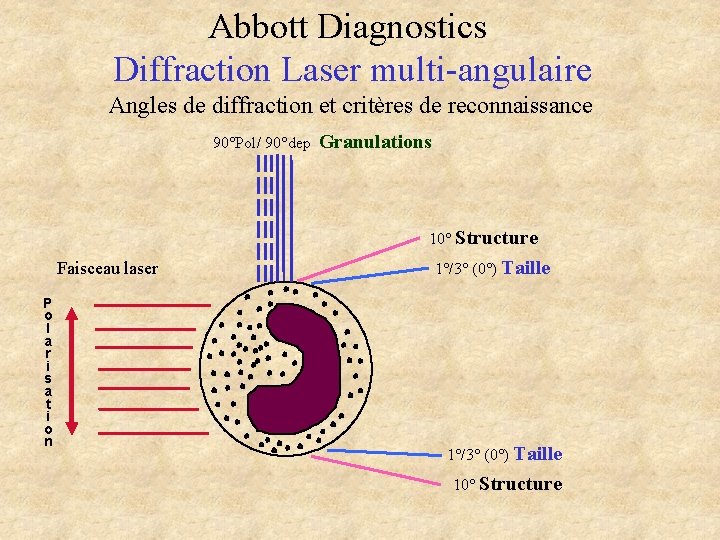
Abbott Diagnostics Diffraction Laser multi-angulaire Angles de diffraction et critères de reconnaissance 90°Pol/ 90°dep Granulations 10° Structure Faisceau laser P o l a r i s a t i o n 1°/3° (0°) Taille 10° Structure
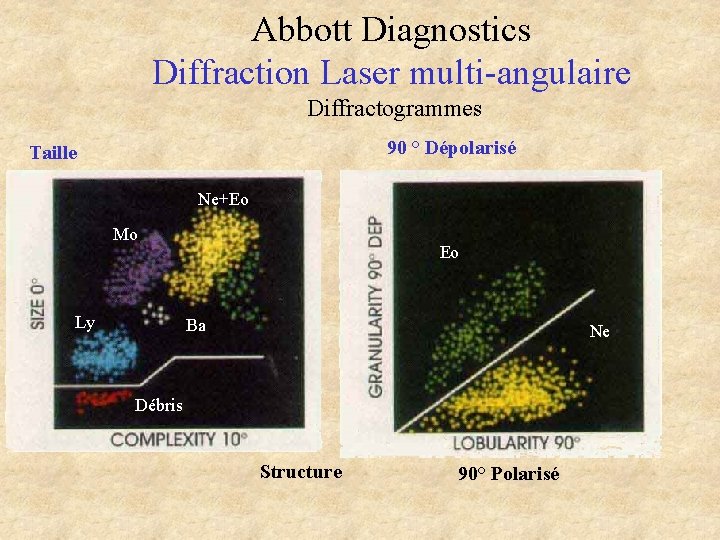
Abbott Diagnostics Diffraction Laser multi-angulaire Diffractogrammes 90 ° Dépolarisé Taille Ne+Eo Mo Ly Eo Ba Ne Débris Structure 90° Polarisé

LA NUMERATION AUTOMATISEE DES RETICULOCYTES Exemple sur automate Pentra 120 Rétic Horiba ABX Marquage fluorescent des ARN résiduels Fluorochrome: Thiazole orange Focalisation dans cellule de mesure, d’une dilution sanguine 1/3000 dans diluant isotonique + thiazole orange 2 informations recueillies: -comptage et volume par impédance (saphir) -signal d’intensité de fluorescence OFL émise à 530 nm, déclenché par excitation transitoire, recueillie à 90° du trajet optique

Matrice Réticulocytes Pentra 120 Horiba ABX Réticulocytes à fluorescence élevée OFL Intensité Fluorescence Réticulocytes à fluorescence moyenne Réticulocytes à fluorescence faible GR matures Volume

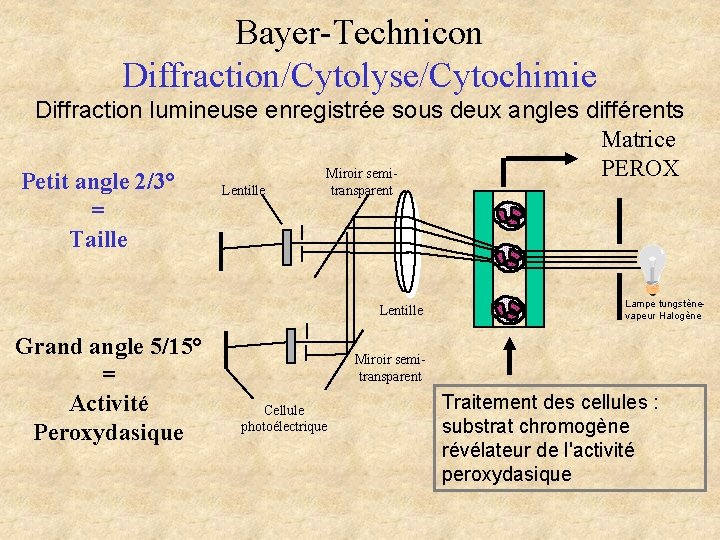
Bayer-Technicon Diffraction/Cytolyse/Cytochimie Diffraction lumineuse enregistrée sous deux angles différents Matrice PEROX Miroir semi. Petit angle 2/3° transparent Lentille = Taille Lentille Grand angle 5/15° = Activité Peroxydasique Lampe tungstènevapeur Halogène Miroir semitransparent Cellule photoélectrique Traitement des cellules : substrat chromogène révélateur de l'activité peroxydasique
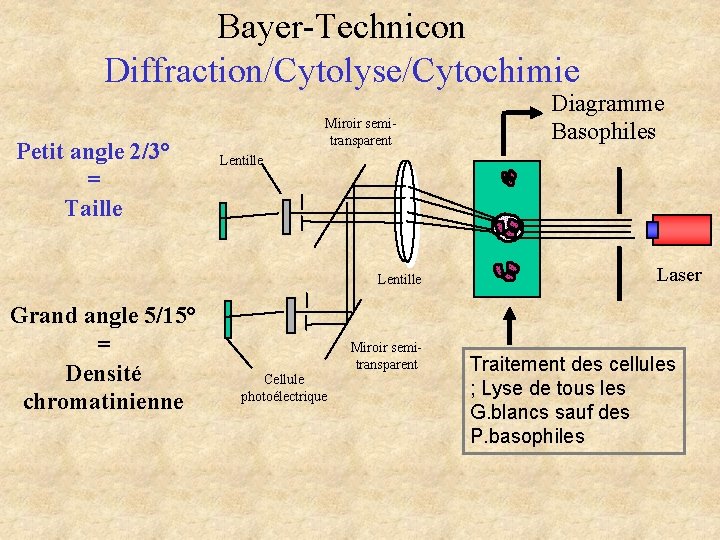
Bayer-Technicon Diffraction/Cytolyse/Cytochimie Petit angle 2/3° = Taille Miroir semitransparent Lentille Grand angle 5/15° = Densité chromatinienne Diagramme Basophiles Cellule photoélectrique Miroir semitransparent Laser Traitement des cellules ; Lyse de tous les G. blancs sauf des P. basophiles
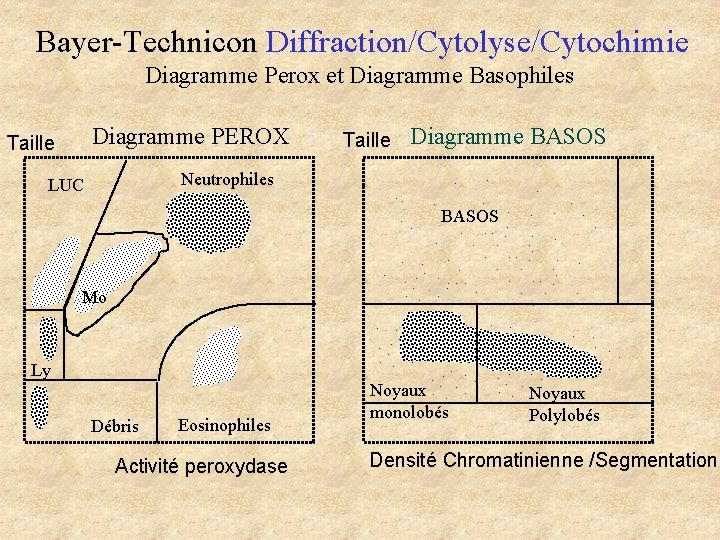
Bayer-Technicon Diffraction/Cytolyse/Cytochimie Diagramme Perox et Diagramme Basophiles Diagramme PEROX Taille Diagramme BASOS Taille Neutrophiles LUC . . . . Mo. BASOS Débris Eosinophiles Activité peroxydase . . . . Noyaux monolobés . . . Ly . . Noyaux Polylobés Densité Chromatinienne /Segmentation
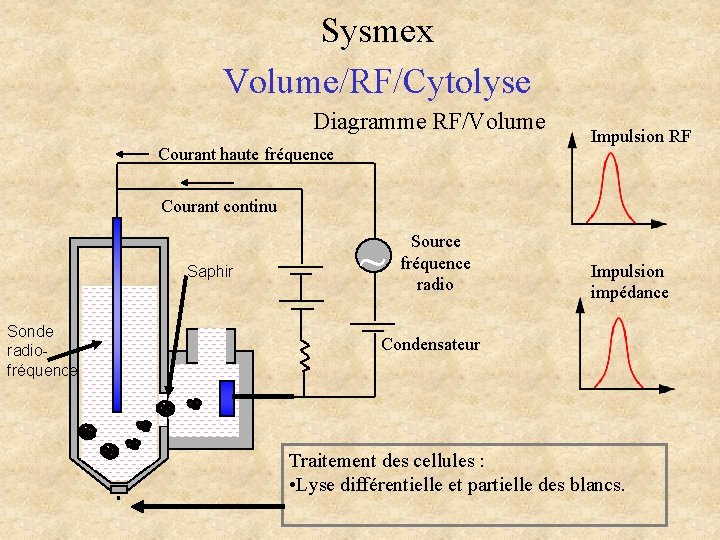
Sysmex Volume/RF/Cytolyse Diagramme RF/Volume Courant haute fréquence Impulsion RF Courant continu Saphir Sonde radiofréquence ~ Source fréquence radio Impulsion impédance Condensateur Traitement des cellules : • Lyse différentielle et partielle des blancs.
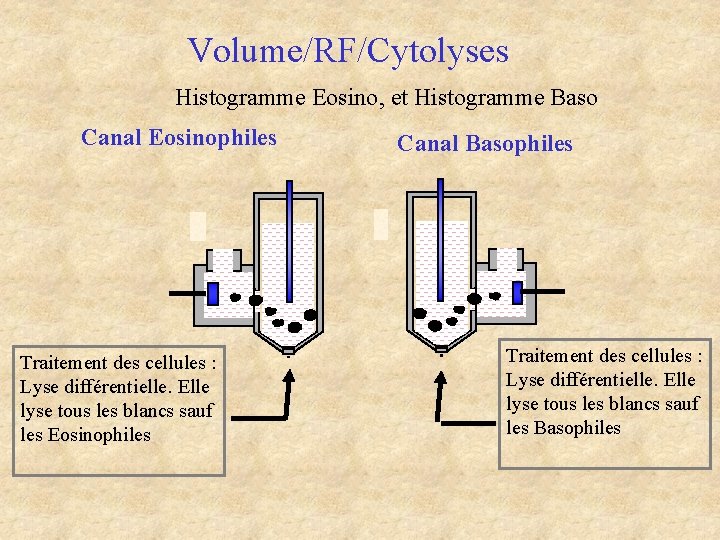
Volume/RF/Cytolyses Histogramme Eosino, et Histogramme Baso Canal Eosinophiles Traitement des cellules : Lyse différentielle. Elle lyse tous les blancs sauf les Eosinophiles Canal Basophiles Traitement des cellules : Lyse différentielle. Elle lyse tous les blancs sauf les Basophiles
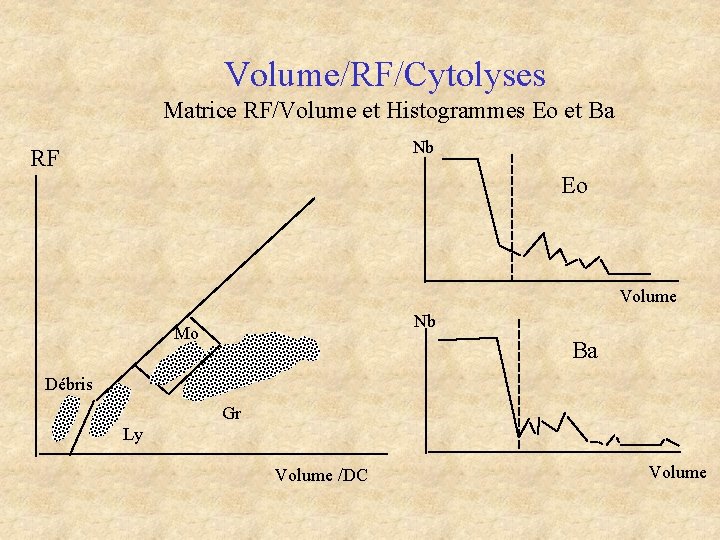
Volume/RF/Cytolyses Matrice RF/Volume et Histogrammes Eo et Ba Nb RF Eo Volume Nb Mo Ba Débris Gr Ly Volume /DC Volume
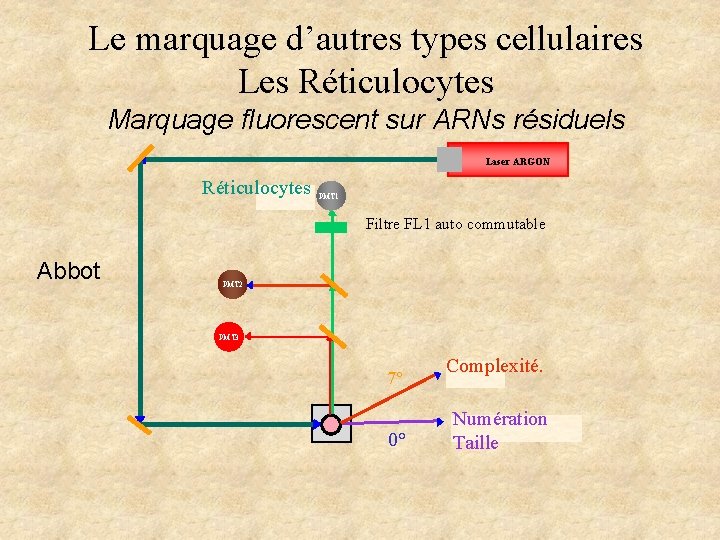
Le marquage d’autres types cellulaires Les Réticulocytes Marquage fluorescent sur ARNs résiduels Laser ARGON Réticulocytes PMT 1 Filtre FL 1 auto commutable Abbot PMT 2 PMT 3 7° 0° Complexité. Numération Taille
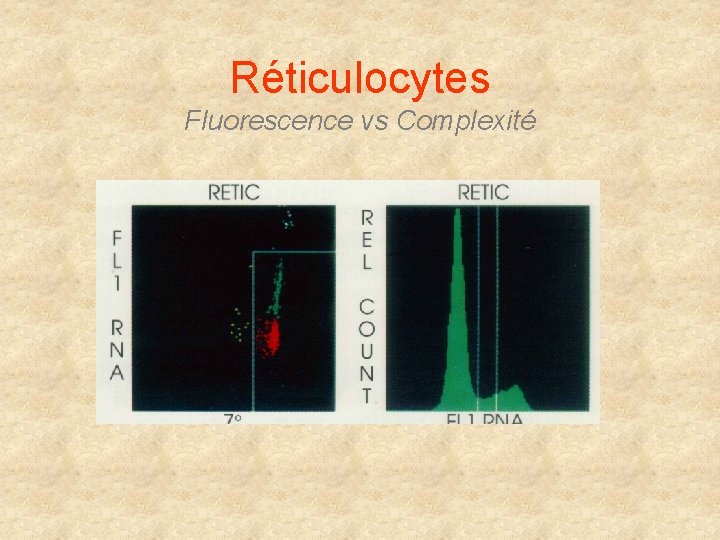
Réticulocytes Fluorescence vs Complexité

Diffraction lumineuse + Cytolyse Sysmex
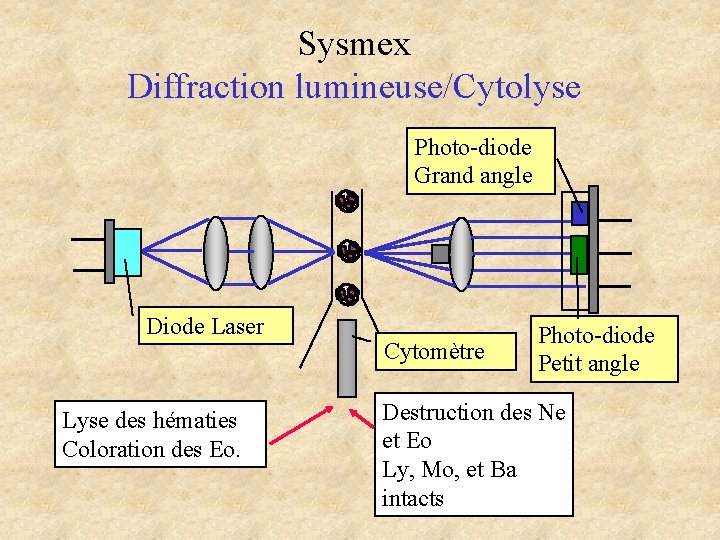
Sysmex Diffraction lumineuse/Cytolyse Photo-diode Grand angle Diode Laser Lyse des hématies Coloration des Eo. Cytomètre Photo-diode Petit angle Destruction des Ne et Eo Ly, Mo, et Ba intacts
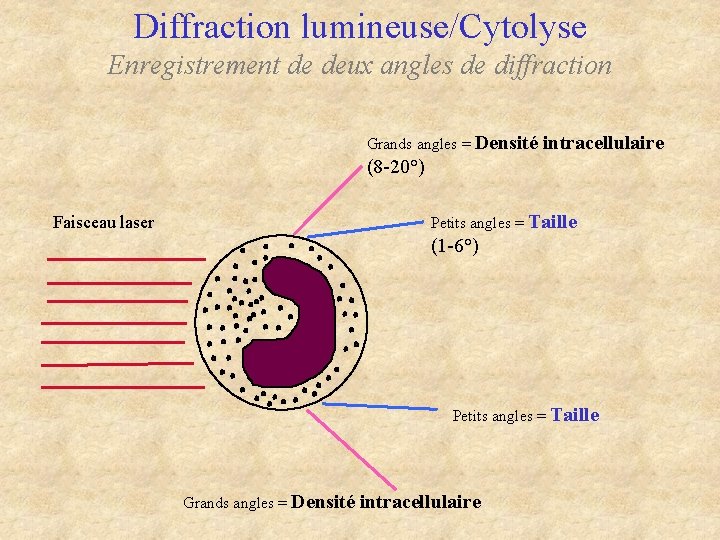
Diffraction lumineuse/Cytolyse Enregistrement de deux angles de diffraction Grands angles = Densité intracellulaire (8 -20°) Faisceau laser Petits angles = Taille (1 -6°) Petits angles = Taille Grands angles = Densité intracellulaire
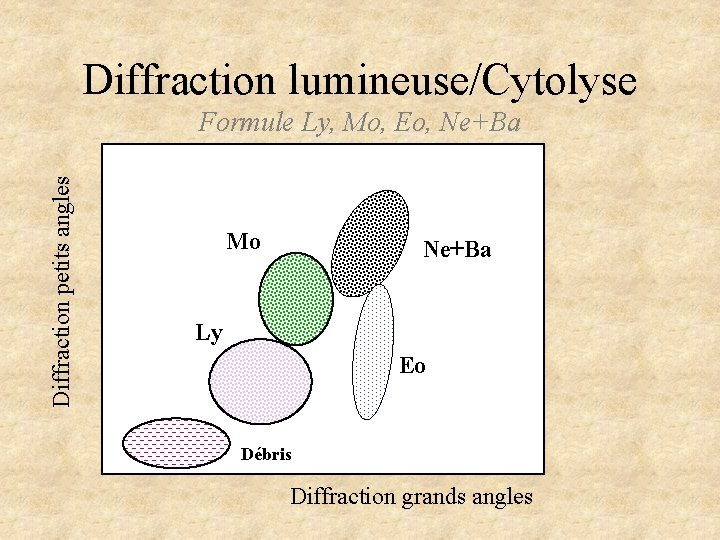
Diffraction lumineuse/Cytolyse Diffraction petits angles Formule Ly, Mo, Eo, Ne+Ba Mo Ne+Ba Ly Eo Débris Diffraction grands angles
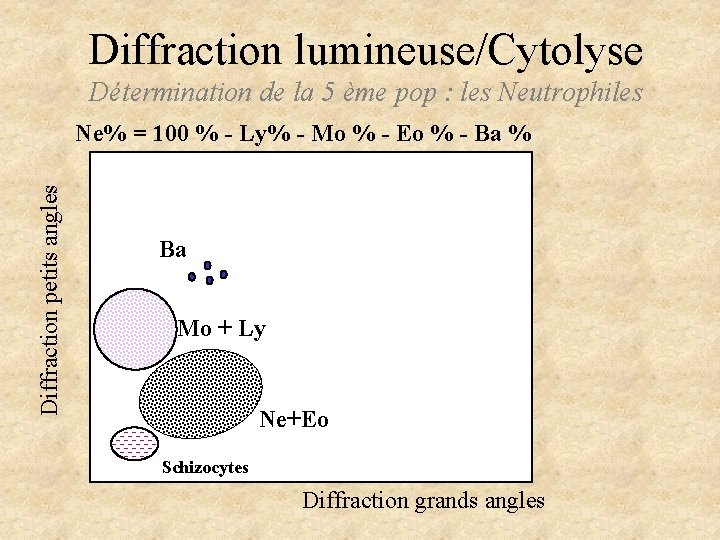
Diffraction lumineuse/Cytolyse Détermination de la 5 ème pop : les Neutrophiles Diffraction petits angles Ne% = 100 % - Ly% - Mo % - Eo % - Ba % Ba Mo + Ly Ne+Eo Schizocytes Diffraction grands angles

Diffraction lumineuse avec ou sans cytolyse complémentaire Abbott
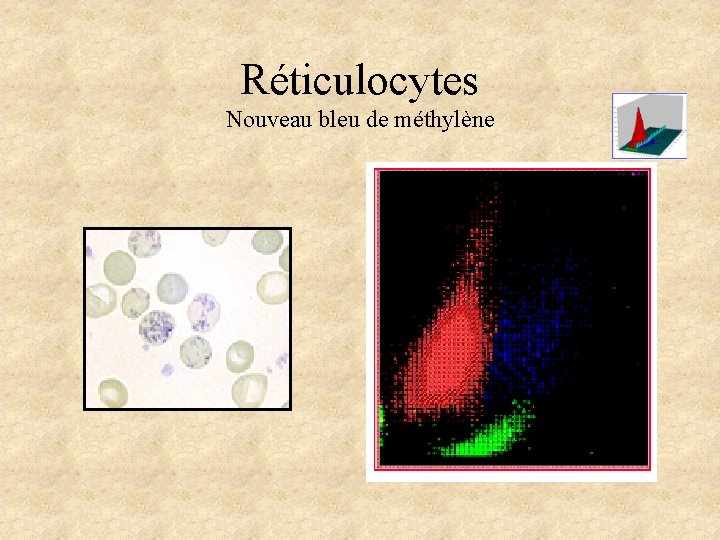
Réticulocytes Nouveau bleu de méthylène

Cytolyse complémentaire Abbott (CD 3200)
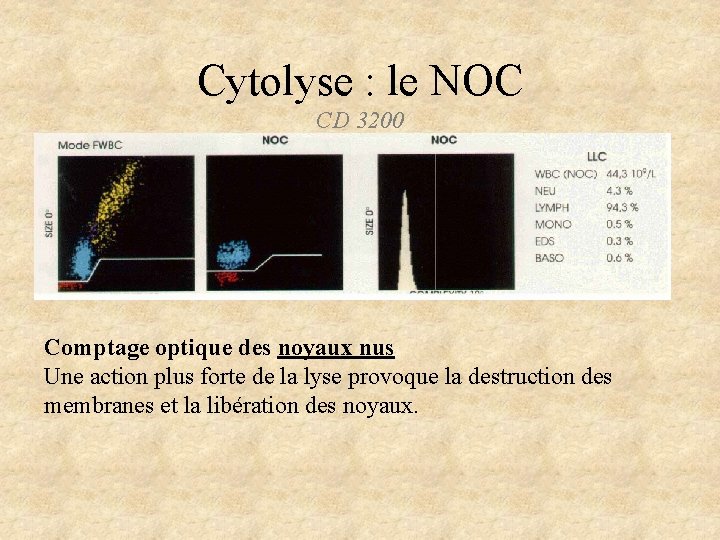
Cytolyse : le NOC CD 3200 Comptage optique des noyaux nus Une action plus forte de la lyse provoque la destruction des membranes et la libération des noyaux.

Diffraction lumineuse + Marquage Abbott
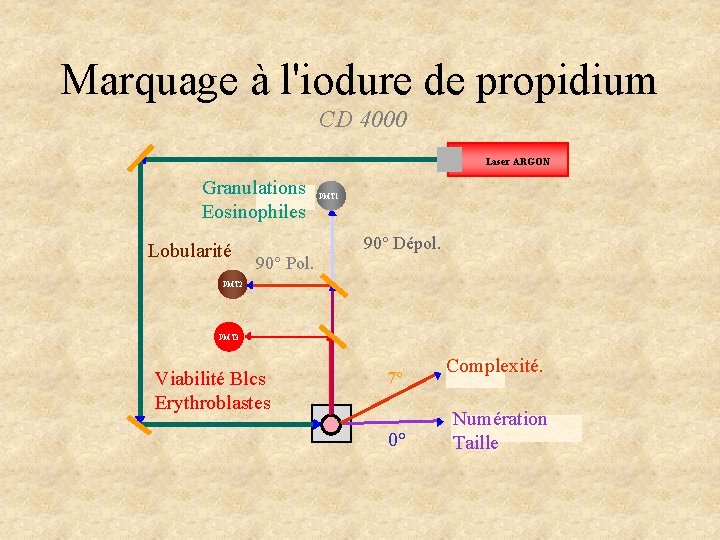
Marquage à l'iodure de propidium CD 4000 Laser ARGON Granulations Eosinophiles Lobularité 90° Pol. PMT 1 90° Dépol. PMT 2 PMT 3 Viabilité Blcs Erythroblastes 7° 0° Complexité. Numération Taille

Analyse de la fluorescence Marquage des noyaux accessibles Lkc viables Lkc non viables Noyaux nus Les noyaux nus des cellules lysées et les noyaux des cellules mortes sont marqués par l'iodure de propidium

LE MARQUAGE D'AUTRES TYPES CELLULAIRES RETICULOCYTES CD 4/CD 8
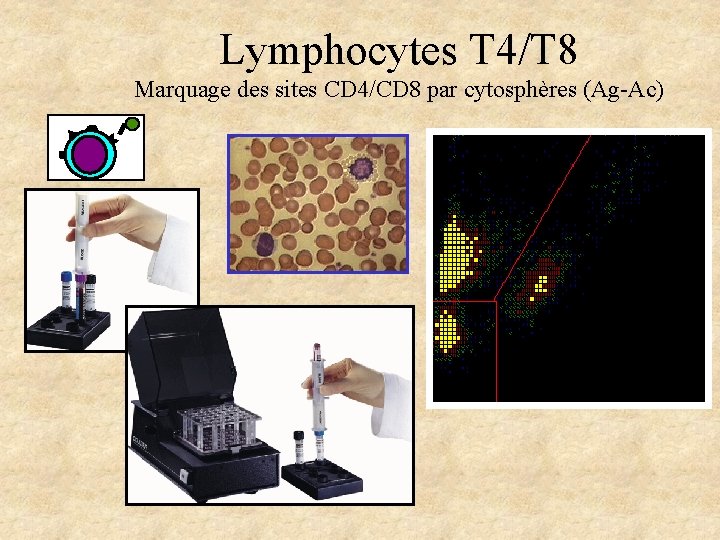
Lymphocytes T 4/T 8 Marquage des sites CD 4/CD 8 par cytosphères (Ag-Ac)
- Slides: 68