COURS DE PARASITOLOGIE DUT ABB 6 Les Filaires

COURS DE PARASITOLOGIE DUT ABB 6 - Les Filaires exotiques Auteur : Bruno Flamand, IUT de Dijon

PROTOZOAIRES • ENTAMOEBA HISTOLYTICA-(Amibiase) • AMIBES intestinales NON PATHOGENES • GIARDIA INTESTINALIS-(Giardiase) • CHILOMASTIX MESNILI-(Chilomastose) • BALANTIDIUM COLI-(Balantidiose) • CYCLOSPORA CAYETANENSIS-(Cyclosporose) • TRICHOMONAS VAGINALIS-(Trichomonase) • TOXOPLASMA GONDII-(Toxoplasmose) • CRYPTOSPORIDIUM PARVUM-(Cryptosporidiose) • PNEUMOCYSTIS CARINII-(Pneumocystose) • MICROSPORIDIES-(Microsporidiose) • ISOSPORA BELLI-(Isosporose) • SARCOSYSTIS-(Sarcocystose) • LEISHMANIA-(Leishmanioses) • TRYPANOSOMA BRUCEI-(Trypanosomose-Maladie du sommeil) • TRYPANOSOMA CRUZI–(Maladie de Chagas) • PLASMODIUM-(PALUDISME)

ENTAMOEBA HISTOLYTICA-(Amibiase) Règne des Protistes, Embranchement des Sarcomastigophora, Sous-Embranchement des Sarcodina, Classe des Lobosasida, Ordre des Amoebida Morphologie: Trophozoïte: Deux aspects chez E. histolytica Forme minuta: 10 à 15 µm, Endoplasme finement granuleux, Ectoplasme réfringent, 1 Noyau périphérique à petit caryosome central et chromatine périphérique en liseré ou pointillé. Forme histolytica: 20 à 30 µm jusqu'à 40 µm, même aspect général que la forme minuta, mais présence d'hématies en voie de digestion dans des vacuoles cytoplasmiques.

kyste: sphérique, réfringent, incolore, à parois minces, 10 - 14 µm de diamètre, 4 noyaux à maturité, un corps chromatoïde épais à bouts arrondis, les kystes immatures contiennent une vacuole, 1 ou 2 noyaux et sont plus grands. Cycle évolutif: cycle direct, Parasites monoxènes obligatoires de l'homme. Transmission passive par ingestion de kystes mûrs. a) Cycle non pathogène: Ingestion d'un kyste mûr à 4 noyaux, éclosion ==> 8 amoebules du type minuta qui se multiplient par division binaire au contact de la muqueuse colique. Elimination intermittente et irrégulière, dans le milieu extérieur, sous forme de kystes fécaux. b) Cycle pathogène accidentel: Les formes minuta coliques se transforment en formes histolytica ==> abcès de la muqueuse colique; elles se multiplient par scissiparité dans les abcès. Retour du parasite à la forme minuta après 3 semaines ==> fin de la crise amibienne. ==> Élimination de kystes. Possibilité de métastases sanguines et/ou lymphatiques à partir d'un abcès colique, conduisant à des localisations extra-coliques (foie, poumon, cerveau etc. . . ).
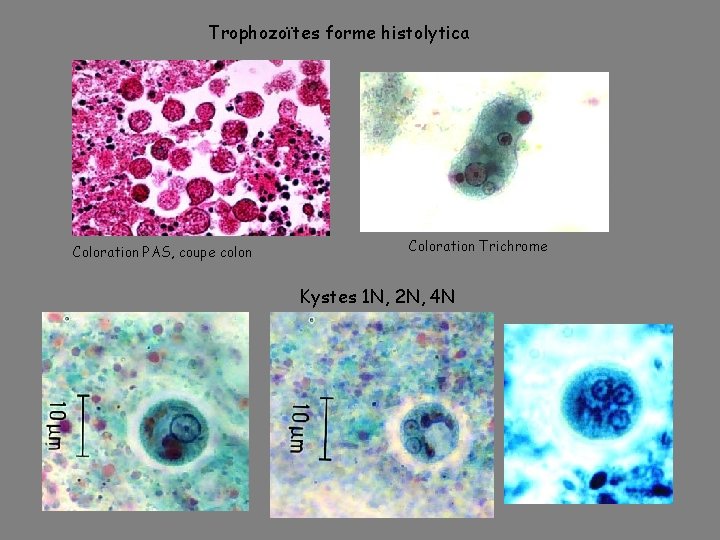
Trophozoïtes forme histolytica Coloration PAS, coupe colon Coloration Trichrome Kystes 1 N, 2 N, 4 N

Actuellement, on distingue 2 espèces d'amibes morphologiquement identiques, mais génétiquement différentes: -Entamoeba histolytica, forme virulente, responsable des formes cliniques graves -Entamoeba dispar, avirulente et non pathogène, la plus fréquente dans les régions tempérées Morphologiquement identiques, ces 2 espèces sont différentiables par: -Électrophorèse d’isoenzymes glycolytiques -PCR -détection d’Ag spécifiques dans les selles

Epidémiologie: maladie liée au péril fécal humain, R de P : homme. Le kyste survit au minimum 15 jours dans l'eau à 18°C, 10 jours dans les selles, 24 h à sec. Il résiste bien aux agents chimiques. (formes végétatives trop fragiles pour survivre dans la nature et jouer un rôle épidémiologique). Parasitose cosmopolite, mais la parasitose est endémique dans les pays chauds et humides. Prévalence mondiale d’E. histolytica: 50 millions de cas. Prévalence mondiale d’E. dispar: 450 millions de porteurs. Dans les pays industrialisés, la majorité des cas sont diagnostiqués chez les immigrants et chez les touristes ayant séjourné dans des pays de forte endémicité amibienne auxquels il faut ajouter 2 catégories à risque, les homosexuels, VIH négatifs ou positifs, et les pensionnaires des institutions pour malades mentaux. Clinique: Le terme amibiase recouvre plusieurs entités: L'Amibiase-infection: (formes minuta coliques), colonisation asymptomatique, correspond à des sujets «semeurs de kystes» ou «porteurs sains» . L'Amibiase-maladie : (formes histolytica pathogènes) provoquant abcès et nécrose tissulaire. Le passage à l'amibiase-maladie dépend: de facteurs de l'hôte (fatigue, stress, maladie intercurrentes) et de facteurs du parasite (virulence de la souche).
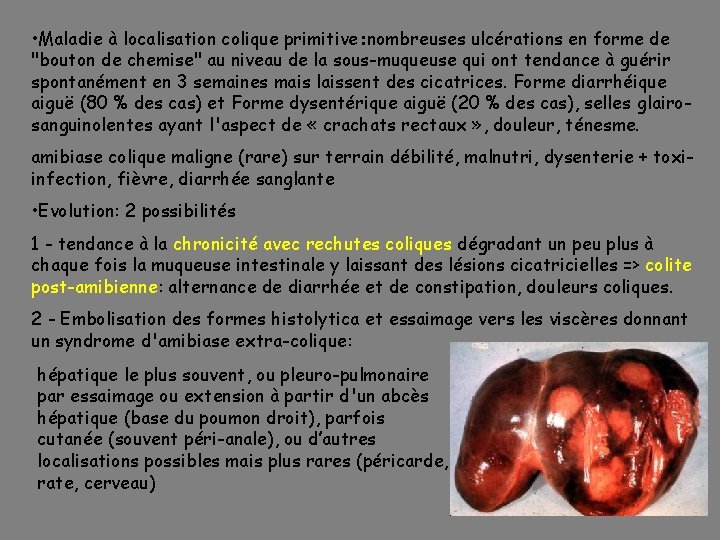
• Maladie à localisation colique primitive: nombreuses ulcérations en forme de "bouton de chemise" au niveau de la sous-muqueuse qui ont tendance à guérir spontanément en 3 semaines mais laissent des cicatrices. Forme diarrhéique aiguë (80 % des cas) et Forme dysentérique aiguë (20 % des cas), selles glairosanguinolentes ayant l'aspect de « crachats rectaux » , douleur, ténesme. amibiase colique maligne (rare) sur terrain débilité, malnutri, dysenterie + toxiinfection, fièvre, diarrhée sanglante • Evolution: 2 possibilités 1 - tendance à la chronicité avec rechutes coliques dégradant un peu plus à chaque fois la muqueuse intestinale y laissant des lésions cicatricielles => colite post-amibienne: alternance de diarrhée et de constipation, douleurs coliques. 2 - Embolisation des formes histolytica et essaimage vers les viscères donnant un syndrome d'amibiase extra-colique: hépatique le plus souvent, ou pleuro-pulmonaire par essaimage ou extension à partir d'un abcès hépatique (base du poumon droit), parfois cutanée (souvent péri-anale), ou d’autres localisations possibles mais plus rares (péricarde, rate, cerveau)

Diagnostic de l'amibiase-infection: -si le sujet émet des selles moulées: recher des kystes matures d'E. histolytica à distinguer des kystes de Entamoeba coli et des kystes d'autres amibes non pathogènes, et de flagellés -si le sujet émet des selles diarrhéiques: recher des kystes immatures d'E. histolytica, recher des formes trophozoïtes minuta d'E. histolytica, Diagnostic de l'amibiase-maladie: -prélèvement au niveau des glaires sanglantes au niveau des selles; examen immédiat à 37°C, le trophozoïte d'E. histolytica forme histolytica est mobile par émission brutale de pseudopodes, et possède des hématies intra-vacuolaires - recto-sigmoïdoscopie: abcès en coup d'ongle où on trouve la forme histolytica - mise en culture sur milieu spécial (NNN) Diagnostic de l'amibiase-maladie de localisation extra colique: -imagerie qui montre un abcès liquidien -prélèvement difficile au niveau des abcès : pus de couleur chocolat généralement dépourvu d'amibes, les formes histolytica se trouvent dans les parois des abcès -la recherche des anticorps sériques est le seul moyen de diagnostic

AMIBES NON PATHOGENES

AMIBES NON PATHOGENES Fréquemment retrouvées dans les examens parasitologiques des selles, leur présence signe une contamination liée au péril fécal, mais elles sont en général non pathogènes. AMIBES NON PATHOGENES Noyau Caryosome Vacuole

ASPECT DES KYSTES d’AMIBES

Entamoeba coli x 40 Entamoeba hartmanni X 40 Entamoeba polecki x 40 Endolimax nana x 40 Iodamoeba butschlii x 40, X 100


GIARDIA INTESTINALIS-(Giardiase) Règne des protistes, Embranchement des Sarcomastigophora, sous embranchement des mastigophora, Classe des Zoomastigophorasida (Giardia intestinalis = G. duodenalis, = G. lamblia) Morphologie: 2 formes connues trophozoïte: corps symétrique, "en cerf-volant" effilé vers l'arrière, 10 à 20 µm x 6 -10 µm 8 flagelles (6 flagelles antérieurs + 2 postérieurs), 2 noyaux, 2 corps parabasaux, une dépression antérieure ventrale à rôle adhésif, Très mobile. Noyau Corps parabasaux

kyste: ovoïde, coque mince, claire, lisse, réfringente, 12 x 8 µm, 2 noyaux à l'émission + un amas flagellaire dans l'axe et deux corps parabasaux en virgule. (4 noyaux après un séjour de 24 - 48 h à l’extérieur). Immobile.

Cycle évolutif: cycle direct, parasite monoxène HD = homme et nombreux animaux Multiplication par division binaire dans la lumière du duodénum sous forme trophozoïte flagellé formation irrégulière des kystes Élimination passive des kystes avec les selles maturation dans le milieu extérieur ingestion des kystes à 4 noyaux avec l'eau et les aliments dékystement dans le duodénum, fixation des trophozoïtes à l'épithélium intestinal. Épidémiologie: cosmopolite, R de P = homme et animaux affection liée au péril fécal, transmission des kystes avec l'alimentation, les eaux souillées, les mains sales causes favorisantes: hypochlorhydrie, déficit immunitaire, jeune âge…. Prévalence: 1, 5 à 20 % chez l'homme en partie selon le niveau d'hygiène. Le kyste résiste très bien au froid (2 mois à + 8°C) et au chlore.

Clinique: porteurs sains = 90 % phase d'incubation: 7 jours, asymptomatique phase d'état: diarrhée ( 5 à 10 selles/j), douleur abdominale, flatulence, plus rarement asthénie, anorexie, amaigrissement, nausées, malabsorption intestinale possible chez l'enfant, stéatorrhée (non digestion des graisses), évolution par crises penser à la giardiose chez un enfant présentant une diarrhée depuis plus d'une semaine, Diagnostic: Recherche des kystes dans les selles si elles sont pâteuses (émission irrégulière => répétition des examens à quelques jours d'intervalle et Recherche des trophozoïtes dans selles si le transit est très accéléré (ou après un tubage duodénal) (les trophozoïtes sont mobiles mais fragiles) la mise en évidence du parasite est positive dans 50 % des cas, refaire l'examen à plusieurs reprises à plusieurs jours d'intervalle en cas de suspicion fondée et de résultat négatif. Recherche des Ag Giardia dans selles (copro-Ag)

CHILOMASTIX MESNILI Règne des protistes, Embranchement des Sarcomastigophora, sous embranchement des mastigophora, Classe des Zoomastigophorasida, Ordre des Retortamonodida Flagellé commensal, capable de coloniser le colon, sa présence indique une contamination par des aliments ou de l’eau contaminée par des matières fécales. Kyste 6 -10µm, forme de poire, noyau latéro-médian, flagelle résiduel Trophozoïte 6 -20µm, axostyle caudal, flagelles antérieurs, noyau 1

BALANTIDIUM COLI (Balantidiose) Règne des Protistes, Embranchement des Ciliophora, Classe des Kinetofragminophorea, Ordre des Trichostomatina Morphologie: trophozoïte: ovoïde, 100 µm x 50 µm, péristome, 2 noyaux (macronucleus et micronucleus), vacuoles pulsatiles et digestives kyste: sphérique, 50µm, 2 noyaux

Cycle évolutif: cycle direct, parasite monoxène HD = porc, homme, chien, … localisation des trophozoïtes dans la lumière intestinale, émission de kystes, transmission féco-orale. Epidémiologie: R de P: porc, Parasitose cosmopolite pour le porc, endémie humaine dans les pays tropicaux, rare en France, limité aux professions en contact avec le porc Clinique: phase d'état: asymptomatique le plus souvent, troubles du transit: diarrhée, dysenterie balantidienne ==> colite, peut être confondue avec une amibiase colique Rq: guérison spontanée possible si le patient est en bonne condition générale, rechutes en cas de malnutrition ou maladie intercurrente Diagnostic: recherche des kystes dans les selles ou rectoscopie: recherche des trophozoïtes au niveau des lésions
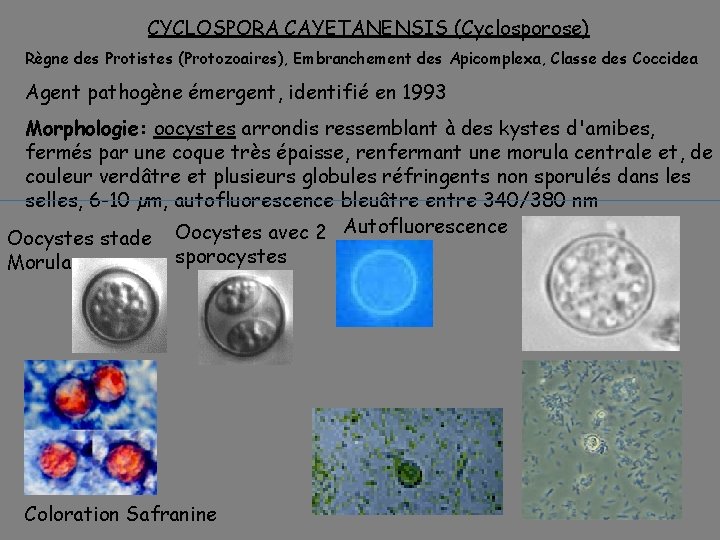
CYCLOSPORA CAYETANENSIS (Cyclosporose) Règne des Protistes (Protozoaires), Embranchement des Apicomplexa, Classe des Coccidea Agent pathogène émergent, identifié en 1993 Morphologie: oocystes arrondis ressemblant à des kystes d'amibes, fermés par une coque très épaisse, renfermant une morula centrale et, de couleur verdâtre et plusieurs globules réfringents non sporulés dans les selles, 6 -10 µm, autofluorescence bleuâtre entre 340/380 nm Autofluorescence Oocystes stade Oocystes avec 2 sporocystes Morula Coloration Safranine

Cycle évolutif: probablement direct dans les entérocytes, élimination fécale des oocystes, L'oocyste n'est pas sporulée lors de son émission, c'est-à-dire ne contient pas encore de sporozoïtes, seul forme infectante, la sporogonie est extérieure. Epidémiologie: parasitose cosmopolite, mais à tendance tropicale. Amérique du Nord et Centrale, Asie, prévalence plus marquée dans certains pays comme, le Népal, le Pérou, Haïti, Java, le Guatemala. . . La transmission du parasite est oro-fécale, par l'intermédiaire des fruits (framboises du Guatemala), des crudités et de l'eau de boisson. Les oocystes de Cyclospora cayetanensis résistent à la chloration, mais sont détruites par l'ébullition. Clinique: syndrome diarrhéique prolongé (7 jours en moyenne), conduisant à l’amaigrissement, guérison spontanée chez l'immunocompétent. Dangereux chez l’immunodéprimé. Diagnostic: oocystes non sporulés dans les selles, ils se colorent irrégulièrement à la coloration de Ziehl modifiée, ou à la safranine. Autofluorescence.

TRICHOMONAS VAGINALIS (Trichomonase)
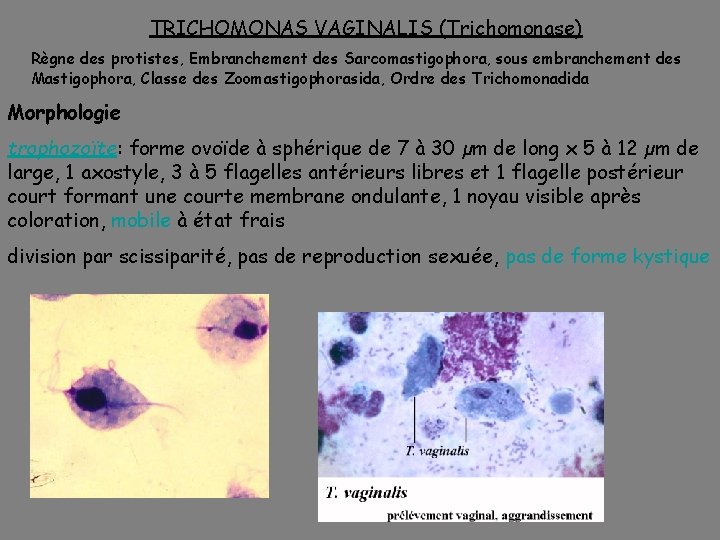
TRICHOMONAS VAGINALIS (Trichomonase) Règne des protistes, Embranchement des Sarcomastigophora, sous embranchement des Mastigophora, Classe des Zoomastigophorasida, Ordre des Trichomonadida Morphologie trophozoïte: forme ovoïde à sphérique de 7 à 30 µm de long x 5 à 12 µm de large, 1 axostyle, 3 à 5 flagelles antérieurs libres et 1 flagelle postérieur court formant une courte membrane ondulante, 1 noyau visible après coloration, mobile à état frais division par scissiparité, pas de reproduction sexuée, pas de forme kystique

Cycle évolutif: cycle direct, parasite monoxène parasite strictement humain localisé dans les voies génitales masculines et féminines, pas de phase extra corporelle, transmission directe par contact sexuel (MST) Epidémiologie : R de P: individus masculins de l'espèce humaine, résistance du trophozoïte faible dans le milieu extérieur prévalence: 15 à 25 % des femmes adultes (jusque 50 % dans certains pays d'Afrique) Clinique chez le sujet féminin: localisation dans le vagin et l'urètre, alcalinisation du milieu qui favorise la prolifération du parasite. formes bénignes parfois asymptomatiques, ou vaginite subaiguë: prurit vulvaire, leucorrhées abondantes (blanchâtres, spumeuses ou glaireuses, parfois verdâtres), ou vaginite aiguë: sensation de brûlures vulvaires, dyspareunie (relations sexuelles douloureuses), leucorrhées abondantes, possibilité d'extension: cystites, urétrites, complications génitales hautes plus rares. Association possible avec Candida albicans, et Neisseria gonorrohae.

chez le sujet masculin: localisation dans l'urètre, la prostate et les vésicules séminales; conditions de vie moins favorables chez l'homme car élimination d'une partie des parasites à chaque miction le plus souvent, porteur asymptomatique ou urétrite subaiguë: écoulement mucopurulent, sensation de démangeaison voire de brûlure à la miction, complications rares (balanites, cystites et prostatites). Diagnostic: précautions lors du prélèvement en raison de la fragilité du parasite et de sa sensibilité au froid et à la dessiccation chez la femme: prélèvement vaginal après la pose d'un spéculum sans lubrifiant, utiliser des curettes ou pipettes pasteur (de préférence ne pas utiliser d'écouvillons). chez l'homme: le matin, avant le premier jet d'urine, prélever les secrétions à l'aide d'une anse stérile, éventuellement effectuer au préalable un massage prostatique le parasite peut être trouvé dans le culot de centrifugation de la première urine du matin, mais il y est rapidement détruit.

Traitement de l'échantillon: -mettre une goutte du prélèvement dans une goutte de sérum physiologique, couvrir d'une lamelle et observer immédiatement au microscope: le parasite est mobile, doué de mouvements brusques. -réaliser un frottis sec coloré au Giemsa: parasites souvent déformés -mise en culture sur milieu diphasique Thérapeutique: la trichomonose est une maladie sexuellement transmissible, pour éviter la re-contamination, il faut traiter simultanément tous les partenaires et éviter les relations sexuelles ou les protéger pendant le traitement antiparasitaire.

Toxoplasma gondii-(Toxoplasmose) (Apicomplexa, Sporozoasida, ordre Coccidie) Cycle évolutif : Cycle monoxène ou hétéroxène HD: félidés (chat, …), localisation: tube digestif, reproduction asexuée puis sexuée => oocystes dans le milieu extérieur: maturation des oocystes qui contiennent 2 fois 4 sporozoïtes infectieux Les oocystes infectieux peuvent être ingérés par l'HD (cycle direct ou court) ou par des HI (cycle indirect ou long) HI: animal à sang chaud (mammifère, oiseau, homme) - ingestion des oocystes murs, les sporozoïtes => tachyzoïtes dans des macrophages, phase sanguine de dissémination ou septicémie -ingestion des kystes contenant les bradyzoïtes Tachyzoïtes dans LBA

Epidémiologie: Zoonose cosmopolite Principales sources de contamination humaine: - ingestion d'oocystes murs telluriques (eau, aliments, mains) (2 % des chats sont semeurs d'oocystes) - ingestion de kystes vivants dans de la viande crue ou insuffisamment cuite (80% des ovins et caprins adultes parasités, < 40% porcs) - passage transplacentaire: toxoplasmose fœtale (cf polycop sérologie) -transmission par greffe d'organe

Le plus souvent, chez le sujet VIH, il s'agira de la réactivation de kystes cérébraux consécutifs à une toxoplasmose acquise faite antérieurement. Le risque de cette réactivation est important quand le taux de CD 4+ du patient devient inférieur à 100/mm 3. La clinique traduit le plus souvent: lésions cérébrales avec fièvre, céphalées et troubles du comportement, lésions oculaires Diagnostic: peu ou pas d'anticorps sériques détectables en raison du déficit immunitaire, utilisation des arguments cliniques et de l'imagerie nécessité de mise en oeuvre de méthodes directes de diagnostic: -la recherche des tachyzoïtes ne serait possible que pendant la phase septicémique de la maladie, leur rareté rend leur mise en évidence peu probable. -la mise en culture du parasite contenu dans un prélèvement (LBA, LCR, sang), sur souris (réponse tardive après quelques semaines), culture sur fibroblaste (réponse plus rapide en quelques jours) -PCR très sensible, elle détecte 1 toxoplasme mort ou vivant dans le prélèvement.

Cryptosporidium parvum - (Cryptosporidiose)

Cryptosporidium parvum- (Cryptosporidiose) (Apicomplexa, Sporozoasida, ordre Coccidie) Epidémiologie: cosmopolite R de P : homme, bétail etc. . . principalement les jeunes animaux (veaux, chevreaux, porcelet, …) chez les immunocompétents: responsable d'environ 5 % des diarrhées dans les pays chauds en voie de développement et d'1 à 2 % dans les régions tempérées. (400 cas, microépidémie Dracy le Fort-71 - sept 2001) (400 000 cas, 100 morts, Milwaukee, USA, 1993) chez les immunodéprimés (VIH): responsable d'environ 20 % des diarrhées en France et 20 à 30 % dans les pays chauds en voie de développement. Contamination orale: ingestion d'oocystes avec l'eau (oocystes résistants au chlore) et les aliments, (piscine, lait cru, cidre. . ) Contact direct homme/animaux (éleveurs, vétérinaires), inter/humains
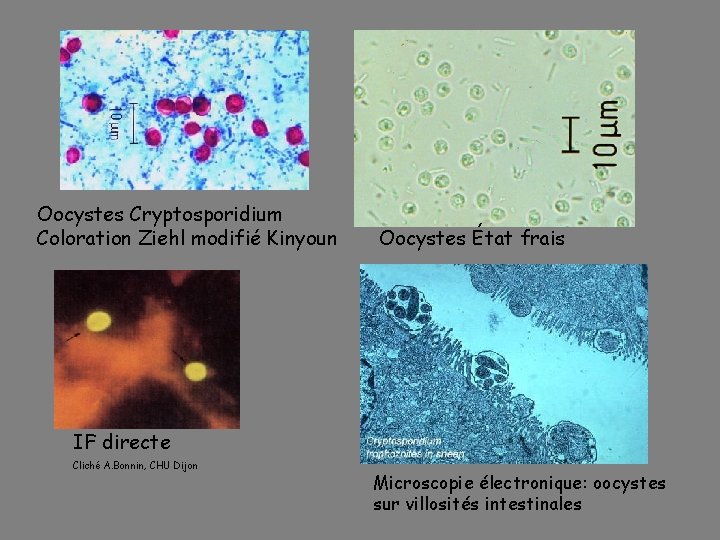
Oocystes Cryptosporidium Coloration Ziehl modifié Kinyoun Oocystes État frais IF directe Cliché A. Bonnin, CHU Dijon Microscopie électronique: oocystes sur villosités intestinales
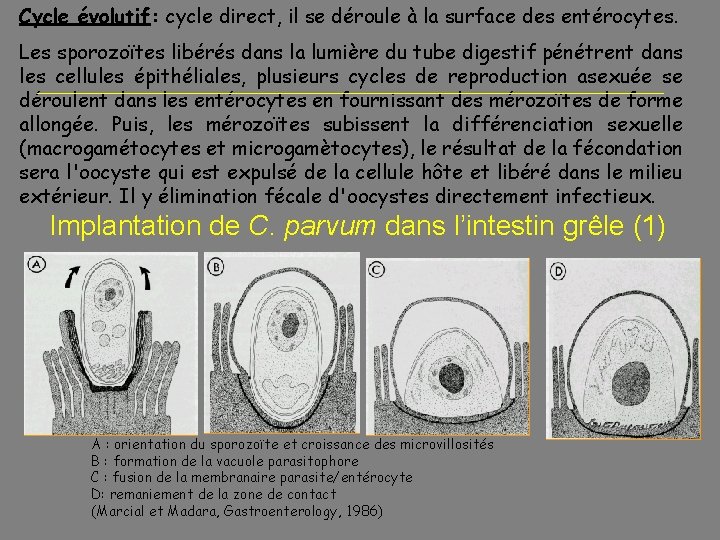
Cycle évolutif: cycle direct, il se déroule à la surface des entérocytes. Les sporozoïtes libérés dans la lumière du tube digestif pénétrent dans les cellules épithéliales, plusieurs cycles de reproduction asexuée se déroulent dans les entérocytes en fournissant des mérozoïtes de forme allongée. Puis, les mérozoïtes subissent la différenciation sexuelle (macrogamétocytes et microgamètocytes), le résultat de la fécondation sera l'oocyste qui est expulsé de la cellule hôte et libéré dans le milieu extérieur. Il y élimination fécale d'oocystes directement infectieux. Implantation de C. parvum dans l’intestin grêle (1) A : orientation du sporozoïte et croissance des microvillosités B : formation de la vacuole parasitophore C : fusion de la membranaire parasite/entérocyte D: remaniement de la zone de contact (Marcial et Madara, Gastroenterology, 1986)
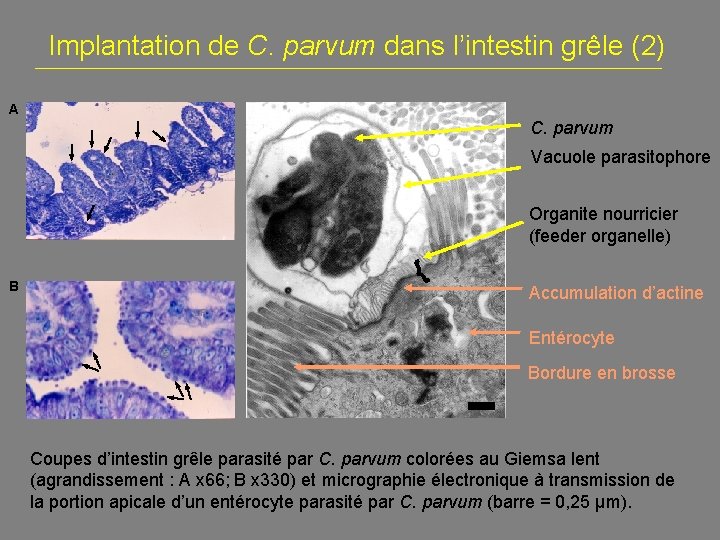
Implantation de C. parvum dans l’intestin grêle (2) A C. parvum Vacuole parasitophore LP Organite nourricier (feeder organelle) C { B Accumulation d’actine LP E Entérocyte Bordure en brosse Coupes d’intestin grêle parasité par C. parvum colorées au Giemsa lent (agrandissement : A x 66; B x 330) et micrographie électronique à transmission de la portion apicale d’un entérocyte parasité par C. parvum (barre = 0, 25 µm).

Clinique: incubation 3 à 12 jours, diarrhées chez les immunocompétents: touche plus souvent les enfants, gastro entérite avec diarrhée, vomissements, fièvre, guérison spontanée après 10 jours chez les immunodéprimés: souvent inaugurale du stade III du SIDA. (facteur de risque: taux de CD 4+ < 140 /mm 3). Diarrhée cholériforme jusque 2 à 6 litres/jour, déshydratation, désordres électrolytiques et importante perte de poids qui imposent l'hospitalisation, pas de tendance à la rémission Diagnostic: diagnostic direct, Trouvés dans les selles, et les biopsies Oocystes de 4 -5 µm à paroi épaisse, sans sporocystes et contenant 4 sporozoïtes. -identification est facilitée par la coloration de Ziehl (parasite en rouge, contre coloration verte, dans ce cas, les levures restent vertes) , -IF, marquage par un anticorps anti-Cryptosporidium -PCR

Pneumocystis (carinii) jirovecii(Pneumocystose)

Pneumocystis (carinii) jirovecii-(Pneumocystose) Ce ne sont pas des protozoaires parasites mais des Champignons opportunistes atypiques Morphologie: 3 formes trophozoïte: 2 à 8 µm de diamètre, amoeboïde, uninucléé prékyste: 3 à 6 µm de diamètre, divisions nucléaires ==> paroi épaissie kyste: 4 à 6 µm , paroi épaisse, contient 8 corps intrakystiques (futurs trophozoïtes) localisation pulmonaire préférentielle (surface des cellules) Epidémiologie: cosmopolite, primo-infestation dans le jeune âge, présence fréquente dans les poumons de sujets sains immunocopmpétents, parasite opportuniste ==> pathologie fréquente des immunodéprimés (VIH, greffés, prématurés) contamination aérienne et expectoration des kystes
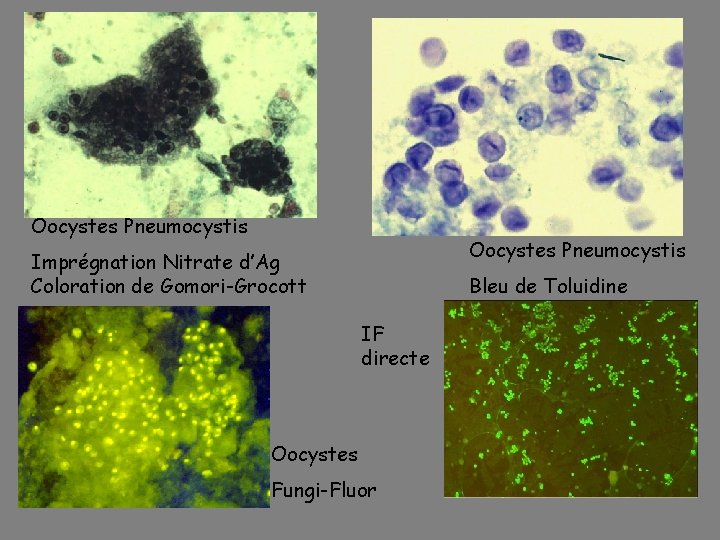
Oocystes Pneumocystis Imprégnation Nitrate d’Ag Coloration de Gomori-Grocott Bleu de Toluidine IF directe Oocystes Fungi-Fluor

Clinique: -sujet immunocompétent: asymptomatique, guérison spontanée -sujet immunodéprimé: prématurés, transplantés, sujets VIH+ (< 200 CD 4+/mm 3 ), touche 60 % des sujets dans la première année du stade SIDA ==> Pneumonie Insterticielle Diffuse, début discret, toux, dyspnée, fièvre 38 -40°C, douleur thoracique, cyanose évolution sévère sans traitement: emphysème, pneumothorax, mort Diagnostic: -mise en évidence du parasite sur LBA ou expectorations: frottis colorés par -bleu de toluidine pour les parois des prékystes et kystes (bleu) -Giemsa pour les trophozoïtes et corps intrakystiques (rouge) -imprégnation argentique pour les kystes (noir sur fond vert) -IF révélation par anticorps marqué -PCR -sur biopsie pulmonaire, coloration classique
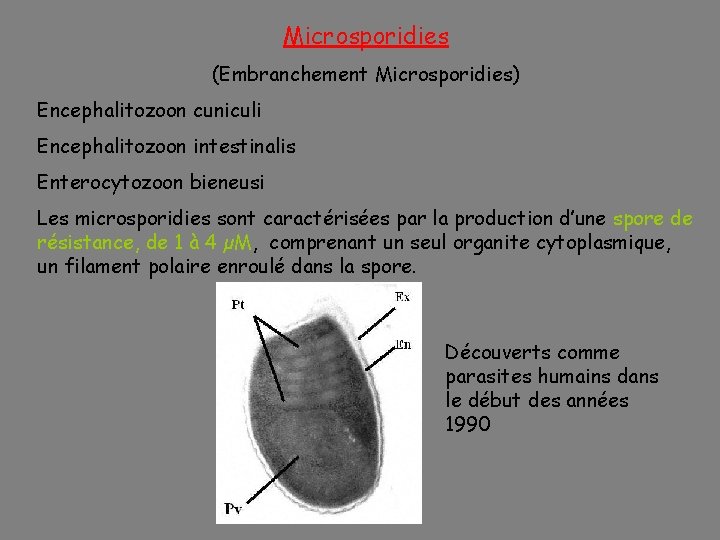
Microsporidies (Embranchement Microsporidies) Encephalitozoon cuniculi Encephalitozoon intestinalis Enterocytozoon bieneusi Les microsporidies sont caractérisées par la production d’une spore de résistance, de 1 à 4 µM, comprenant un seul organite cytoplasmique, un filament polaire enroulé dans la spore. Découverts comme parasites humains dans le début des années 1990
![Life Cycle: [1] The infective form of microsporidia is the resistant spore and it Life Cycle: [1] The infective form of microsporidia is the resistant spore and it](http://slidetodoc.com/presentation_image_h/d42ec942c2555412c54d3be39a67800f/image-43.jpg)
Life Cycle: [1] The infective form of microsporidia is the resistant spore and it can survive for a long time in the environment. [2] The spore hatches by extruding its polar tubule and infects the host cell. [3] The spore injects the infective sporoplasm into the eukaryotic host cell through the polar tubule. [4] Inside the cell, the sporoplasm undergoes extensive multiplication either by merogony (binary fission) or schizogony (multiple fission). This development can occur either in direct contact with the host cell cytoplasm (A) or inside a vacuole termed parasitophorous vacuole (B). [5] Either free in the cytoplasm (A) or inside a parasitophorous vacuole (B), microsporidia develop by sporogony to mature spores. During sporogony, a thick wall is formed around the spore which provides resistance to adverse environmental conditions. [6] When the spores increase in number and completely fill the host cell cytoplasm, the cell membrane is disrupted and releases the spores to the surroundings. These free mature spores can infect new cells thus continuing the cycle.
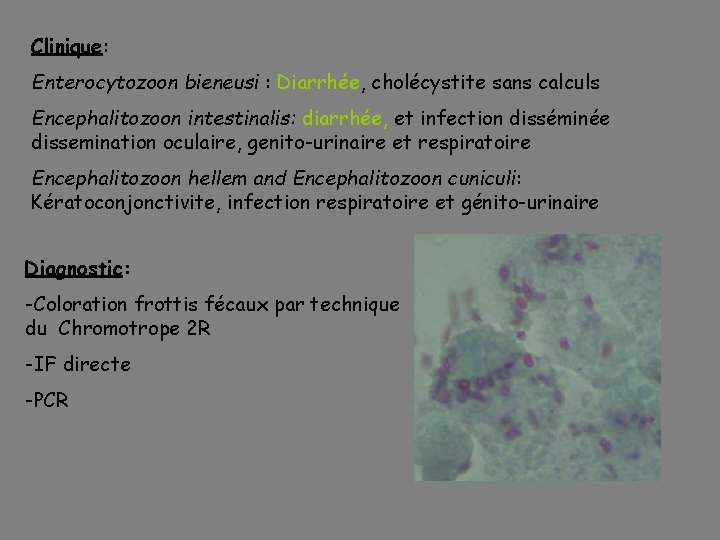
Clinique: Enterocytozoon bieneusi : Diarrhée, cholécystite sans calculs Encephalitozoon intestinalis: diarrhée, et infection disséminée dissemination oculaire, genito-urinaire et respiratoire Encephalitozoon hellem and Encephalitozoon cuniculi: Kératoconjonctivite, infection respiratoire et génito-urinaire Diagnostic: -Coloration frottis fécaux par technique du Chromotrope 2 R -IF directe -PCR

Isospora belli (Apicomplexa, Sporozoasida, ordre Coccidie) Morphologie: oocyste : de forme elliptique, >20 µm de long, à l'émission, il contient 2 sporocystes ronds (les sporozoïtes ne se distinguent qu'après plusieurs jours de maturation à l'extérieur) Cycle évolutif: cycle direct HD: homme, localisé dans les cellules épithéliales du tube digestif les sporozoïtes libérés dans la lumière du tube digestif pénètrent dans les cellules épithéliales reproduction asexuée: plusieurs cycles se déroulent dans entérocytes en fournissant des mérozoïtes de forme allongée. les reproduction sexuée: dans entérocytes, les mérozoïtes subissent la différenciation sexuelle (macrogamétocytes et microgamètocytes), le résultat de la fécondation sera l'oocyste qui est expulsé de la cellule hôte et libéré dans le milieu extérieur.
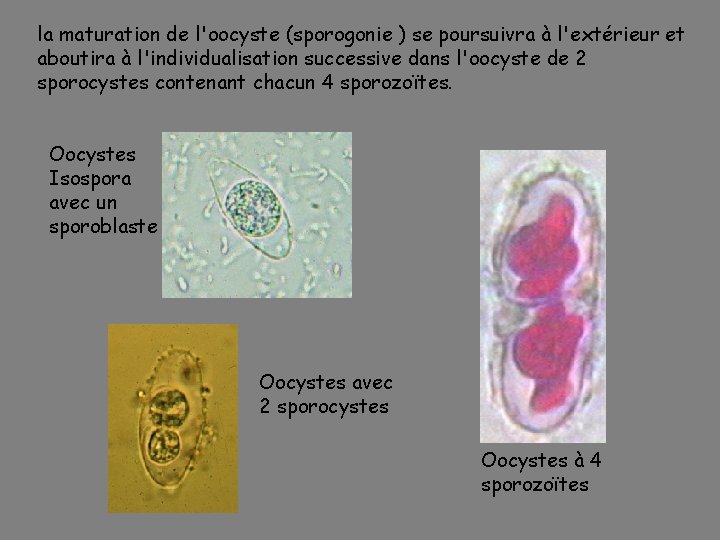
la maturation de l'oocyste (sporogonie ) se poursuivra à l'extérieur et aboutira à l'individualisation successive dans l'oocyste de 2 sporocystes contenant chacun 4 sporozoïtes. Oocystes Isospora avec un sporoblaste Oocystes avec 2 sporocystes Oocystes à 4 sporozoïtes

Epidémiologie: R de P : homme contamination par ingestion d'oocystes murs contenus dans l'eau et les aliments (péril fécal humain) prévalence en zone tropicale: 1 % chez immunocompétents, 10 % chez immunodéprimés Clinique: diarrhée chez les immunocompétents: entérite avec diarrhée aiguë, guérison en quelques semaines chez les immunodéprimés: diarrhée persistante avec selles glairosanglantes à répétition, risque de déshydratation, (parasitose parfois inaugurale du stade III du SIDA) Diagnostic: mise en évidence des oocystes dans les selles directement ou après concentration.
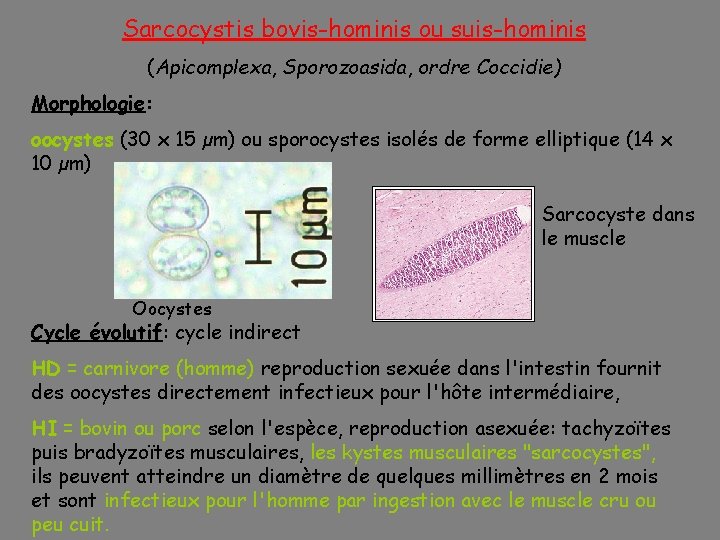
Sarcocystis bovis-hominis ou suis-hominis (Apicomplexa, Sporozoasida, ordre Coccidie) Morphologie: oocystes (30 x 15 µm) ou sporocystes isolés de forme elliptique (14 x 10 µm) Sarcocyste dans le muscle Oocystes Cycle évolutif: cycle indirect HD = carnivore (homme) reproduction sexuée dans l'intestin fournit des oocystes directement infectieux pour l'hôte intermédiaire, HI = bovin ou porc selon l'espèce, reproduction asexuée: tachyzoïtes puis bradyzoïtes musculaires, les kystes musculaires "sarcocystes", ils peuvent atteindre un diamètre de quelques millimètres en 2 mois et sont infectieux pour l'homme par ingestion avec le muscle cru ou peu cuit.

Epidémiologie: contamination orale (ingestion des bradyzoïtes dans la viande) cosmopolite mais il s'agit surtout d'une maladie vétérinaire car 98 % des bovins sont infectés par diverses espèces de Sarcocystis. chez les humains la prévalence est très faible. Clinique: souvent asymptomatique chez l'immunocompétent; diarrhées chez l'immunodéprimé Diagnostic: oocystes (30 x 15 µm) ou sporocystes de forme elliptique (14 x 10 µm) dans les selles confusion possible avec oocystes d'Isospora belli et kystes de Giardia intestinalis, les sporocystes contiennent, dès l'émission, 4 sporozoïtes en forme de banane et une masse granuleuse à un des pôles.

- Slides: 50