Cours 3 Premier Principe de la thermodynamique 1














- Slides: 16

Cours 3 : Premier Principe de la thermodynamique 1. 1 Les 4 transformations de base 1. 2 Le 1 er Principe de la thermodynamique 1. 3 Implications du 1 er principe 1. 4 Enthalpie

3. 1 Les 4 transformations de base Les transformations réelles, généralement complexes, peuvent se décomposées en une succession de transformations élémentaires : Transformation « isobare » La pression du système reste constante lors de la transformation. Transformation « isochore » W = 0 Le volume du système reste constant lors de la transformation. Transformation « isotherme » La température du système reste constante lors de la transformation. Transformation « adiabatique » Q = 0 Aucune chaleur n’est échangée avec l’extérieur (transformation rapide et/ou calorifugée) L’intérêt de ces transformations : Expression simple de W, ou de Q, ou de W+Q.

3. 2 Le 1 er principe de la thermodynamique 1 er principe : bilan énergétique U 12 = W 12 + Q 12 Le 1 er principe exprime la conservation de l’énergie : Une variation d’énergie interne est due à une apparition de chaleur et/ou de travail. Remarque 1 : L’énergie interne U d’un système est une fonction d’état U 1 Énergie interne du système dans l’état 1 U 2 Énergie interne du système dans l’état 2 U 12 Variation d’énergie interne W 1 ou W 2 n’a aucun sens (contrairement à W 12) , W n’est pas une fonction d’état (un corps ne possède pas un travail). Idem pour la chaleur Q. La variation d’une fonction d’état est indépendante du chemin suivi, elle ne dépend que de l’état initial et de l’état final Fonctions d’état : T, m, V, nbre de moles, concentrations, …

3. 2 Le 1 er principe de la thermodynamique Remarque 2 : L’énergie interne U d’un système est une variable extensive Variation d’énergie interne de deux corps A et B UA+B = UA + UB Variables extensives (proportionnelles à la quantité de matière): m, V… Variables intensives : P, T … Remarques utiles pour les exercices : · Pour une transformation adiabatique (Q 12= 0) , on aura toujours U 12 = W 12 · Pour 2 transformations successives 1 -2 puis 2 -3 alors U 13 = U 12 + U 23 Exercices 1 et 2

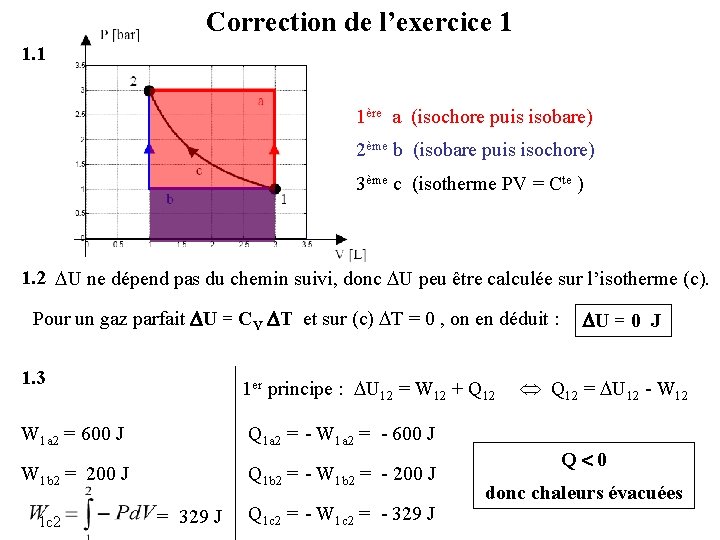
Exercice 1 Chaleurs et travaux échangés avec l’extérieur On effectue de 3 manières différentes, une compression qui amène du diazote N 2 (~air) de l’état 1 à l’état 2. État 1 : P 1 = P 0 = 1 bar et V 1 = 3 V 0 État 2 : P 2 = 3 P 0 et V 2 = V 0 = 1 litre La 1ère transformation est isochore puis isobare. La 2ème transformation est isobare puis isochore. La 3ème transformation est isotherme (PV = Cte). 1. Représenter les 3 transformations en coordonnées de Clapeyron. 2. Sachant que U = CV T (gaz parfait) , calculer U (variation d’énergie interne entre les états 1 et 2). 3. Calculez les travaux échangés dans les 3 cas. Déduisez-en les chaleurs échangées : sont-elles reçues ou évacuées ?

Correction de l’exercice 1 1ère a (isochore puis isobare) 2ème b (isobare puis isochore) 3ème c (isotherme PV = Cte ) 1. 2 U ne dépend pas du chemin suivi, donc U peu être calculée sur l’isotherme (c). Pour un gaz parfait U = CV T et sur (c) T = 0 , on en déduit : U = 0 J 1. 3 1 er principe : U 12 = W 12 + Q 12 = U 12 - W 12 W 1 a 2 = 600 J Q 1 a 2 = - W 1 a 2 = - 600 J W 1 b 2 = 200 J Q 1 b 2 = - W 1 b 2 = - 200 J 1 c 2 = 329 J Q 1 c 2 = - W 1 c 2 = - 329 J Q 0 donc chaleurs évacuées

Exercice 2 Élévation de température d’un tube de mercure retourné plusieurs fois Un tube cylindrique de verre calorifugé a un diamètre D=3 cm, une hauteur H=1, 1 m et contient une masse M=1 kg de mercure à la température T (masse volumique =13600 kg. m-3, chaleur massique C = 138 J. kg-1 ). Le tube étant vertical, on le retourne 50 fois et on constate que la température du mercure s’est élevée de T. 1. Calculez le travail développé par la masse M du mercure (on donne l’accélération due à la pesanteur g~9, 81 ms-2). 2. Calculez alors la variation d’énergie interne du mercure. 3. Calculez la variation de température T sachant que tout le travail a servi à échauffer le mercure.

Correction de l’exercice 2 2. 1 Travail W = M. g. (H – h). 50 Travail des forces de pesanteur Calcul de h : M = . V = . S. h = . (D/2)2. h donc A. N. Travail des forces de pesanteur W = 1. 9, 81. (1, 1 – 0, 104). 50 W = 489 J

Correction de l’exercice 2 2. 2 Variation d’énergie interne 1 er principe : U = W + Q or le tube cylindrique est calorifugé : Q = 0 donc : U = W U = 489 J 2. 3 Variation de température T Le travail des forces de pesanteur s’est transformé en chaleur grâce aux frottements (viscosité du mercure). Attention : cette chaleur reçue par le mercure n’est pas une chaleur échangée avec l’extérieur (Q=0). On a finalement W = Qfrottement = M. C. T A. N. ou °C

1. 3 Implications du 1 er principe W et Q sont deux grandeurs dépendantes du chemin suivi alors que leur somme W + Q est indépendante du chemin suivi, W + Q = U 12 ne dépend que des états final et initial. U 12 = U 2 - U 1 La variable U est caractéristique de l’état du gaz, c’est une variable d’état, au même titre que P, V et T. Implication n° 1 : évaluation de U 12 pour une transformation compliquée U 1 A 2 = U 1 B 2 = U 2 - U 1 C WC , QC Il n’est pas nécessaire de connaître dans les détails une transformation compliquée, il suffit de connaître précisément l’état initial et l’état final. U 1 C 2 = U 2 - U 1 Utilisation du chemin C (succession de transformations élémentaires : isochore + isobare + isochore)

1. 3 Implications du 1 er principe Implication n° 2 Importance des cycles : effectuer un cycle est le seul moyen d’avoir un fonctionnement périodique d’une machine. Un cycle est composée de 2 transformations au minimum Ucycle = Ufinal - Uinitial = U 1 – U 1 = 0 Ucycle = U 1 B 2 + U 2 A 1 = WB + QB + WA + QA = 0 Remarque : U = 0 pour les transformations cycliques et pour les transformations isolées (aucun échange avec l’extérieur) Uisolé = 0 Exercice 3

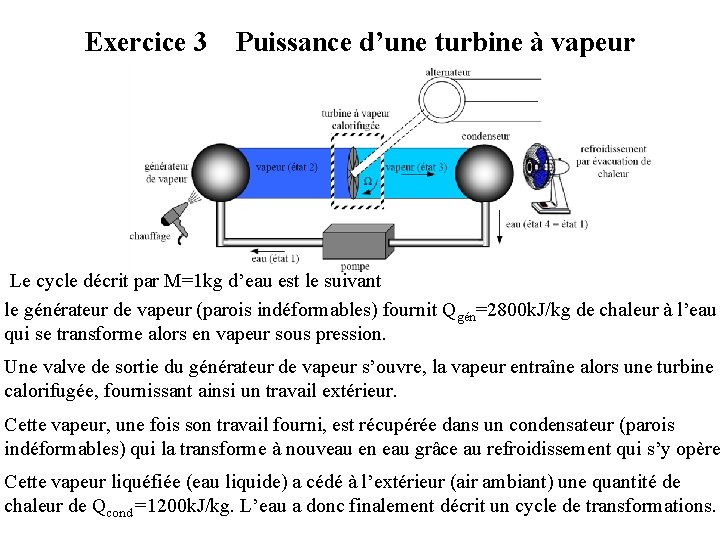
Exercice 3 Puissance d’une turbine à vapeur Le cycle décrit par M=1 kg d’eau est le suivant le générateur de vapeur (parois indéformables) fournit Qgén=2800 k. J/kg de chaleur à l’eau qui se transforme alors en vapeur sous pression. Une valve de sortie du générateur de vapeur s’ouvre, la vapeur entraîne alors une turbine calorifugée, fournissant ainsi un travail extérieur. Cette vapeur, une fois son travail fourni, est récupérée dans un condensateur (parois indéformables) qui la transforme à nouveau en eau grâce au refroidissement qui s’y opère Cette vapeur liquéfiée (eau liquide) a cédé à l’extérieur (air ambiant) une quantité de chaleur de Qcond =1200 k. J/kg. L’eau a donc finalement décrit un cycle de transformations.

Exercice 3 Puissance d’une turbine à vapeur 3. 1 A l’aide du 1 er principe, calculez la variation d’énergie interne massique (U 2 – U 1)/M et (U 4 – U 3)/M. U 12 = Q 12 + W 12 Or les parois du générateur de vapeur sont indéformables donc V=0 donc pas d’échange de travail avec l’extérieur W 12 = 0 U 12 = Q 12 = + M. Qgén Chaleur reçue U 34 = Q 34 + W 34 Or les parois du condensateur sont indéformables donc W 34 = 0 U 34 = Q 34 = - M. Qcond Chaleur cédée

Exercice 3 3. 2 Sachant que l’eau décrit un cycle, déduisez-en la variation d’énergie interne massique (U 3 – U 2)/M et le travail massique W 23/M qui est fourni à la turbine. Ucycle = U 12 + U 23 + U 34 = 0 donc U 23 = Q 23 + W 23 Or les parois de la turbine sont calorifugée Q 23 = 0 donc U 23 = W 23

Exercice 3 3. 3 La turbine entraînant l’alternateur possède dans ce cas un débit massique qturb= 4 kg/s. Calculez la puissance P développée par la turbine. On connaît: - le travail massique qui est fourni à la turbine : W 23/M - le débit massique de la turbine : qturb Utilisons une équation au dimension pour trouver l’expression de P : Donc A. N. P = 4. 1600 103 P = 6, 4 MW

1. 4 Enthalpie Détermination de la chaleur échangée Q 12 • Utilisation de la grandeur « enthalpie » : H = U + PV L’enthalpie H est une variable d’état. • Application : Transformations isobares (cas des réactions chimiques à pression atmosphérique) Q 12 p = H 12 p