Corso residenziale Dai sintomi alla diagnosi e alla












- Slides: 26

Corso residenziale Dai sintomi alla diagnosi e alla gestione: possibili percorsi in pediatria Protocollo APPROCCIO DIAGNOSTICO AL BAMBINO CON IMMUNODEFICIENZA GRAVE COMBINATA Tutor Prof. C. Pignata AIF Dott. ssa V. Gallo 08 Marzo 2017

Immunodeficienze primitive (IDP) Le immunodeficienze primitive (IDP) comprendono un gruppo eterogeneo di malattie, prevalentemente monogeniche, caratterizzate da alterazioni funzionali o di sviluppo del sistema immunitario e aumentata suscettibilità a sviluppare infezioni gravi e/o ricorrenti, autoimmunità e tumori Anni ’ 70 Oggi ~ 20 > 300 Deficit anticorpali Difetto dei fagociti Deficit del complemento Immunodeficienze Malattie. Combinate autoinfiammatorie Difetto (SCID, CID) dell’ immunità innata Immunodeficienze sindromiche Malattie da immunodisregolazione

Severe Combined Immuno. Deficiencies Gruppo eterogeneo di disordini ereditari, caratterizzati da assenza o presenza di linfociti T disfunzionali, sempre associato a deficit grave dell’immunità sia umorale che cellulare L’organismo è incapace di difendersi nei confronti di qualsiasi agente infettivo Rappresenta la forma più grave di immunodeficienza primitiva congenita Emergenza Pediatrica Incidenza = 1/58. 000 -100. 000 nati vivi 5 nuovi casi diagnosticati nel 2016 presso la nostra struttura Incidenza Campania 2016 1/12. 000

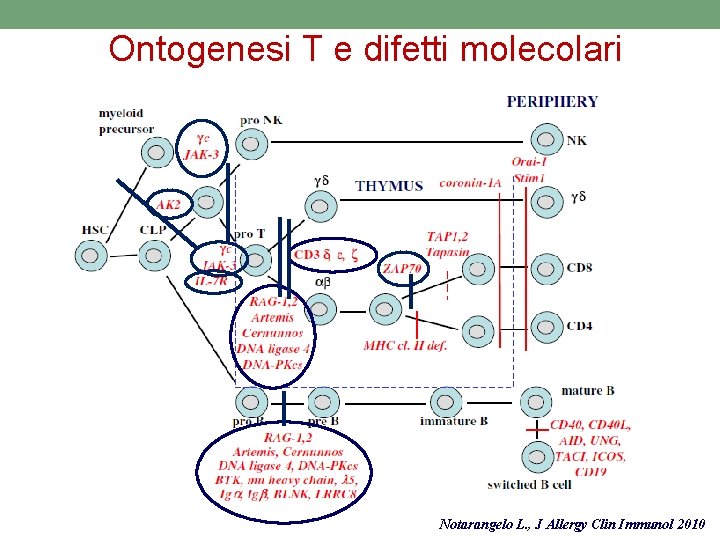
Ontogenesi T e difetti molecolari Notarangelo L. , J Allergy Clin Immunol 2010

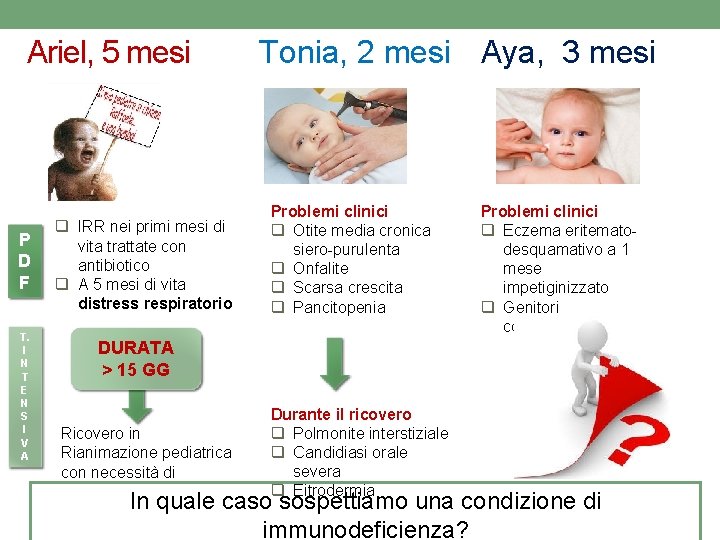
Ariel, 5 mesi P D F T. I N T E N S I V A q IRR nei primi mesi di vita trattate con antibiotico q A 5 mesi di vita distress respiratorio Tonia, 2 mesi Aya, 3 mesi Problemi clinici q Otite media cronica siero-purulenta q Onfalite q Scarsa crescita q Pancitopenia Problemi clinici q Eczema eritematodesquamativo a 1 mese impetiginizzato q Genitori consanguinei DURATA > 15 GG Ricovero in Rianimazione pediatrica con necessità di ventilazione invasiva Durante il ricovero q Polmonite interstiziale q Candidiasi orale severa q Eitrodermia In quale caso sospettiamo una condizione di immunodeficienza?

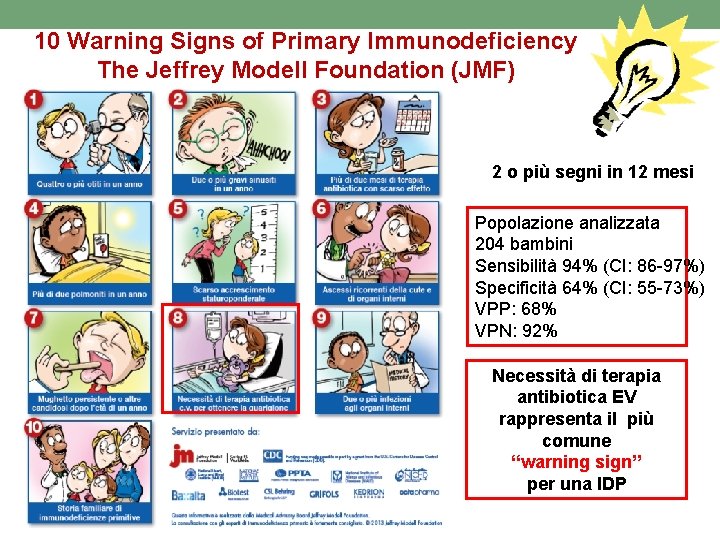
10 Warning Signs of Primary Immunodeficiency The Jeffrey Modell Foundation (JMF) 2 o più segni in 12 mesi Popolazione analizzata 204 bambini Sensibilità 94% (CI: 86 -97%) Specificità 64% (CI: 55 -73%) VPP: 68% VPN: 92% Necessità di terapia antibiotica EV rappresenta il più comune “warning sign” per una IDP

Quando sospettare una SCID? I campanelli di allarme Esordio precoce entro il 1 anno di vita q Diarrea persistente/ricorrente, refrattaria al trattamento, associata o meno ad atrofia dei villi intestinali, responsabile di malassorbimento e di grave distrofia q Interstiziopatia di lunga durata o Broncopolmoniti gravi e resistenti al trattamento, a elevato rischio di ricovero in terapia intensiva q Sepsi, meningite, encefalite q “Eczema importante” = Eritrodermia q Candidiasi sistemica q Infezioni causate dai comuni patogeni, o opportunisti (Candida albicans, Aspergillo, Pneumocystis jiroveci, CMV, EBV, HSV, adenovirus) germi intracellulari (Salmonella typhi, Listeria, Toxoplasma), spesso responsabili di quadri clinici di particolare gravità q Micobatteriosi disseminata, anche dopo vaccinazione q Reazione avversa a vaccino con virus vivo attenuato q Scarsa crescita staturo-ponderale q Consanguineità, familiarità per morti precoci da causa non nota o infettiva

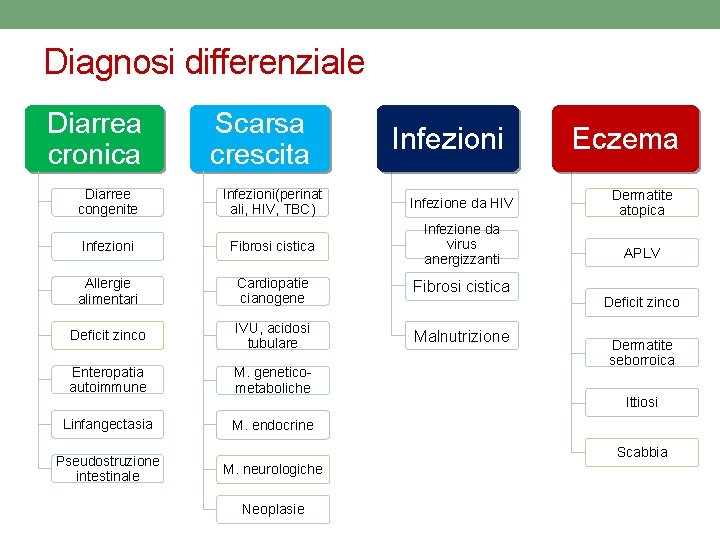
Diagnosi differenziale Diarrea cronica Diarree congenite Scarsa crescita Infezioni Eczema Infezioni(perinat ali, HIV, TBC) Infezione da HIV Dermatite atopica Infezioni Fibrosi cistica Infezione da virus anergizzanti APLV Allergie alimentari Cardiopatie cianogene Fibrosi cistica Deficit zinco IVU, acidosi tubulare Malnutrizione Enteropatia autoimmune M. geneticometaboliche Linfangectasia M. endocrine Pseudostruzione intestinale Deficit zinco Dermatite seborroica Ittiosi Scabbia M. neurologiche Neoplasie

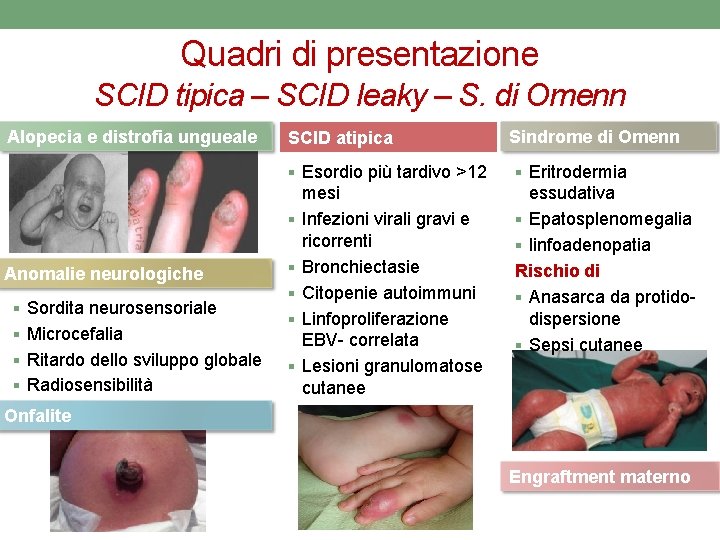
Quadri di presentazione SCID tipica – SCID leaky – S. di Omenn Alopecia e distrofia ungueale SCID atipica § Esordio più tardivo >12 § Anomalie neurologiche § Sordita neurosensoriale § Microcefalia § Ritardo dello sviluppo globale § Radiosensibilità § § mesi Infezioni virali gravi e ricorrenti Bronchiectasie Citopenie autoimmuni Linfoproliferazione EBV- correlata Lesioni granulomatose cutanee Sindrome di Omenn § Eritrodermia essudativa § Epatosplenomegalia § linfoadenopatia Rischio di § Anasarca da protidodispersione § Sepsi cutanee Onfalite Engraftment materno

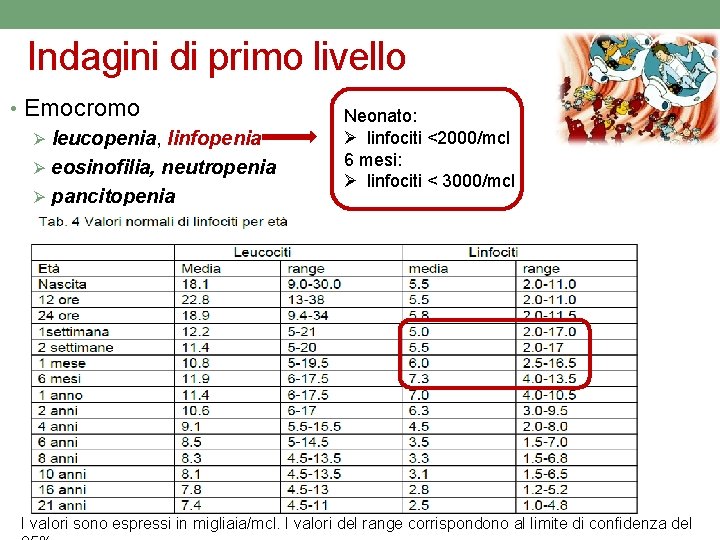
Indagini di primo livello • Emocromo Ø leucopenia, linfopenia Ø eosinofilia, neutropenia Ø pancitopenia Neonato: Ø linfociti <2000/mcl 6 mesi: Ø linfociti < 3000/mcl I valori sono espressi in migliaia/mcl. I valori del range corrispondono al limite di confidenza del

La conta leucocitaria • Linfociti >>neutrofili fino ai 4 -5 anni • Linfocitopenia leucopenia • Linfocitopenia secondaria Ø Malattie infettive (HIV, M. tubercolosis, HBV, HCV, EBV, CMV, VRS, virus influenzale, adenovirus, enterovirus, salmonella, rickettsia, borrelia) Ø Sepsi Ø Disordini autoimmuni (LES, vasculiti, sarcoidosi) Ø Iatrogena (terapia immunosoppressiva, glucocorticoidi, chemioterapia, RT) Ø Carenze nutrizionali (malnutrizione, deficit zinco ridotta produzione) Ø Aplasia midollare ØN. B. Linfangectasia intestinale Un numero normaleprimitiva di linfociti non consente di escludere una diagnosi di SCID! ~ 30% SCID linfopenia assente Ø Linfociti T autologhi oligoclonali Ø Linfociti T materni Ø Espansione linfociti B e NK

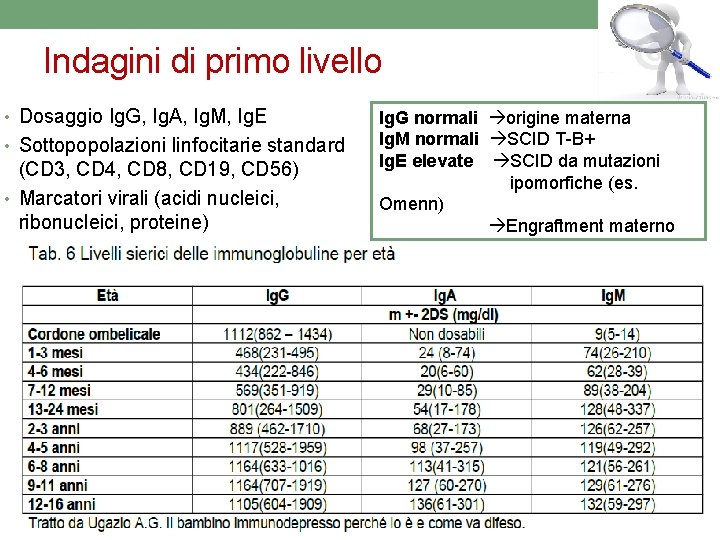
Indagini di primo livello • Dosaggio Ig. G, Ig. A, Ig. M, Ig. E • Sottopopolazioni linfocitarie standard (CD 3, CD 4, CD 8, CD 19, CD 56) • Marcatori virali (acidi nucleici, ribonucleici, proteine) Ig. G normali origine materna Ig. M normali SCID T-B+ Ig. E elevate SCID da mutazioni ipomorfiche (es. Omenn) Engraftment materno

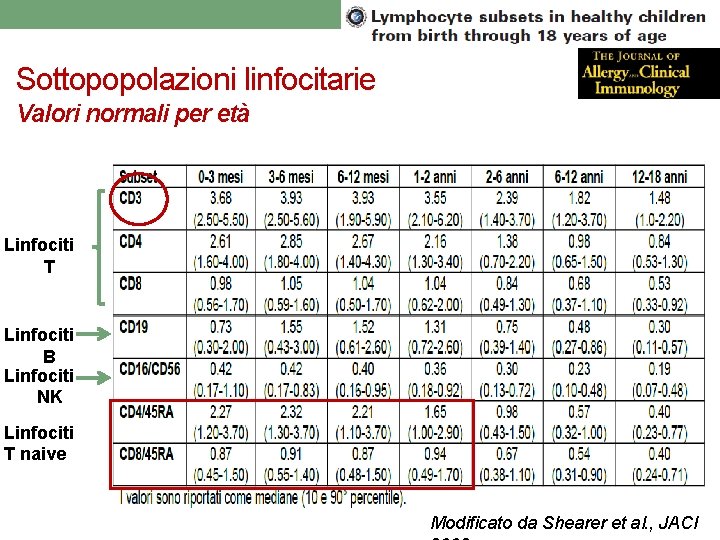
Sottopopolazioni linfocitarie Valori normali per età Linfociti T Linfociti B Linfociti NK Linfociti T naive Modificato da Shearer et al. , JACI

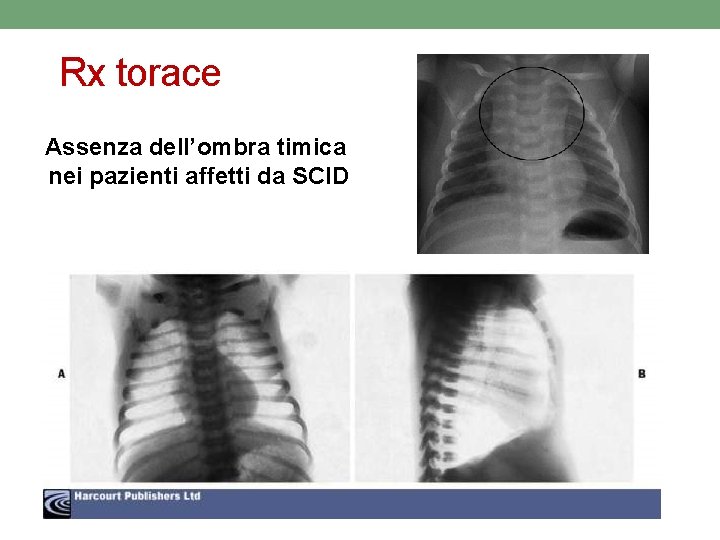
Rx torace Assenza dell’ombra timica nei pazienti affetti da SCID

C Indagini di secondo livello E • Risposta proliferativa ai mitogeni (PHA, anti CD 3, PMA+ionomicina) N • Sottopopolazioni linfocitarie estese (linfociti T naive e memory, TCR T gamma/delta) R O • Titoli anticorpali specifici anti-herpes, anti-varicella, anti-HCV, anti-EBV, anti. D CMV I • Ricerca di DNA, RNA e materiale proteico virale • Cariotipo standard T Indagini di terzo livello • Isoemoagglutinine E • TRECs (T-cell receptor excision circles) indice dell’output di linfociti T dal timo R • KRECs (kappa-deleting recombination excision circles) indice dell’output di Z linfociti B dal midollo O • Dosaggio enzimatico (ADA, PNP) L • Dosaggio su spot dei metaboliti adenosina, 2 -deossiadenosina, I deossiguanosina, deossinosina, inosina V • Test di radiosensibilità E • Indagine molecolare mediante sequenziamento L diretto del gene candidato L • Next-Generation Sequencing O

SCID: Criteri Diagnostici S. di Omenn SCID tipica • Assenza o riduzione severa dei linfociti T (CD 3+<300 cell/mm 3) e risposta proliferativa alla PHA assente o particolarmente ridotta (<10% dei limiti inferiori della norma) o presenza di engraftment materno Leaky SCID • Riduzione dei linfociti CD 3+ • Bambini <2 anni: <1000 cell/mm 3 • Bambini tra i 2 e i 4 anni: <800 cell/mm 3 • Bambini >4 anni: < 600 cell/mm 3 • Risposta proliferativa alla PHA <30% del controllo • Assenza di engraftment materno Shearer et al. , JACI • • Rash cutaneo generalizzato Assenza di engraftment materno Linfociti T CD 3+ >300 cell/mm 3 Assente o ridotta (≤ 30% della norma) risposta proliferativa ad antigeni cui il paziente è stato esposto o in assenza di quest’ultimo almeno 1 tra: • linfociti T oligoclonali • 80% di CD 3+ oppure dei CD 4+ sono linfociti della memoria • Risposta proliferativa alla PHA <30% • Mutazione di un gene SCID • Epatomegalia • Splenomegalia • Linfadenopatia • Aumento delle Ig. E sieriche • Aumento della conta assoluta degli

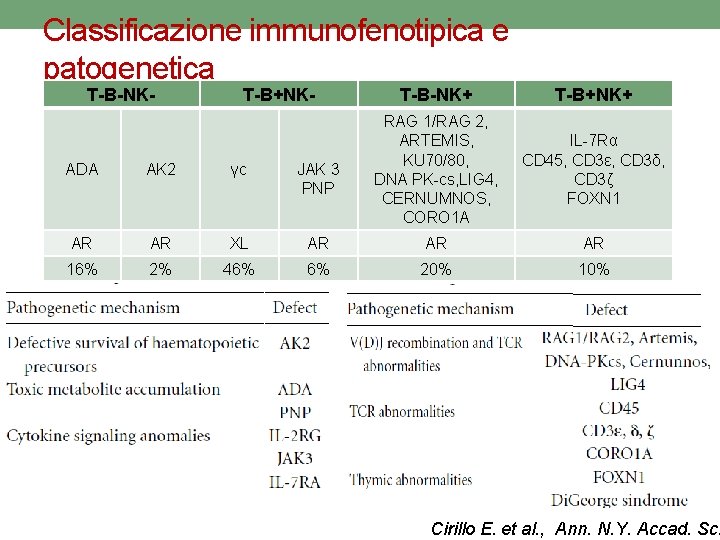
Classificazione immunofenotipica e patogenetica T-B-NK- T-B+NK- T-B-NK+ T-B+NK+ RAG 1/RAG 2, ARTEMIS, KU 70/80, DNA PK-cs, LIG 4, CERNUMNOS, CORO 1 A IL-7 Rα CD 45, CD 3ε, CD 3δ, CD 3ζ FOXN 1 ADA AK 2 γc JAK 3 PNP AR AR XL AR AR AR 16% 2% 46% 6% 20% 10% Cirillo E. et al. , Ann. N. Y. Accad. Sci

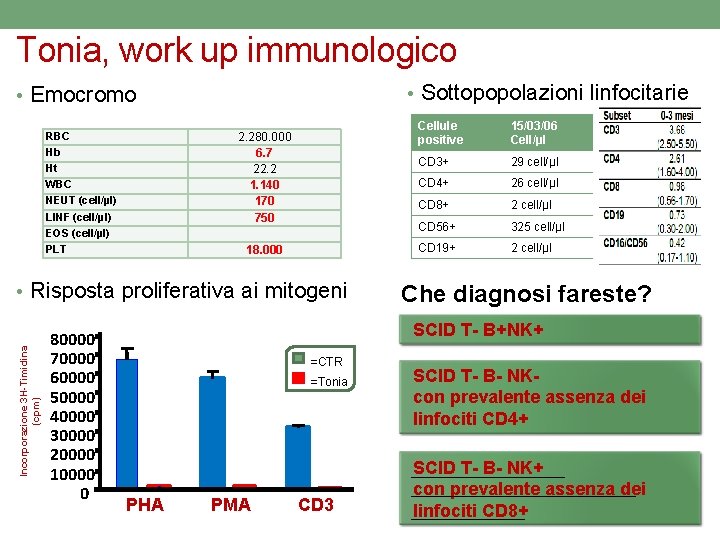
Tonia, work up immunologico • Sottopopolazioni linfocitarie • Emocromo RBC Hb Ht WBC NEUT (cell/µl) LINF (cell/µl) EOS (cell/µl) PLT 2. 280. 000 6. 7 22. 2 1. 140 170 750 18. 000 Incorporazione 3 H-Timidina (cpm) • Risposta proliferativa ai mitogeni 80000 70000 60000 50000 40000 30000 20000 10000 0 Cellule positive 15/03/06 Cell/µl CD 3+ 29 cell/µl CD 4+ 26 cell/µl CD 8+ 2 cell/µl CD 56+ 325 cell/µl CD 19+ 2 cell/µl Che diagnosi fareste? SCID T- B+NK+ =CTR =Tonia PHA PMA CD 3 SCID T- B- NKcon prevalente assenza dei linfociti CD 4+ SCID T- B- NK+ con prevalente assenza dei linfociti CD 8+

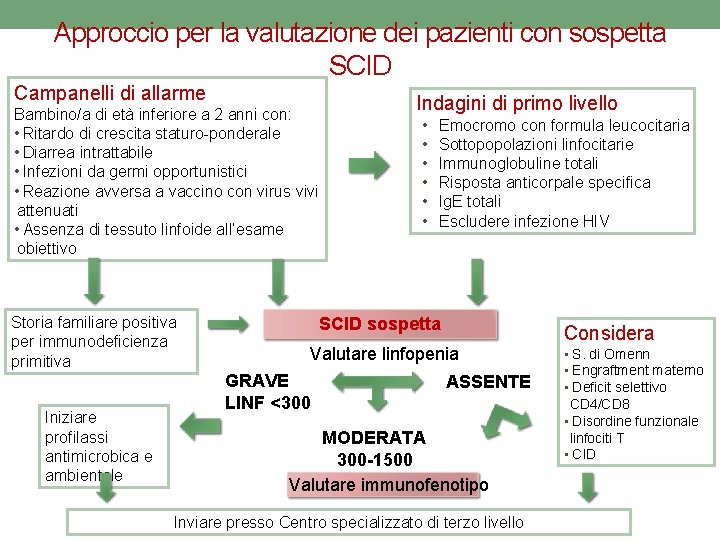
Approccio per la valutazione dei pazienti con sospetta SCID Campanelli di allarme Bambino/a di età inferiore a 2 anni con: • Ritardo di crescita staturo-ponderale • Diarrea intrattabile • Infezioni da germi opportunistici • Reazione avversa a vaccino con virus vivi attenuati • Assenza di tessuto linfoide all’esame obiettivo Storia familiare positiva per immunodeficienza primitiva Iniziare profilassi antimicrobica e ambientale Indagini di primo livello • • • Emocromo con formula leucocitaria Sottopopolazioni linfocitarie Immunoglobuline totali Risposta anticorpale specifica Ig. E totali Escludere infezione HIV SCID sospetta Valutare linfopenia GRAVE LINF <300 ASSENTE MODERATA 300 -1500 Valutare immunofenotipo Inviare presso Centro specializzato di terzo livello Considera • S. di Omenn • Engraftment materno • Deficit selettivo CD 4/CD 8 • Disordine funzionale linfociti T • CID

Opzioni terapeutiche • HSCT terapia di scelta • Terapia genica • ADA-SCID • yc-SCID Sopravvivenza a lungo termine: 7090% Prognosi eccellente se: - trapianto da fratello HLA identico - trapianto entro i 3. 5 mesi - anamnesi negativa per infezioni • Terapia enzimatica • ADA-SCID: somministrazione periodica, per via intramuscolare, di ADA di origine bovina, coniugata con polietilenglicole (PEG) In attesa del trapianto • Terapia sostitutiva con Ig EV o SC • Profilassi antimicrobica • Profilassi ambientale • Supporto nutrizionale (SNG, NPT)

Misure profilattiche • Profilassi antimicrobica ü Infezione da Pneumocystis jiroveci Cotrimossazolo 5 mg/kg/die di TMP in una o due dosi giornaliere per 3 giorni a settimana ü Candidiasi mucocutanea Fluconazolo 3 mg/kg/die per 3 giorni a settimana ü Infezione erpetica Ø Storia positiva: Acyclovir 15 mg/kg/die in 3 somministrazioni Ø Contatto con VZV: Immunoglobuline specifiche ü Infezione VRS Ø Età <2 aa, SCID o CD 4+ < a 200/mm 3: Pavilizumab 15 mg/kg IM una volta/mese nel periodo Ottobre-Febbraio • Profilassi ambientale • Ambiente ospedaliero in letti a flusso laminare, con filtri HEPA a pressione positiva • Rispettare le norme igieniche di aspesi nel corso di visite e Allattamento materno Consigliato se madre CMVnegativa!

Trasfusioni di emoderivati • Richiedere emoderivati • Irradiati con 3000 rad • Leucodepleti • CMV-negativi Rischio di GVHD! Vaccinazioni Vietate • Virus vivi e attenuati (morbillo, parotite, rosolia, varicella, rotavirus, virus dell'influenza attenuato, febbre gialla, poliovirus tipo Sabin) • Batteri attenuati (Bacillo di Calmette-Guerin -BCG- e Salmonella typhi Ty 21 a) üPermesse ma inefficaci • Anti-pneumococco, anti-Haemophilus influenza tipo b, anti-influenzale inattivato

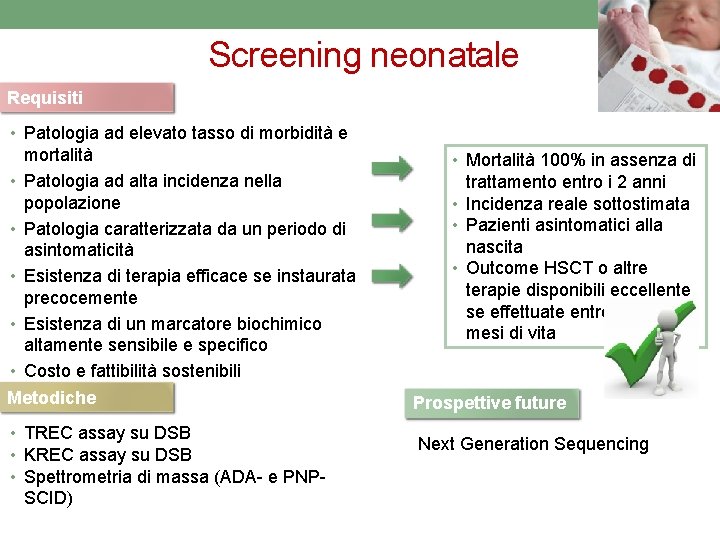
Screening neonatale Requisiti • Patologia ad elevato tasso di morbidità e mortalità • Patologia ad alta incidenza nella popolazione • Patologia caratterizzata da un periodo di asintomaticità • Esistenza di terapia efficace se instaurata precocemente • Esistenza di un marcatore biochimico altamente sensibile e specifico • Costo e fattibilità sostenibili Metodiche • TREC assay su DSB • KREC assay su DSB • Spettrometria di massa (ADA- e PNPSCID) • Mortalità 100% in assenza di trattamento entro i 2 anni • Incidenza reale sottostimata • Pazienti asintomatici alla nascita • Outcome HSCT o altre terapie disponibili eccellente se effettuate entro i primi 3 -4 mesi di vita Prospettive future Next Generation Sequencing

Take home messages • Considerare la possibilità di una ID è la chiave per diagnosticarla • La SCID rappresenta un’emergenza pediatrica • Le SCIDs sono malattie curabili se diagnosticate e se la gestione è affidata a un Centro specializzato in Immunodeficienze (la contaminazione ambientale rappresenta un enorme rischio per la vita del paziente !!! HLH secondaria) • La diagnosi molecolare richiede test funzionali e studi genetici di nuova generazione che devono essere effettuati presso centri specializzati per le enormi difficoltà di interpretazione

