Corso ECM di aggiornamento per Medici di Medicina




















- Slides: 55

Corso ECM di aggiornamento per Medici di Medicina Generale “L’uso razionale degli antibiotici per il Medico di Medicina generale: criticità e nuove indicazioni terapeutiche” “Indicazioni alla vaccinazione nell‘era della globalizzazione” Aula Congressuale - Ospedale di Cona (Fe) 11 febbraio 2017 Epidemiologia microbiologica territoriale M. Rita Rossi UO Semplice di Microbiologia e Sierologia Laboratorio Unico Provinciale AOU S. Anna Ferrara

Cosa chiede il clinico al microbiologo? ¡ Fondamentalmente le domande sono tre: 1. La malattia del mio paziente è causata da un microrganismo? 2. Se si, quale microrganismo? 3. Qual’é il profilo di sensibilità del germe in questione? Per soddisfare questi quesiti il laboratorio ha bisogno di informazioni dettagliate e di un campione selezionato, raccolto e trasportato in maniera appropriata IDSA GUIDELINES A Guide to Utilization of the Microbiology Laboratory for Diagnosis of Infectious Diseases: 2013

Appropriatezza del campione ¡ L’impatto dell’appropriatezza del campione sulla gestione della cura del paziente è enorme in termini di l l l esito decisioni terapeutiche impatto sul controllo delle infezioni durata del ricovero costo dell’ ospedalizzazione costo per indagini di laboratorio ed efficienza del laboratorio

Ruolo del laboratorio di Microbiologia Non disponendo di elementi per esprimere un giudizio sull’appropriatezza della richiesta ØIl laboratorio partecipa alla discussione con i clinici e alla stesura di linee guida utili nella selezione dei casi in cui esiste l’indicazione all’indagine microbiologia anche in relazione alle evidenze dei dati epidemiologici ØDefinisce le modalità corrette di raccolta, conservazione e trasporto del campione ØStabilisce le regole di interpretazione dei risultati delle indagini microbiologiche in correlazione al distretto e alle modalità di raccolta ØOffre un supporto nell’interpretazione del referto, referto in particolare nella lettura dell’antibiogramma in relazione al tipo di germe e al distretto colpito dall’infezione ØRende disponibili report epidemiologici sulle resistenze agli antibiotici utili nella scelta della terapia empirica

Il ruolo del microrganismo Microbiota Commensale Patogeno

Microbiota ¡ ¡ Si definisce microbiota l’insieme dei microrganismi che condividono una nicchia ecologica e “convivono” con l’organismo umano senza danneggiarlo Per diverse tipologie di campioni microbiologici esiste un “rumore di fondo” legato al microbiota normale (es. basse vie respiratorie, ferite superficiali, fistole) che può determinare un risultato falsamente positivo

Colonizzazione e infezione Un batterio è considerato patogeno quando è in grado di invadere i tessuti, di moltiplicarsi e di produrre una o più sostanze tossiche recano danno all’ospite Un patogeno deve trovare nell’ospite una nicchia da colonizzare, colonizzare dove potersi moltiplicare in competizione eventualmente con i batteri commensali abituali La proliferazione di un patogeno associata alla produzione di fattori di virulenza determina l’infezione

L’urina è normalmente sterile La presenza di microrganismi nelle urine indica ¡ Batteriuria Indica la colonizzazione del tratto urinario da parte di batteri, senza invasione dei tessuti ¡ Infezione del tratto urinario(UTI) 1. In Paziente asintomatico Esempi: donne gravide, diabetici 1. In Paziente sintomatico Indica un paziente con o senza batteriuria, portatore di sintomi Sintomi UTI Minzione frequente, disuria (dolore e difficoltà alla minzione), urgenza, nocturia o enuresi notturna, incontinenza, prostatismo, colica renale

Urinocoltura, quali indicazioni? UTI non complicate ¡ ¡ La sensibilità diagnostica per le UTI non complicate basata sui sintomi tipici e sui fattori di rischio varia dal 50 al 90% Il trattamento empirico può essere avviato sulla base dei soli sintomi Tra i limiti delle indagini microbiologiche il tempo di refertazione: 24 -72 ore La preoccupazione nel trattamento di queste infezioni è la resistenza antimicrobica… Guidelines for the diagnosis and treatment of uncomplicated UTI from several groups, including the American College of Obstetricians and Gynecologists (ACOG) (2008), the Scottish Intercollegiate Guidelines Network (SIGN) (2012), the University of Michigan Health System (UMHS) (2005), and the Infectious Disease Society of America (IDSA) (2011).

Patogeni urinari Comuni Meno comuni ¡ ¡ ¡ E. coli Enterococcus spp Klebsiella pneumoniae Proteus mirabilis Enterobacter spp Pseudomonas aeruginosa Staphylococcus aureus Staphylococcus saprophyticus Streptococus agalactiae Candida spp ¡ Aerococcus urinae Corynebacterium urealyticum ¡ Enterobacteriaceae spp Acinetobacter spp e altri non fermentanti ¡ Mycobacterium spp ¡ Mycoplasma hominis Ureaplasma urealyticum Chlamydia trachomatis Neisseria gonorrhoeae Trichomonas vaginalis ¡ ¡ ¡ JOURNAL OF CLINICAL MICROBIOLOGY, Sept. 2011, p. S 34–S 38 VOL. 49, NO. 9 SUPPL.

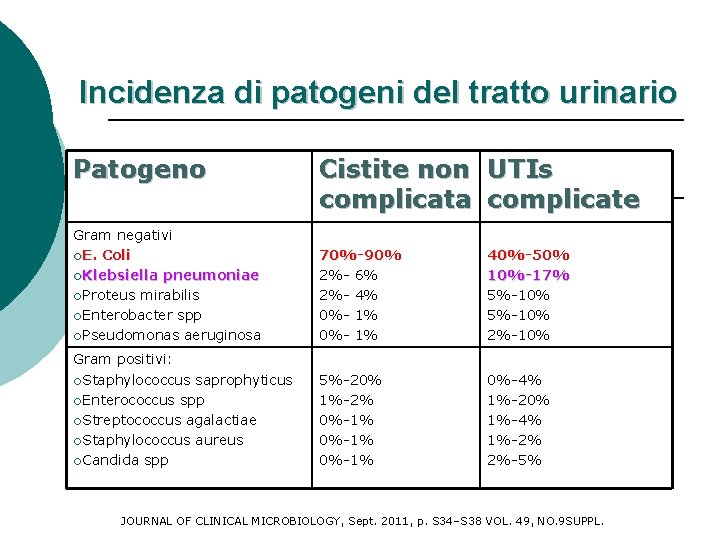
Incidenza di patogeni del tratto urinario Patogeno Cistite non UTIs complicata complicate Gram negativi ¡E. Coli ¡Klebsiella pneumoniae ¡Proteus mirabilis ¡Enterobacter spp ¡Pseudomonas aeruginosa 70%-90% 2%- 6% 2%- 4% 0%- 1% 40%-50% 10%-17% 5%-10% 2%-10% Gram positivi: ¡Staphylococcus saprophyticus ¡Enterococcus spp ¡Streptococcus agalactiae ¡Staphylococcus aureus ¡Candida spp 5%-20% 1%-2% 0%-1% 0%-4% 1%-20% 1%-4% 1%-2% 2%-5% JOURNAL OF CLINICAL MICROBIOLOGY, Sept. 2011, p. S 34–S 38 VOL. 49, NO. 9 SUPPL.

Manifestazione clinica e carica batterica significativa Tipologia infezione Manifestazione clinica Conta batterica significativa (CFU/ml) CFU/ml Tratto urinario alto: Acuta: febbre, brividi, dolore al fianco, nausea, vomito, WBC Cronica: asintomatico, sintomatologia mite o acuta, WBC, lesioni > 105 Sintomatico: disuria, minzione frequente Asintomatico >105 ¡Prostatite Acuta: febbre, brividi, mal di schiena Cronica: asintomatica o acuta > 103 ¡Uretrite Disuria, frequenza > 102 ¡Pielonefrite Basso tratto urinario: ¡Cistite

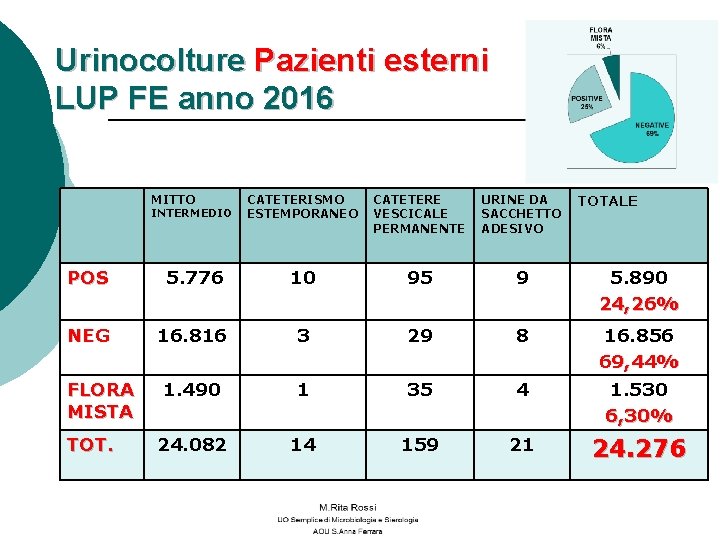
Urinocolture Pazienti esterni LUP FE anno 2016 MITTO TOTALE INTERMEDIO CATETERISMO ESTEMPORANEO CATETERE VESCICALE PERMANENTE URINE DA SACCHETTO ADESIVO POS 5. 776 10 95 9 5. 890 24, 26% NEG 16. 816 3 29 8 16. 856 69, 44% 1. 490 1 35 4 1. 530 6, 30% 24. 082 14 159 21 24. 276 FLORA MISTA TOT.

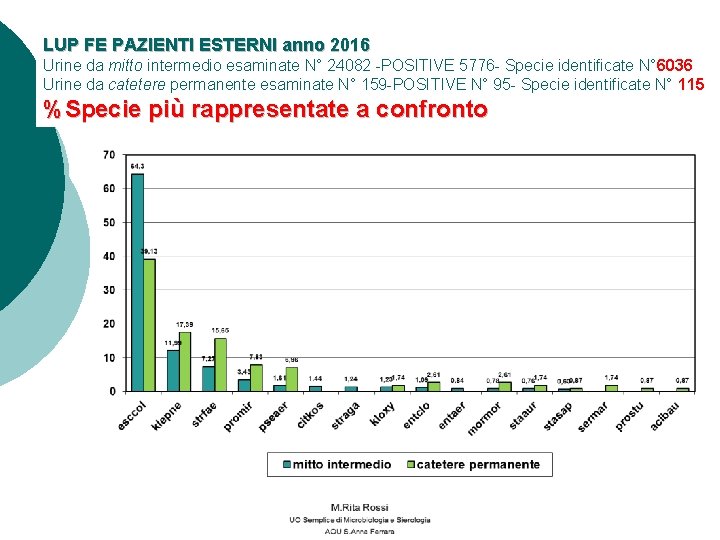
LUP FE PAZIENTI ESTERNI anno 2016 Urine da mitto intermedio esaminate N° 24082 -POSITIVE 5776 - Specie identificate N° 6036 Urine da catetere permanente esaminate N° 159 -POSITIVE N° 95 - Specie identificate N° 115 %Specie più rappresentate a confronto

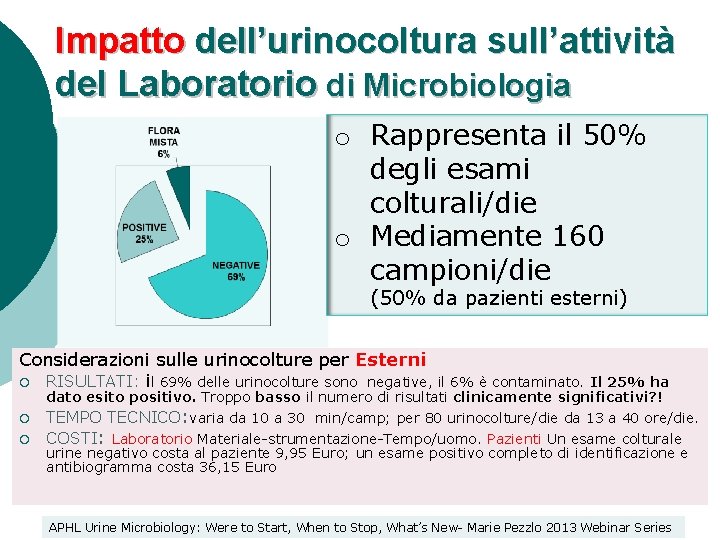
Impatto dell’urinocoltura sull’attività del Laboratorio di Microbiologia o Rappresenta il 50% degli esami colturali/die o Mediamente 160 campioni/die (50% da pazienti esterni) Considerazioni sulle urinocolture per Esterni ¡ RISULTATI: il 69% delle urinocolture sono negative, il 6% è contaminato. ¡ ¡ Il 25% ha dato esito positivo. Troppo basso il numero di risultati clinicamente significativi? ! TEMPO TECNICO: varia da 10 a 30 min/camp; per 80 urinocolture/die da 13 a 40 ore/die. COSTI: Laboratorio Materiale-strumentazione-Tempo/uomo. Pazienti Un esame colturale urine negativo costa al paziente 9, 95 Euro; un esame positivo completo di identificazione e antibiogramma costa 36, 15 Euro APHL Urine Microbiology: Were to Start, When to Stop, What’s New- Marie Pezzlo 2013 Webinar Series

Quando è indicata l’urinocoltura? La coltura trova indicazione: ¡In tutti casi di infezione del tratto urinario superiore e nelle infezioni complicate l l l perché la diagnosi può essere difficile l’eziologia microbica è diversa la resistenza antimicrobica più comune ¡Se non si osserva miglioramento clinico entro 48 ore o in caso di recidiva ¡Se i dati epidemiologici locali dimostrano un tasso di resistenza >20% per gli antibiotici di prima linea Management of suspected bacterial urinary tract infection in adults. Edinburgh: SIGN; 2012. (SIGN publication no. 88). [July 2012].

Premessa ai dati di sensibilità Società Italiana Multidisciplinare per la Prevenzione delle Infezioni nelle Organizzazioni Sanitarie M. Sarti L’antibiotico giusto al momento giusto. 8 marzo 2011 Baggiovara MO

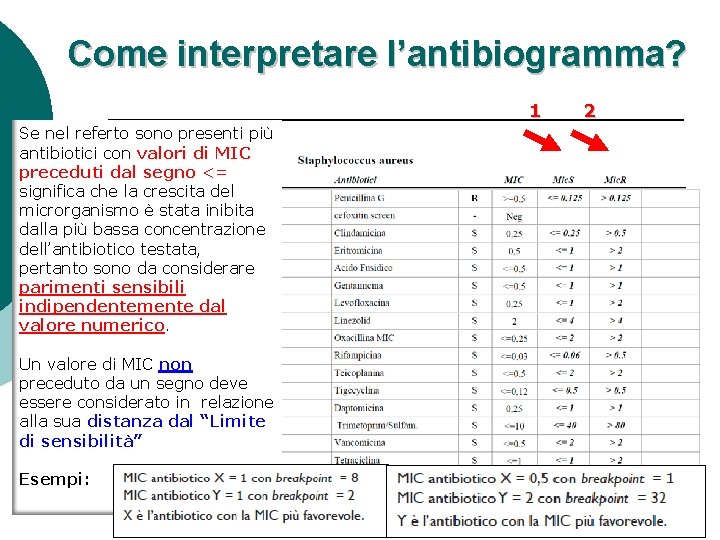
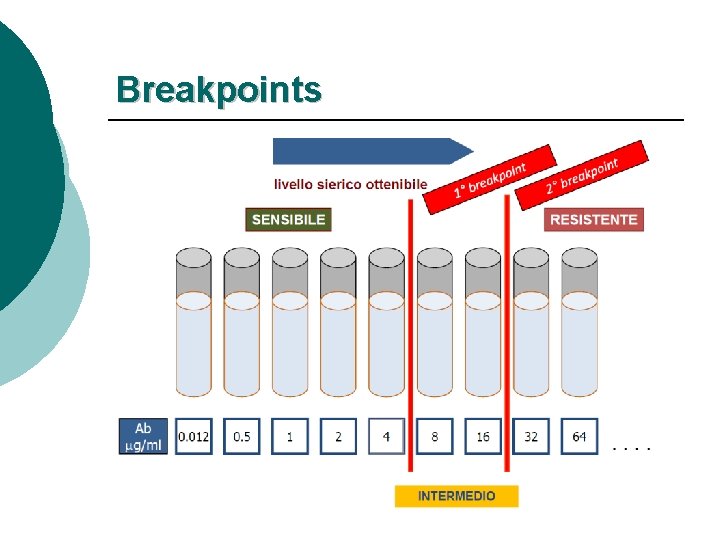
Come interpretare l’antibiogramma? 1 Se nel referto sono presenti più antibiotici con valori di MIC preceduti dal segno <= significa che la crescita del microrganismo è stata inibita dalla più bassa concentrazione dell’antibiotico testata, pertanto sono da considerare parimenti sensibili indipendentemente dal valore numerico. Un valore di MIC non preceduto da un segno deve essere considerato in relazione alla sua distanza dal “Limite di sensibilità” Esempi: 2

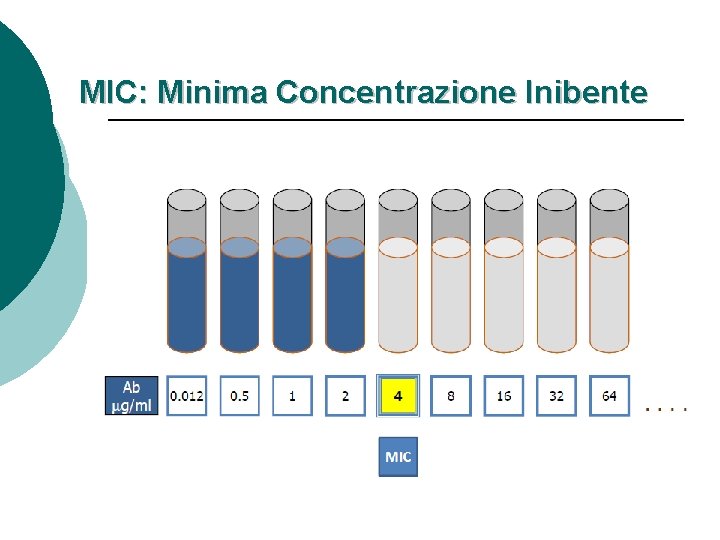
MIC: Minima Concentrazione Inibente

Breakpoints

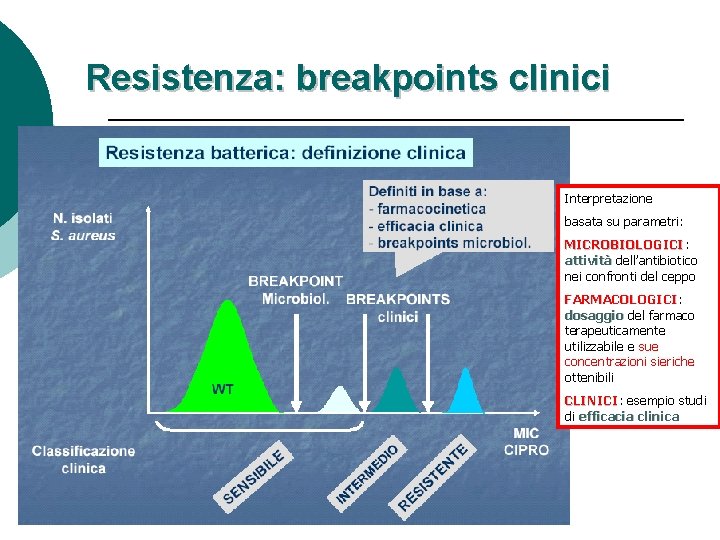
Resistenza: breakpoints clinici Interpretazione basata su parametri: MICROBIOLOGICI attività dell’antibiotico nei confronti del ceppo FARMACOLOGICI: FARMACOLOGICI dosaggio del farmaco terapeuticamente utilizzabile e sue concentrazioni sieriche ottenibili CLINICI: CLINICI esempio studi di efficacia clinica

EUCAST S= sensibile, il livello di attività dell’antibiotico nei confronti del microrganismo è associato ad una elevata probabilità di successo terapeutico R= resistente, il livello di attività dell’antibiotico nei confronti del microrganismo è associato ad una elevata probabilità di fallimento terapeutico I=intermedio, il livello di attività dell’antibiotico nei confronti del microrganismo è associato ad un effetto terapeutico incerto. Non è escluso che l’infezione possa essere trattata appropriatamente in distretti corporei in cui il farmaco è attivamente concentrato o utilizzando alti dosaggi

La correlazione tra categorie S/I/R e clinica non è assoluta ma dipende da : 1. Effettivo ruolo clinico del microrganismo esaminato 2. Sede dell’infezione e possibilità del farmaco di raggiungerla in concentrazione adeguata 3. Caratteristiche fisiopatologiche del paziente che deve essere trattato 4. Corretto dosaggio e corretta modalità e tempistica di somministrazione anche in relazione alle caratteristiche farmacocinetiche e farmacodinamiche delle molecole

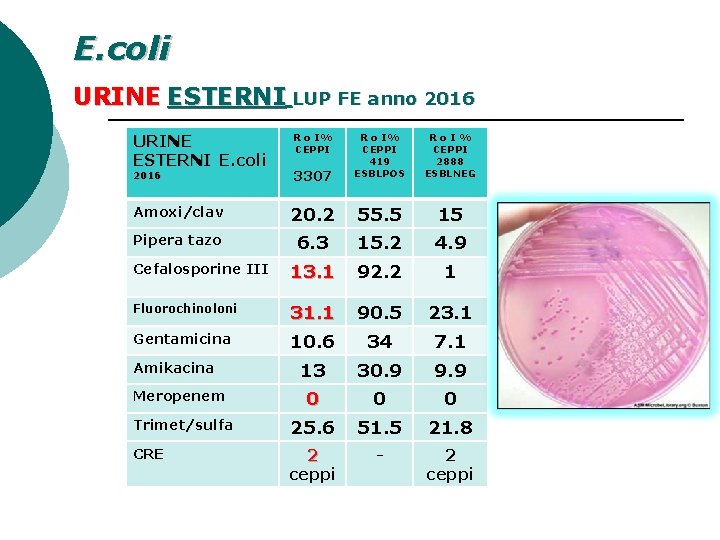
E. coli URINE ESTERNI LUP FE anno 2016 URINE ESTERNI E. coli 2016 3307 R o I% CEPPI 419 ESBLPOS Amoxi/clav 20. 2 55. 5 15 Pipera tazo 6. 3 15. 2 4. 9 Cefalosporine III 13. 1 92. 2 1 Fluorochinoloni 31. 1 90. 5 23. 1 Gentamicina 10. 6 34 7. 1 13 30. 9 9. 9 Meropenem 0 0 0 Trimet/sulfa 25. 6 51. 5 21. 8 CRE 2 ceppi - 2 ceppi Amikacina R o I% CEPPI Ro. I% CEPPI 2888 ESBLNEG

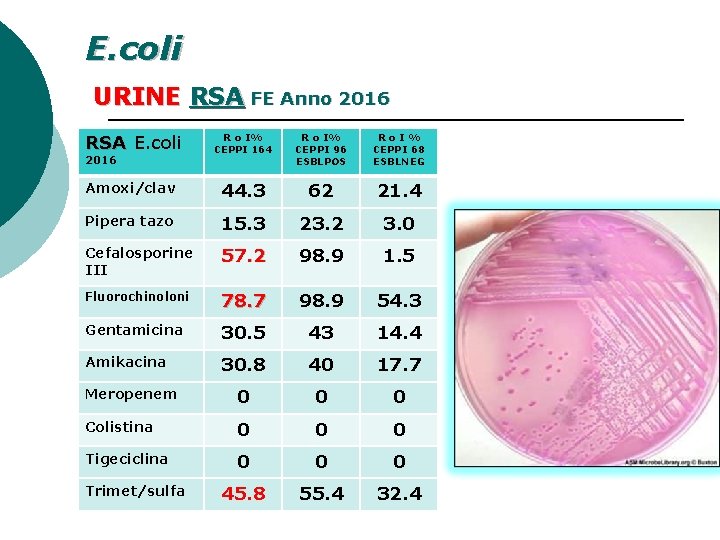
E. coli URINE RSA FE Anno 2016 RSA E. coli R o I% CEPPI 164 R o I% CEPPI 96 ESBLPOS Ro. I% CEPPI 68 ESBLNEG Amoxi/clav 44. 3 62 21. 4 Pipera tazo 15. 3 23. 2 3. 0 Cefalosporine III 57. 2 98. 9 1. 5 Fluorochinoloni 78. 7 98. 9 54. 3 Gentamicina 30. 5 43 14. 4 Amikacina 30. 8 40 17. 7 Meropenem 0 0 0 Colistina 0 0 0 Tigeciclina 0 0 0 45. 8 55. 4 32. 4 2016 Trimet/sulfa

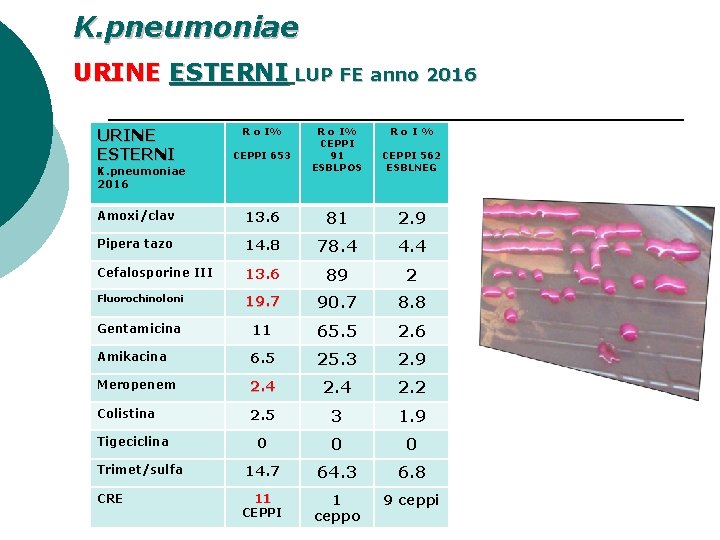
K. pneumoniae URINE ESTERNI LUP FE anno 2016 URINE ESTERNI CEPPI 653 Amoxi/clav R o I% CEPPI 91 ESBLPOS CEPPI 562 ESBLNEG 13. 6 81 2. 9 Pipera tazo 14. 8 78. 4 4. 4 Cefalosporine III 13. 6 89 2 Fluorochinoloni 19. 7 90. 7 8. 8 Gentamicina 11 65. 5 2. 6 Amikacina 6. 5 25. 3 2. 9 Meropenem 2. 4 2. 2 Colistina 2. 5 3 1. 9 0 0 0 Trimet/sulfa 14. 7 64. 3 6. 8 CRE 11 CEPPI 1 ceppo 9 ceppi K. pneumoniae 2016 Tigeciclina Ro. I%

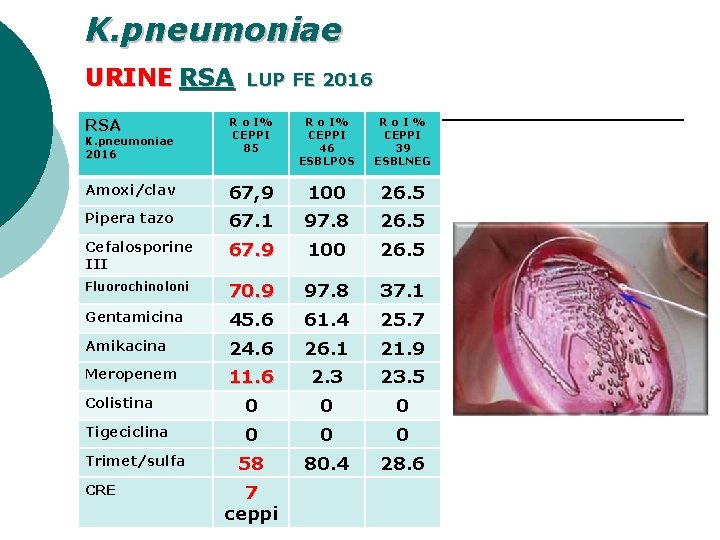
K. pneumoniae URINE RSA LUP FE 2016 RSA R o I% CEPPI 85 R o I% CEPPI 46 ESBLPOS Ro. I% CEPPI 39 ESBLNEG Amoxi/clav 67, 9 100 26. 5 Pipera tazo 67. 1 97. 8 26. 5 Cefalosporine III 67. 9 100 26. 5 Fluorochinoloni 70. 9 97. 8 37. 1 Gentamicina 45. 6 61. 4 25. 7 Amikacina 24. 6 26. 1 21. 9 Meropenem 11. 6 2. 3 23. 5 Colistina 0 0 0 Tigeciclina 0 0 0 58 80. 4 28. 6 K. pneumoniae 2016 Trimet/sulfa CRE 7 ceppi

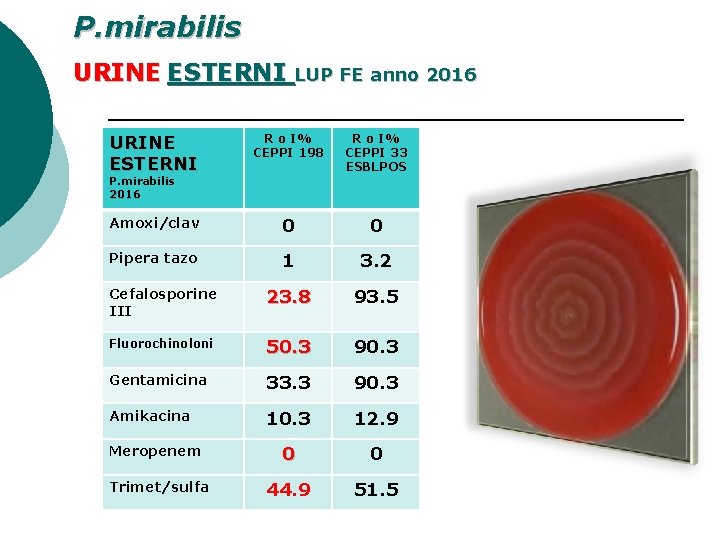
P. mirabilis URINE ESTERNI LUP FE anno 2016 URINE ESTERNI R o I% CEPPI 198 R o I% CEPPI 33 ESBLPOS Amoxi/clav 0 0 Pipera tazo 1 3. 2 Cefalosporine III 23. 8 93. 5 Fluorochinoloni 50. 3 90. 3 Gentamicina 33. 3 90. 3 Amikacina 10. 3 12. 9 Meropenem 0 0 Trimet/sulfa 44. 9 51. 5 P. mirabilis 2016

P. mirabilis URINE RSA LUP FE ANNO 2016 RSA Proteus mirabilis R o I% CEPPI 62 R o I% CEPPI 21 ESBLPOS Amoxi/clav 8. 1 0 Pipera tazo 0 0 57. 4 100 Fluorochinoloni 87 100 Gentamicina 57. 4 88 8. 1 4 Meropenem 0 0 Trimet/sulfa 41 28 2016 Cefalosporine III Amikacina

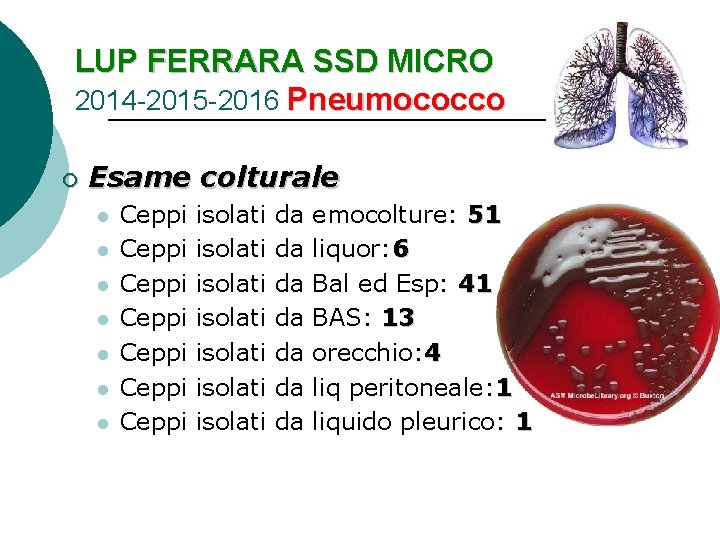
LUP FERRARA SSD MICRO 2014 -2015 -2016 Pneumococco ¡ Esame colturale l l l l Ceppi Ceppi isolati isolati da da emocolture: 51 liquor: 6 Bal ed Esp: 41 BAS: 13 orecchio: 4 liq peritoneale: 1 liquido pleurico: 1

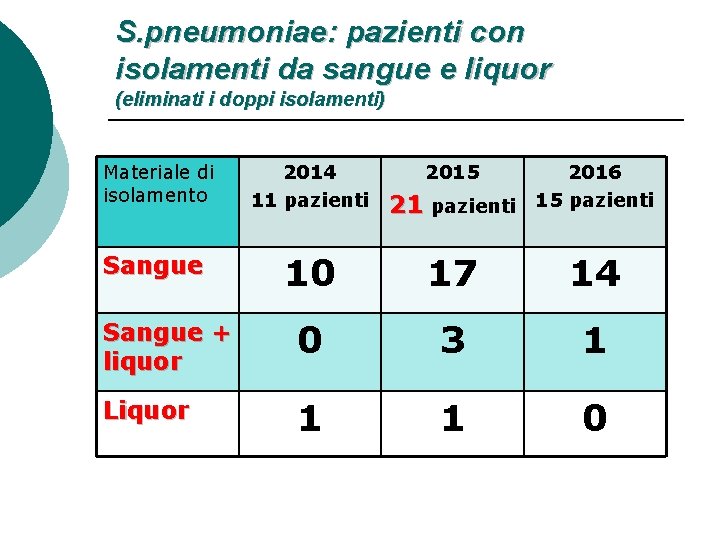
S. pneumoniae: pazienti con isolamenti da sangue e liquor (eliminati i doppi isolamenti) Materiale di isolamento 2014 11 pazienti 2015 Sangue 10 17 14 Sangue + liquor 0 3 1 Liquor 1 1 0 21 pazienti 2016 15 pazienti

Binax. NOW ®Streptococcus pneumoniae Tipo di campione: urine, liquido cerebrospinale ¡ Tempi di attesa per il risultato: 15 minuti ¡ Dati sulle prestazioni: ¡ l l Sensibilità/Specificità urine: 86% / 94% Sensibilità/Specificità liquido cerebrospinale: 97% / 99% LUP FE Anni 2014 -2015 -2016 Ricerca antigene urinario S. pneumoniae pazienti positivi: 168/4179 (4%) 168 4%

S. pneumoniae LUP FE 2014 -2015 -2016 LUP FE S. pneumoniae Esp bal sangue lcr Penicillina Io. R% 2014 -2015 58 pazienti Io. R% 2016 30 pazienti 16 (10 I+ 6 R) 6. 6 (1 I+ 1 R) Eritromicina 23 32 Ceftriaxone 4 3. 3 Levofloxacina 2 6. 6 13 3. 3 Trimet/sulfa

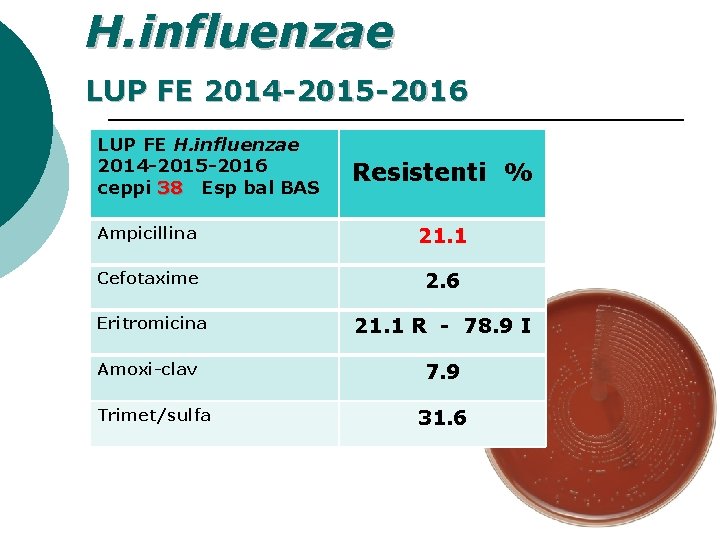
H. influenzae LUP FE 2014 -2015 -2016 LUP FE H. influenzae 2014 -2015 -2016 ceppi 38 Esp bal BAS Resistenti % Ampicillina 21. 1 Cefotaxime 2. 6 Eritromicina 21. 1 R - 78. 9 I Amoxi-clav Trimet/sulfa 7. 9 31. 6

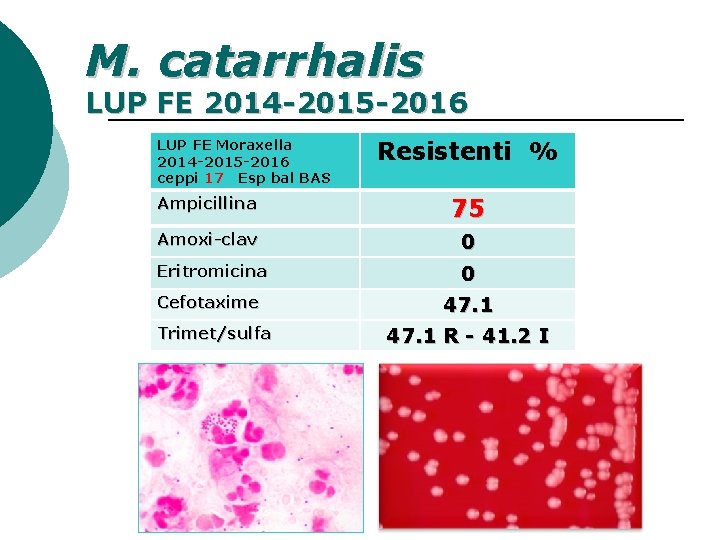
M. catarrhalis LUP FE 2014 -2015 -2016 LUP FE Moraxella 2014 -2015 -2016 ceppi 17 Esp bal BAS Resistenti % Ampicillina 75 Amoxi-clav 0 Eritromicina 0 Cefotaxime 47. 1 Trimet/sulfa 47. 1 R - 41. 2 I

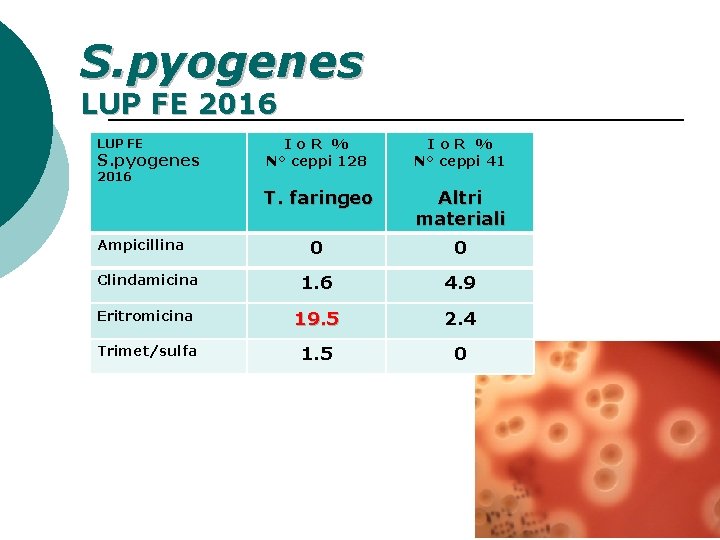
S. pyogenes LUP FE 2016 Io. R % N° ceppi 128 Io. R % N° ceppi 41 T. faringeo Altri materiali 0 0 Clindamicina 1. 6 4. 9 Eritromicina 19. 5 2. 4 Trimet/sulfa 1. 5 0 LUP FE S. pyogenes 2016 Ampicillina

Antigene urinario Legionella Binax. NOW® ¡ Test immunocromatografico validato solo su urine ¡ Rileva un antigene solubile di natura lipopolisaccaridica di Legionella pneumophila sierogruppo 1 L’antigene è rilevabile dopo 3 giorni dalla comparsa dei sintomi e può persistere fino a un anno ¡ ¡ ( fresche o conservate a +2 -8°C per 14 giorni o a – 20°C periodi prolungati) Sensibilità = 95% Specificità = 95% Accuratezza = 95% LUP FE Anni 2014 -2015 -2016 Ricerca antigene urinario Legionella 43/3873 (1, 11%) pazienti indagati positivi 43

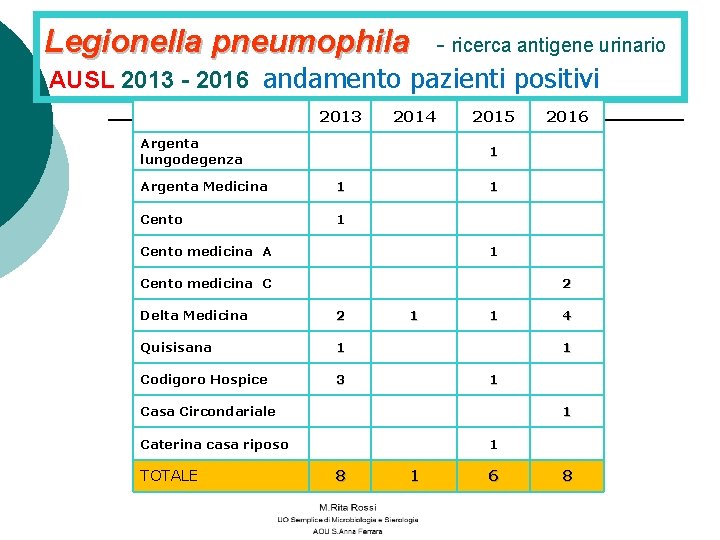
Legionella pneumophila - ricerca antigene urinario AUSL 2013 - 2016 andamento pazienti positivi 2013 2014 Argenta lungodegenza 2015 1 Argenta Medicina 1 Cento 1 1 Cento medicina A 1 Cento medicina C 2 Delta Medicina 2 Quisisana 1 Codigoro Hospice 3 1 1 4 1 1 Casa Circondariale 1 Caterina casa riposo TOTALE 2016 1 8 1 6 8

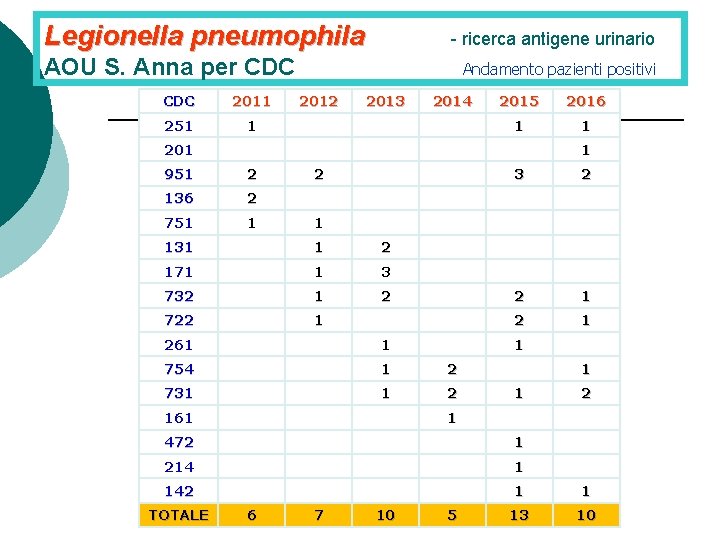
Legionella pneumophila - ricerca antigene urinario AOU S. Anna per CDC 2011 251 1 Andamento pazienti positivi 2012 2013 2014 2015 2016 1 1 201 1 951 2 136 2 751 1 2 3 2 2 1 1 131 1 2 171 1 3 732 1 2 722 1 261 1 754 1 2 731 1 2 161 1 2 1 472 1 214 1 142 1 1 13 10 TOTALE 6 7 10 5

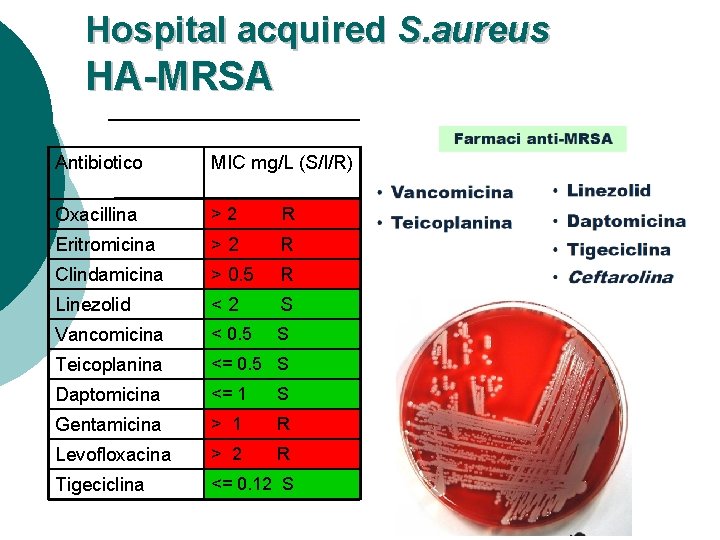
Hospital acquired S. aureus HA-MRSA Antibiotico MIC mg/L (S/I/R) Oxacillina >2 R Eritromicina >2 R Clindamicina > 0. 5 R Linezolid <2 S Vancomicina < 0. 5 S Teicoplanina <= 0. 5 S Daptomicina <= 1 S Gentamicina > 1 R Levofloxacina > 2 R Tigeciclina <= 0. 12 S

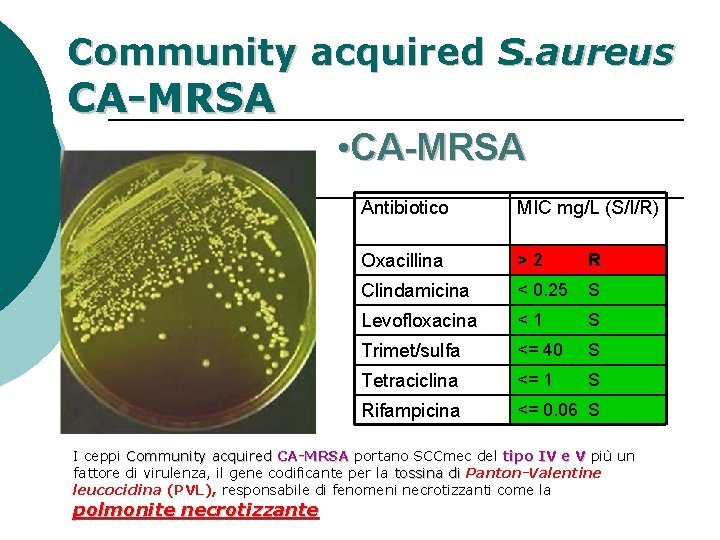
Community acquired S. aureus CA-MRSA • CA-MRSA Antibiotico MIC mg/L (S/I/R) Oxacillina >2 R Clindamicina < 0. 25 S Levofloxacina <1 S Trimet/sulfa <= 40 S Tetraciclina <= 1 S Rifampicina <= 0. 06 S I ceppi Community acquired CA-MRSA portano SCCmec del tipo IV e V più un fattore di virulenza, il gene codificante per la tossina di Panton-Valentine leucocidina (PVL), responsabile di fenomeni necrotizzanti come la polmonite necrotizzante

Community acquired S. aureus CA-MRSA Nel 2016 individuati in base al fenotipo dell’antibiogramma • N° 1 ceppo tra gli esterni • N° 7 ceppi tra i ricoverati • CA-MRSA Antibiotico MIC mg/L (S/I/R) Oxacillina >2 R Clindamicina < 0. 25 S Levofloxacina < 1 S Trimet/sulfa <= 40 S Tetraciclina <= 1 S Rifampicina <= 0. 06 S

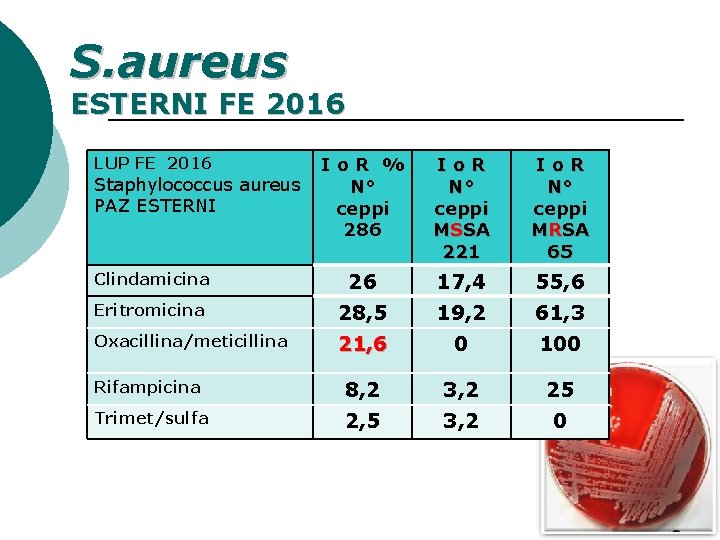
S. aureus ESTERNI FE 2016 LUP FE 2016 Io. R % N° ceppi 286 Io. R N° ceppi MSSA 221 Io. R N° ceppi MRSA 65 Clindamicina 26 17, 4 55, 6 Eritromicina 28, 5 19, 2 61, 3 Oxacillina/meticillina 21, 6 0 100 Rifampicina 8, 2 3, 2 25 Trimet/sulfa 2, 5 3, 2 0 Staphylococcus aureus PAZ ESTERNI

Clostridium difficile La terapia antibiotica, soprattutto se qcombinata e/o protratta qeffettuata con farmaci ad ampio spettro d’azione, che riduce la resistenza alla colonizzazione da C. difficile alterano la normale flora batterica intestinale SIMPIOS Prevenzione e controllo delle infezioni da Clostridium difficile GIIO, vol. 16, n. 1, Gennaio-Marzo 2009

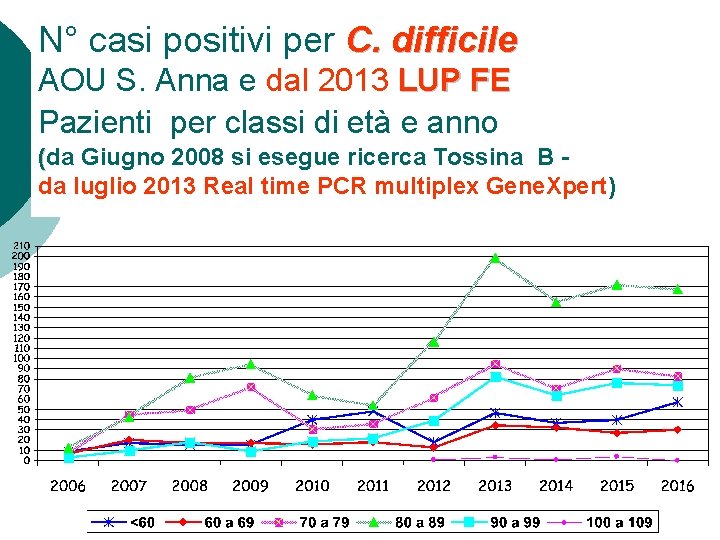
N° casi positivi per C. difficile AOU S. Anna e dal 2013 LUP FE Pazienti per classi di età e anno (da Giugno 2008 si esegue ricerca Tossina B da luglio 2013 Real time PCR multiplex Gene. Xpert)

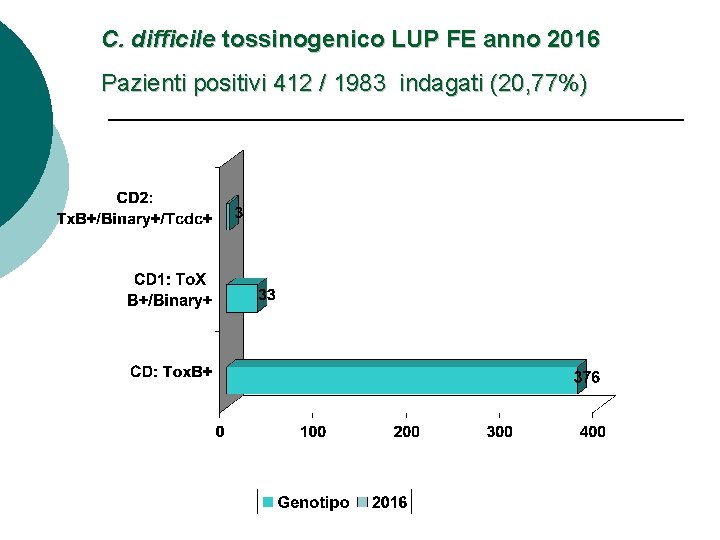
C. difficile tossinogenico LUP FE anno 2016 Pazienti positivi 412 / 1983 indagati (20, 77%)

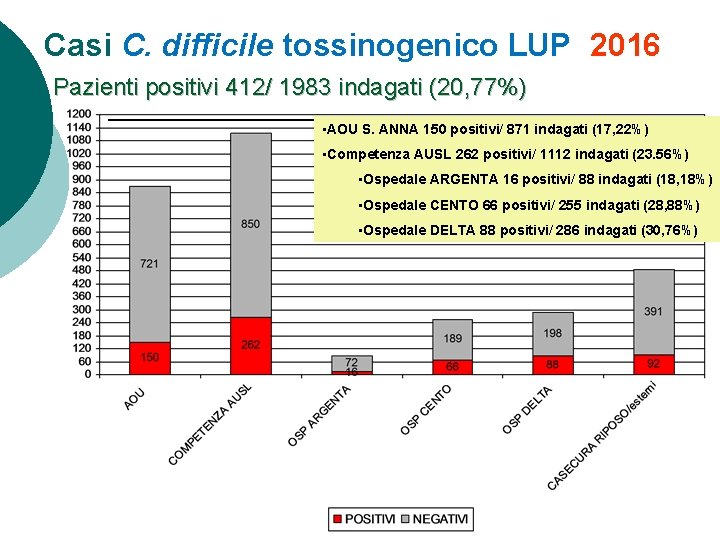
Casi C. difficile tossinogenico LUP 2016 Pazienti positivi 412/ 1983 indagati (20, 77%) • AOU S. ANNA 150 positivi/ 871 indagati (17, 22%) • Competenza AUSL 262 positivi/ 1112 indagati (23. 56%) • Ospedale ARGENTA 16 positivi/ 88 indagati (18, 18%) • Ospedale CENTO 66 positivi/ 255 indagati (28, 88%) • Ospedale DELTA 88 positivi/ 286 indagati (30, 76%)

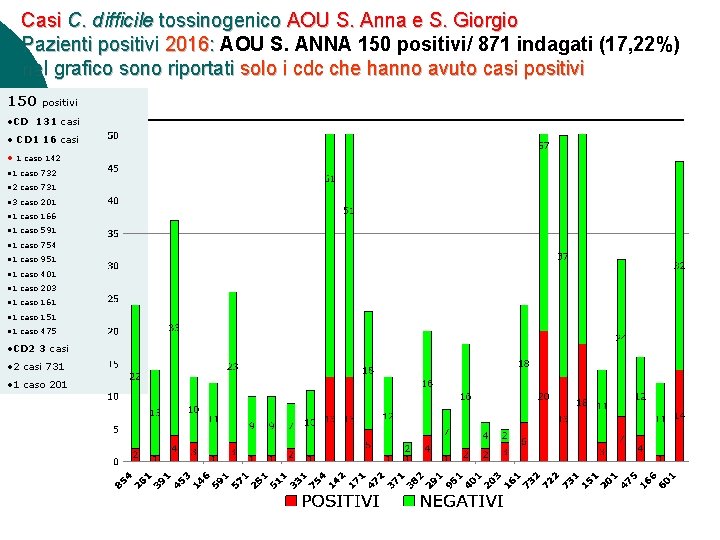
Casi C. difficile tossinogenico AOU S. Anna e S. Giorgio Pazienti positivi 2016: AOU S. ANNA 150 positivi/ 871 indagati (17, 22%) nel grafico sono riportati solo i cdc che hanno avuto casi positivi 150 positivi • CD 131 casi • CD 1 16 casi • 1 caso 142 • 1 caso 732 • 2 caso 731 • 3 caso 201 • 1 caso 166 • 1 caso 591 • 1 caso 754 • 1 caso 951 • 1 caso 401 • 1 caso 203 • 1 caso 161 • 1 caso 151 • 1 caso 475 • CD 2 3 casi • 2 casi 731 • 1 caso 201

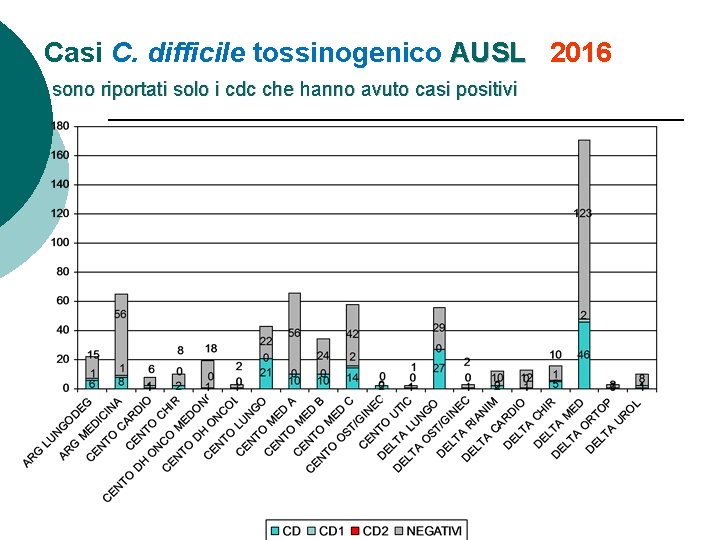
Casi C. difficile tossinogenico AUSL 2016 sono riportati solo i cdc che hanno avuto casi positivi

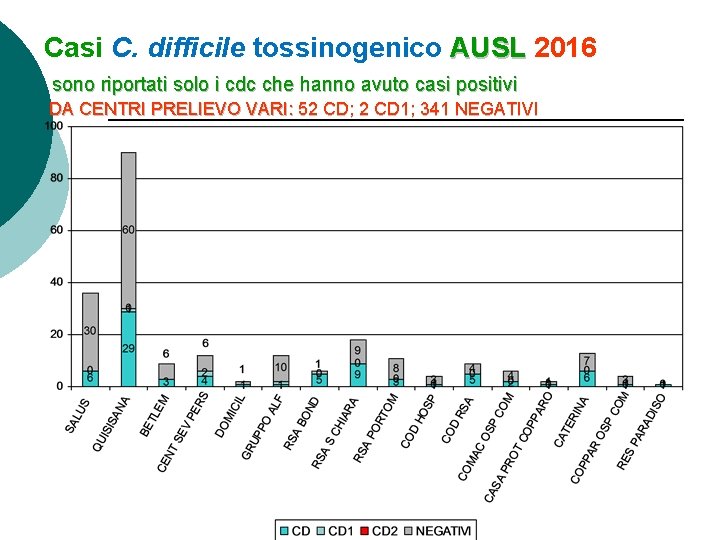
Casi C. difficile tossinogenico AUSL 2016 sono riportati solo i cdc che hanno avuto casi positivi DA CENTRI PRELIEVO VARI: 52 CD; 2 CD 1; 341 NEGATIVI

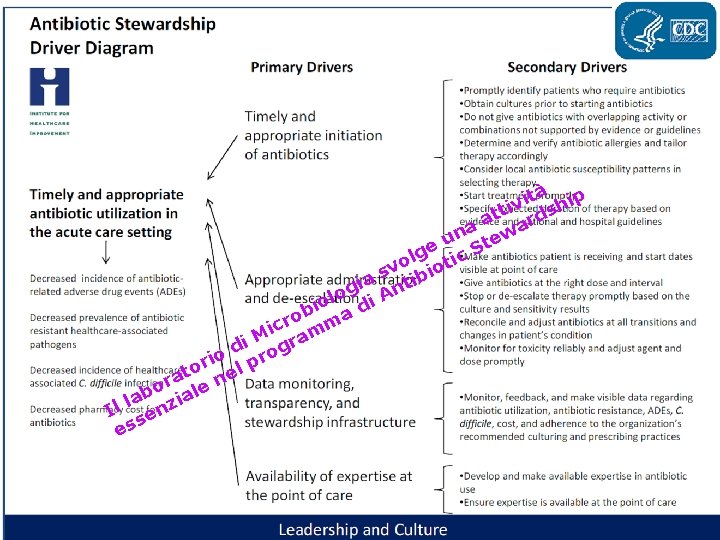
tà ip i v tti rdsh a na ewa u e c St g l vo ioti s ia ntib g lo i A o i d b a o r ic mm M i ra d g o rio l pr o at ne r bo iale a l Il senz es

Grazie a tutti per l’attenzione!

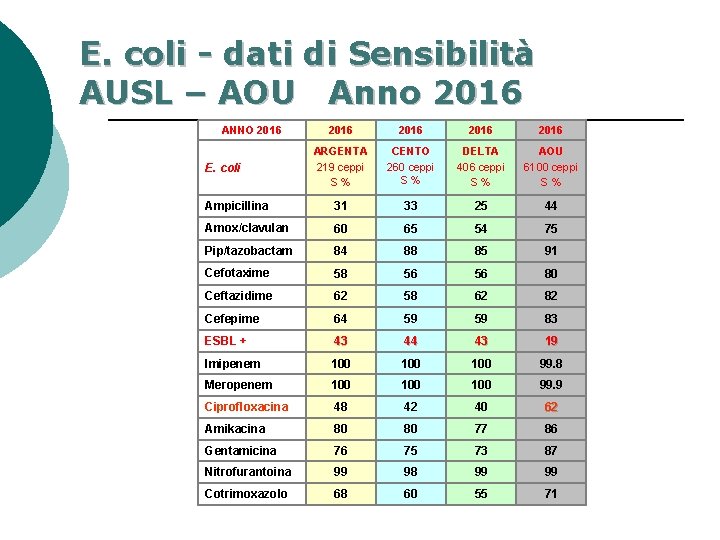
E. coli - dati di Sensibilità AUSL – AOU Anno 2016 ANNO 2016 2016 ARGENTA 219 ceppi S% CENTO 260 ceppi S% DELTA 406 ceppi S% AOU 6100 ceppi S% Ampicillina 31 33 25 44 Amox/clavulan 60 65 54 75 Pip/tazobactam 84 88 85 91 Cefotaxime 58 56 56 80 Ceftazidime 62 58 62 82 Cefepime 64 59 59 83 ESBL + 43 44 43 19 Imipenem 100 100 99. 8 Meropenem 100 100 99. 9 Ciprofloxacina 48 42 40 62 Amikacina 80 80 77 86 Gentamicina 76 75 73 87 Nitrofurantoina 99 98 99 99 Cotrimoxazolo 68 60 55 71 E. coli

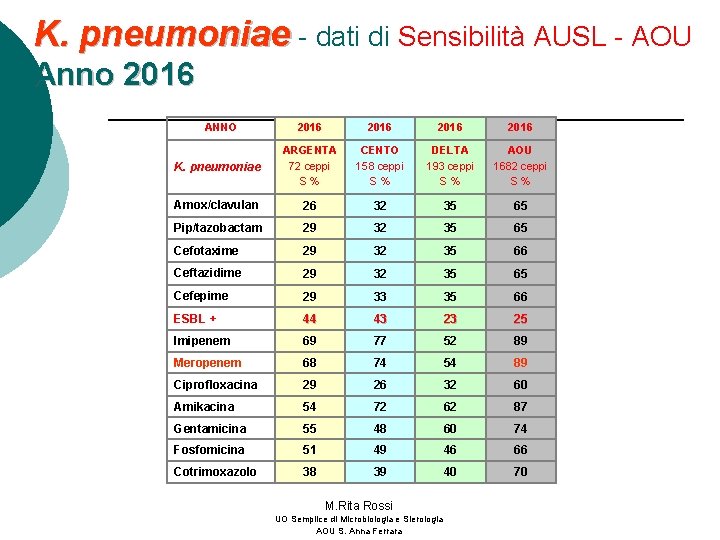
K. pneumoniae - dati di Sensibilità AUSL - AOU Anno 2016 ANNO 2016 K. pneumoniae ARGENTA 72 ceppi S% CENTO 158 ceppi S% DELTA 193 ceppi S% AOU 1682 ceppi S% Amox/clavulan 26 32 35 65 Pip/tazobactam 29 32 35 65 Cefotaxime 29 32 35 66 Ceftazidime 29 32 35 65 Cefepime 29 33 35 66 ESBL + 44 43 23 25 Imipenem 69 77 52 89 Meropenem 68 74 54 89 Ciprofloxacina 29 26 32 60 Amikacina 54 72 62 87 Gentamicina 55 48 60 74 Fosfomicina 51 49 46 66 Cotrimoxazolo 38 39 40 70 M. Rita Rossi UO Semplice di Microbiologia e Sierologia AOU S. Anna Ferrara

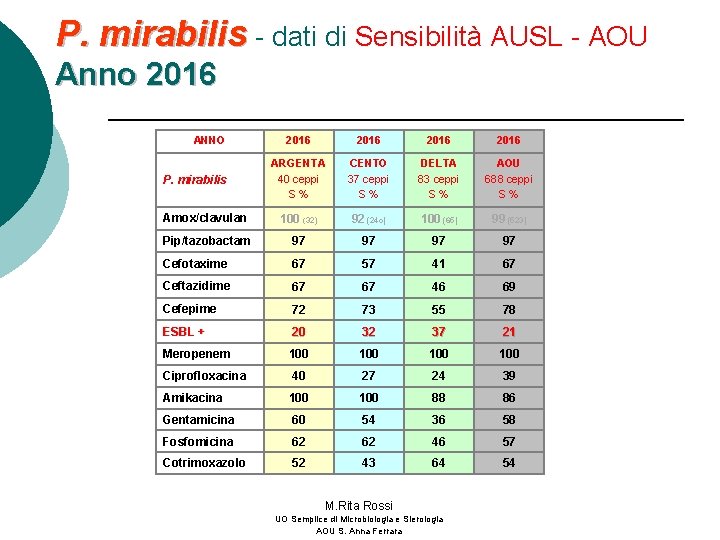
P. mirabilis - dati di Sensibilità AUSL - AOU Anno 2016 ANNO 2016 ARGENTA 40 ceppi S% CENTO 37 ceppi S% DELTA 83 ceppi S% AOU 688 ceppi S% Amox/clavulan 100 (32) 92 (24 c) 100 (65) 99 (523) Pip/tazobactam 97 97 Cefotaxime 67 57 41 67 Ceftazidime 67 67 46 69 Cefepime 72 73 55 78 ESBL + 20 32 37 21 Meropenem 100 100 Ciprofloxacina 40 27 24 39 Amikacina 100 88 86 Gentamicina 60 54 36 58 Fosfomicina 62 62 46 57 Cotrimoxazolo 52 43 64 54 P. mirabilis M. Rita Rossi UO Semplice di Microbiologia e Sierologia AOU S. Anna Ferrara