Conducibilit elettrica in soluzioni elettrolitiche Esperimenti con sostanze

Conducibilità elettrica in soluzioni elettrolitiche Esperimenti con sostanze varie isolate , unite, in soluzione Distinzione tra sostanze conduttrici e isolanti tra soluzioni conduttrici e non conduttrici distinzione tra elettroliti(sali, acidi, basi) e non elettroliti Leggi della conducibilità in soluzioni elettrolitiche ipotesi sulle cause del fenomeno e interpretazione
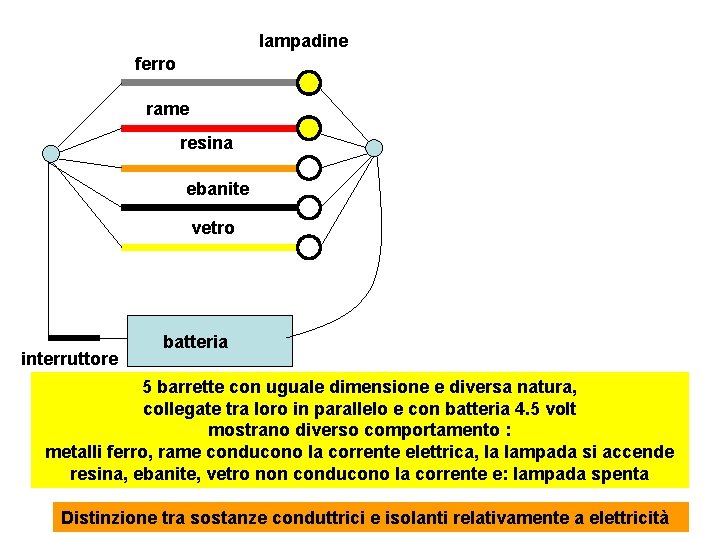
lampadine ferro rame resina ebanite vetro interruttore batteria 5 barrette con uguale dimensione e diversa natura, collegate tra loro in parallelo e con batteria 4. 5 volt mostrano diverso comportamento : metalli ferro, rame conducono la corrente elettrica, la lampada si accende resina, ebanite, vetro non conducono la corrente e: lampada spenta Distinzione tra sostanze conduttrici e isolanti relativamente a elettricità
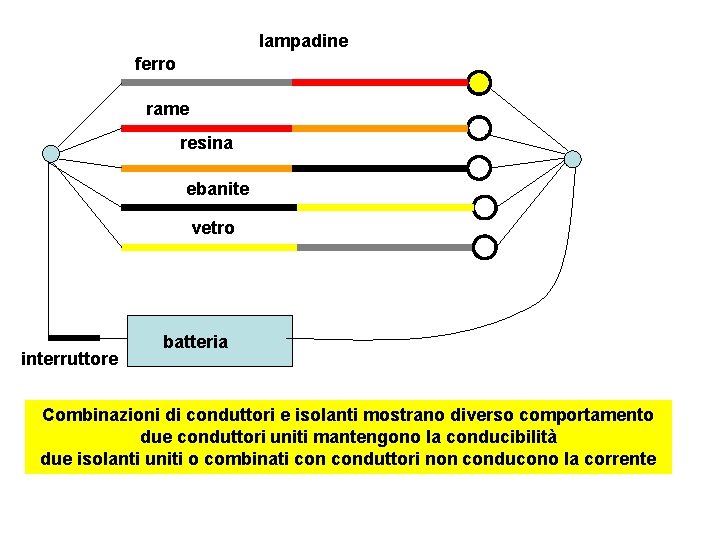
lampadine ferro rame resina ebanite vetro interruttore batteria Combinazioni di conduttori e isolanti mostrano diverso comportamento due conduttori uniti mantengono la conducibilità due isolanti uniti o combinati conduttori non conducono la corrente
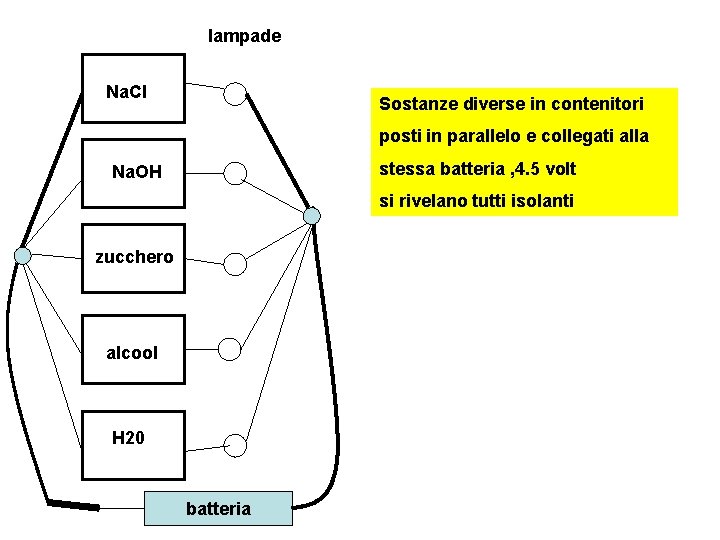
lampade Na. Cl Sostanze diverse in contenitori posti in parallelo e collegati alla stessa batteria , 4. 5 volt Na. OH si rivelano tutti isolanti zucchero alcool H 20 batteria
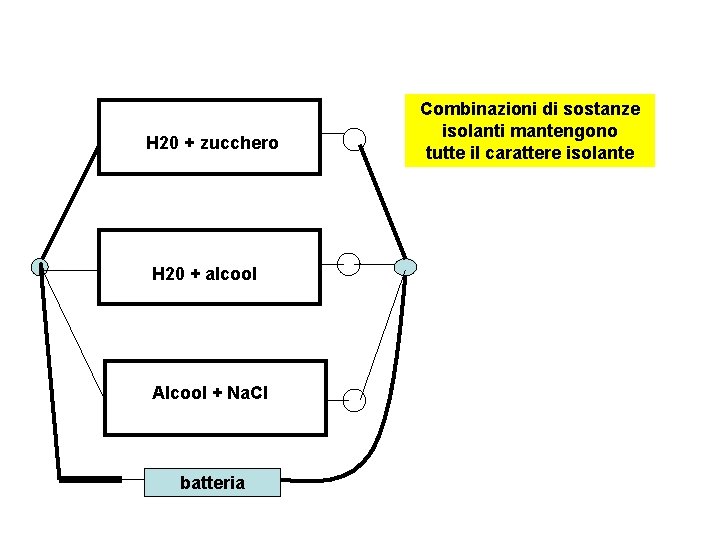
H 20 + zucchero H 20 + alcool Alcool + Na. Cl batteria Combinazioni di sostanze isolanti mantengono tutte il carattere isolante
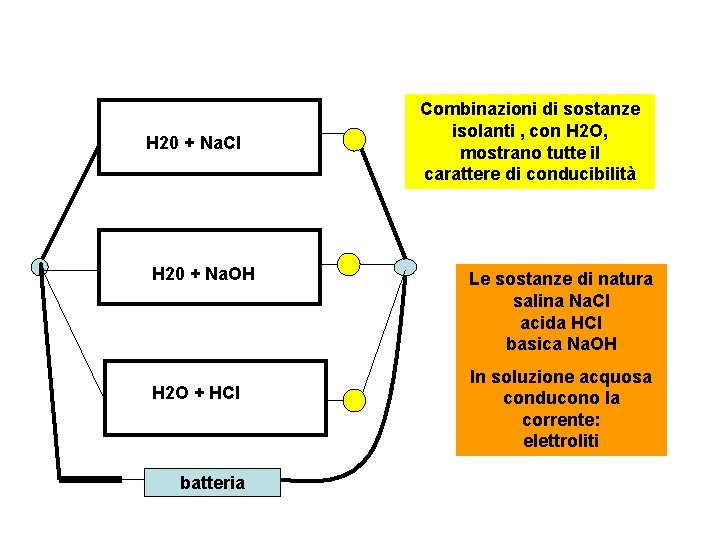
H 20 + Na. Cl H 20 + Na. OH H 2 O + HCl batteria Combinazioni di sostanze isolanti , con H 2 O, mostrano tutte il carattere di conducibilità Le sostanze di natura salina Na. Cl acida HCl basica Na. OH In soluzione acquosa conducono la corrente: elettroliti
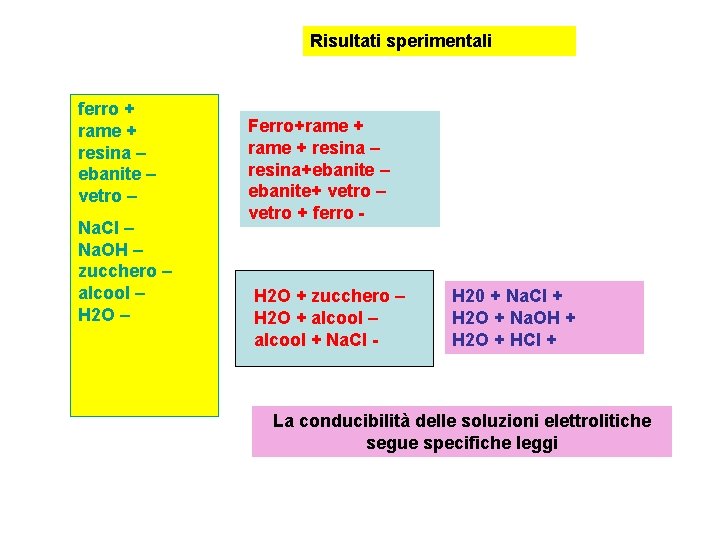
Risultati sperimentali ferro + rame + resina – ebanite – vetro – Na. Cl – Na. OH – zucchero – alcool – H 2 O – Ferro+rame + resina – resina+ebanite – ebanite+ vetro – vetro + ferro - H 2 O + zucchero – H 2 O + alcool – alcool + Na. Cl - H 20 + Na. Cl + H 2 O + Na. OH + H 2 O + HCl + La conducibilità delle soluzioni elettrolitiche segue specifiche leggi
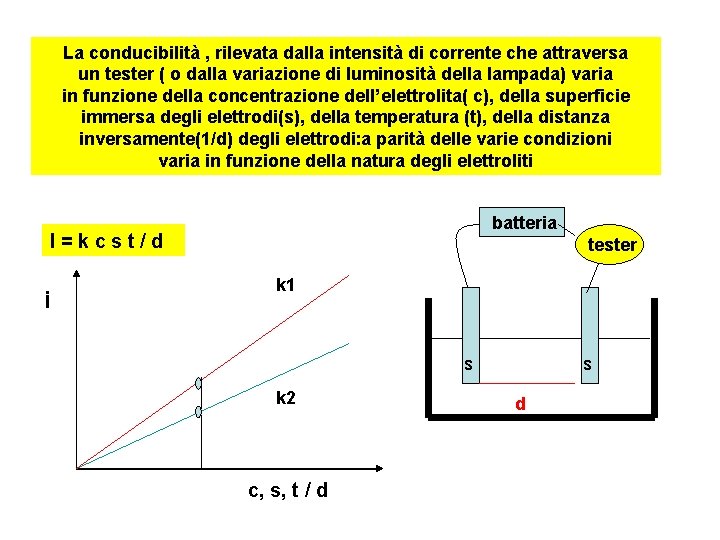
La conducibilità , rilevata dalla intensità di corrente che attraversa un tester ( o dalla variazione di luminosità della lampada) varia in funzione della concentrazione dell’elettrolita( c), della superficie immersa degli elettrodi(s), della temperatura (t), della distanza inversamente(1/d) degli elettrodi: a parità delle varie condizioni varia in funzione della natura degli elettroliti batteria I=kcst/d i tester k 1 s k 2 c, s, t / d s d
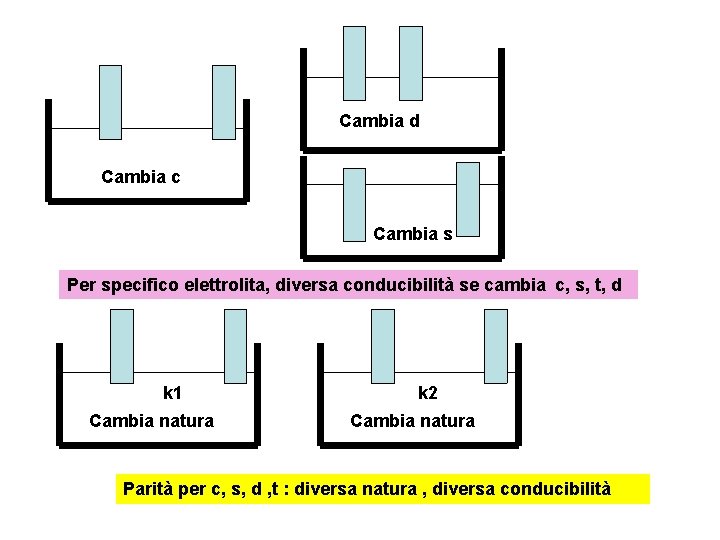
Cambia d Cambia c Cambia s Per specifico elettrolita, diversa conducibilità se cambia c, s, t, d k 1 Cambia natura k 2 Cambia natura Parità per c, s, d , t : diversa natura , diversa conducibilità

Interpretazione del fenomeno e delle sue leggi Gli elettroliti in soluzione acquosa si dissociano, ionizzano in particelle positive (cationi) e negative(anioni) AB >>>> A+ B Gli ioni migrano verso gli elettrodi : cationi A+ verso il catodo(negativo - ) anioni B- verso l’anodo(positivo +) I cationi ricevono elettroni dal catodo A+ + e- A° (riducendosi) gli anioni cedono elettroni all’anodo B- - e- B°(ossidandosi) gli elettroni e- , attraverso la batteria vengono riportati al catodo e mostrano il loro passaggio attraverso il tester o la lampada A+B- >>>>> A+ B- ionizzazione catodo (-) A+ >>>> A° riduzione anodo (+) B- >>>> B° ossidazione
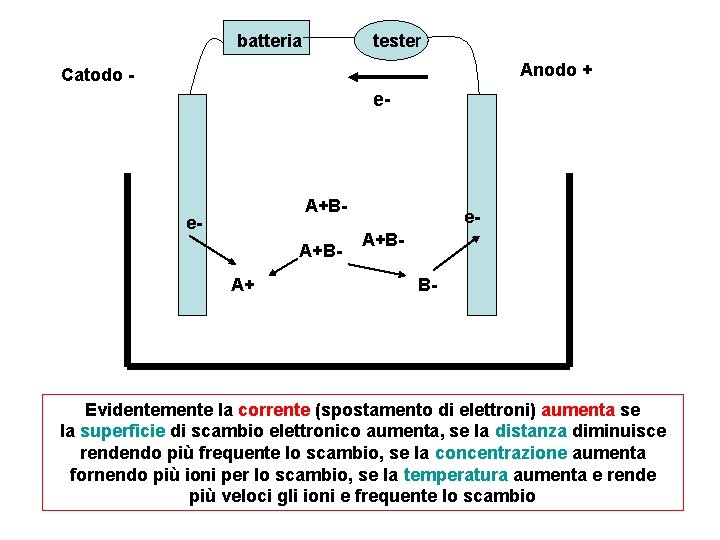
batteria tester Anodo + Catodo - e- A+BA+ e. A+BB- Evidentemente la corrente (spostamento di elettroni) aumenta se la superficie di scambio elettronico aumenta, se la distanza diminuisce rendendo più frequente lo scambio, se la concentrazione aumenta fornendo più ioni per lo scambio, se la temperatura aumenta e rende più veloci gli ioni e frequente lo scambio

Perché varia con la natura degli elettroliti ? Varia con la natura perché una molecola può dissociarsi in numero diverso di ioni, con carica diversa, con dimensioni e difficoltà a spostarsi diversa, può dissociarsi con diverso grado Na. Cl >>>> Na+ Cl due ioni per molecola, carica +1 , -1 Cu. Cl 2 >>>> Cu++ 2 Cl- tre ioni per molecola, carica +2, -1 Al. Cl 3 >>>> Al+++ 3 Cl- quattro ioni per molecola, carica 3+, -1, -1 100 AB >>>> 100 A+ 100 B- : dissociazione 100% 100 moli generano 100 A+ 100 B 100 AC >>>> 60 A+ 60 C- 40 AC : dissociazione 60% 100 moli generano 60 A+ 60 C- 40 AC

Immagini di strumentazione

Ebanite-vetro- resina e ferro- rame-zinco-piombo- alcool-acqua Metalli : rame, ferro, zinco, piombo : isolati o uniti , conduttori ebanite, vetro, resina, alcool, acqua distillata: isolanti ferro-resina : non conduce Metalli : conduttori ebanite, vetro, resina, alcool, acqua distillata: isolanti

Na. OH Na. Cl saccarosio Solidi, non conducono

Soluzioni non conducono H 2 O + alcool H 2 O + saccarosio Alcool+Na. OH Alcool + Na. Cl

Soluzioni elettrolitiche conducono H 2 O + HCl H 2 O + Na. OH

Rivelatore di corrente batteria Soluzione ed elettrodi

Lampada accesa se passa corrente Alimentatore 220 V Soluzione con elettrodi

fine descrizione arrivederci
- Slides: 20