Conceptos previos Cationes y aniones Compuestos binarios Hidruros

Conceptos previos Cationes y aniones Compuestos binarios Hidruros Óxidos Bases o Hidróxidos Ácidos Sales

U 12 |Conceptos previos • En la fórmula de un compuesto binario, el número total de valencias de cada uno de los elementos que se combinan debe ser el mismo. • En una fórmula siempre se cumple que la suma algebraica de los productos de los subíndices de cada elemento por los correspondientes números de oxidación es zero. • La fórmula de un elemento es su símbolo acompañado de un subíndice que indica el número de átomos que forman la unidad estructural. • Los elementos formados por moléculas se denominan con el nombre del elemento añadiéndole delante el prefijo numeral griego correspondiente al número de átomos presentes en la molécula. • Los elementos que forman grandes redes cristalinas, se denominan con el nombre del elemento.

U 12 |Formulación y nomenclatura de los cationes y de los aniones Catión: Átomo o grupo de átomos con carga eléctrica positiva. K+ , Ba 2+ , H 3 O+ , NH 4+. . . La fórmula de un catión monoatómico es el símbolo del elemento, y la de un catión poliatómico los de los átomos que lo constituyen, y se escribe en los dos casos en la parte superior derecha la carga eléctrica que presenta. Los cationes monoatómicos se denominan con la palabra ión o catión seguida del nombre del elemento. Si el elemento puede formar más de un catión, se indica su número de oxidación con números romanos y entre paréntesis. Anión: Átomo o grupo de átomos con carga eléctrica negativa. H- , Cl- , Se 2 - , S 2 -. . . La fórmula de un anión monoatómico es el símbolo del elemento, y la de un anión poliatómico los de los átomos que lo constituyen; y se escribe en los dos casos, en la parte superior derecha, la carga eléctrica que presentan. Los aniones monoatómicos, se denominan con la raíz del nombre del elemento acabado en –uro.

U 12 |Formulación de los compuestos binarios Compuestos binarios: Compuestos formados por combinación de dos elementos químicos diferentes. HCl , CO 2 , PCl 3. . . El peróxido de hidrógeno (H 2 O 2) es una combinación binaria del hidrógeno. Formulación • En primer lugar, se escriben juntos los símbolos de los dos elementos en el orden que da la IUPAC: • Se deben conocer las valencias con las que actúan los dos elementos. • El número total de valencias aportadas por cada uno de los elementos que se combinan debe ser el mismo.

U 12 |Formulación y nomenclatura de los hidruros Hidruros: Combinaciones binarias del hidrógeno con otro elemento. Hidruros de no–metales de carácter ácido: Combinaciones del hidrógeno con los elementos más electronegativos. HF Fluoruro de hidrógeno HCl Cloruro de hidrógeno H 2 S Sulfuro de hidrógeno H 2 Te Telururo de hidrógeno Otros hidruros de no-metales: Combinaciones del hidrógeno con otros nometales. H 2 O Agua CH 4 Metano NH 3 Amoníaco PH 3 Fosfina Hidruros de los metales: Combinaciones del hidrógeno con un metal. Ba. H 2 Hidruro de bario Cr. H 2 Hidruro de cromo (II) o Dihidruro de cromo
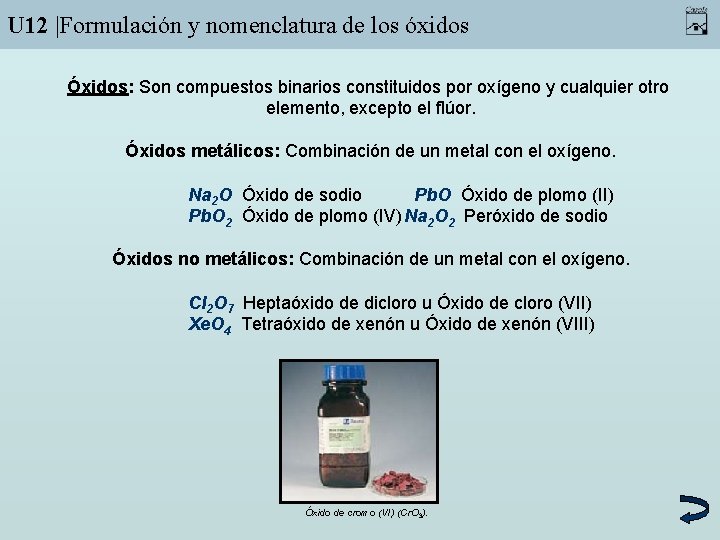
U 12 |Formulación y nomenclatura de los óxidos Óxidos: Son compuestos binarios constituidos por oxígeno y cualquier otro elemento, excepto el flúor. Óxidos metálicos: Combinación de un metal con el oxígeno. Na 2 O Óxido de sodio Pb. O Óxido de plomo (II) Pb. O 2 Óxido de plomo (IV) Na 2 O 2 Peróxido de sodio Óxidos no metálicos: Combinación de un metal con el oxígeno. Cl 2 O 7 Heptaóxido de dicloro u Óxido de cloro (VII) Xe. O 4 Tetraóxido de xenón u Óxido de xenón (VIII) Óxido de cromo (VI) (Cr. O 3).

U 12 |Formulación y nomenclatura de los hidróxidos o bases Hidróxidos o bases: Compuestos formados por la combinación de un catión metálico con el ión o los iones hidróxido, OH-. Paraformularlos hay que escribir, primero, el catión metálico y, después, tantos iones hidróxido como cargas positivas tenga el catión. Para denominarlos se utiliza la nomenclatura de Stock o la nomenclatura estequiométrica. Li+, OH– → Li. OH Fe 2+, 2 OH– → Fe(OH)2 Fe 3+, 3 OH– → Fe(OH)3 Hidróxido de litio Hidróxido de hierro (II) Hidróxido de hierro (III) Hidróxido de potasio (KOH).

U 12 |Formulación y nomenclatura de los ácidos Ácido: Sustancia que da iones hidrógeno H+ en solución acuosa. Hidrácidos: Ácidos formados por un no-metal, concretamente F, Cl, Br, I, S, Se, Te y el hidrógeno. HF Ácido fluorhídrico H 2 S Ácido sulfhídrico Oxácidos: Ácidos que en su molécula, además de hidrógeno tienen oxígeno. HCl. O Ácido hipocloroso HMn. O 4 Ácido permangánico Diácidos: Compuestos resultantes de la condensación (o unión) de dos moléculas de un oxoácido con pérdida de una molécula de agua. H 2 S 2 O 7 Ácido disulfúrico H 2 S 2 O 5 Ácido disulfuroso

U 12 |Formulación y nomenclatura de las sales Sal: Compuesto que deriva de un ácido por sustitución del ión hidrógeno o los iones hidrógenos por cationes metálicos o por el ión amonio NH 4+. Sales de los hidrácidos: Sales que se obtienen cuando los aniones F-, Cl–, Br–, I –, S 2 -, Se 2 - y Te 2 - se combinan con cationes metálicos (o con el ión amonio). Fe 2 S 3 Sulfuro de hierro (III) o Trisulfuro de dihierro Sales de los oxoácidos: Sales que se obtienen cuando un anión de un oxoácido se combina con un catión metálico. Ag. NO 3 Nitrato de plata Sales ácidas: Sales en las que no todos los iones hidrógenos del ácido del que derivan han sido sustituidos por cationes metálicos. Ba(HSO 3)2 Hidrogenosulfito de bario Sales hidratadas: Sales que tienen los iones de la estructura cristalina envueltos en moléculas de agua. Fe. SO 4 • 7 H 2 O Sulfato de hierro (II) heptahidratado
- Slides: 9