Conceptos bsicos en Qumica Orgnica M Gloria Quintanilla

Conceptos básicos en Química Orgánica Mª Gloria Quintanilla López Prof. Titular de Química Orgánica
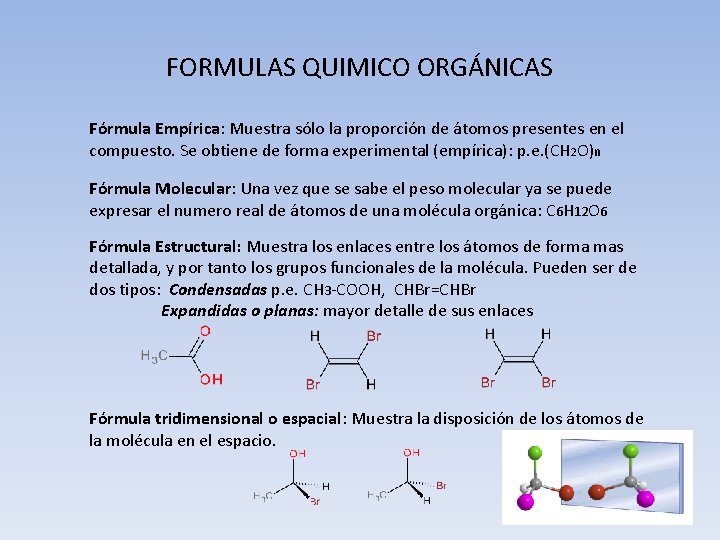
FORMULAS QUIMICO ORGÁNICAS Fórmula Empírica: Muestra sólo la proporción de átomos presentes en el compuesto. Se obtiene de forma experimental (empírica): p. e. (CH 2 O)n Fórmula Molecular: Una vez que se sabe el peso molecular ya se puede expresar el numero real de átomos de una molécula orgánica: C 6 H 12 O 6 Fórmula Estructural: Muestra los enlaces entre los átomos de forma mas detallada, y por tanto los grupos funcionales de la molécula. Pueden ser de dos tipos: Condensadas p. e. CH 3 -COOH, CHBr=CHBr Expandidas o planas: mayor detalle de sus enlaces Fórmula tridimensional o espacial: Muestra la disposición de los átomos de la molécula en el espacio.
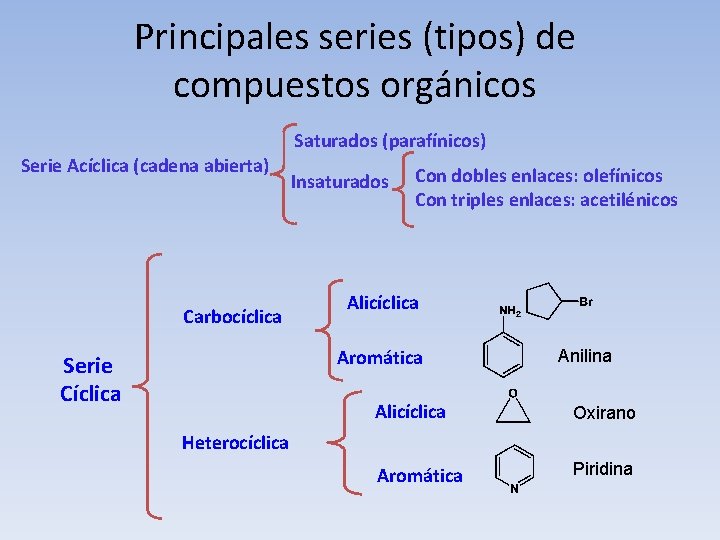
Principales series (tipos) de compuestos orgánicos Saturados (parafínicos) Serie Acíclica (cadena abierta) Carbocíclica Insaturados Con dobles enlaces: olefínicos Con triples enlaces: acetilénicos Alicíclica Aromática Serie Cíclica Anilina Alicíclica Oxirano Aromática Piridina Heterocíclica

Grupo funcional, Radical, Insaturacion, Grupo funcional es un átomo o grupo de átomos que unido o inserto en una cadena carbonada confiere a ésta unas propiedades características de ese grupo funcional. P. e. : -OH en los alcoholes, -CO- en las cetonas, -COOH en los ácidos carboxílicos etc Radical es un agrupamiento atómico con una valencia libre por la que se unirá al grupo funcional, si lo hay, o a la cadena principal de la molécula. P. e. CH 3 -CH 2 - Etilo Insaturación en una molécula organica existe una insaturación cuando contiene una pareja de atomos de H menos que el hidrocarburo saturado correspondiente. Cn. H 2 n+2: hidroc. saturado p. e. C 3 H 8, propano Cn. H 2 n : 1 insaturación ; p. e C 3 H 6 propeno Cn. H 2 n-2: 2 insaturaciones; C 3 H 4 p. e. propino. . o bien?
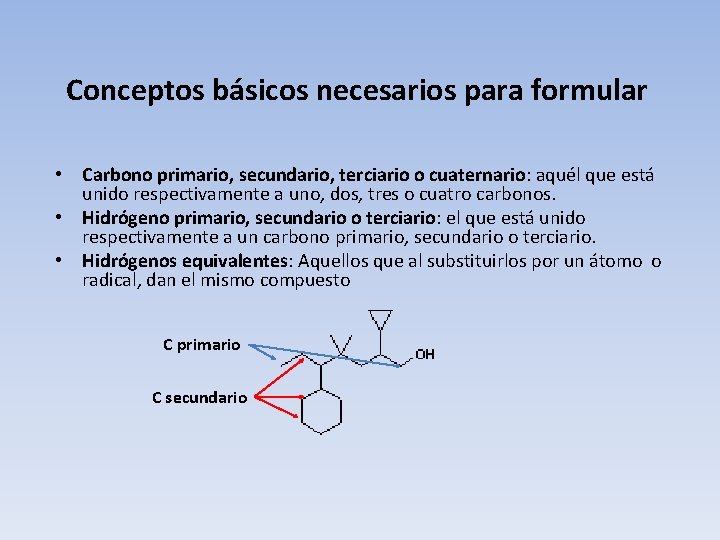
Conceptos básicos necesarios para formular • Carbono primario, secundario, terciario o cuaternario: aquél que está unido respectivamente a uno, dos, tres o cuatro carbonos. • Hidrógeno primario, secundario o terciario: el que está unido respectivamente a un carbono primario, secundario o terciario. • Hidrógenos equivalentes: Aquellos que al substituirlos por un átomo o radical, dan el mismo compuesto C primario C secundario

Nombres de los radicales Saturados: El nombre termina en –ilo Iso- (prefijo no separable)Dos extremos iguales. Solo el isopropilo es un radical secundario, el resto son radicales primarios. Sec- y terc- (prefijos separables)- Indican que la valencia libre esta situada respectivamente sobre un carbono secundario o sobre un carbono terciario. Insaturados: monovalentes: -enilo (si tiene un doble enlace) CH 2=CH- etenilo (vinilo); inilo (triple enlace) divalentes: - ilideno CH 2= Metilideno o Metileno (-CH 2 -) CH 3 -CH= Etilideno, pero : -CH 2 - (Etilen) CH 2 OH-CH 2 OH (Etilenglicol) CH 3 -CH 2 -CH= Propilideno , pero Propilen: CH 3 -CH-CH-; Propilenglicol
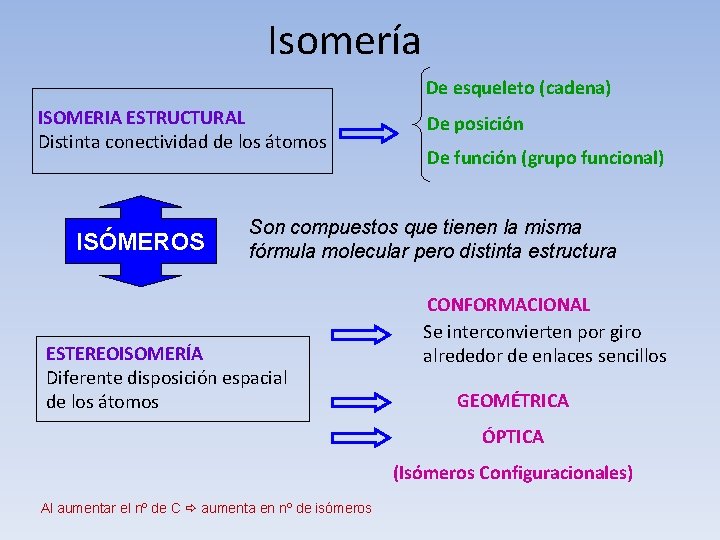
Isomería De esqueleto (cadena) ISOMERIA ESTRUCTURAL Distinta conectividad de los átomos ISÓMEROS De posición De función (grupo funcional) Son compuestos que tienen la misma fórmula molecular pero distinta estructura ESTEREOISOMERÍA Diferente disposición espacial de los átomos CONFORMACIONAL Se interconvierten por giro alrededor de enlaces sencillos GEOMÉTRICA ÓPTICA (Isómeros Configuracionales) Al aumentar el nº de C aumenta en nº de isómeros
- Slides: 7