Comparacin inhibidores de la integrasa vs IP FLAMINGO

Comparación inhibidores de la integrasa vs IP § FLAMINGO § GS-236 -0103 § ACTG A 5257
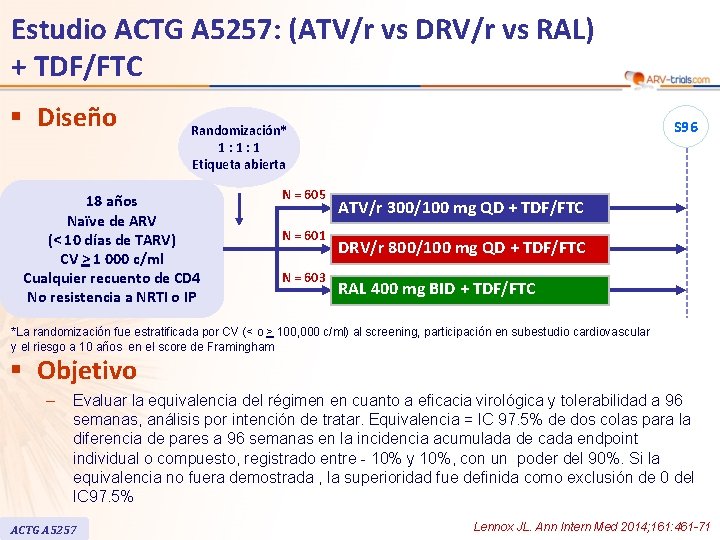
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC § Diseño S 96 Randomización* 1: 1: 1 Etiqueta abierta 18 años Naïve de ARV (< 10 días de TARV) CV > 1 000 c/ml Cualquier recuento de CD 4 No resistencia a NRTI o IP N = 605 N = 601 N = 603 ATV/r 300/100 mg QD + TDF/FTC DRV/r 800/100 mg QD + TDF/FTC RAL 400 mg BID + TDF/FTC *La randomización fue estratificada por CV (< o > 100, 000 c/ml) al screening, participación en subestudio cardiovascular y el riesgo a 10 años en el score de Framingham § Objetivo – Evaluar la equivalencia del régimen en cuanto a eficacia virológica y tolerabilidad a 96 semanas, análisis por intención de tratar. Equivalencia = IC 97. 5% de dos colas para la diferencia de pares a 96 semanas en la incidencia acumulada de cada endpoint individual o compuesto, registrado entre - 10% y 10%, con un poder del 90%. Si la equivalencia no fuera demostrada , la superioridad fue definida como exclusión de 0 del IC 97. 5% ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71

Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC § Endpoints – Fallo virológico: CV confirmada > 1000 c/ml en semana 16 o > 200 c/ml a semana 24 – Fallo de tolerabilidad: tiempo desde la randomización a la discontinuación del régimen randomizado por toxicidad (la sustitución de TDF o FTC no se consideró como fallo de tolerabilidad) – Endpoint compuesto: fallo virológico o de tolerabilidad, cualquiera que ocurra primero – ITT-TLOVR, con CV limite de 200 c/ml – CV < 50 c/ml a S 96 por ITT, snapshot – Análisis de sensibilidad : as-treated (según tratamiento) (el fallo virológico incluyó discontinuación como un evento competitivo) – Endpoint secundario de toxicidad: tiempo desde la iniciación del tratamiento hasta el primer signo o síntoma grado 2, 3 o 4 (grado 3 o 4 si es después de semana 48) o cualquier anomalía de laboratorio grado 3 o 4 mientras el paciente recibía el tratamiento (as-treated) • Análisis de sensibilidad excluyó hiperbilirrubinemia y niveles elevados de CPK • Análisis de sensibilidad adicionales incluyeron todos los eventos adversos independientemente del status al momento de la randomización (análisis) ITT ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
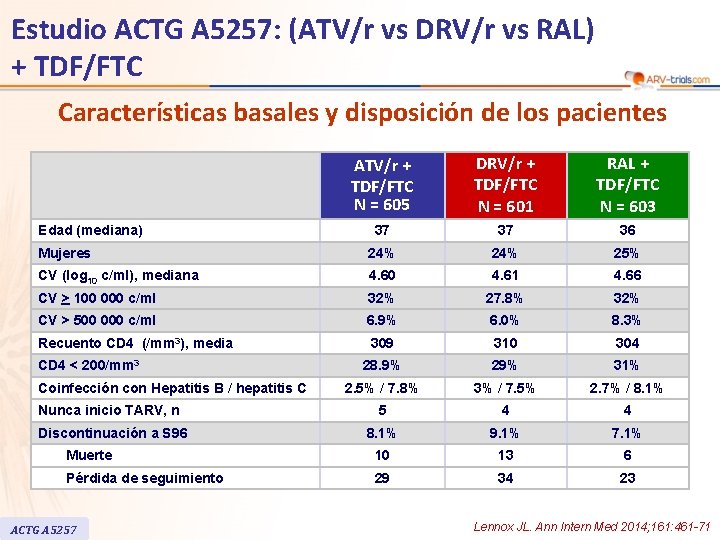
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Características basales y disposición de los pacientes ATV/r + TDF/FTC N = 605 DRV/r + TDF/FTC N = 601 RAL + TDF/FTC N = 603 37 37 36 Mujeres 24% 25% CV (log 10 c/ml), mediana 4. 60 4. 61 4. 66 CV > 100 000 c/ml 32% 27. 8% 32% CV > 500 000 c/ml 6. 9% 6. 0% 8. 3% 309 310 304 28. 9% 29% 31% 2. 5% / 7. 8% 3% / 7. 5% 2. 7% / 8. 1% Nunca inicio TARV, n 5 4 4 Discontinuación a S 96 8. 1% 9. 1% 7. 1% Muerte 10 13 6 Pérdida de seguimiento 29 34 23 Edad (mediana) Recuento CD 4 (/mm 3), media CD 4 < 200/mm 3 Coinfección con Hepatitis B / hepatitis C ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
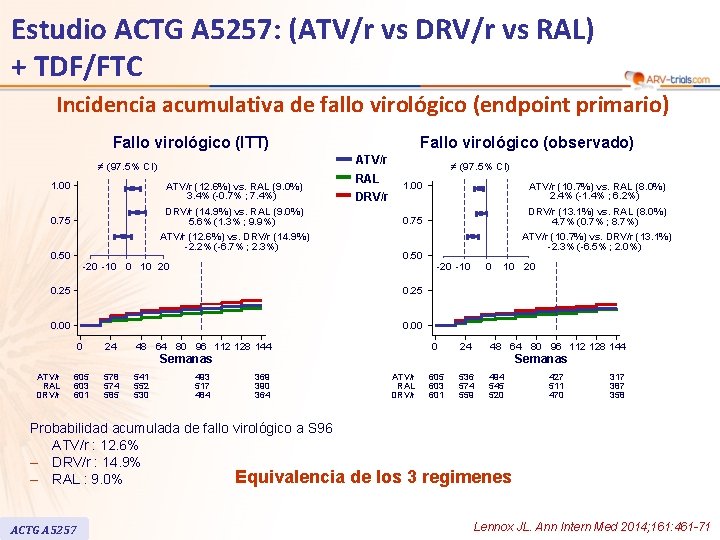
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Incidencia acumulativa de fallo virológico (endpoint primario) Fallo virológico (ITT) ATV/r ≠ (97. 5% CI) 1. 00 ATV/r (12. 6%) vs. RAL (9. 0%) 3. 4% (-0. 7% ; 7. 4%) DRV/r (14. 9%) vs. RAL (9. 0%) 5. 6% (1. 3% ; 9. 9%) 0. 75 ATV/r (12. 6%) vs. DRV/r (14. 9%) -2. 2% (-6. 7% ; 2. 3%) 0. 50 Fallo virológico (observado) RAL DRV/r ≠ (97. 5% CI) 1. 00 ATV/r (10. 7%) vs. DRV/r (13. 1%) -2. 3% (-6. 5% ; 2. 0%) 0. 50 -20 -10 0. 25 0. 00 24 DRV/r (13. 1%) vs. RAL (8. 0%) 4. 7% (0. 7% ; 8. 7%) 0. 75 -20 -10 0 10 20 0 ATV/r (10. 7%) vs. RAL (8. 0%) 2. 4% (-1. 4% ; 6. 2%) 48 64 80 96 112 128 144 0 0 24 10 20 48 64 80 96 112 128 144 Semanas ATV/r RAL DRV/r 605 603 601 578 574 585 541 552 530 493 517 484 Semanas 369 390 364 Probabilidad acumulada de fallo virológico a S 96 ATV/r : 12. 6% – DRV/r : 14. 9% Equivalencia – RAL : 9. 0% ACTG A 5257 ATV/r RAL DRV/r 605 603 601 536 574 559 494 545 520 427 511 470 317 387 358 de los 3 regimenes Lennox JL. Ann Intern Med 2014; 161: 461 -71
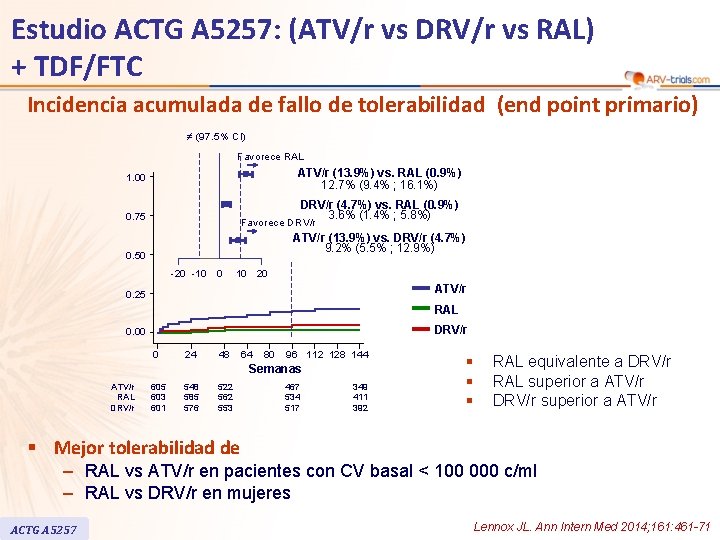
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Incidencia acumulada de fallo de tolerabilidad (end point primario) ≠ (97. 5% CI) Favorece RAL ATV/r (13. 9%) vs. RAL (0. 9%) 12. 7% (9. 4% ; 16. 1%) 1. 00 DRV/r (4. 7%) vs. RAL (0. 9%) 3. 6% (1. 4% ; 5. 8%) 0. 75 Favorece DRV/r ATV/r (13. 9%) vs. DRV/r (4. 7%) 9. 2% (5. 5% ; 12. 9%) 0. 50 -20 -10 0 10 20 ATV/r 0. 25 RAL DRV/r 0. 00 0 24 48 64 80 96 112 128 144 Semanas ATV/r RAL DRV/r 605 603 601 548 585 576 522 562 553 467 534 517 349 411 392 § § § RAL equivalente a DRV/r RAL superior a ATV/r DRV/r superior a ATV/r § Mejor tolerabilidad de – RAL vs ATV/r en pacientes con CV basal < 100 000 c/ml – RAL vs DRV/r en mujeres ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
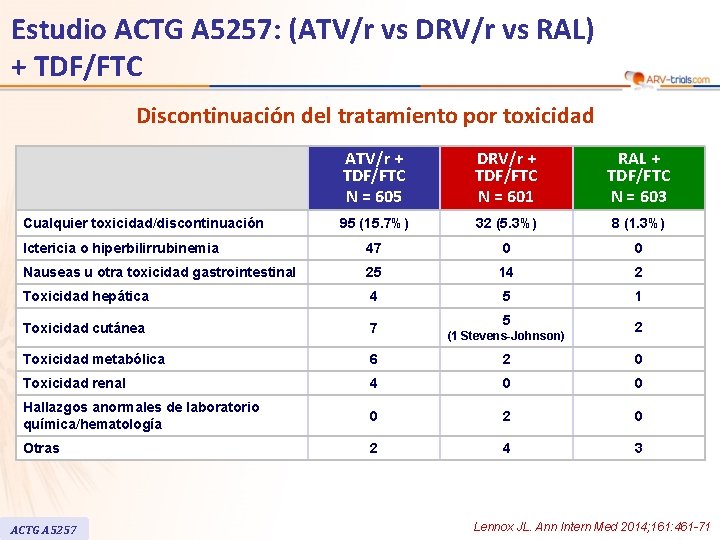
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Discontinuación del tratamiento por toxicidad ATV/r + TDF/FTC N = 605 DRV/r + TDF/FTC N = 601 RAL + TDF/FTC N = 603 95 (15. 7%) 32 (5. 3%) 8 (1. 3%) Ictericia o hiperbilirrubinemia 47 0 0 Nauseas u otra toxicidad gastrointestinal 25 14 2 Toxicidad hepática 4 5 1 Toxicidad cutánea 7 5 2 Toxicidad metabólica 6 2 0 Toxicidad renal 4 0 0 Hallazgos anormales de laboratorio química/hematología 0 2 0 Otras 2 4 3 Cualquier toxicidad/discontinuación ACTG A 5257 (1 Stevens-Johnson) Lennox JL. Ann Intern Med 2014; 161: 461 -71
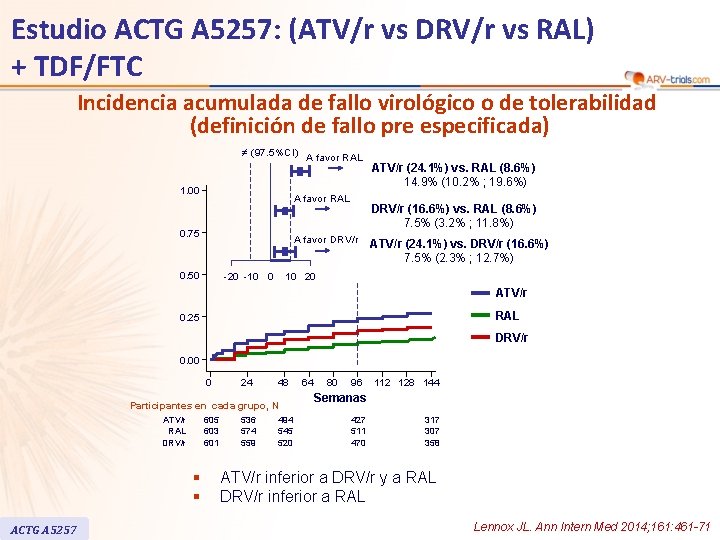
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Incidencia acumulada de fallo virológico o de tolerabilidad (definición de fallo pre especificada) ≠ (97. 5%CI) A favor RAL 1. 00 A favor RAL 0. 75 DRV/r (16. 6%) vs. RAL (8. 6%) 7. 5% (3. 2% ; 11. 8%) A favor DRV/r 0. 50 -20 -10 0 ATV/r (24. 1%) vs. RAL (8. 6%) 14. 9% (10. 2% ; 19. 6%) ATV/r (24. 1%) vs. DRV/r (16. 6%) 7. 5% (2. 3% ; 12. 7%) 10 20 ATV/r RAL 0. 25 DRV/r 0. 00 0 24 48 Participantes en cada grupo, N ATV/r RAL DRV/r 605 603 601 § § ACTG A 5257 536 574 559 494 545 520 64 80 96 112 128 144 Semanas 427 511 470 317 307 358 ATV/r inferior a DRV/r y a RAL DRV/r inferior a RAL Lennox JL. Ann Intern Med 2014; 161: 461 -71
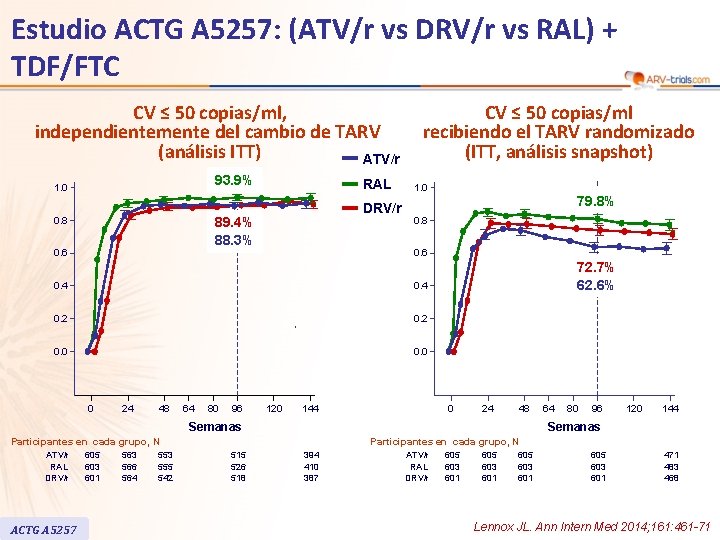
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC CV ≤ 50 copias/ml, independientemente del cambio de TARV (análisis ITT) ATV/r 93. 9% 1. 0 RAL DRV/r 89. 4% 88. 3% 0. 8 0. 6 CV ≤ 50 copias/ml recibiendo el TARV randomizado (ITT, análisis snapshot) 1. 0 79. 8% 0. 8 0. 6 0. 4 0. 2 0. 0 0 24 48 64 80 96 120 144 72. 7% 62. 6% 0 24 48 Semanas ACTG A 5257 605 603 601 563 566 564 553 555 542 80 96 120 144 Semanas Participantes en cada grupo, N ATV/r RAL DRV/r 64 Participantes en cada grupo, N 515 526 518 394 410 387 ATV/r RAL DRV/r 605 603 601 471 483 468 Lennox JL. Ann Intern Med 2014; 161: 461 -71
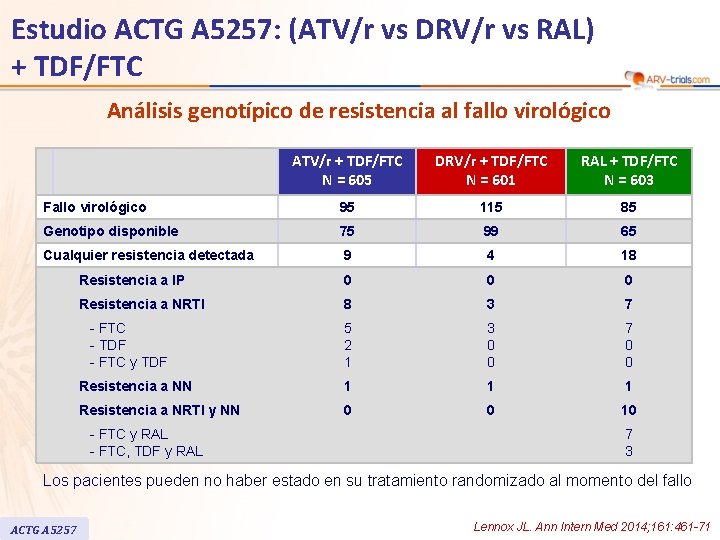
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Análisis genotípico de resistencia al fallo virológico ATV/r + TDF/FTC N = 605 DRV/r + TDF/FTC N = 601 RAL + TDF/FTC N = 603 Fallo virológico 95 115 85 Genotipo disponible 75 99 65 Cualquier resistencia detectada 9 4 18 Resistencia a IP 0 0 0 Resistencia a NRTI 8 3 7 5 2 1 3 0 0 7 0 0 Resistencia a NN 1 1 1 Resistencia a NRTI y NN 0 0 10 - FTC - TDF - FTC y RAL - FTC, TDF y RAL 7 3 Los pacientes pueden no haber estado en su tratamiento randomizado al momento del fallo ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
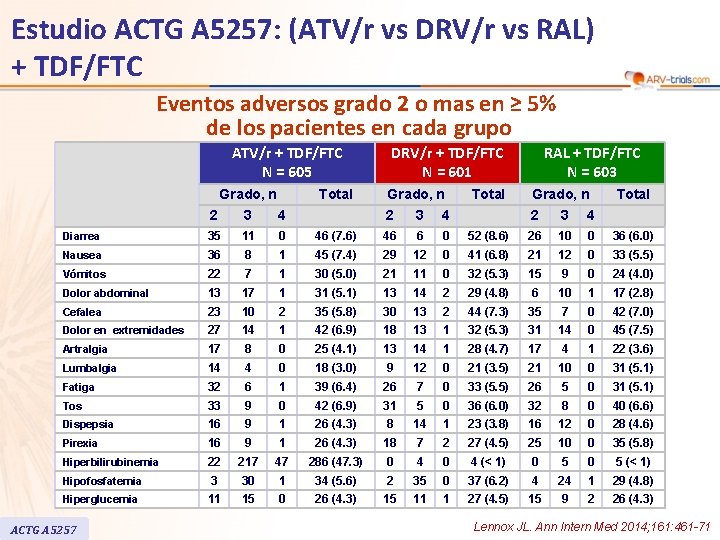
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Eventos adversos grado 2 o mas en ≥ 5% de los pacientes en cada grupo ATV/r + TDF/FTC N = 605 Grado, n Total 2 3 4 Diarrea 35 11 0 Nausea 36 8 Vómitos 22 Dolor abdominal DRV/r + TDF/FTC N = 601 Grado, n 2 3 4 46 (7. 6) 46 6 0 1 45 (7. 4) 29 12 7 1 30 (5. 0) 21 13 17 1 31 (5. 1) Cefalea 23 10 2 Dolor en extremidades 27 14 Artralgia 17 Lumbalgia Total RAL + TDF/FTC N = 603 Grado, n Total 2 3 4 52 (8. 6) 26 10 0 36 (6. 0) 0 41 (6. 8) 21 12 0 33 (5. 5) 11 0 32 (5. 3) 15 9 0 24 (4. 0) 13 14 2 29 (4. 8) 6 10 1 17 (2. 8) 35 (5. 8) 30 13 2 44 (7. 3) 35 7 0 42 (7. 0) 1 42 (6. 9) 18 13 1 32 (5. 3) 31 14 0 45 (7. 5) 8 0 25 (4. 1) 13 14 1 28 (4. 7) 17 4 1 22 (3. 6) 14 4 0 18 (3. 0) 9 12 0 21 (3. 5) 21 10 0 31 (5. 1) Fatiga 32 6 1 39 (6. 4) 26 7 0 33 (5. 5) 26 5 0 31 (5. 1) Tos 33 9 0 42 (6. 9) 31 5 0 36 (6. 0) 32 8 0 40 (6. 6) Dispepsia 16 9 1 26 (4. 3) 8 14 1 23 (3. 8) 16 12 0 28 (4. 6) Pirexia 16 9 1 26 (4. 3) 18 7 2 27 (4. 5) 25 10 0 35 (5. 8) Hiperbilirubinemia 22 217 47 286 (47. 3) 0 4 (< 1) 0 5 (< 1) Hipofosfatemia 3 30 1 34 (5. 6) 2 35 0 37 (6. 2) 4 24 1 29 (4. 8) Hiperglucemia 11 15 0 26 (4. 3) 15 11 1 27 (4. 5) 15 9 2 26 (4. 3) ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
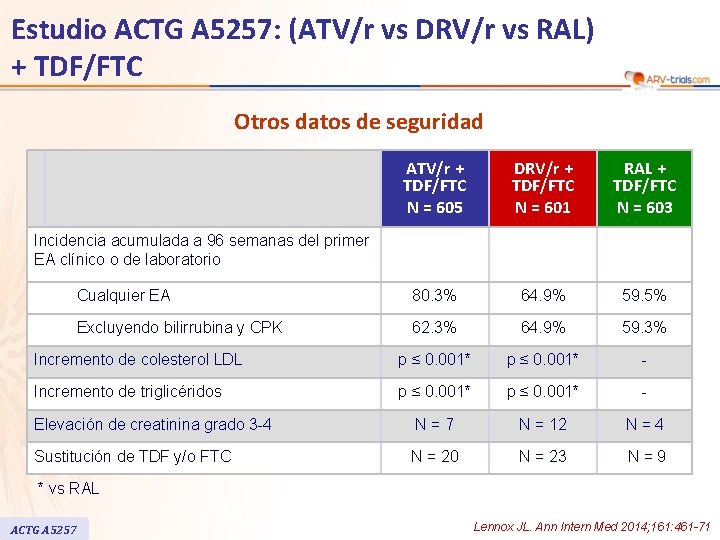
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Otros datos de seguridad ATV/r + TDF/FTC N = 605 DRV/r + TDF/FTC N = 601 RAL + TDF/FTC N = 603 Cualquier EA 80. 3% 64. 9% 59. 5% Excluyendo bilirrubina y CPK 62. 3% 64. 9% 59. 3% Incremento de colesterol LDL p ≤ 0. 001* - Incremento de triglicéridos p ≤ 0. 001* - Elevación de creatinina grado 3 -4 N=7 N = 12 N=4 Sustitución de TDF y/o FTC N = 20 N = 23 N=9 Incidencia acumulada a 96 semanas del primer EA clínico o de laboratorio * vs RAL ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
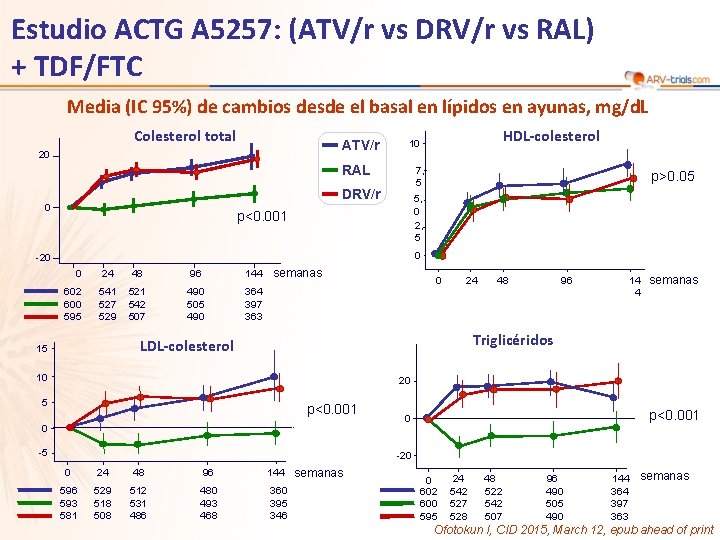
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Media (IC 95%) de cambios desde el basal en lípidos en ayunas, mg/d. L Colesterol total ATV/r 20 RAL 7, 5 DRV/r 0 HDL-colesterol 10 p>0. 05 5, 0 2, 5 p<0. 001 0 -20 0 24 48 96 144 semanas 602 600 595 541 527 529 521 542 507 490 505 490 364 397 363 0 24 96 14 semanas 4 Triglicéridos LDL-colesterol 15 48 10 20 5 p<0. 001 0 -20 0 24 48 96 593 581 529 518 508 512 531 486 480 493 468 144 semanas 360 395 346 0 602 600 595 24 542 527 528 48 522 542 507 96 490 505 490 144 semanas 364 397 363 Ofotokun I, CID 2015, March 12, epub ahead of print
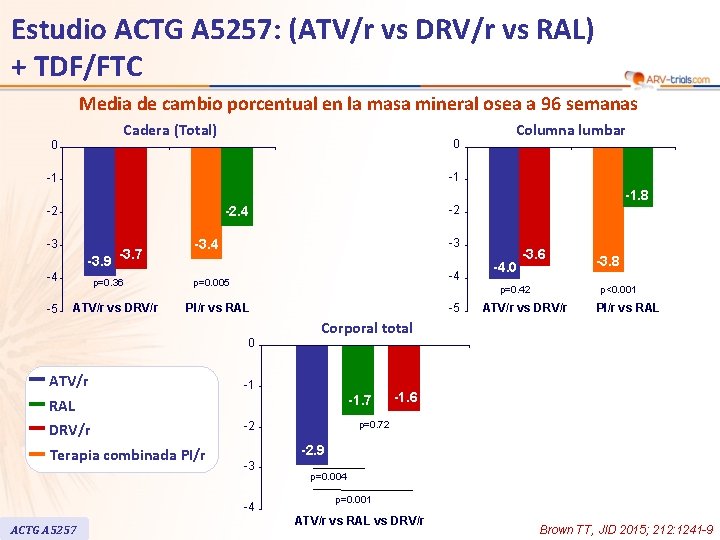
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Media de cambio porcentual en la masa mineral osea a 96 semanas Cadera (Total) 0 0 Columna lumbar -1 -1 -1. 8 -3 -3. 9 -3. 7 -4 -5 -2 -2. 4 -2 p=0. 36 ATV/r vs DRV/r -3 -3. 4 -4 p=0. 005 p=0. 42 PI/r vs RAL 0 ATV/r RAL DRV/r Terapia combinada PI/r -5 -3. 8 p<0. 001 ATV/r vs DRV/r PI/r vs RAL Corporal total -1 -1. 7 -1. 6 p=0. 72 -2 -2. 9 -3 -4 ACTG A 5257 -4. 0 -3. 6 p=0. 004 p=0. 001 ATV/r vs RAL vs DRV/r Brown TT, JID 2015; 212: 1241 -9
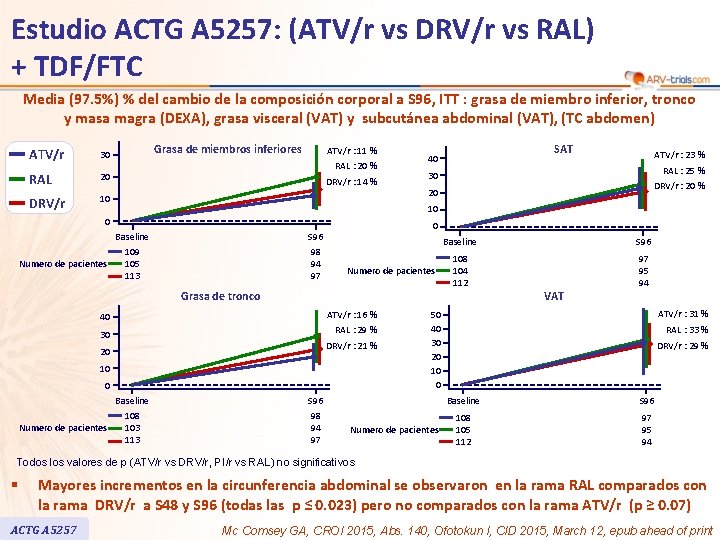
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC Media (97. 5%) % del cambio de la composición corporal a S 96, ITT : grasa de miembro inferior, tronco y masa magra (DEXA), grasa visceral (VAT) y subcutánea abdominal (VAT), (TC abdomen) ATV/r 30 RAL 20 DRV/r 10 Grasa de miembros inferiores ATV/r : 11 % RAL : 20 % DRV/r : 14 % SAT 40 RAL : 25 % 30 DRV/r : 20 % 20 10 0 Baseline 109 105 Numero de pacientes 113 S 96 98 94 97 0 Numero de pacientes Baseline S 96 108 104 112 97 95 94 Grasa de tronco VAT 40 ATV/r : 16 % 30 RAL : 29 % DRV/r : 21 % 20 10 0 Baseline 108 103 Numero de pacientes 113 ATV/r : 23 % S 96 98 94 97 ATV/r : 31 % 50 40 30 20 10 0 Numero de pacientes RAL : 33 % DRV/r : 29 % Baseline S 96 108 105 112 97 95 94 Todos los valores de p (ATV/r vs DRV/r, PI/r vs RAL) no significativos § Mayores incrementos en la circunferencia abdominal se observaron en la rama RAL comparados con la rama DRV/r a S 48 y S 96 (todas las p ≤ 0. 023) pero no comparados con la rama ATV/r (p ≥ 0. 07) ACTG A 5257 Mc Comsey GA, CROI 2015, Abs. 140, Ofotokun I, CID 2015, March 12, epub ahead of print
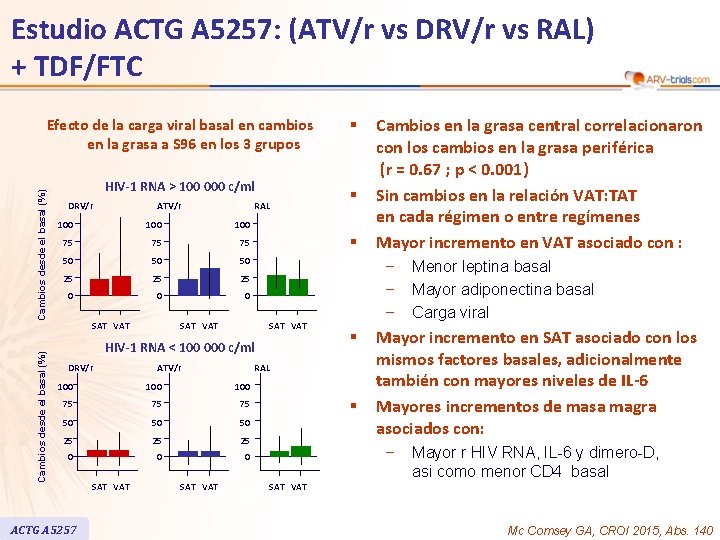
Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC § HIV-1 RNA > 100 000 c/ml § Cambios desde el basal (%) Efecto de la carga viral basal en cambios en la grasa a S 96 en los 3 grupos DRV/r ATV/r RAL 100 100 75 75 75 50 50 50 25 25 25 0 0 0 SAT VAT § SAT VAT HIV-1 RNA < 100 000 c/ml DRV/r ATV/r 100 75 75 75 50 50 50 25 25 25 0 0 0 ACTG A 5257 SAT VAT – – – § RAL 100 Cambios en la grasa central correlacionaron con los cambios en la grasa periférica (r = 0. 67 ; p < 0. 001) Sin cambios en la relación VAT: TAT en cada régimen o entre regímenes Mayor incremento en VAT asociado con : § Menor leptina basal Mayor adiponectina basal Carga viral Mayor incremento en SAT asociado con los mismos factores basales, adicionalmente también con mayores niveles de IL-6 Mayores incrementos de masa magra asociados con: – Mayor r HIV RNA, IL-6 y dimero-D, asi como menor CD 4 basal SAT VAT Mc Comsey GA, CROI 2015, Abs. 140

Estudio ACTG A 5257: (ATV/r vs DRV/r vs RAL) + TDF/FTC § Conclusión – ATV/r, RAL y DRV/r fueron equivalentes en cuanto a eficacia virológica administrados con TDF/FTC – ATV/r + TDF/FTC fue peor tolerado que DRV/r + TDF/FTC o RAL + TDF/FTC – La evaluación compuesta de eficacia virológica y tolerabilidad demostró que • RAL + TDF/FTC fue superior a los dos regímenes que contienen IP • DRV/r + TDF/FTC fue superior a ATV/r + TDF/FTC – Los resultados de tolerabilidad fueron causados primariamente por ictericia por ATV/r y toxicidad gastrointestinal por ambos IP/r • ATV/r fue menos tolerado que DRV/r y RAL en todos los subgrupos • El beneficio de tolerabilidad de RAL sobre DRV/r fue mayor en mujeres – Limitaciones : diseño de etiqueta abierta, se permitió el cambio a otra rama por problemas de tolerabilidad o toxicidad – Cuando la tolerabilidad y respuesta virológica fueron consideradas en conjunto, RAL + TDF/FTC fue superior a ambos esquemas basados en IP y DRV/r fue superior a ATV/r. Una ventaja de IP sobre RAL es la reducción de la probabilidad de resistencia y fallo virológico ACTG A 5257 Lennox JL. Ann Intern Med 2014; 161: 461 -71
- Slides: 17