Comparacin de INNTR vs INNTR ENCORE EFV vs




- Slides: 15

Comparación de INNTR vs INNTR § ENCORE § EFV vs RPV – ECHO-THRIVE – STAR § EFV vs ETR – SENSE

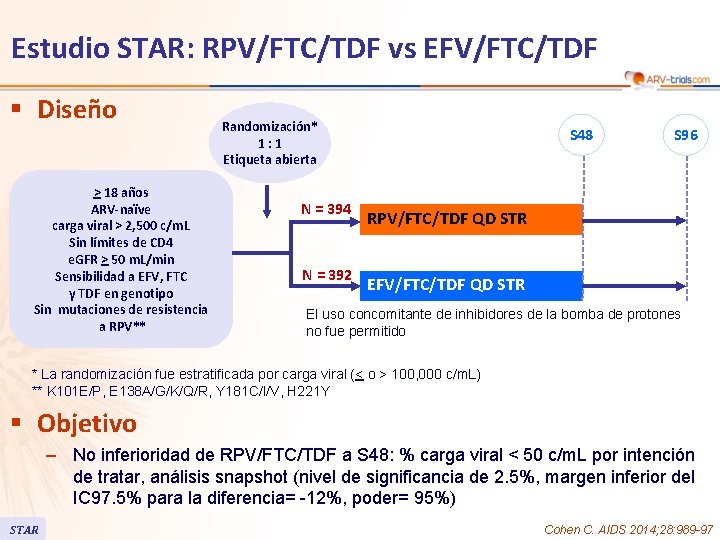
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF § Diseño > 18 años ARV-naïve carga viral > 2, 500 c/m. L Sin límites de CD 4 e. GFR > 50 m. L/min Sensibilidad a EFV, FTC y TDF en genotipo Sin mutaciones de resistencia a RPV** Randomización* 1: 1 Etiqueta abierta N = 394 N = 392 S 48 S 96 RPV/FTC/TDF QD STR EFV/FTC/TDF QD STR El uso concomitante de inhibidores de la bomba de protones no fue permitido * La randomización fue estratificada por carga viral (< o > 100, 000 c/m. L) ** K 101 E/P, E 138 A/G/K/Q/R, Y 181 C/I/V, H 221 Y § Objetivo – No inferioridad de RPV/FTC/TDF a S 48: % carga viral < 50 c/m. L por intención de tratar, análisis snapshot (nivel de significancia de 2. 5%, margen inferior del IC 97. 5% para la diferencia= -12%, poder= 95%) STAR Cohen C. AIDS 2014; 28: 989 -97

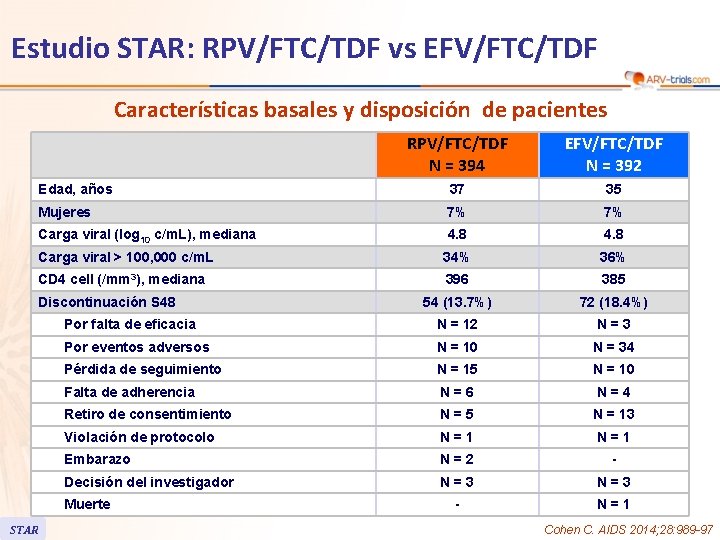
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Características basales y disposición de pacientes RPV/FTC/TDF N = 394 EFV/FTC/TDF N = 392 Edad, años 37 35 Mujeres 7% 7% Carga viral (log 10 c/m. L), mediana 4. 8 Carga viral > 100, 000 c/m. L 34% 36% CD 4 cell (/mm 3), mediana 396 385 54 (13. 7%) 72 (18. 4%) Por falta de eficacia N = 12 N=3 Por eventos adversos N = 10 N = 34 Pérdida de seguimiento N = 15 N = 10 Falta de adherencia N=6 N=4 Retiro de consentimiento N=5 N = 13 Violación de protocolo N=1 Embarazo N=2 - Decisión del investigador N=3 - N=1 Discontinuación S 48 Muerte STAR Cohen C. AIDS 2014; 28: 989 -97

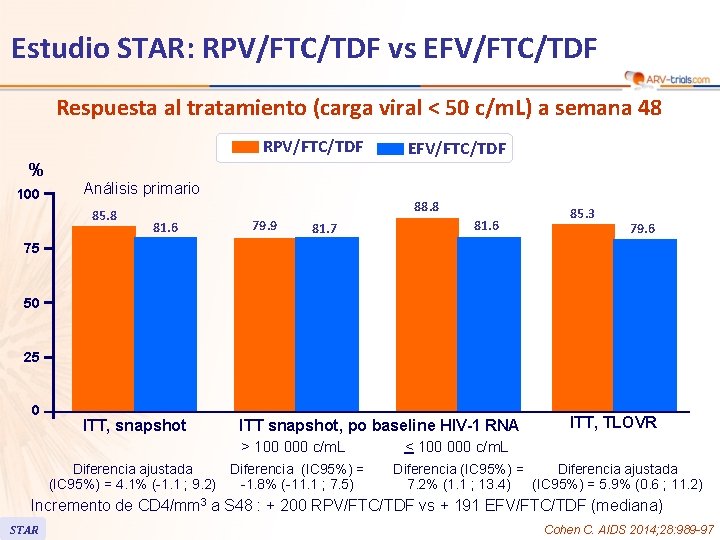
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Respuesta al tratamiento (carga viral < 50 c/m. L) a semana 48 RPV/FTC/TDF % 100 EFV/FTC/TDF Análisis primario 85. 8 88. 8 81. 6 79. 9 81. 7 81. 6 85. 3 79. 6 75 50 25 0 ITT, snapshot ITT snapshot, po baseline HIV-1 RNA > 100 000 c/m. L Diferencia ajustada (IC 95%) = 4. 1% (-1. 1 ; 9. 2) Diferencia (IC 95%) = -1. 8% (-11. 1 ; 7. 5) ITT, TLOVR < 100 000 c/m. L Diferencia (IC 95%) = Diferencia ajustada 7. 2% (1. 1 ; 13. 4) (IC 95%) = 5. 9% (0. 6 ; 11. 2) Incremento de CD 4/mm 3 a S 48 : + 200 RPV/FTC/TDF vs + 191 EFV/FTC/TDF (mediana) STAR Cohen C. AIDS 2014; 28: 989 -97

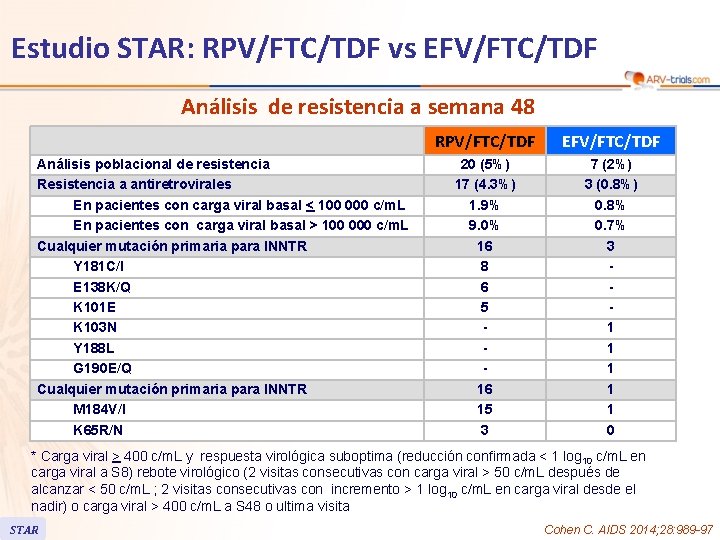
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Análisis de resistencia a semana 48 Análisis poblacional de resistencia Resistencia a antiretrovirales En pacientes con carga viral basal < 100 000 c/m. L En pacientes con carga viral basal > 100 000 c/m. L Cualquier mutación primaria para INNTR Y 181 C/I E 138 K/Q K 101 E K 103 N Y 188 L G 190 E/Q Cualquier mutación primaria para INNTR M 184 V/I K 65 R/N RPV/FTC/TDF EFV/FTC/TDF 20 (5%) 17 (4. 3%) 1. 9% 9. 0% 16 8 6 5 16 15 3 7 (2%) 3 (0. 8%) 0. 8% 0. 7% 3 1 1 1 0 * Carga viral > 400 c/m. L y respuesta virológica suboptima (reducción confirmada < 1 log 10 c/m. L en carga viral a S 8) rebote virológico (2 visitas consecutivas con carga viral > 50 c/m. L después de alcanzar < 50 c/m. L ; 2 visitas consecutivas con incremento > 1 log 10 c/m. L en carga viral desde el nadir) o carga viral > 400 c/m. L a S 48 o ultima visita STAR Cohen C. AIDS 2014; 28: 989 -97

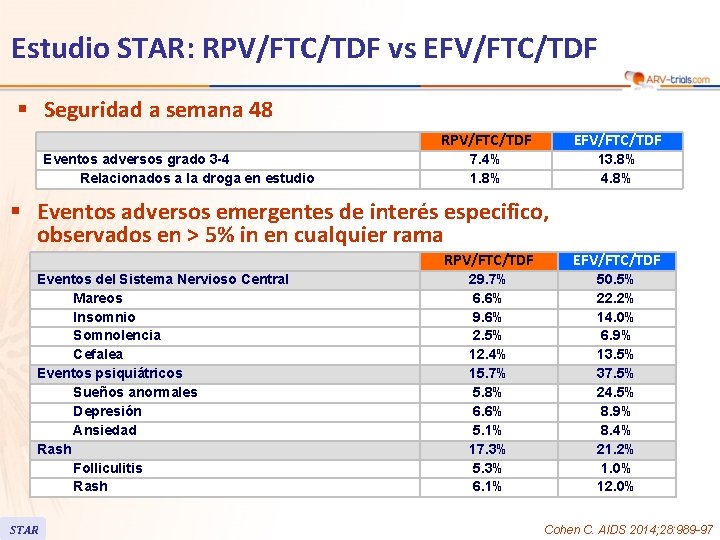
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF § Seguridad a semana 48 Eventos adversos grado 3 -4 Relacionados a la droga en estudio RPV/FTC/TDF EFV/FTC/TDF 7. 4% 1. 8% 13. 8% 4. 8% § Eventos adversos emergentes de interés especifico, observados en > 5% in en cualquier rama Eventos del Sistema Nervioso Central Mareos Insomnio Somnolencia Cefalea Eventos psiquiátricos Sueños anormales Depresión Ansiedad Rash Folliculitis Rash STAR RPV/FTC/TDF EFV/FTC/TDF 29. 7% 6. 6% 9. 6% 2. 5% 12. 4% 15. 7% 5. 8% 6. 6% 5. 1% 17. 3% 5. 3% 6. 1% 50. 5% 22. 2% 14. 0% 6. 9% 13. 5% 37. 5% 24. 5% 8. 9% 8. 4% 21. 2% 1. 0% 12. 0% Cohen C. AIDS 2014; 28: 989 -97

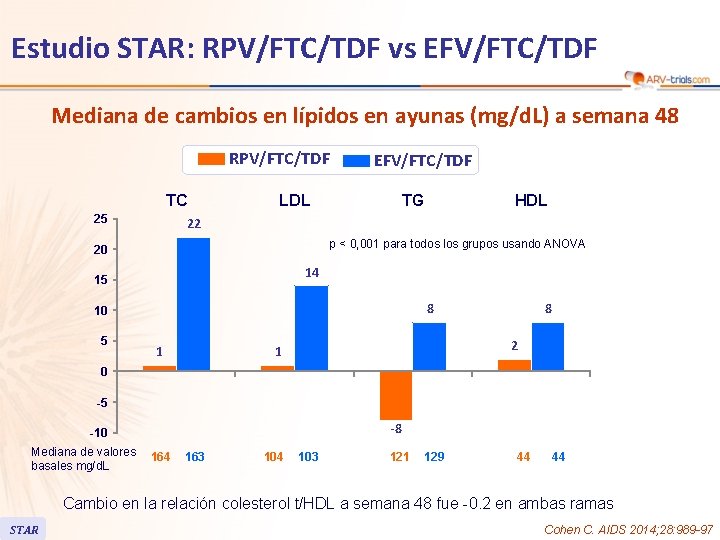
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Mediana de cambios en lípidos en ayunas (mg/d. L) a semana 48 RPV/FTC/TDF TC 25 EFV/FTC/TDF LDL TG 22 p < 0, 001 para todos los grupos usando ANOVA 20 14 15 8 10 5 HDL 1 8 2 1 0 -5 -8 -10 Mediana de valores basales mg/d. L 164 163 104 103 121 129 44 44 Cambio en la relación colesterol t/HDL a semana 48 fue -0. 2 en ambas ramas STAR Cohen C. AIDS 2014; 28: 989 -97

Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF § Conclusión semana 48 – En pacientes HIV+, naïve de TARV, RPV/FTC/TDF demostró no inferioridad en eficacia y mejor tolerabilidad comparado con EFV/FTC/TDF, a semana 48 • RPV/FTC/TDF fue superior (estadísticamente significativo) en eficacia en pacientes con CV basal ≤ 100 000 copias/m. L • La eficacia virológica fue similar en pacientes con CV basal > 100 000 copias/m. L – Mas discontinuaciones por eventos adversos en la rama EFV/FTC/TDF – Significativa menor tasa de eventos adversos del sistema nervioso central y psiquiátricos con RPV/FTC/TDF comparado con la rama EFV/FTC/TDF • Las diferencias primariamente debidas a mareos y sueños anormales du – Tasa de fallo virológico similar entre ramas. Mayor proporción de pacientes en rama RPV/FTC/TDF desarrollaron resistencia primara emergente a INTR o INNTR al fallo virológico STAR Cohen C. AIDS 2014; 28: 989 -97

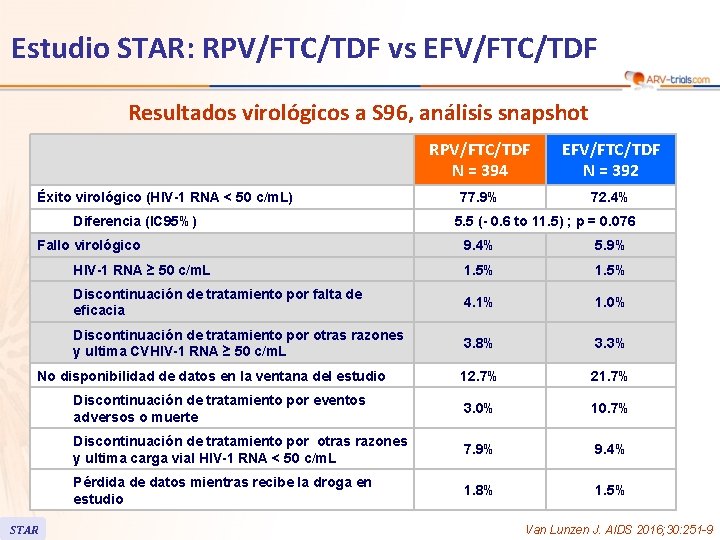
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Resultados virológicos a S 96, análisis snapshot Éxito virológico (HIV-1 RNA < 50 c/m. L) Diferencia (IC 95%) Fallo virológico EFV/FTC/TDF N = 392 77. 9% 72. 4% 5. 5 (- 0. 6 to 11. 5) ; p = 0. 076 9. 4% 5. 9% HIV-1 RNA ≥ 50 c/m. L 1. 5% Discontinuación de tratamiento por falta de eficacia 4. 1% 1. 0% Discontinuación de tratamiento por otras razones y ultima CVHIV-1 RNA ≥ 50 c/m. L 3. 8% 3. 3% 12. 7% 21. 7% Discontinuación de tratamiento por eventos adversos o muerte 3. 0% 10. 7% Discontinuación de tratamiento por otras razones y ultima carga vial HIV-1 RNA < 50 c/m. L 7. 9% 9. 4% Pérdida de datos mientras recibe la droga en estudio 1. 8% 1. 5% No disponibilidad de datos en la ventana del estudio STAR RPV/FTC/TDF N = 394 Van Lunzen J. AIDS 2016; 30: 251 -9

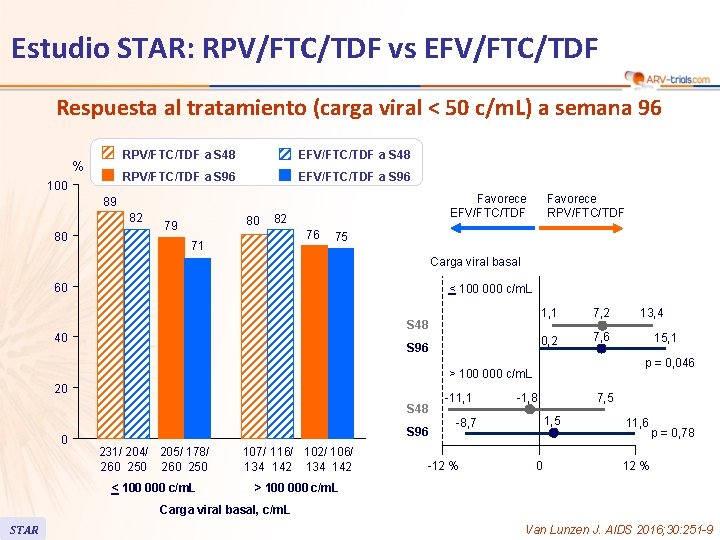
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Respuesta al tratamiento (carga viral < 50 c/m. L) a semana 96 % 100 RPV/FTC/TDF a S 48 EFV/FTC/TDF a S 48 RPV/FTC/TDF a S 96 EFV/FTC/TDF a S 96 Favorece EFV/FTC/TDF 89 82 80 80 79 82 76 71 Favorece RPV/FTC/TDF 75 Carga viral basal 60 < 100 000 c/m. L S 48 40 S 96 1, 1 7, 2 0, 2 7, 6 S 48 0 S 96 231/ 204/ 205/ 178/ 260 250 107/ 116/ 102/ 106/ 134 142 < 100 000 c/m. L > 100 000 c/m. L -11, 1 -1, 8 7, 5 1, 5 -8, 7 -12 % 15, 1 p = 0, 046 > 100 000 c/m. L 20 13, 4 0 11, 6 p = 0, 78 12 % Carga viral basal, c/m. L STAR Van Lunzen J. AIDS 2016; 30: 251 -9

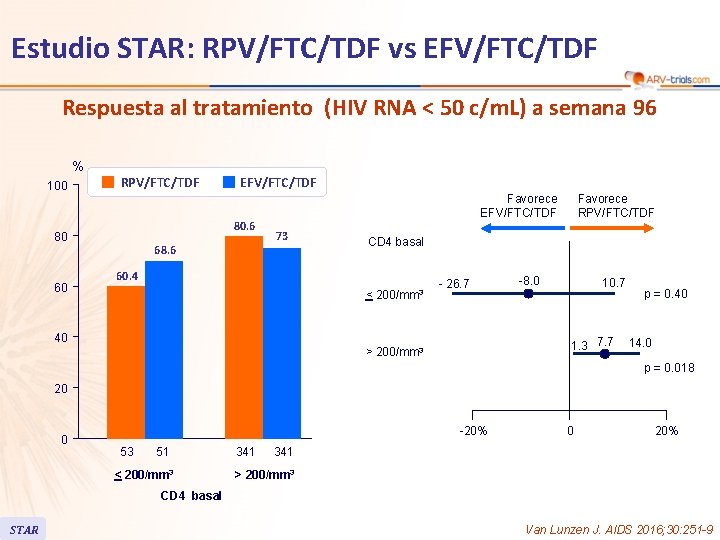
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Respuesta al tratamiento (HIV RNA < 50 c/m. L) a semana 96 % 100 RPV/FTC/TDF 80. 6 80 60 EFV/FTC/TDF 68. 6 Favorece EFV/FTC/TDF 73 Favorece RPV/FTC/TDF CD 4 basal 60. 4 < 200/mm 3 - 26. 7 40 -8. 0 10. 7 1. 3 7. 7 > 200/mm 3 p = 0. 40 14. 0 p = 0. 018 20 0 -20% 53 51 < 200/mm 3 341 0 20% 341 > 200/mm 3 CD 4 basal STAR Van Lunzen J. AIDS 2016; 30: 251 -9

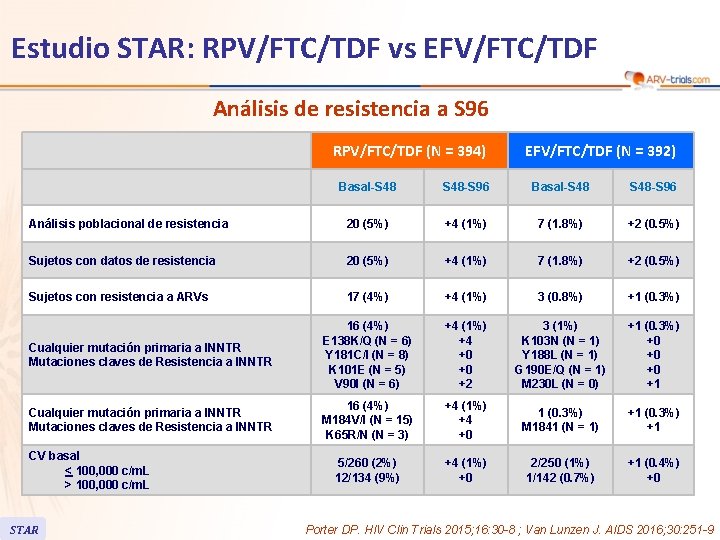
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Análisis de resistencia a S 96 RPV/FTC/TDF (N = 394) EFV/FTC/TDF (N = 392) Basal-S 48 -S 96 Análisis poblacional de resistencia 20 (5%) +4 (1%) 7 (1. 8%) +2 (0. 5%) Sujetos con datos de resistencia 20 (5%) +4 (1%) 7 (1. 8%) +2 (0. 5%) Sujetos con resistencia a ARVs 17 (4%) +4 (1%) 3 (0. 8%) +1 (0. 3%) Cualquier mutación primaria a INNTR Mutaciones claves de Resistencia a INNTR 16 (4%) E 138 K/Q (N = 6) Y 181 C/I (N = 8) K 101 E (N = 5) V 90 I (N = 6) +4 (1%) +4 +0 +0 +2 3 (1%) K 103 N (N = 1) Y 188 L (N = 1) G 190 E/Q (N = 1) M 230 L (N = 0) +1 (0. 3%) +0 +0 +0 +1 Cualquier mutación primaria a INNTR Mutaciones claves de Resistencia a INNTR 16 (4%) M 184 V/I (N = 15) K 65 R/N (N = 3) +4 (1%) +4 +0 1 (0. 3%) M 1841 (N = 1) +1 (0. 3%) +1 5/260 (2%) 12/134 (9%) +4 (1%) +0 2/250 (1%) 1/142 (0. 7%) +1 (0. 4%) +0 CV basal < 100, 000 c/m. L > 100, 000 c/m. L STAR Porter DP. HIV Clin Trials 2015; 16: 30 -8 ; Van Lunzen J. AIDS 2016; 30: 251 -9

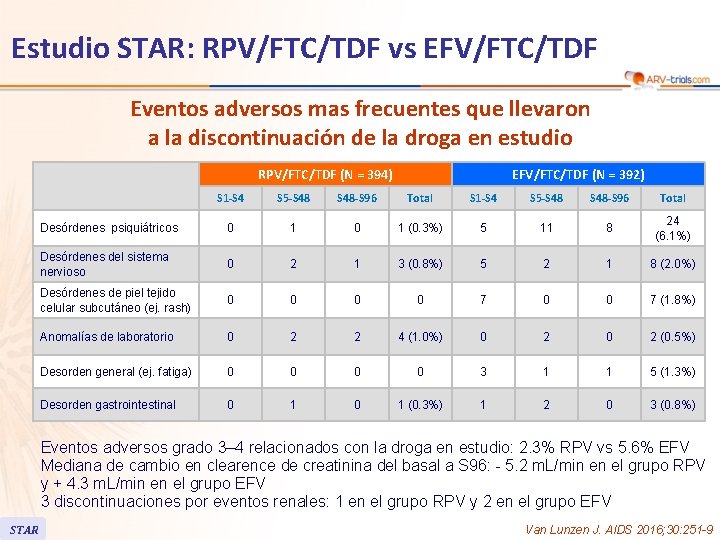
Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF Eventos adversos mas frecuentes que llevaron a la discontinuación de la droga en estudio RPV/FTC/TDF (N = 394) EFV/FTC/TDF (N = 392) S 1 -S 4 S 5 -S 48 -S 96 Total Desórdenes psiquiátricos 0 1 (0. 3%) 5 11 8 24 (6. 1%) Desórdenes del sistema nervioso 0 2 1 3 (0. 8%) 5 2 1 8 (2. 0%) Desórdenes de piel tejido celular subcutáneo (ej. rash) 0 0 7 (1. 8%) Anomalías de laboratorio 0 2 2 4 (1. 0%) 0 2 (0. 5%) Desorden general (ej. fatiga) 0 0 3 1 1 5 (1. 3%) Desorden gastrointestinal 0 1 (0. 3%) 1 2 0 3 (0. 8%) Eventos adversos grado 3– 4 relacionados con la droga en estudio: 2. 3% RPV vs 5. 6% EFV Mediana de cambio en clearence de creatinina del basal a S 96: - 5. 2 m. L/min en el grupo RPV y + 4. 3 m. L/min en el grupo EFV 3 discontinuaciones por eventos renales: 1 en el grupo RPV y 2 en el grupo EFV STAR Van Lunzen J. AIDS 2016; 30: 251 -9

Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF § Cuestionario Índice de Síntomas HIV a S 96 – RPV/FTC/TDF: significativa reducción en la ocurrencia de 18/20 síntomas vs basal (p < 0. 039) – EFV/FTC/TDF: significativa reducción en la ocurrencia de 7/20 síntomas vs basal (p < 0. 033) – Significativa diferencia entre grupos en la ocurrencia de síntomas vs basal para 8 síntomas, todos favoreciendo a RPV/FTC/TDF § Satisfacción global (cuestionario de satisfacción al tratamiento de HIV) a S 96 – Elevado en ambos grupos § Calidad de vida (SF-12 V 2) – La diferencia entre grupos en la mediana de cambio desde el basal a S 96 para el score compuesto de salud física fue no significativa – La diferencia para el score compuesto de salud mental fue significativa, favoreciendo a RPV/FTC/TDF (p = 0. 014) STAR Van Lunzen J. AIDS 2016; 30: 251 -9

Estudio STAR: RPV/FTC/TDF vs EFV/FTC/TDF § Conclusiones a S 96 – En adultos HIV+ naïve de tratamiento, a 96 semanas, RPV/FTC/TDF demostró no inferioridad en eficacia y mejor tolerabilidad que EFV/FTC/TDF • Diferencias significativas en éxito virológico entre los grupos con CV ≤ 100, 000 c/m. L y > 200 CD 4/mmm 3 podrían deberse a la mayor tasa de discontinuación por eventos adversos en el grupo EFV/FTC/TDF • La mayor tasa de fallo virológico observadas para RPV/FTC/TDF con CV basal > 500 000 c/m. L y CD 4+ ≤ 200/mm 3 fueron principalmente por la mayor tasa de discontinuación por falta de eficacia en este grupo (limitación: bajo numero de pacientes en estas categorías) – Las tasas de desarrollo de resistencia a S 96 fueron bajas (5. 3% RPV/FTC/TDF; 1. 0% EFV/FTC/TDF) con infrecuente emergencia de resistencia luego de S 48 STAR • Desarrollo de resistencia al fallo: 88% RPV/FTC/TDF vs 44% EFV/FTC/TDF; la resistencia en el grupo RPV/FTC/TDF fue mas frecuente si la CV basal era > 100, 000 c/m. L – Mejor seguridad y perfil de tolerabilidad de RPV/FTC/TDF vs. EFV/FTC/TDF luego de 96 semanas de tratamiento (limitación: estudio de etiqueta abierta) Van Lunzen J. AIDS 2016; 30: 251 -9