Combustion 1re partie Notions Guili septembre 2016 I

Combustion (1ère partie) Notions Guilié septembre 2016

I Rappels (structure de la matière, forces naturelles) I-1 Généralités Atome = Protons masse 1 g/mole charge positive Noyau : Neutrons masse 1 g/mole neutre + Électrons: Guilié septembre 2016 Masse faible charge négative identique proton

Même nombre d’électrons manquants sur la dernière couche =>mêmes propriétés chimiques Tableau périodique Nb protons = N° atomique Nb nucléons = masse atomique Même nombre couches Gaz rares Couches saturées Guilié septembre 2016
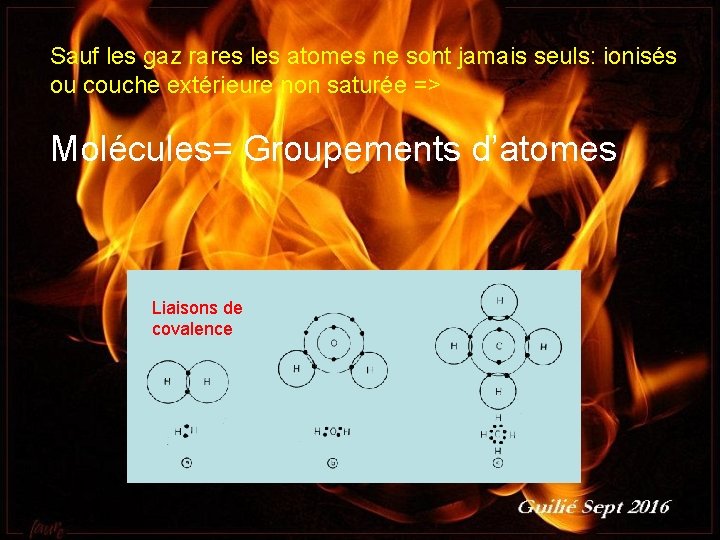
Sauf les gaz rares les atomes ne sont jamais seuls: ionisés ou couche extérieure non saturée => Molécules= Groupements d’atomes Liaisons de covalence Guilié septembre 2016
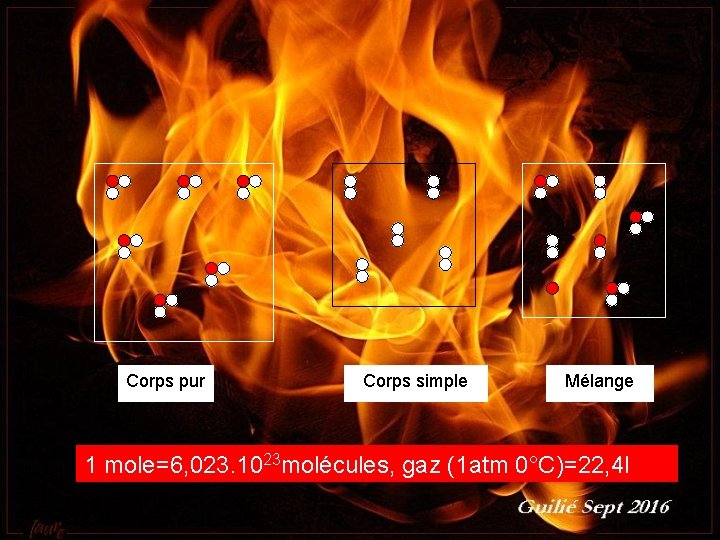
Corps pur Corps simple Mélange 1 mole=6, 023. 1023 molécules, gaz (1 atm 0°C)=22, 4 l Guilié septembre 2016

I-2 Quelques ordres de grandeur : Diamètre atomique : 1 Amström (10 -10 m) (molécules même ordre) Diamètre noyau, nucléons et électrons : 2. 10 -5 Amström (10. 000 à 50000 fois moins) Liquides, solides 3 Amström Distance intermoléculaire => denses et incompressibles Gaz 30 Amström Vitesse 700 m/s forces nucléaires : 1013 J/mole (20. 000 xchimie) forces électrostatiques inter atomiques: 5. 105 J/mole (chimie) forces intermoléculaires: 5. 104 J/mole (Chg de phase) Guilié septembre 2016

II Équations chimiques globales Avant: -stable mavant=maprès Après: +stable 3 C+1 O+1 OO 1 COO+1 C+1 CO 3 C+O+O 2 CO 2+C+CO Guilié septembre 2016

Équilibrer une équation chimique H 2+O 2 H 2 O Même nb d’atomes de même espèce de chaque côté H 2+(1/2)O 2 H 2 O : c’est équilibré Mélange stœchiométrique: Tout le mélange initial peut devenir produits de réaction complète C + 2 02 C 02 + 02 il y a trop d'oxygène 2 C + 02 C 02 + C il y a trop de carbone C + 02 C 02 le mélange C+O 2 est stœchiométrique Équilibrer l’équation de la réaction complète Guilié septembre 2016

II-2 Dosage: Équilibrons: Cx. Hy + O 2 CO 2 + H 2 O Cx. Hy + (x + y/4) O 2 x CO 2 + (y/2) H 2 O , Pouvoir comburivore = Q comburant Q combustible Liquide ou solide Gaz Guilié septembre 2016

Pour les liquides ou les solides nous utiliserons aussi: En Nm 3 d’air /kg Pour un mélange quelconque: richesse R et facteur d'air l: Guilié septembre 2016 e=l-1 : excès d’air

Combustions d'hydrocarbures dans l’air Air=78, 084% N 2+ 20, 9476% O 2+ 0, 934% Ar+ 0, 0314% CO 2+ 0, 001818%Ne. . . ~ 79, 05%N 2+20, 95%O 2 Cx. Hy + (x+ y/4) (O 22 + 3, 77 N 22) x. CO CO 22++ (y/2) H 22 O + 3, 77 (x +y/4)N N 22 diluant Combustibles gazeux Combustibles liquides ou solides Guilié septembre 2016
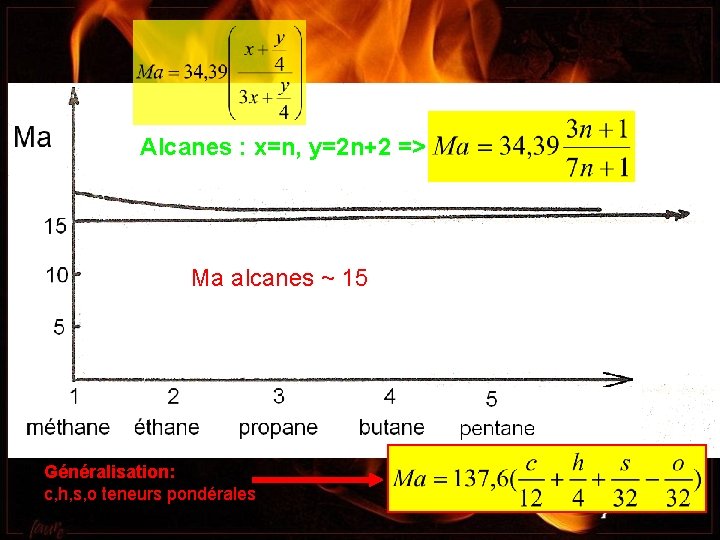
Alcanes : x=n, y=2 n+2 => Ma alcanes ~ 15 Généralisation: c, h, s, o teneurs pondérales Guilié septembre 2016

Exemples: essence : c=84% h=16% Ma=15, 1 gaz-oil ou fuel domestique : c=85%, h=15% (autre<0, 3%) Ma=15 fuel lourd c=85, 9% h=10, 5% s=3% n=0, 24 o=0, 36% Ma=13, 6 Les pouvoirs comburivores massiques sont pratiquement identiques pour tous les hydrocarbures: Ma = 15 Pour les alcools ils sont très différents : Méthanol CH 3 OH : c=12/32=37, 5%, h=4/32=12, 5%, O=16/32=50% Ma=6, 45 Ethanol C 2 H 5 OH : c=24/46=52%, h=6/46=13%, O=16/46=35% Ma=8, 93 Guilié septembre 2016

II-3 Composition théorique des produits de combustion Nécessité du calcul • 1°) Calcul du Cp des produits de combustion pour déterminer la chaleur sensible perdue • 2°) Connaître XH 2 O pour connaître la chaleur latente perdue • 3°) Faire un diagnostique de la combustion Guilié septembre 2016

Hypothèses possibles: 1°) Combustion complète du carburant : l>1 (Tout le C et H du carburant devient CO 2 et H 2 O) 2°) Combustion complète de l’oxygène : R>1 Tout l’H devient H 2 O, C devient CO et CO 2, et pas d’O 2 restant 3°) Combustion incomplète: Il reste toutes les espèces CO, O 2, CH… Calcul de la composition théorique: Cx. Hy + (O 2+3, 77 N 2) l>1 1 l(x+y/4) l<1 1 l(x+y/4) Guilié septembre 2016 CO 2 x + H 2 O + O 2 + y/2 (l-1)(x+y/4) x-2(1 -l)(x+y/4) y/2 0 CO + N 2 0 3, 77 l(x+y/4) 2(1 -l)(x+y/4) 3, 77 l(x+y/4)
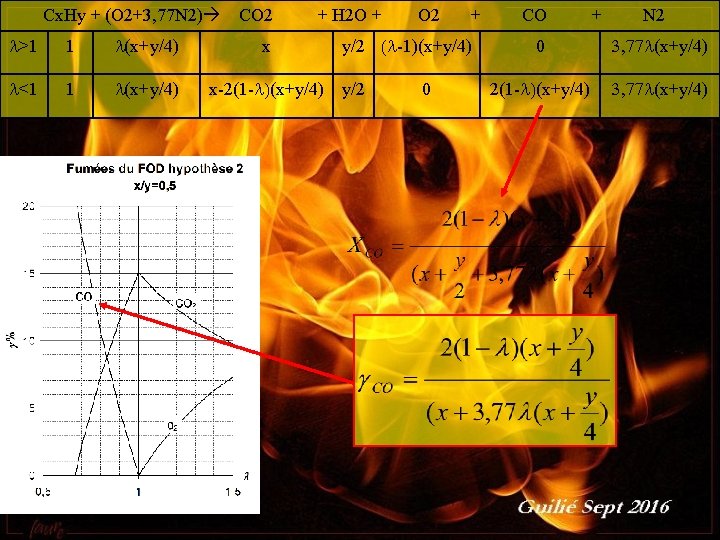
Cx. Hy + (O 2+3, 77 N 2) l>1 1 l(x+y/4) l<1 1 l(x+y/4) Guilié septembre 2016 CO 2 x + H 2 O + O 2 + y/2 (l-1)(x+y/4) x-2(1 -l)(x+y/4) y/2 0 CO + N 2 0 3, 77 l(x+y/4) 2(1 -l)(x+y/4) 3, 77 l(x+y/4)
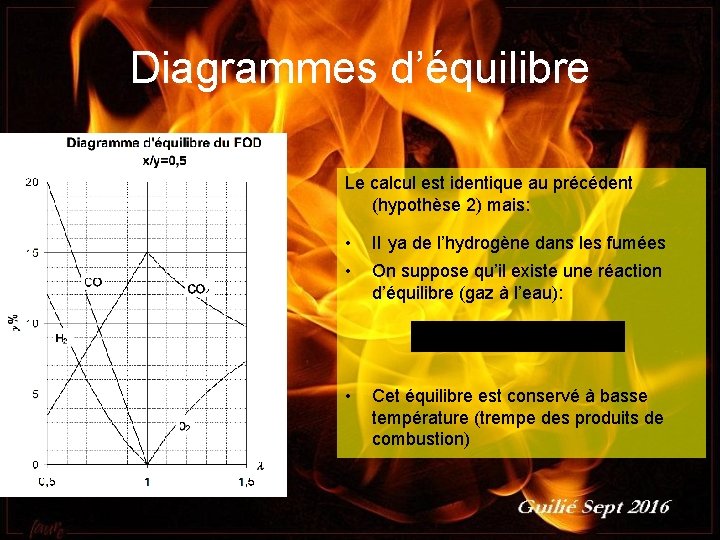
Diagrammes d’équilibre Le calcul est identique au précédent (hypothèse 2) mais: Guilié septembre 2016 • Il ya de l’hydrogène dans les fumées • On suppose qu’il existe une réaction d’équilibre (gaz à l’eau): • Cet équilibre est conservé à basse température (trempe des produits de combustion)

III Thermodynamique de la combustion III-1 premier principe Combustion R Réactants Travail We Chaleur Qe P Produits de combustion Premier principe en système fermé We+Qe=UP-UR Guilié septembre 2016

Conservation de la quantité de matière: m. P=m. R=m Origine des fonctions thermodynamiques (indice 0) U’P= UP-UP 0 , U’R= UR-UR 0 1 er Ppe SF: We+Qe = U’P -U’R+(UP 0 -UR 0)=> We+Qe -( UP 0 -UR 0)= U’P - U’R Définition: chaleur de réaction isochore : Qc= -( UP 0 -UR 0)= UP 0 -UR 0 Premier principe SF avec combustion: We+Qe+Qc= U’P - U’R Qc >0 : réaction exothermique (cas des combustions) (Produits réaction exothermique plus stables : U plus faible) Guilié septembre 2016

Calcul du second membre: Hypothèse GP: Hypothèse GI : u’P - u’R =Cv. P(TP-298)- Cv. R(TR-298) Cv. P Cv. R TR 298 K. Guilié septembre 2016 =>u’P - u’R =Cv. P(TP-TR)
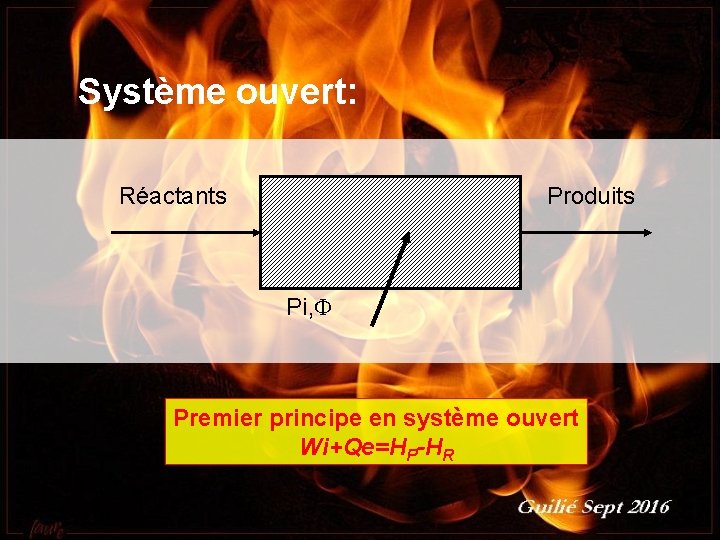
Système ouvert: Réactants Produits Pi, F Premier principe en système ouvert Wi+Qe=HP-HR Guilié septembre 2016

On pose H'R=HR-HR 0 et H'P=HP-HP 0 HR 0 et HP 0 enthalpies de réf. des gaz frais et produits de combustion La chaleur de réaction isobare. Q’c=-(HP 0 - HR 0) Le premier principe système ouvert avec combustion: Wi+Qe+Q'c=DH'+DEp+DEc Sous forme de puissance et en généralisant : Pi+F+Pc=Sqms(h’s+eps+ecs)-Sqme(h’e+epe+ece) Guilié septembre 2016

Chaleur de combustion à pression et à volume constant: H=U+p. V =>Q'c=HR 0 - HP 0=UR 0 -UP 0+p 0 VR 0 – p 0 VP 0) =Qc +p 0 VR 0 – p 0 VP 0 Hypothèse de GP: Dp. V=Dn. RT =>Q’c=Qc+(n. R-n. P). RT 0 =>Qc=Q’c à 0, 1% près => négligé Calcul du second membre: Hypothèse de GP: Hypothèse GI: h’P - h’R =Cp. P(TP-298)- Cp. R(TR-298) Guilié septembre 2016 Cp. P Cp. R=>h’P - h’R =Cp. P(TP-TR)

Enthalpie de formation: Référence: corps simple dans son état le plus stable= (Hcorps simple)25°, 1 atm =0 Enthalpie de formation=Hf 0= (Hcorps composé)25°, 1 atm =-Q’c Q’c=241, 8 k. J/mole Exemple: => Hfo. H 2 O=-241, 8 k. J/mole Autres exemples: Guilié septembre 2016 Hf 0 CO 2=-393, 5 k. J/mole Hf 0 CH 4=-74, 9 k. J/mole

Énergie de liaison: Liaison C-H C-C C=C C-O H-H O=O C=O Energie k. J/mole 415 345 609 357 432 462 493 803 Graphite Cgaz 718 Exemple: briser 1 liaison H-H, ½ liaison O=O et recréer 2 liaisons O-H. => Guilié septembre 2016

Pour calculer la chaleur de réaction Q’c une combustion quelconque il suffit d’écrire: Q’c=HR 0 - HP 0 HR 0 est la somme des enthalpies de formation des réactants et HP 0 celle des produits (affectées des coefficients stœchiométriques) Guilié septembre 2016

II-2 Pouvoir calorifique: Quantité de combustible en: - Nm 3 pour les gaz - kg pour les liquides ou les solides Notation: PC Inférieur IP, IV (eau fumée vapeur) PC Supérieur: PP, PV (eau fumée condensée) Guilié septembre 2016

Chaleur de combustion massique et rendement: Trois cas: - Combustion complète du carburant (l>1): - Combustion totale de l’oxygène (l<1): Guilié septembre 2016
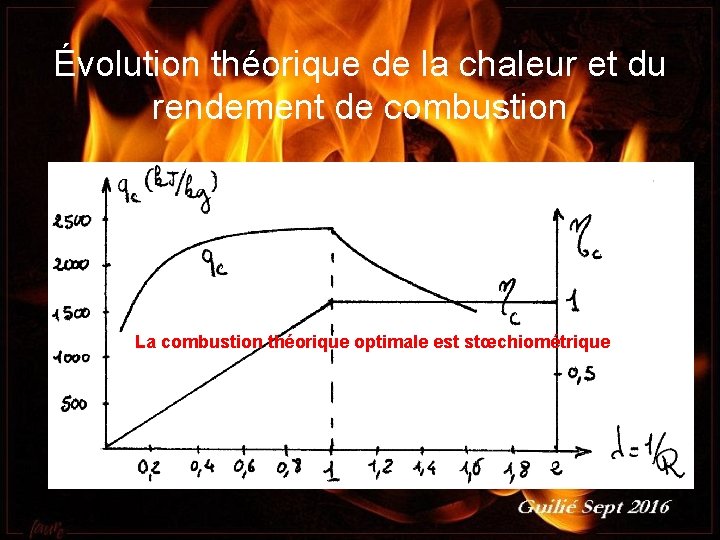
Évolution théorique de la chaleur et du rendement de combustion La combustion théorique optimale est stœchiométrique Guilié septembre 2016

- Combustion incomplète: PC=PCM-PI Avec : PCM =qm. CIp (liq ou solide), gaz: qv. CI’p Imbrulés gazeux=>qv. I=XI. qv. P g. I: Teneurs par rapport aux fumées sèches: XI=g. I. (1 -XH 2 O) PI =qv. P. (1 -XH 2 O)S g. I. I’p. I Guilié septembre 2016

PI =qv. P. (1 -XH 2 O)S g. I. I’p. I Valeurs pratiques approximatives: qv. P=vp. qmp=0, 78. qm. P (qm. P=qma+qmc=(1+l. Ma)qmc) XH 2 O =13% (hydrocarbure lourd) à 19% (méthane) Si l>1: I’p. CO=12600 k. J/Nm 3 et I’p. H 2=10760 k. J/Nm 3 Plus précisément, on verra (2ème partie) que : qv. P. (1 -XH 2 O) qui est le débit des fumées sèches (en Nm 3/s) peut s’exprimer aussi par qm. CV’FS pour les liquides et les solides ou par qvc. V’FS pour les gaz (avec V’FS=VFS +e. Va) Guilié septembre 2016

Les analyseurs ne donnent que g. CO=> Réaction d’équilibre (gaz à l’eau) à haute température: Pour les moteurs (équilibre supposé à 1850°C) : g. CO /g. H 2 =8 x/y Pour les fours ou chaudières (1450°C) : g. CO /g. H 2 =5 x/y Pour les hydrocarbures lourds : x/y~1/2. Exemple pour le fuel c=86%, h=13, 3%, x=c /12, y=h x/y=0, 54 Valeurs de x/y, v. P, XH 2 O pour quelques combustibles H 2 CH 3 OH CH 4 C 2 H 5 OH C 3 H 8 C 4 H 10 C 8 H 18 Ess FOD FO Bois Char. C x/y 0 0, 252 0, 25 0, 33 0, 37 0, 44 0, 54 0, 64 0 , 72 2, 24 infini v. FN 0, 91 0, 814 0, 811 0, 796 0, 79 0, 78 0, 77 0, 76 0, 74 0, 72 35 23 19 18 15 15 14 13 12 12 10 6, 5 0 (Nm 3/kg) XH 2 O (%) Guilié septembre 2016
- Slides: 32