Colegio Agustiniano El Bosque Un proyecto educativo nico

Colegio Agustiniano - El Bosque Un proyecto educativo único y propio Química /2° Medio Reactivo limitante en exceso y % de rendimiento Química 2º Medio
Objetivo El objetivo de aprendizaje a alcanzar es: § Establecer, aplicar y resolver relaciones cuantitativas utilizando los conceptos de reactivos limitantes, en exceso y % de rendimiento. Contenidos § Reactivo limitante. § Reactivo en exceso. § % de Rendimiento.

Instrucciones § Iniciaremos con la sección Antes de comenzar que permite reforzar los contenidos relevantes de la clase anterior. § Con la actividad Recordando iniciaremos este nuevo estudio sobre Reactivo limitante, reactivo en exceso y % de rendimiento , aquí se rescatarán los conocimientos previos sobre relaciones estequiométricas y cálculos estequiométricos que servirán para construir los nuevos aprendizajes. § Luego se desarrollarán los contenidos sobre reactivo limitante y reactivo en exceso, además de % de rendimiento. Cada uno de estos conceptos se encuentran apoyados con videos, páginas del texto escolar de Química 1º medio y los llamados de Atención que te avisan donde poner mayor énfasis en los contenidos que te permitirán resolver la guía de ejercitación. § Para saber cuánto has aprendido sobre reactivo limitante y en exceso así como % de rendimiento, al final del ppt, te encontrarás con una sección llamada ¿Qué aprendiste? , la que te permitirá evaluar tus nuevos conocimientos. Esta sección está apoyada por un Solucionario

Antes de comenzar Para reforzar los contenidos de la clase anterior, trabajaremos la siguiente pregunta. Para la ecuación de formación del amoniaco determinar: N 2(g) + 3 H 2(g) → 2 NH 3(g) A. ¿Cuántos litros de amoníaco se producen a partir de 100 g de N 2 ? B. ¿Qué masa de H 2 se requieren para formar 5 L de NH 3? C. ¿Cuántos mol y moléculas de NH 3 se producirán si hacen reaccionar 6 g de N 2 con suficiente H 2? Los pasos a seguir para responder a este tipo de preguntas son los siguientes : 1. Comprobar que la ecuación se encuentre balanceada. 2. Rescatar toda la información estequiométrica que nos entregue la ecuación. 3. Reconocer qué tipo de relaciones estequiométricas vamos a trabajar. Por ejemplo relaciones del tipo: mol-volumen; mol-moléculas o tal vez molmasa. 4. Desarrollo matemático de cada una de las preguntas. 5. Finalmente construir la respuesta.

Recordando Es importante que reconozcas aquello que sabes en relación con las temáticas que trabajaremos , dado que tus concepciones previas son el cimiento sobre el cual construiremos estos nuevos aprendizajes. Te invito a resolver las preguntas formuladas en la diapositiva anterior, para la ecuación de formación del amoníaco. Solucionario

Solucionario
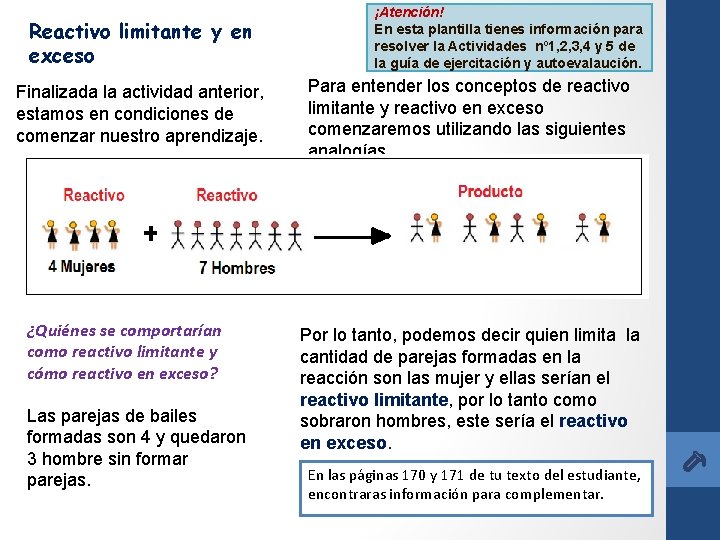
Reactivo limitante y en exceso Finalizada la actividad anterior, estamos en condiciones de comenzar nuestro aprendizaje. ¿Quiénes se comportarían como reactivo limitante y cómo reactivo en exceso? Las parejas de bailes formadas son 4 y quedaron 3 hombre sin formar parejas. ¡Atención! En esta plantilla tienes información para resolver la Actividades nº 1, 2, 3, 4 y 5 de la guía de ejercitación y autoevalaución. Para entender los conceptos de reactivo limitante y reactivo en exceso comenzaremos utilizando las siguientes analogías. Por lo tanto, podemos decir quien limita la cantidad de parejas formadas en la reacción son las mujer y ellas serían el reactivo limitante, por lo tanto como sobraron hombres, este sería el reactivo en exceso. En las páginas 170 y 171 de tu texto del estudiante, encontraras información para complementar.

Reactivo en Exceso Reactivo Limitante Se llama reactivo limitante al que se ha consumido por completo en una reacción química y determina o limita la cantidad de producto formado. Se llama reactivo en exceso al que se encuentra en mayor cantidad que lo necesario para reaccionar con la cantidad de reactivo limitante, o sea es el reactante que sobra, el queda sin reaccionar. Si lo llevamos a un ejemplo químico, este dice que debemos formar la siguiente ecuación: Para formar esta reacción contamos con 5 átomos de Na y 2 átomos de Cl, cuál de los dos reactivos se comportara como el reactivo limitante y quién como el reactivo en exceso. Si representamos lo anterior con esferas (quienes representan a los átomos), tenemos: Se forman solo 2 moléculas de Na. Cl y ¡Atención! En esta plantilla tienes información para resolver la Actividades nº 1, 2, 3, 4 y 5 de la guía de ejercitación y autoevalaución. quedan 3 átomos de Na, por lo tanto podemos concluir que el reactivo quien limita esta reacción o reactivo limitante es el Cl y el Na es el reactivo en exceso. Para profundizar el tema reactivo limitante y en exceso puedes ver el video: https: //www. youtube. com/watch? v=2 x. Ry 35 V e 9 c. M
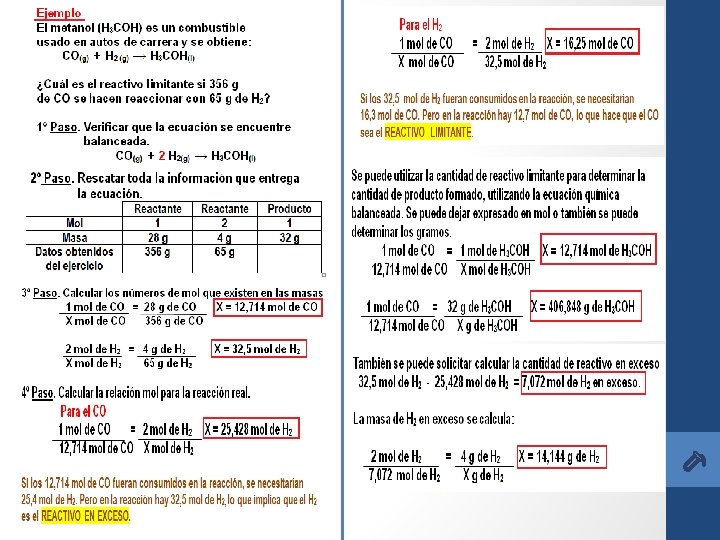
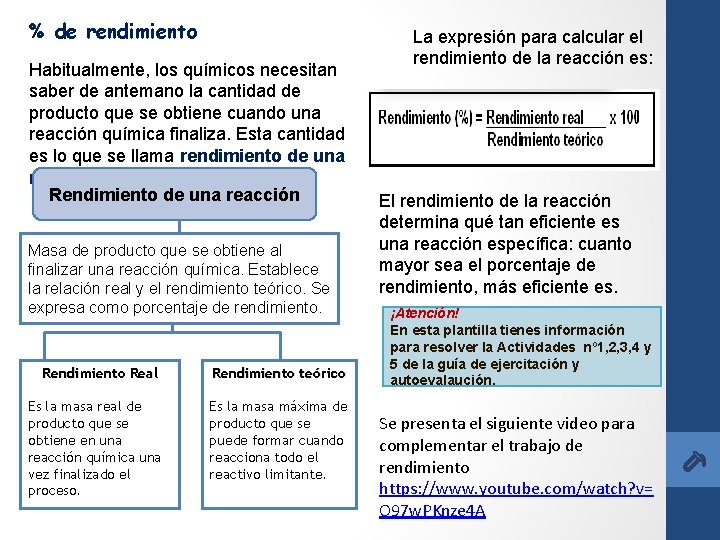
% de rendimiento Habitualmente, los químicos necesitan saber de antemano la cantidad de producto que se obtiene cuando una reacción química finaliza. Esta cantidad es lo que se llama rendimiento de una reacción. Rendimiento de una reacción Masa de producto que se obtiene al finalizar una reacción química. Establece la relación real y el rendimiento teórico. Se expresa como porcentaje de rendimiento. Rendimiento Real Rendimiento teórico Es la masa real de producto que se obtiene en una reacción química una vez finalizado el proceso. Es la masa máxima de producto que se puede formar cuando reacciona todo el reactivo limitante. La expresión para calcular el rendimiento de la reacción es: El rendimiento de la reacción determina qué tan eficiente es una reacción específica: cuanto mayor sea el porcentaje de rendimiento, más eficiente es. ¡Atención! En esta plantilla tienes información para resolver la Actividades nº 1, 2, 3, 4 y 5 de la guía de ejercitación y autoevalaución. Se presenta el siguiente video para complementar el trabajo de rendimiento https: //www. youtube. com/watch? v= O 97 w. PKnze 4 A

¿Qué aprendiste? En las páginas 172 y 173, encontraras información para complementar. El tricloruro de fósforo (PCl 3) es un compuesto muy utilizado a nivel industrial para la preparación de compuestos organofosforados. Determinar el reactivo limitante, reactivo en exceso y % de rendimiento, cuando se hacen reaccionar 124 g de tetrafósforo (P 4) con 323 g de gas cloro (Cl 2). La ecuación que representa dicha reacción es: P 4(s) + 6 Cl 2(g) → 4 PCl 3(l) La masa de tricloruro de fósforo formado realmente es de 350 g.

Solucionario
- Slides: 12