Colegio Agustiniano El Bosque Un proyecto educativo nico

Colegio Agustiniano - El Bosque Un proyecto educativo único y propio Química /2° Medio Cantidades químicas Química 2º Medio

Los objetivos de aprendizaje a alcanzar son: Objetivos v Representar reacciones químicas en una ecuación, reconociendo reactantes y productos. v Explicar el concepto estequiometría. v Identificar y trabajar la magnitud atómica: masa atómica. v Relacionar el mol como unidad de cantidad de sustancias con el número de Avogadro. Los contenidos que estudiaremos son: v ¿Qué es la estequiometría? v Magnitud atómica: masa atómica. v Mol y número de Avogadro.

Instrucciones § Iniciaremos este nuevo estudio sobre Cantidades químicas, con la actividad Recordando, Recordando aquí se rescataran los conocimientos previos sobre átomos, moléculas y ecuaciones químicas y su composición, que servirán en la construcción de los nuevos conocimientos a § Luego se desarrollan los contenidos sobre estequiometría, desarrollar. magnitudes atómicas: masa atómica; mol y número de Avogadro. Cada uno de estos conceptos se encuentran apoyados con videos y páginas del texto escolar de Química 1º medio, para entender con mayor facilidad esta nueva información. § Para saber cuanto has aprendido sobre Cantidades químicas, al final del ppt, te encontrarás con una sección llamada ¿Qué aprendiste? , la que te servirá para conocer cuánto has aprendido sobre este tema. Esta sección está apoyada por un Solucionario § Al final del ppt te encontrarás con link que te llevará a la Autoevaluación, Autoevaluación la cual se encuentra en el Classroom y te permitirá saber tus logros de aprendizaje sobre este tema.
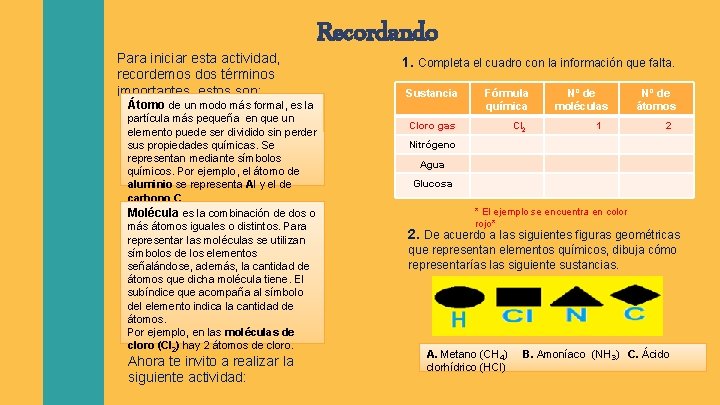
Para iniciar esta actividad, recordemos dos términos importantes, estos son: Recordando Átomo de un modo más formal, es la partícula más pequeña en que un elemento puede ser dividido sin perder sus propiedades químicas. Se representan mediante símbolos químicos. Por ejemplo, el átomo de aluminio se representa Al y el de carbono C. Molécula es la combinación de dos o más átomos iguales o distintos. Para representar las moléculas se utilizan símbolos de los elementos señalándose, además, la cantidad de átomos que dicha molécula tiene. El subíndice que acompaña al símbolo del elemento indica la cantidad de átomos. Por ejemplo, en las moléculas de cloro (Cl 2) hay 2 átomos de cloro. Ahora te invito a realizar la siguiente actividad: 1. Completa el cuadro con la información que falta. Sustancia Fórmula química Cloro gas Cl 2 Nº de moléculas 1 Nº de átomos 2 Nitrógeno Agua Glucosa * El ejemplo se encuentra en color rojo* 2. De acuerdo a las siguientes figuras geométricas que representan elementos químicos, dibuja cómo representarías las siguiente sustancias. A. Metano (CH 4) clorhídrico (HCl) B. Amoníaco (NH 3) C. Ácido

¿Qué es la estequiometría? Vienen de una reacción química, las cuales se representan de una ecuación química. ¿Cómo se representan las ecuaciones químicas? ¿Qué información nos entrega? La medición de la cantidad de una sustancia es algo que haces todos los días. Supón por un momento que eres un químico y que estas tratando de desarrollar un medicamento, para ello se realizan experimentos y cálculos. Cada sustancia que usamos en el laboratorio de química se mide de modo que funcione adecuadamente en un experimento. La fórmula de una sustancia dice el número y tipos de átomos que Para complementar el tema de ecuaciones química, visita el siguiente video: https: //www. youtube. com/watch? v=Gp. KNu. ZBZf. Y Los químicos en los laboratorios e industrias, deben calcular la cantidad de reactantes necesarias para elaborar un determinado producto. ¿Qué rama de la química se encarga de realizar los cálculos necesarios para obtener un nuevo producto? La rama de la química que estudia las relaciones cuantitativa o ponderales entre los reactantes y productos que participan en una reacción química se conoce como «Estequiometría» .

Para comenzar el estudio de la estequiometría, era importante recordar los conceptos de átomos, molécula, reacción química y ecuación química, ¡Ahora entiendes porque partimos con la actividad Recordando! Para explicar la relación entre reactantes y productos, comenzaremos a estudiar las magnitudes atómicas, las que corresponden al conjunto de medidas de los átomos. Magnitudes atómicas 1. Unidad de masa atómica (u. m. a) Los científicos del siglo XX no podían obtener el valor absoluto de la masa de un átomo y la comparaban con la masa del mismo número de átomos de otros elemento que tomaban como referencia. En 1961 la IUPAC, acordó determinar la masa atómica de los elementos tomando como referencia la masa del isótopo* de C 12 a esta la llamó unidad de masa atómica (u. m. a). *Se denomina isótopos a los átomos de un mismo elemento, cuyos núcleos tienen una cantidad diferente de La u. m. a, corresponde a la doceava parte de la masa de un átomo de C-12. Según esta definición, la masa de 1 u. m. a será igual a: 1 uma = 1, 6606 x 10 -27 kg 1 uma = 1, 6606 x 10 -24 g Veamos su aplicación en el siguiente Ejemplo - 1. Calcular la masa del átomo de aluminio (Al) en gramos, sabiendo que equivale a 26, 98 u. m. a. 1 u. m. a = 1, 66 x 10 -24 g 26, 98 u. m. a Xg X = 26, 98 x 1, 66 x 10 -24 g = 4, 48 x 10 g Ejemplo-2 sería el siguiente. Otro Calcular la masa del átomo de sodio (Na) en u. m. a, si su masa en gramos es 3, 81 x 10 -23 g. 1 u. m. a = 1, 66 x 10 -24 g X 3, 81 x 10 -23 g X = 3, 81 x 10 -23 / 1, 66 x 10 -24 u. m. a = 23 Te invito, vayas a la guía de ejercicios y realices las u. m. a 5 A y 5 B. ¡Terminaste! Ahora puedes actividades 23 revisar el solucionario. Compara tus respuestas y corrige aquello en que te hayas equivocado.

Para calcular la masa atómica, la contribución de cada isótopo se determina al multiplicar la masa de cada isótopo por su abundancia y sumar los resultados. Por ejemplo, en una muestra de cloro (Cl) tiene una masa de 75, 78% de los átomos de Cl tienen una masa de 34, 969 u. m. a y 24, 22% de los átomos de Cl tienen una masa de 36, 966 u. m. a. Masa atómica del Cl = 34, 969 x 75, 78 + 36, 966 x 24, 22 100 Masa atómica del Cl = 35, 45 u. m. a La masa atómica 35, 45 u. m. a es la masa promedio ponderada de una muestra de átomos de Cl. 35, 45 Cl Masa atómica La masa atómica que aparece en la tabla periódica corresponde al promedio de las amasa atómicas de los isótopos de cada elemento y no a la masa en gramos. 2. Mol ¿Te has preguntado lo pequeño que debe ser un átomo? Casi es imposible poder imaginarlo. Por lo mismo, no se puede obtener la masa de un solo átomo. Para ello se ha creado una magnitud que indica el número de partículas que se encuentran en una porción de materia. Esta magnitud es la cantidad de sustancia y su unidad es el mol. Un mol es la cantidad de sustancia que hay en 6, 022 x 1023 entidades elementales (átomos, iones, moléculas, electrones, entre otras). Un mol de cualquier elemento contiene el mismo número de partículas, pero su masa depende del elemento de que se trate. Los videos presentados, te servirán para profundizar los contenidos de u. m. a y mol. • https: //www. youtube. com/watch? v=_EJYu. Qv. A F 7 I • https: //www. youtube. com/watch? v=dm 4 czxecif U • https: //www. youtube. com/watch? v=Frf. RSi. DGVj

3. Número de Avogadro Este número 6, 022 x 1023 se conoce como número de Avogadro (NA) en honor al físico y químico Amadeo Avogadro. La constante de Avogadro representa la cantidad de átomos, moléculas u otras partículas que hay un mol de las mismas. Así: NA = 6, 022 x 1023 entidades elementales (átomos, iones, moléculas, electrones, entre Tabla. Número de partículas en muestras de un otros). mol Este número también se puede escribir: 60220000000000 Sustancia Nº y tipo de partículas ¿Con qué puedes asociar también el número de Avogadro? Distancia de la Tierra al Sol: 149 600 000 km. 1 mol de átomos de carbono (C) 6, 022 x 1023 átomos de C 1 mol de iones de hierro (Fe 3+) 6, 022 x 1023 iones de Fe 3+ 1 mol de molécula de sacarosa (C 12 H 22 O 11) 6, 022 x 1023 molécula de C 12 H 22 O 11 1 mol de vitamina C (C 6 H 8 O 6) 6, 022 x 1023 molécula de vitamina C Para resumir lo estudiado hasta ahora, te dejo los siguientes vídeos • https: //www. youtube. com/watch? v=Qo. CWPLBJSGI • https: //www. youtube. com/watch? v=Pi. Ggc. Qarod. Y

Ejemplo-3. Mol – átomo Calcular el número de átomos que hay en 2, 3 mol de Zn. 1 mol de Zn = 6, 022 x 1023 átomos de Zn 2, 3 mol de Zn X átomos de Zn Ejemplo-5. Mol – iones ¿Cuántos iones de plata (Ag+), existen 5 mol de ión plata? X = 6, 022 x 1023 átomos de Zn x 2, 3 mol de Zn ÷ 1 mol de Zn la 24 guía y realiza actividad 4 de XAhora, = 1, 38 vexa 10 átomos dela. Zn X = 5 mol x 6, 022 x 1023 ion plata ÷ 1 mol de ion la guía de ejercitación. ¿Cómo te fue? Ejemplo-4. Mol – molécula ¿Cuál es la cantidad de sustancia de agua que contiene 2, 60 x 1023 moléculas de agua? 1 mol de agua = 6, 022 x 10 23 moléculas de agua x mol de agua 2, 60 x 10 23 moléculas de agua X = 1 mol de agua x 2, 60 x 1023 moléculas de agua ÷ 6, 022 x 1023 moléculas de agua No olvides que al terminar de revisar este ejemplo, en práctica, X = 0, 43 puedes mol deponerlo las moléculas de agua. trabajando la actividad 3 de la guía de ejercitación. 1 mol de ion plata = 6, 022 x 1023 ion plata 5 mol de ion plata X ion plata 24 comprendiste bien como utilizar la X =Para 3, 01 saber x 10 si ion plata relación mol-ion, detente a realizar la actividad 2 de la guía de ejercitación. ¡No olvides! Una vez que termines de realizar las actividades sugeridas en la guía de ejercitación, revisa el solucionario, de esta forma podrás identificar los errores que pudieras haber cometido y corregirlos.

3. Resuelve: 1. Realice un esquema conceptual con los términos: Estequiometría, Magnitudes atómicas; u. m. a; masa atómica; mol y número de Avogadro. A. ¿Qué cantidad de átomos existen en 45 mol de calcio (Ca). B. ¿Cuál es la cantidad de iones cobre (Cu 2+) presentes en 10 mol de iones cobre? 2. Explica con tus palabras los conceptos trabajados en el esquema de la pregunta anterior. C. ¿Cuál es la cantidad de sustancia de metano (CH 4) que contiene 5, 60 x 1023 moléculas de metano? Solucionario Recordando 1. Sustancia Fórmula química Cloro gas Cl 2 Nitrógeno N Agua H 2 O Glucosa C 6 H 12 O 6 Nº de molécula s 2. Nº de átomos 1 ----- 2 1 H=2 O= 1 1 C=6 H=

Solucionario ¿Qué aprendimos sobre cantidades químicas? 1.

Solucionario 3. A. 1 mol de Ca = 6, 022 x 1023 átomos de Ca 45 mol de Ca X átomos de Ca X = 6, 022 x 1023 átomos de Ca x 45 mol de Ca ÷ 1 mol de Ca X = 2, 70 x 10 -25 átomos de Ca 3. B 1 mol de ion cobre = 6, 022 x 1023 ion cobre 10 mol de ion cobre X = 10 mol x 6, 022 x 1023 ion cobre ÷ 1 mol de ion cobre X = 6, 022 x 1024 ion cobre Una vez que hayas trabajado en el ppt, realizado la guía de Cantidades químicas, estas en condiciones de realizar la autoevaluación. Para ello puedes ingresar a través de este enlace: https: //forms. gle/jb. MExt 38 Bt. TF 4 h. F 48 Y ante cualquier consulta, puedes escribirme al correo: quimica 2 med@colegioagustiniano. cl 3. C 1 mol de metano = 6, 022 x 1023 moléculas de metano x mol de metano 5, 60 x 1023 moléculas de metano X = 1 mol de metano x 5, 60 x 1023 moléculas de metano ÷ 6, 022 x 1023 moléculas de metano. X = 0, 93 mol de las moléculas de metano.
- Slides: 12