Cncer de pncreas Dr Roberto delgado R 2

Cáncer de páncreas Dr. Roberto delgado R 2 MI

PROGRAMA HISTORIA EPIDEMIOLOGÍA FACTORES DE RIESGO CUADRO CLINICO DIAGNOSTICO CLASIFICACION TNM FACTORES PRONÓSTICOS SCREENING SEGUIMIENTO

HISTORIA PANCREAS Rufus de Ephesus GRIEGO “PANKREAS” “ PAN DULCE ” “TODO CARNE” Patología Estructural y Funcional. Robins. 7 ma ed. Skandalakis' Surgical Anatomy Cap. 21. Páncreas

Herofilo de Calcedonia (334 -280 a. c) lo describió por primera vez. Galeno describió la irrigación y drenaje venoso Wirsung describió su conducto principal en 1642 Graaf descubrió su secreción en 1664 Vater describe a mayor detalle la papila duodenal, descrito inicialmente por Bidloo. Langerhans en 1869 describe la estructura de la glandula ( islotes ). Whipple en 1935 describe su técnica para reseccion cáncer pancreático a nivel de la cabeza. Sleissenger & Fordtran's Gastrointestinal and Liver Disease, 8 th ed Skandalakis' Surgical Anatomy Cap. 21. Pancreas
Allen O. Whipple Pancreatic Cáncer, M. D. Anderson Solid Tumor Oncology Series, 2002. En 1935 describió 3 casos de resecciòn de tumores de cabeza de páncreas Popularizo la técnica de resecciòn de Tumores en cabeza de páncreas en 2 etapas Importancia Vitamina K

EPIDEMIOLOGÍA Es la 4ª causa de muerte en EUA Hay 40, 000 nuevos casos de cáncer pancreático cada año en EU y 170, 000 casos a nivel mundial 2 da causa de muerte a nivel mundial de neoplasia gastrointestinales después del ca. colo-rectal. Gastroenterol Clin N Am 36 (2007) 831– 849 Annals of Oncology 18 : vii 1–vii 10, 2007
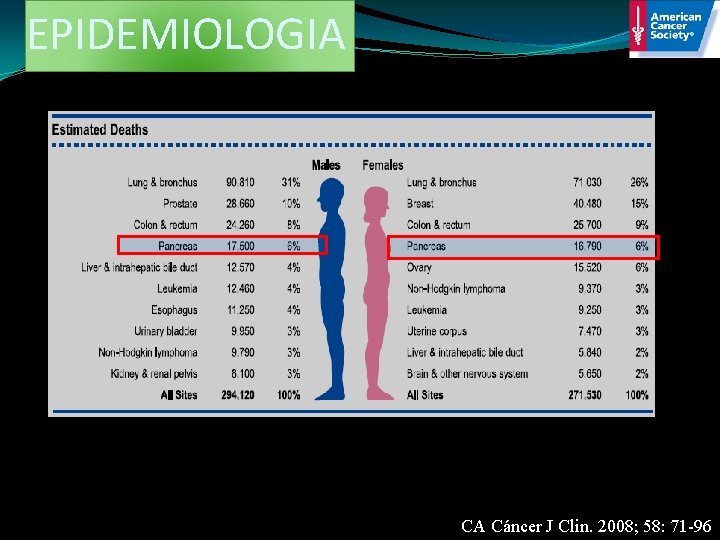
EPIDEMIOLOGIA CA Cáncer J Clin. 2008; 58: 71 -96

EPIDEMIOLOGIA La incidencia del cáncer pancreático incrementa después de los 50 años, y tiene un pico entre la 7ª-8ª década de la vida. Menos del 20% de los pacientes se presentan con tumores locales potencialmente curables. La sobrevida global a 5 años entre los pacientes con cáncer pancreático es <5%. 15 % candidatos a cirugía 3 % Tx Qx curación Pancreatic Cancer. Manuel Hidalgo MD. N Engl J Med. 2010; 362: 1605 -17.

EPIDEMIOLOGIA Relación Hombres-Mujeres 1. 5 -1. Mas frecuente en países desarrollados. Afroamericanos tienen un alto riesgo de desarrollar cáncer pancreático y por lo tanto exhiben altas tasas de mortalidad. Gastroenterol Clin N Am 36 (2007) 831– 849 Jpn J Clin Oncol 2004; 34(5)238– 244
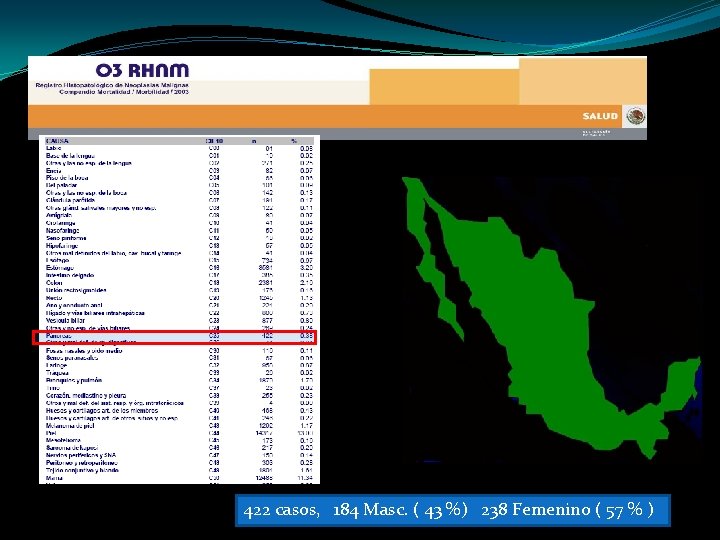
422 casos, 184 Masc. ( 43 %) 238 Femenino ( 57 % )

FACTORES DE RIESGO DE VITA, HELLMAN AND ROSENBERG'S. CANCER. PRINCIPLES & PRACTICE OF ONCOLOGY. 8 TH. LIPPINCOT WILLIAMS & WILKINS.

FACTORES DE RIESGO Br Med J 1994; 309: 901– 11. Jpn J Clin Oncol 2004; 34(5)238– 244

FACTORES DE RIESGO Br Med J 1994; 309: 901– 11. Jpn J Clin Oncol 2004; 34(5)238– 244

Sx hereditarios relac. cáncer pancreático Alto riesgo Sx Peutz-Jegher * ( RR 57 -100) Melanoma Multiple familiar RR 22 Pancreatitis hereditaria Bajo Riesgo Ca colorectal Herd. No asoc. , polipos Ca mama/ovario Poliposos adenomatosa fam. Ataxia telangiectsia Sx Lifraumeni Cancer Res 2004; 64(7): 2634 -8. Dis Mon oct 2004 50: 545 -55 Endocrinol Metab Clin N Am 35 (2006) 405– 415
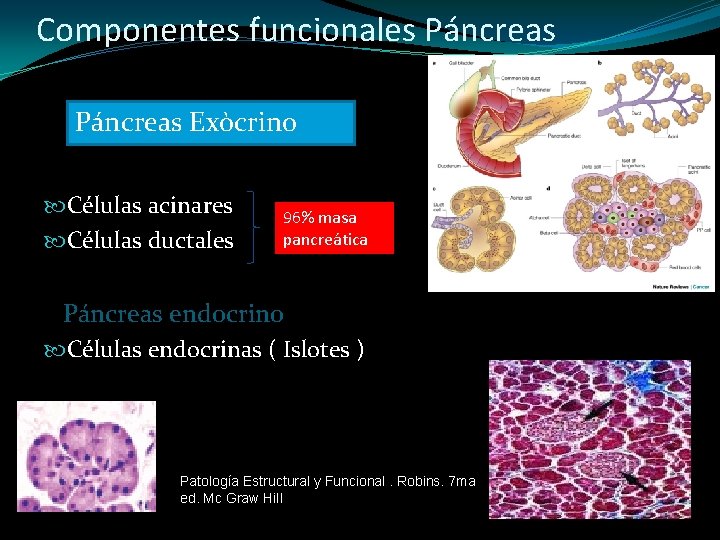
Componentes funcionales Páncreas Exòcrino Células acinares Células ductales 96% masa pancreática Páncreas endocrino Células endocrinas ( Islotes ) Patología Estructural y Funcional. Robins. 7 ma ed. Mc Graw Hill

Lesiones precursoras Neoplasia mucinosa papilar intraductal ( IPMNs) Neoplasia mucinosa quìstica Neoplasia pancreática intraepitelial ( Pan. NI) Gastroenterology Clin Of N Am. 26 2007. 831 -849
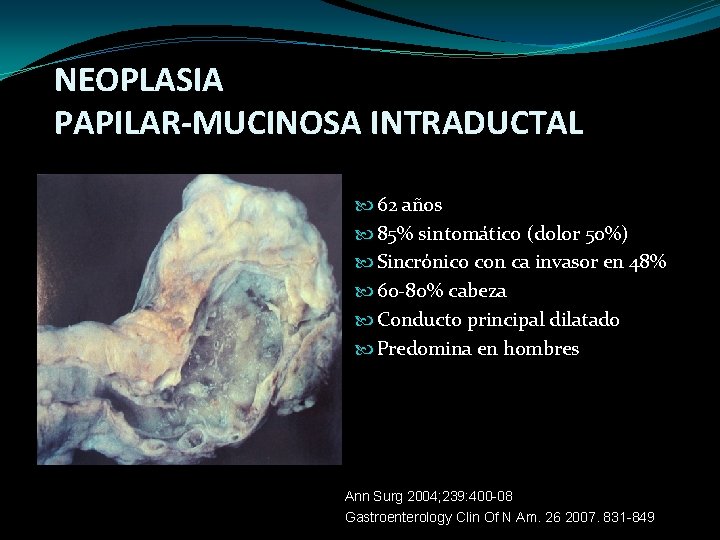
NEOPLASIA PAPILAR-MUCINOSA INTRADUCTAL 62 años 85% sintomático (dolor 50%) Sincrónico con ca invasor en 48% 60 -80% cabeza Conducto principal dilatado Predomina en hombres Ann Surg 2004; 239: 400 -08 Gastroenterology Clin Of N Am. 26 2007. 831 -849
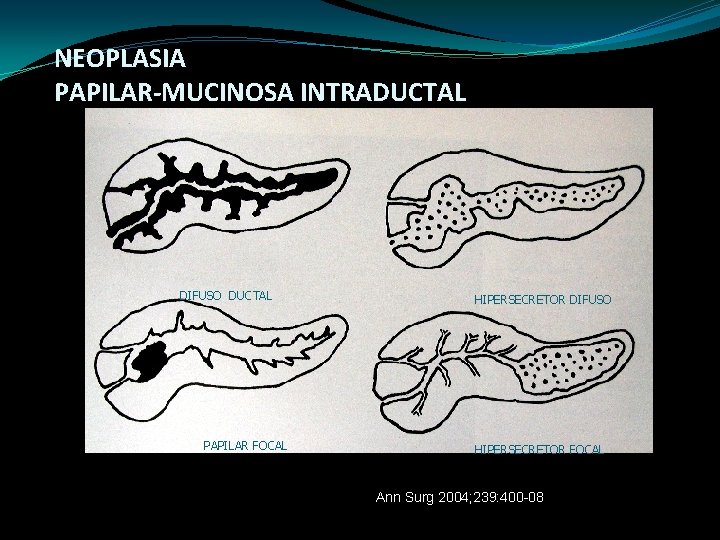
NEOPLASIA PAPILAR-MUCINOSA INTRADUCTAL DIFUSO DUCTAL PAPILAR FOCAL HIPERSECRETOR DIFUSO HIPERSECRETOR FOCAL Ann Surg 2004; 239: 400 -08

Neoplasia Mucinosa quìstica Mas frec. En mujeres Relación 20 : 1 Cuerpo y cola del páncreas 40 años ( 15 -95 años) Dolor abdominal Sensación de plenitud 1/3 relacionan adenocarcinoma No tiene comunicación con el conducto principal. Gastroenterol Clin Of N Am 2007
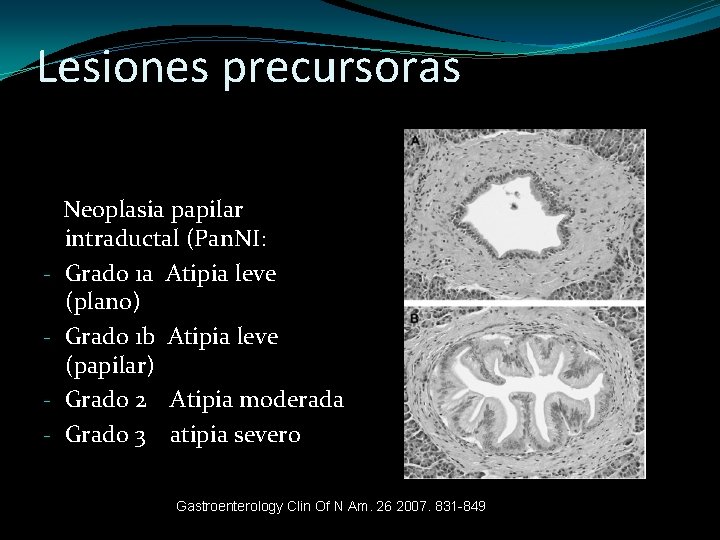
Lesiones precursoras - Neoplasia papilar intraductal (Pan. NI: Grado 1 a Atipia leve (plano) Grado 1 b Atipia leve (papilar) Grado 2 Atipia moderada Grado 3 atipia severo Gastroenterology Clin Of N Am. 26 2007. 831 -849
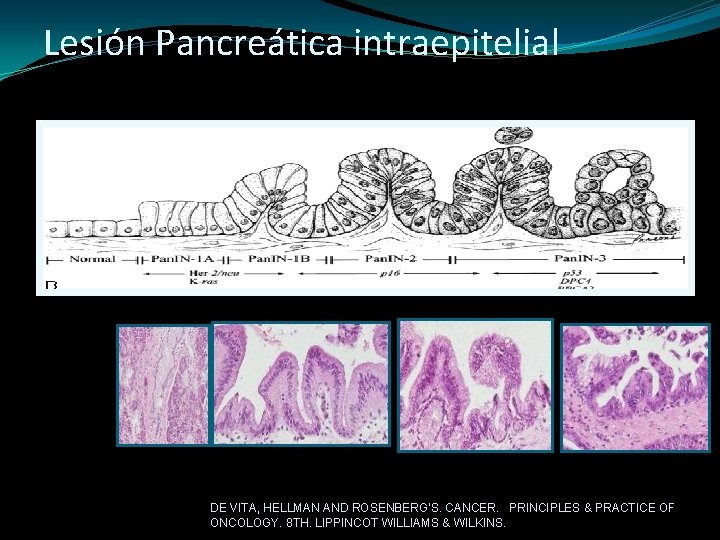
Lesión Pancreática intraepitelial DE VITA, HELLMAN AND ROSENBERG'S. CANCER. PRINCIPLES & PRACTICE OF ONCOLOGY. 8 TH. LIPPINCOT WILLIAMS & WILKINS.

Secuencia Pan. NI-Carcinoma Invasor Distribución de las Pan. NI es paralela a la del carcinoma inv. Pan. NI se encuentran en el parénquima adyacentes a los carcinomas inv. Las alteraciones genéticas en las Pai. NI son similares e las descritas en Ca. Invasor Células del Pa. NI muestran un marcado acortamiento de telomeros. Devita, Principles and Practice Onc. 7 th Ed

Alteraciones Moleculares en cáncer de páncreas Genes supresores P 53 P 16 P 21 p 27 Oncogenes K -Ras SMAD/DPC 4 CICLIN D-1 FACTORES DE CRECIMIENTO TGF B EGF FGF VEGF P D-FG MATRIZ EXTRACELULAR E INTERACCION ESTROMA Metaloproteinasas u. PA Catepsinas Heparanasas Lamininas integrinas Eur. J Of Cáncer 41, 2005 2213 -2236 Endocrinol Metab Clin N Am 35 (2006) 405– 415

Neoplasias Pancreáticas Sólidas Diferenciación Exocrina Quisticas Diferenciación Endocrina Páncreas 2007, 35: 120 -129

CLASIFICACION DE LA OMS I. Benignos Cistadenoma Seroso Cistadenoma Mucinoso Adenoma Mucinoso papilar Intraductal II Limitrofes ( Potencial Maligno Incierto) Tumor Quisticomucinoso con displasia mod. Tumor Pseudopapilar solido Tumor Mucinoso Papilar Intraductal limitrofe III Malignos Adenocarcinoma Ductal Adenoc. Ductal Clasico Carcinoma Mucinoso no quistico Carcinoma De cel. Anillo sello Carcinoma Adenoescamoso Carcinoma Indiferenciado Carcinoma Mixto ( Ductal-endocrino) Carcino. Celulas Gigantes de tipo Ostoeclastico Cistadenocarcinoma seroso Cistadenocarcinoma Mucinoso Carcinoma Mucinoso Papilar Intraductal Carcinoma de Células Acinares Pancreatoblastoma Tumors of the digestive Sistem OMS 2000

Neoplasias Exocrinas Sólidas 95 % Quísticas 5 % Adeno Carcinoma ductal 90 %. 60 -70 años Altamente letal Páncreas 2007, 35: 120 -129 Adenoc. Ductlal clasico Carcinoma Mucinoso no quistico Carcinoma De cel. Anillo de sello Carcinoma Adenoescamoso Carcinoma Indiferenciado Carcinoma Mixto ( Ductal-endocrino)

LESIONES QUISTICAS PANCREATICAS • Congénitas. • Retención. • Pseudoquistes 75% • Malignidad 5 -15% Tumours of the Páncreas AFIP, 1997 Sem Diag Pathol 2000; 17(1): 1 -6

Neoplasias Endocrinas Insulinoma Gastrinoma Glucagonoma Somatostanima VIPoma Endocrine related cancer, 2008, 15: 409 -427
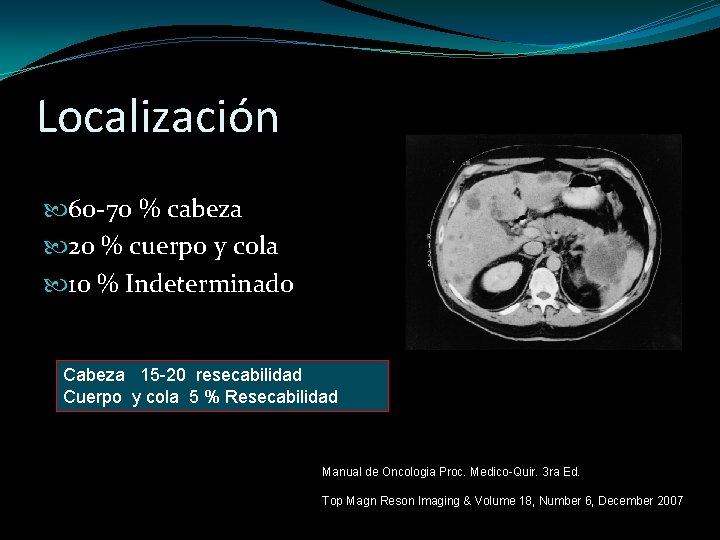
Localización 60 -70 % cabeza 20 % cuerpo y cola 10 % Indeterminado Cabeza 15 -20 resecabilidad Cuerpo y cola 5 % Resecabilidad Manual de Oncologia Proc. Medico-Quir. 3 ra Ed. Top Magn Reson Imaging & Volume 18, Number 6, December 2007
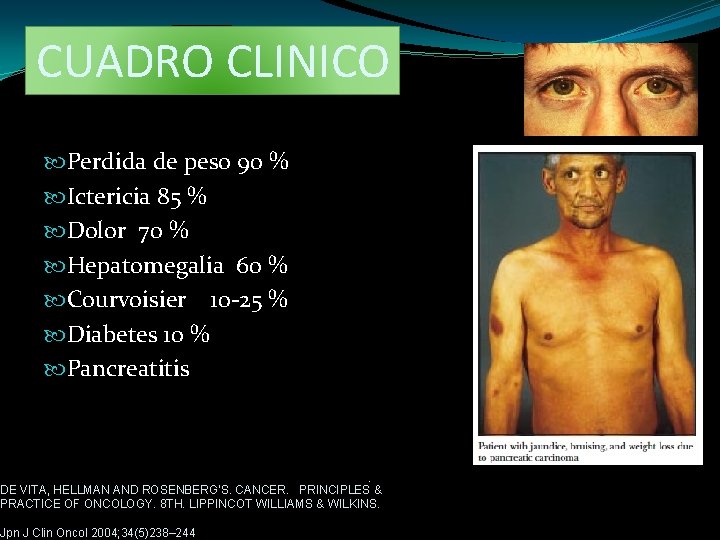
CUADRO CLINICO Perdida de peso 90 % Ictericia 85 % Dolor 70 % Hepatomegalia 60 % Courvoisier 10 -25 % Diabetes 10 % Pancreatitis . DE VITA, HELLMAN AND ROSENBERG'S. CANCER. PRINCIPLES & PRACTICE OF ONCOLOGY. 8 TH. LIPPINCOT WILLIAMS & WILKINS. Jpn J Clin Oncol 2004; 34(5)238– 244

SIGNOS Y SÍNTOMAS EN CANCER LOCALIZADO EN CUERPO Y COLA DE PANCREAS Hígado palpable 33 % Dolor 27 % Masa abdominal 23 % Ascitis 20 % Ictericia 13 % Devita, Principles and Practice Onc. 7 th Ed

Patrón de Diseminación Extensión Directa ( 60 -70 %) Vía Linfática Vía Hematógena Transcelomica ( 2 do sitio extranodal) Manual de Oncologia Proc. Medico-Quir. 3 ra Ed. Mc. Graw Hill
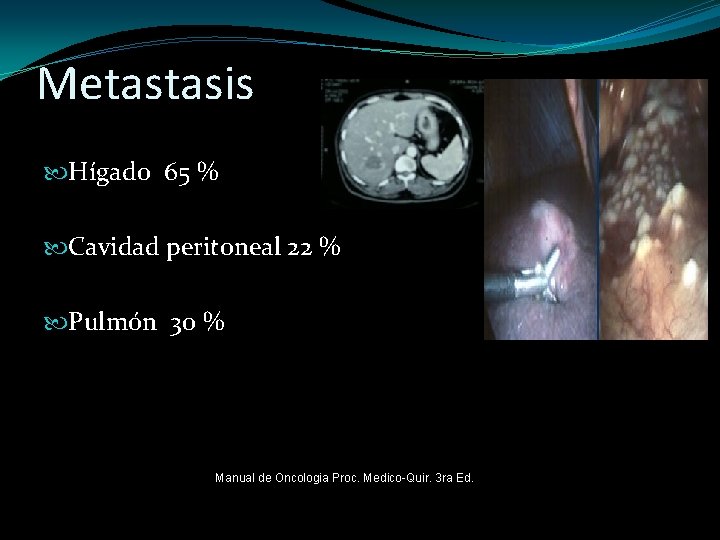
Metastasis Hígado 65 % Cavidad peritoneal 22 % Pulmón 30 % Manual de Oncologia Proc. Medico-Quir. 3 ra Ed.

DIAGNOSTICO US TRANSABDOMINAL US ENDOSCOPICO TAC HELICOIDAL CPRE RMN BIOPSIA POR EUS PET-CT LAPAROSCOPIA MARCADORES TUM. Am J of Surg 194 2007 S 87–S 90 Manual de Oncologia Proc. Medico-Quir. .
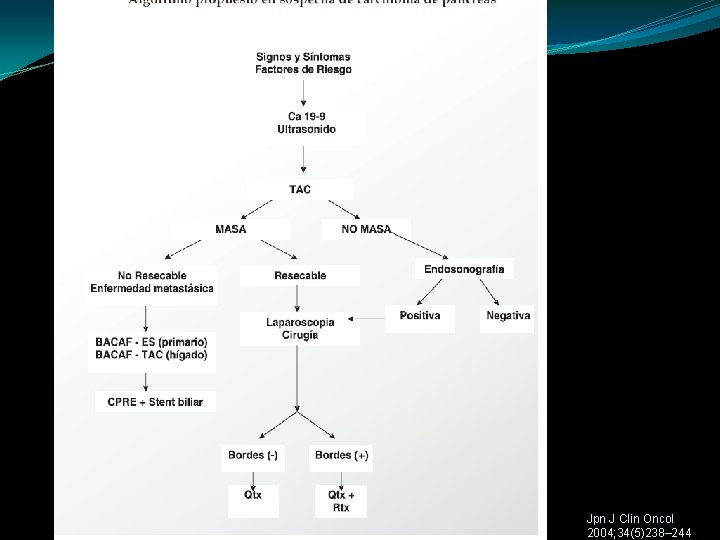
Jpn J Clin Oncol 2004; 34(5)238– 244
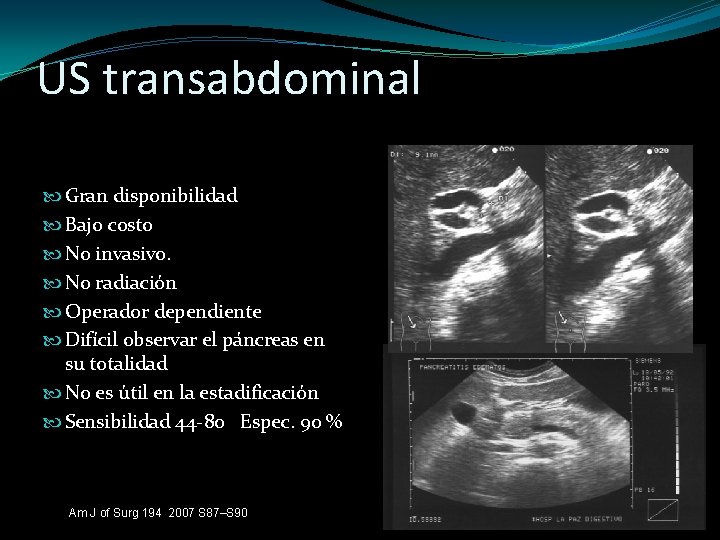
US transabdominal Gran disponibilidad Bajo costo No invasivo. No radiación Operador dependiente Difícil observar el páncreas en su totalidad No es útil en la estadificación Sensibilidad 44 -80 Espec. 90 % Am J of Surg 194 2007 S 87–S 90

TAC HELICOIDAL Piedra angular en la evaluación del tamaño y Extensión del tumor Infiltración vascular Dx Sensibilidad 85 -90 % Especificidad 90 -95 % Precisión Dx 85 -95 % N: Sesn 55 % M. Sens. 71 -75 % Am J of Surg 194 2007 S 87–S 90
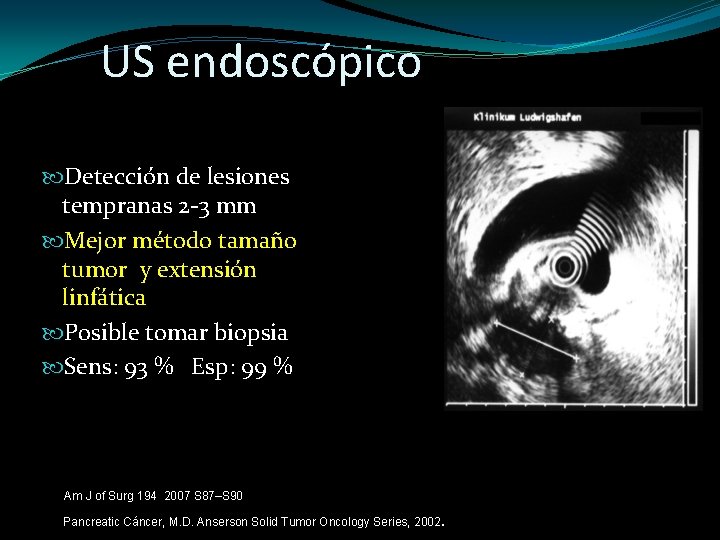
US endoscópico Detección de lesiones tempranas 2 -3 mm Mejor método tamaño tumor y extensión linfática Posible tomar biopsia Sens: 93 % Esp: 99 % Am J of Surg 194 2007 S 87–S 90 Pancreatic Cáncer, M. D. Anserson Solid Tumor Oncology Series, 2002.
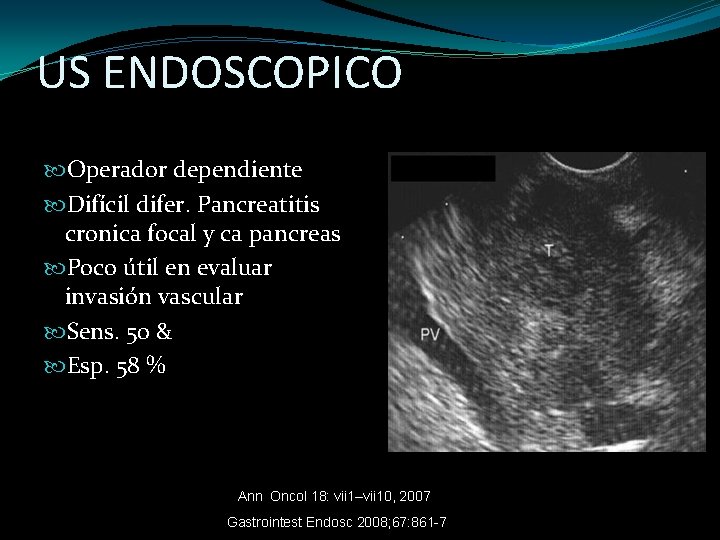
US ENDOSCOPICO Operador dependiente Difícil difer. Pancreatitis cronica focal y ca pancreas Poco útil en evaluar invasión vascular Sens. 50 & Esp. 58 % Ann Oncol 18: vii 1–vii 10, 2007 Gastrointest Endosc 2008; 67: 861 -7
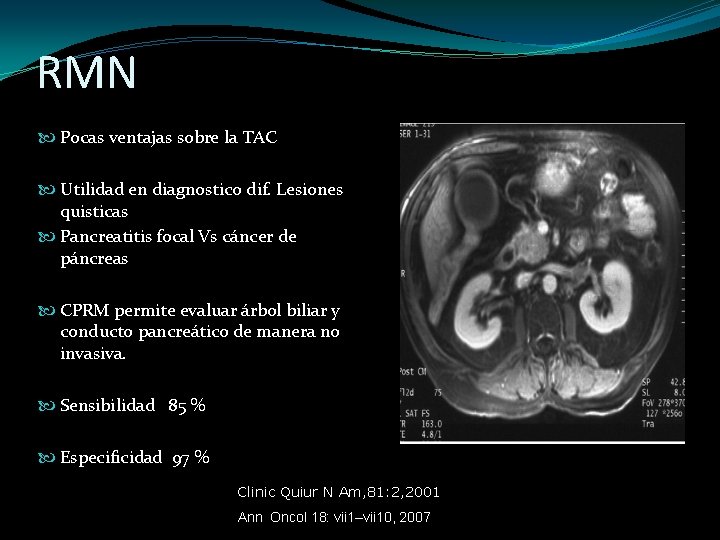
RMN Pocas ventajas sobre la TAC Utilidad en diagnostico dif. Lesiones quisticas Pancreatitis focal Vs cáncer de páncreas CPRM permite evaluar árbol biliar y conducto pancreático de manera no invasiva. Sensibilidad 85 % Especificidad 97 % Clinic Quiur N Am, 81: 2, 2001 Ann Oncol 18: vii 1–vii 10, 2007

C PRE No es un método Dx usado rutinariamente. Cuando son inconclusos los hallazgos por TAC o US Mayor utilidad en tumores cabeza Método invasivo Complicaciones 5 -10 % Sensibilidad 90 % Especificidad 95 % Tx paliativo. Ann Oncol 18: vii 1–vii 10, 2007 Clinic Quiur N Am, 81: 2, 2001 Ses. 50 -60 % Esp. 70 % Prec. Dx 60 -70 %
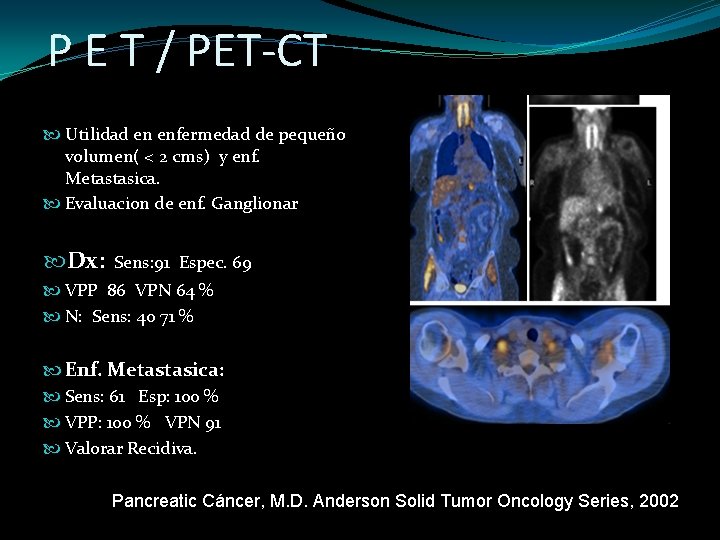
P E T / PET-CT Utilidad en enfermedad de pequeño volumen( < 2 cms) y enf. Metastasica. Evaluacion de enf. Ganglionar Dx: Sens: 91 Espec. 69 VPP 86 VPN 64 % N: Sens: 40 71 % Enf. Metastasica: Sens: 61 Esp: 100 % VPP: 100 % VPN 91 Valorar Recidiva. Pancreatic Cáncer, M. D. Anderson Solid Tumor Oncology Series, 2002

Laparoscopia Mets hepáticas ocultas por TAC es de 5 -40 %. Cambio plan terapéutico 25 % de los pacientes. Disminuye el numero de LAPEs innecesarias. VPP 100 % VPN 91 % Prec: 94 % US laparoscópico. VPP 100 % VPN 98 % Prec 98 % Mayor utilidad en lesiones cuerpo y cola de Mas de 4 cms. J pancreas 2005 ; 6: 552 -561 Ann Oncol 18: vii 1–vii 10, 2007

Confirmación histológica, cuando es necesaria? Preoperatoria ? ? Antes de iniciar terapia neoadyuvante Enfermedad irresecable candidatos a QT/RT paliativa Sospecha Clínica y por imagen de lesiones pancreáticas neoplásicas poco comunes ( linfoma, TNE, ) Devita, Principles and Practice Onc. 7 th Ed
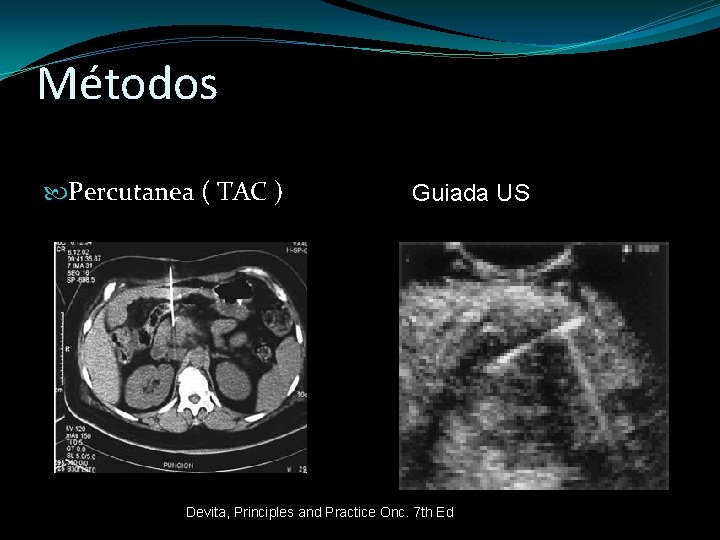
Métodos Percutanea ( TAC ) Guiada US Devita, Principles and Practice Onc. 7 th Ed
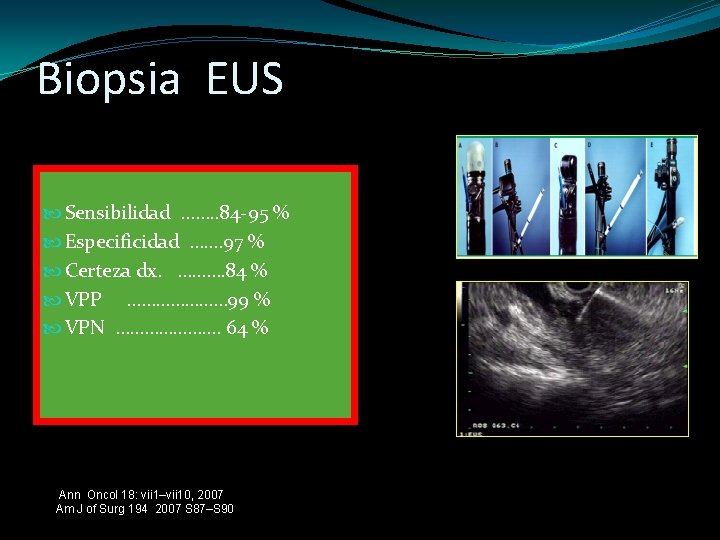
Biopsia EUS Sensibilidad ……. . 84 -95 % Especificidad …. … 97 % Certeza dx. ………. 84 % VPP ………………… 99 % VPN …………………. 64 % Ann Oncol 18: vii 1–vii 10, 2007 Am J of Surg 194 2007 S 87–S 90

Marcadores Tumorales en Ca páncreas Cualquier substancia bioquímica producida por células tumorales y cuya presencia o concentración anormal puede dar a conocer una neoplasia o su origen. Marcadores sanguineos Marcadores DNA y RNA Marcadores en jugo pancreatico Marcadores tisulares Oncogenes y Genes sup. Curr Opin Gastroenterol 2007 23: 508 -514 Eur J Cancer 2005 ; 41: 2213 -2236
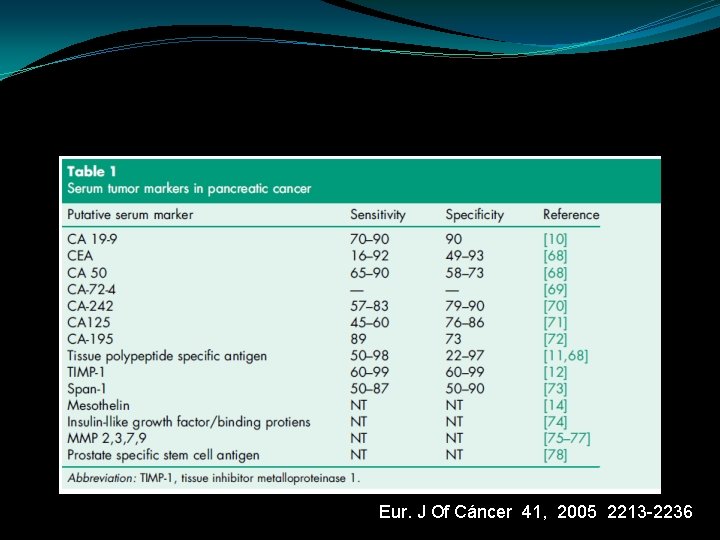
Eur. J Of Cáncer 41, 2005 2213 -2236

Ca 19 -9 Expresado en neoplasias pancreáticas, vías biliares, gástricas y colonicas. Pancreatitis, colestasis, cirrosis hepática, colangitis aguda. nefropatías Valor normal 30 -40 U/L Vida Media Curr Opin Gastroenterol 2007 23: 508 -514 Eur J Cancer 2005 ; 41: 2213 -2236

CA 19 -9 No se utiliza como detección o tamizaje S 70 -90 % E 68 -91% VPP 72 % VPN 65 -98 % Valores > 1000 U/ml se trata de enfermedad irresecable VPP 97% Utilidad en el seguimiento, valorara respuesta a QT, recaídas Dism. 20 % en 8 semanas pos QT predice buena respuesta Clinical oncology 3 rd. Ed. 2004 Eur. J Of Cáncer 41, 2005 2213 -2236 Pancreas. Campuzano-Herrera. Ed Mc. Graw-Hill. 1 ra ed.
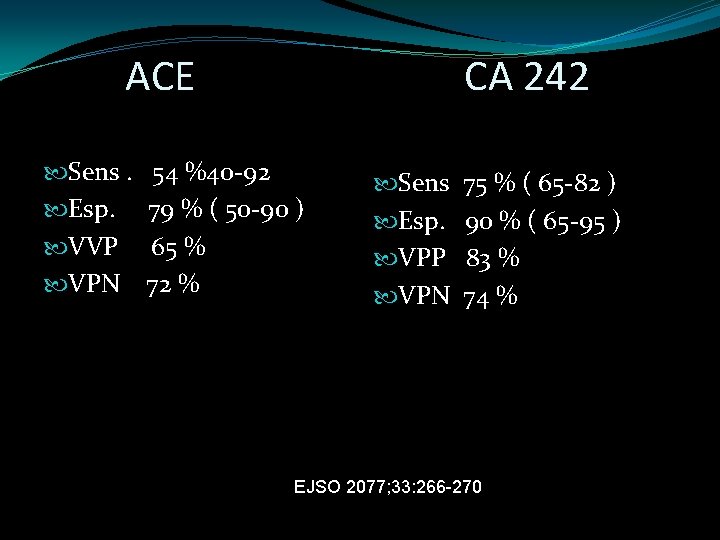
ACE Sens. Esp. VVP VPN CA 242 54 %40 -92 79 % ( 50 -90 ) 65 % 72 % Sens Esp. VPP VPN 75 % ( 65 -82 ) 90 % ( 65 -95 ) 83 % 74 % EJSO 2077; 33: 266 -270
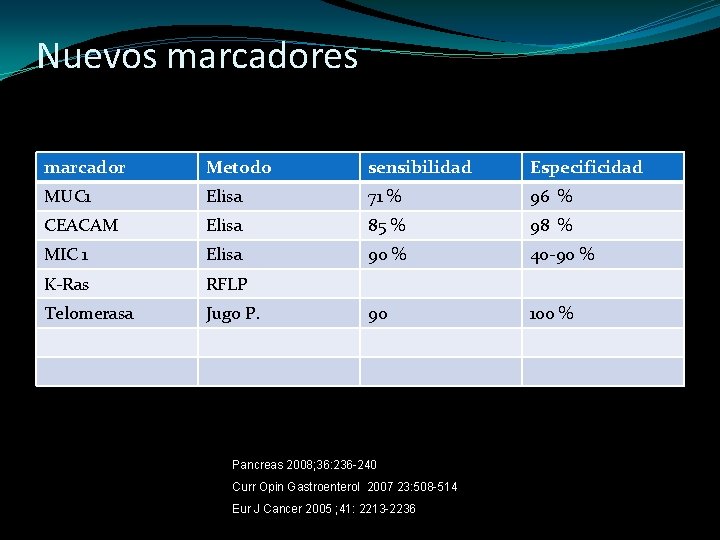
Nuevos marcadores marcador Metodo sensibilidad Especificidad MUC 1 Elisa 71 % 96 % CEACAM Elisa 85 % 98 % MIC 1 Elisa 90 % 40 -90 % K-Ras RFLP Telomerasa Jugo P. 90 100 % Pancreas 2008; 36: 236 -240 Curr Opin Gastroenterol 2007 23: 508 -514 Eur J Cancer 2005 ; 41: 2213 -2236

http: //www. pharmastrategyblog. com/2010/01/asco-early-detection-of-pancreaticcancer-using-pam 4 -as-a-biomarker. html

Predictores de malignidad en pacientes sin Dx Histopatológico Perdida de peso > 20 libras Ca 19 -9 > 37 Bilirrubina > 3 mgs Masa en TAC O EUS Sens. Espec. VPP VPN 86 % 100 % 66 % Am J of Surg 191 2006 191 -197


TNM T Tx No valorable T 0 Sin evidencia de tumor primario T is Carcinoma In Situ T 1 Tumor limitado al páncreas menor 2 cms. T 2 Tumor Limitado al páncreas, mayor de 2 cms. T 3 Tumor con extensión extrapancreática sin afectar AMS ni Tronco celiaco T 4 invasión extrapancreatica con afeccion de la AMS o tronco celiaco

TNM N NX NO PUEDEN SER EVALUADOS N 0 SIN METASTASIS A GANGLIOS LINF. REGIONALES N 1 CON METASTASIS A GANGLIOS LINFATICOS REGIONALES

TNM MX M M 0 M 1 NO PUEDEN SER EVALUADAS SIN METASTASIS A DISTANCIA CON METASTTASIS A DISTANCIA

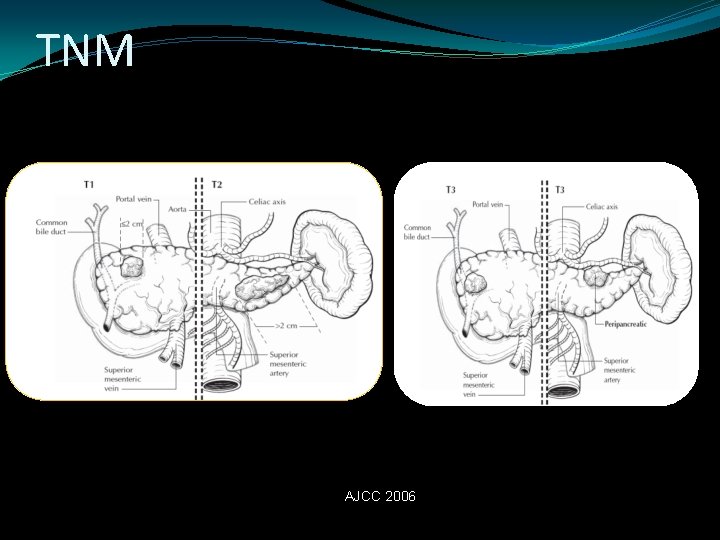
TNM AJCC 2006
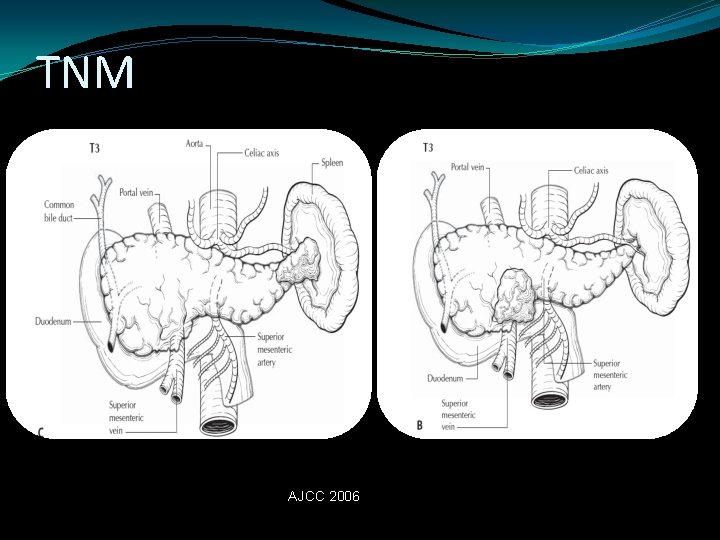
TNM AJCC 2006
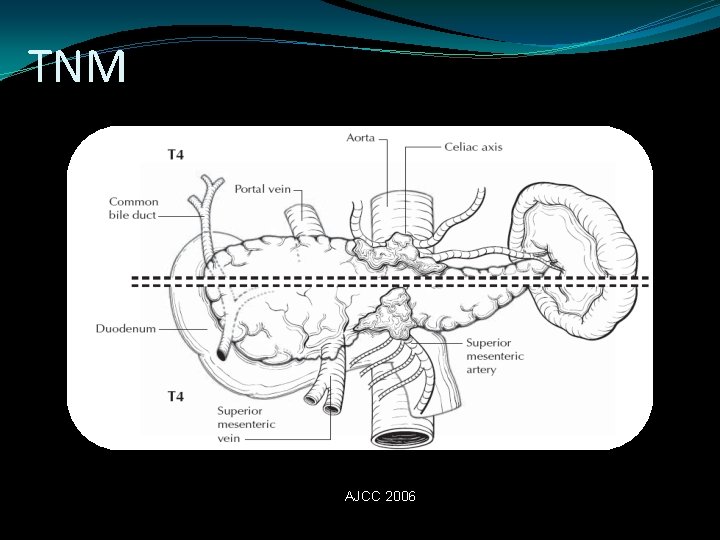
TNM AJCC 2006
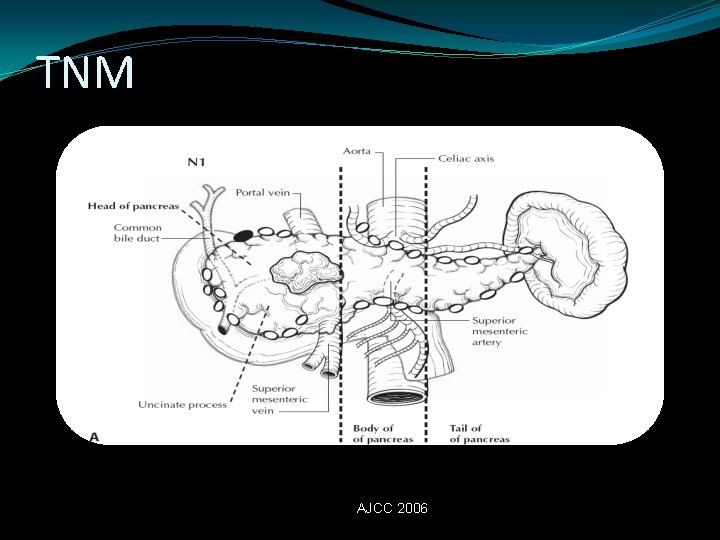
TNM AJCC 2006
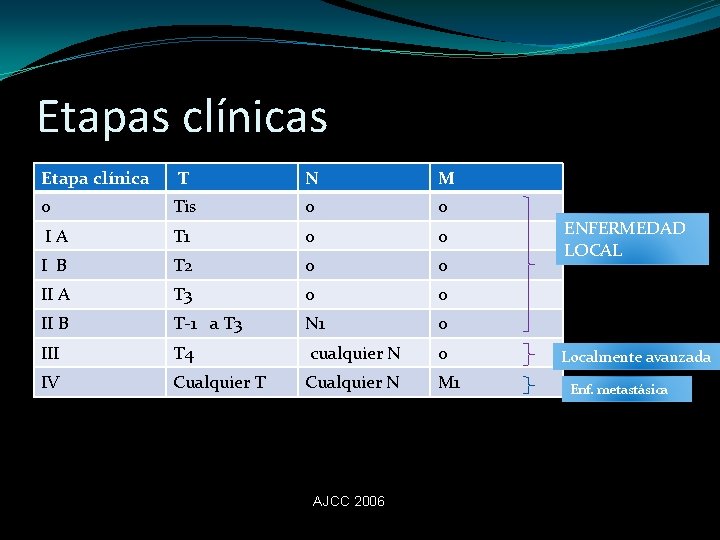
Etapas clínicas Etapa clínica T N M 0 Tis 0 0 IA T 1 0 0 I B T 2 0 0 II A T 3 0 0 II B T-1 a T 3 N 1 0 III T 4 cualquier N 0 IV Cualquier T Cualquier N M 1 AJCC 2006 ENFERMEDAD LOCAL Localmente avanzada Enf. metastásica
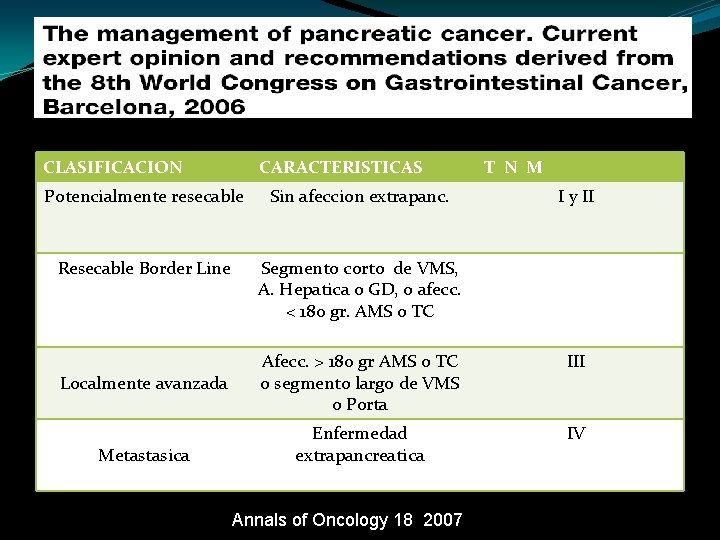
CLASIFICACION CARACTERISTICAS Potencialmente resecable Sin afeccion extrapanc. Resecable Border Line Segmento corto de VMS, A. Hepatica o GD, o afecc. < 180 gr. AMS o TC Localmente avanzada Metastasica T N M I y II Afecc. > 180 gr AMS o TC o segmento largo de VMS o Porta III Enfermedad extrapancreatica IV Annals of Oncology 18 2007

FACTORES PRONÓSTICOS Sometidos a Pancreatoduodenectomia Enfermedad Metastásica en ganglios regionales Ganglios - SV a 36 meses es 25 - 30 %, ganglios + SV 6 -8 meses Histología Pobremente diferenciados Tamaño del Tumor ( - 3 cms SV 28 %, mas 3 cms 15 %) Margen positivo ( resecc. Incompleta) AJCC 2006 J Clin Gastroenterol 2008; 42: 86– 91

FACTORES PRONÓSTICOS No sometidos a cirugía TNM Modalidad de tratamiento Ca 19 -9 Inicial J Clin Gastroenterol Volume 42, Number 1, Jan 2008

TNM SOBREVIDA POR EC I - 5 -35 % II - 2 -15 % IV - 1 -5 % Annals of Oncology 18 2007 J Clin Gastroenterol 2008; 42: 86– 91 Sobrevida Global a 5 años 5 %

SOBREVIDA Cirugía por enf. local 5 -25 % a 5 años promedio 11 -20 meses ( < 2 cms y N 0) Enf. Localmente avanzada no metastasica 6 -11 meses Enf. Metastásica 2 - 6 meses Eur Radiol (2007) 17: 638– 649

Recurrencia Locorregional Recidiva 70 -80 % 2 años ( 9 -11 meses) Hígado Cavidad peritoneal Lecho pancreático 90 % No llevados a R 0 Pulmonar y a distancia 10 % Am J of Surg 194 2007 S 87–S 90 J Clin Gastroenterol 2008; 42: 86– 91

Tumores Metastáticos Pacientes con linfoma…. ……. . . 25%. Cáncer de Mama………………… 20%. Cáncer de Pulmón………………. 19%. Cáncer colorectal………………… 10%. Melanoma……………. . . 9%. Cáncer de estómago…………. . . . 7%. De Vitta, 7 th Ed, 2005 Clinic Quiur N Am, 81: 2, 2001
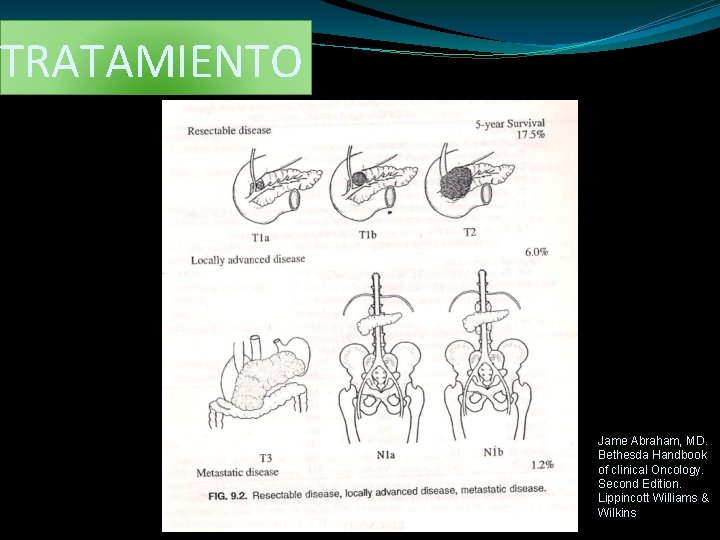
TRATAMIENTO Jame Abraham, MD. Bethesda Handbook of clinical Oncology. Second Edition. Lippincott Williams & Wilkins
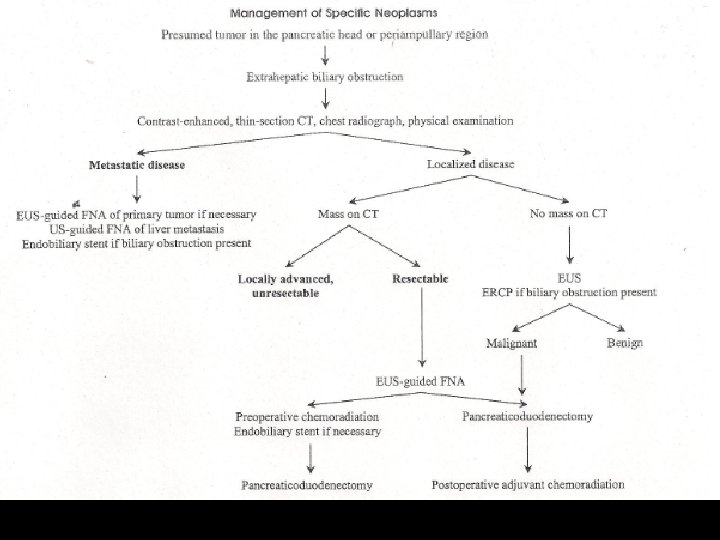

ENFERMEDAD LOCALIZADA MENOS DEL 10 % DE LOS PACIENTES TIENEN ENFERMEDAD RESECABLE AL MOMENTO DEL DX WHIPPLE O PROCEDIMIENTO MODIFICADO QUE PRESERVE EL PILORO ES EL PROC QX DE ELECCION. AUN DESPUES DE LA COMPLETA RESECCION, EL RIESGO DE RECURENCIA LOCOREGIONAL ES >70%.

El tratamiento estándar es la resección pancreática radical. Una pancreatoduodenectomia con preservación del piloro es el procedimiento de elección para los pacientes con tumores de la cabeza de l páncreas. La cirugía mas común para los tumores del cuerpo y cola es una pancreatectomia distal, que incluye esplenectomía.
ENFERMEDAD LOCALMENTE AVANZADA QUIMIO/RADIOTERAPIA ANTE POBRE ESTADO FUNCIONAL: PALIATIVOS QUIMIOTERAPIA (GEMCITABINA) Jame Abraham, MD. Bethesda Handbook of clinical Oncology. Second Edition. Lippincott Williams & Wilkins

ENFERMEDAD LOCALMENTE AVANZADA 25% TIENEN INVOLUCRO REGIONAL AL MOMENTO DEL DIAGNOSTICO. EL TX CON QT/RT HA MOSTRADO MEJORIA EN LA SOBREVIDA QUE CON EL TRATAMIENTO DE MONOTERAPIA. LOS PACIENTES CON TUMOR NO RESECABLE, CON BUEN ESTADO FUNCIONAL, SE TX CON 45 -54 Gy radiación con 5 FU a dosis de 500 mg/m/dia en el día 1 y 3 de RT. Jame Abraham, MD. Bethesda Handbook of clinical Oncology. Second Edition. Lippincott Williams & Wilkins

ENFERMEDAD METASTASICA 50% DE LOS PACIENTES DX DE CA PANCREAS TIENEN METASTASIS. EL TRATAMIENTO PALIATIVO CON QT SISTEMICA DEBE SER OFRECIDO A PATICIES CON BUEN ESTADO FUNCIONAL(KARNOSFKY 80 -90, ECOG 0 -2) GEMCITABINA ES EL TRATAMIENTO ESTÁNDAR DE PRIMERA LÍNEA EN PACIENTES CON CÁNCER PANCREÁTICO METASTASICO Jame Abraham, MD. Bethesda Handbook of clinical Oncology. Second Edition. Lippincott Williams & Wilkins

Screening ? ? ? Korea ca 19 -9 o US 70 940 pac. Asint. 4 casos de cancer. Japon. Ca 19 -9 o US 10162 pac. . > 40 años Asintomat. 4 casos cancer Panc. Cancer 1993: 72: 381 -8

Screening No existe screening aplicable a toda la población. 10 años antes a la edad de presentación en cáncer pancreático familiar Después de los 35 años en pancreatitis hereditaria TAC helicoidal Ultrasonido endoscópico. AGA GUIDELINE. Gastroenterology 1999;

QUIMIOPREVENCIÓN, ES POSIBLE ? ? ? Estatinas Cox 2 Aspirina Cancer 2001; 91: 333– 8. Páncreas 2007; 34: 260 J Natl Cáncer Inst 2002; 94: 1168– 71.

Seguimiento y vigilancia Examen fisico 3 -6 meses 2 años Después anualmente Ca 19 -9 y TAC
- Slides: 82