Cncer de Mama Jorge Snchez Cibantos F E

Cáncer de Mama Jorge Sánchez Cibantos F. E. A Obstetricia y Ginecología H. U. Puerto Real

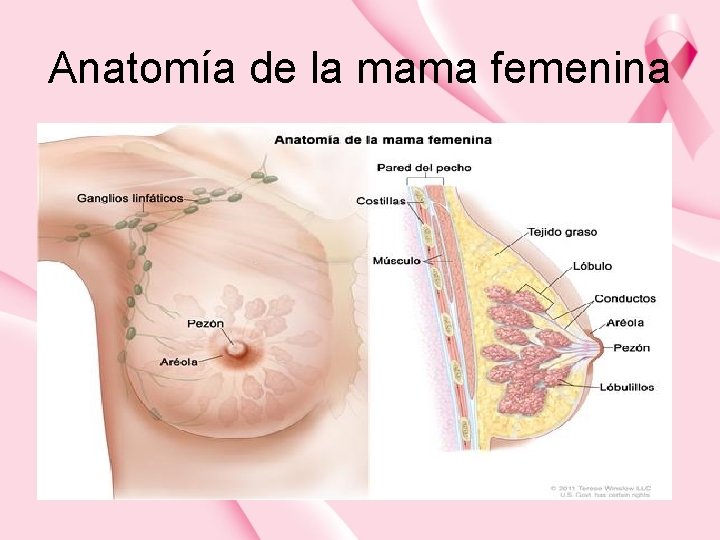
Anatomía de la mama femenina
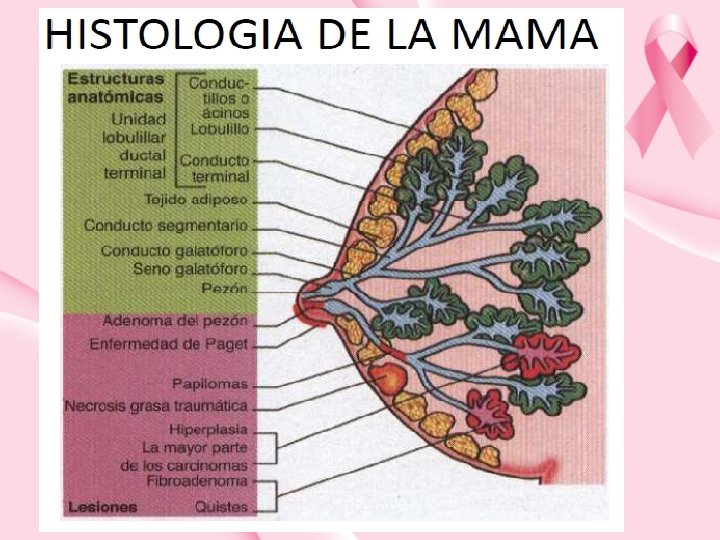

IMPORTANCIA DEL CÁNCER DE MAMA 1 de cada 8 mujeres desarrollará un cáncer de mama a lo largo de su vida (es decir, el riesgo que tiene una mujer de la población general, sin antecedentes familiares, de padecer CM a lo largo de su vida, es de un 12%). De ellas 1/3 morirán

IMPORTANCIA Es el cáncer más frecuente en la mujer. Cada año se diagnostican 25000 casos en España. Tanto el número de casos como las tasas de incidencia aumentan lentamente, probablemente debido al envejecimiento de la población y a un diagnóstico cada vez más precoz. El aumento de la incidencia: 1 -2% anual. Es la segunda causa de muerte de mujeres a cualquier edad. La principal causa de muerte por cáncer en la mujer. Unos 6 500 fallecimientos al año en España. La principal causa de muerte en mujeres de 35 a 55 años. El periodo de máxima incidencia es entre los 50 y 70 años (está aumentando en mujeres jóvenes). SI UN TUMOR DE MAMA ES DETECTADO TEMPRANAMENTE ES POSIBLE SU CURACIÓN

FACTORES DE RIESGO Tener un factor de riesgo, o varios, no significa que vaya a aparecer la enfermedad, sólo indica cierta predisposición Además, muchas mujeres que tienen cáncer de mama no tienen factores de riesgo. En el 50% de los casos no se observa ningún factor de riesgo Se han identificado una serie de factores que pueden aumentar el riesgo de desarrollar un cáncer de mama a lo largo de la vida.
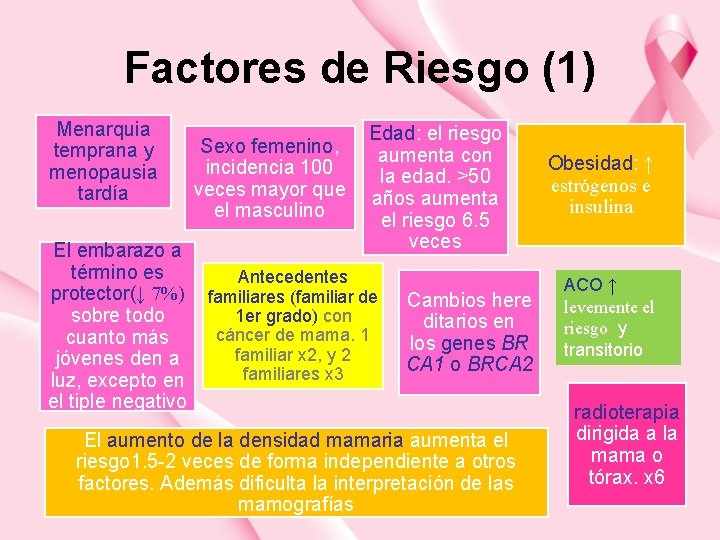
Factores de Riesgo (1) Menarquia temprana y menopausia tardía Sexo femenino, incidencia 100 veces mayor que el masculino Edad: el riesgo aumenta con la edad. >50 años aumenta el riesgo 6. 5 veces El embarazo a término es Antecedentes protector(↓ 7%) familiares (familiar de 1 er grado) con sobre todo cáncer de mama. 1 cuanto más familiar x 2, y 2 jóvenes den a familiares x 3 luz, excepto en el tiple negativo Cambios here ditarios en los genes BR CA 1 o BRCA 2 El aumento de la densidad mamaria aumenta el riesgo 1. 5 -2 veces de forma independiente a otros factores. Además dificulta la interpretación de las mamografías Obesidad: ↑ estrógenos e insulina ACO ↑ levemente el riesgo y transitorio radioterapia dirigida a la mama o tórax. x 6
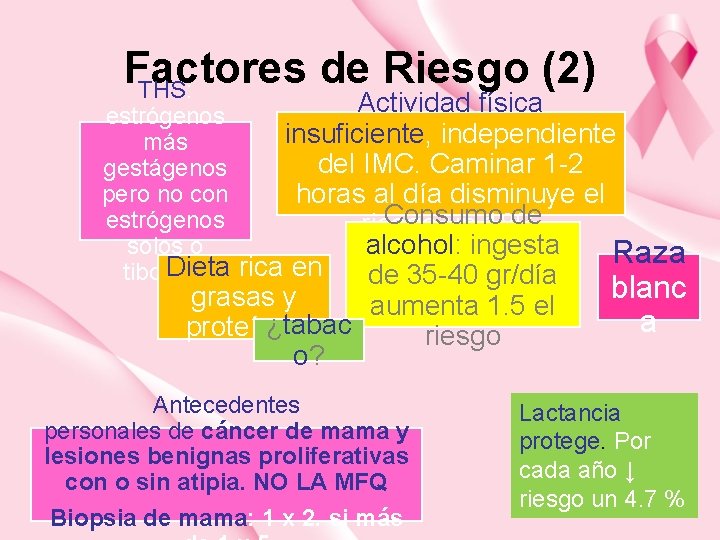
Factores de Riesgo (2) THS: Actividad física estrógenos insuficiente, independiente más del IMC. Caminar 1 -2 gestágenos pero no con horas al día disminuye el Consumo de estrógenos riesgo un 18% solos o alcohol: ingesta Raza Dieta rica en tibolona de 35 -40 gr/día grasas y aumenta 1. 5 el ¿tabac proteínas riesgo o? Antecedentes personales de cáncer de mama y lesiones benignas proliferativas con o sin atipia. NO LA MFQ Biopsia de mama: 1 x 2. si más blanc a Lactancia protege. Por cada año ↓ riesgo un 4. 7 %

Mutaciones genéticas heredadas en el Cáncer de Mama • CM esporádico: sin antecedentes familiares. El más común, 70% • CM familiar: existen antecedentes familiares pero no está ligado a mutación en gen supresor tumoral. 20% • CM hereditario: 10%. Antecedentes familiares de CM y otros cánceres (ovario o colon). Suele aparecer a edades tempranas y/o bilateral. Existe mutación de algún gen supresor tumoral. - BRCA 1: mama y ovario - BRCA 2: mama - p 53: síndrome de Li-Fraumeni (sarcomas, leucemias, tumor cerebral, CM, etc. )

Mutaciones genéticas heredadas en el Cáncer de Mama • El cáncer de mama hereditario representa alrededor de 5 a 10% de todos los casos de cáncer de mama. • Las mutaciones genéticas, como la de los genes BRCA 1 o BRCA 2 suponen un aumento de riesgo de cáncer de mama y de ovario. Existen otros genes menos prevalentes como TP 53 (síndrome de Li-Fraumeni), STK 11 (síndrome de Peutz-Jeghers), PTEN (síndrome de Cowden) y PLAB 2. • Las mujeres que tuvieron un CM, sea infiltrante o ductal in situ, tienen un riesgo aumentado de 3 a 4 veces para desarrollar un nuevo cáncer ya sea en la misma mama o en la contralateral.

Mutaciones genéticas heredadas en el Cáncer de Mama • La prevalencia de mutaciones BRCA 1 y BRCA 2 en pacientes con CM u ovario no seleccionadas (población general) son bajas (2% para CM y 10% para CO) • La penetrancia (probabilidad de que un sujeto portador de la alteración genética manifieste la enfermedad) CM CO BRCA 1 52% 22% BRCA 2 47% 18%

¿Cuándo solicitar estudio genético BRCA? (SEOM) • 2 o más CM y/o CO en la misma línea familiar, si al menos uno fue diagnosticado antes de los 50 años • CM antes de los 35 años • CM y CO en la misma mujer • CM en el varón • CM bilateral (uno de ellos diagnosticado < 50 años) • CM triple negativo antes de los 50 años • CO epitelial invasivo no mucinoso de alto grado • Familiares con mutación conocida BRCA 1 o BRCA 2

Detección precoz de CM en casos de mutación BRCA • Autoexploración mensual 18 años 25 años • Exploración clínica semestral • Mamografía y/o RMN a partir de los 25 -30 años (se puede plantear Mx alternante con RMN cada 6 meses)

Detección precoz de cáncer de ovario en casos de mutación BRCA • Eco STV y CA 125 cada 6 -12 meses A partir de 30 años o empezar 5 años antes de la edad del diagnostico de CO del familiar Hasta decidir SOB Nota: no está demostrado que este abordaje haya logrado reducir el estadio inicial al diagnóstico ni mejorar la supervivencia

Cirugías reductoras de riesgo en casos de mutación BRCA SALPINGOOFORECTOMIA BILATERAL PROFILACTICA MASTECTOMA PROFILACTICA • Se han descrito reducciones del 79 -96 % del cáncer epitelial de ovario (existe riesgo de carcinoma peritoneal primario que se comporta como el CO) y del 50% para el cáncer de mama (por la ↓ de estrógenos) • La SOBP no sólo reduce el riesgo de CM y CO, sino también prolonga la supervivencia por cáncer celómico • El momento óptimo para la intervención genera controversias ya que la edad media de aparición de CO en mujeres con mutación BRCA 1/2 es de 53 a 57 años; y que el efecto protector sobre CM se observa en pacientes en las que se realizó la SOBP antes de los 40 años • Reduce el riesgo de CM en un 90 -95 %, aunque sin afectar a la supervivencia • La más recomendada es la mastectomía conservadora de piel con extirpación del CAP. Si se conserva el CAP se asume un riesgo de necrosis del 1. 7% y se debe biopsiar el tejido ductal existente debajo del pezón para descartar carcinoma in situ o invasor • En aquellas mujeres que no desean la mastectomía profiláctica el seguimiento con RM y mamografía anuales tiene similares resultados en términos de supervivencia
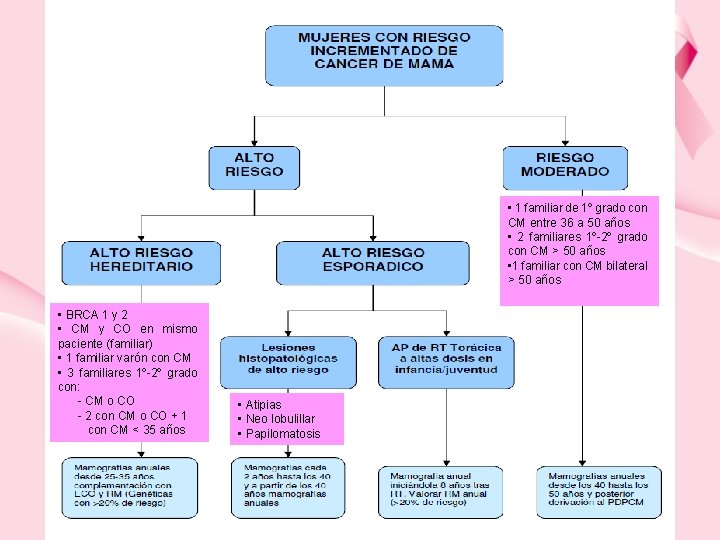
• 1 familiar de 1º grado con CM entre 36 a 50 años • 2 familiares 1º-2º grado con CM > 50 años • 1 familiar con CM bilateral > 50 años • BRCA 1 y 2 • CM y CO en mismo paciente (familiar) • 1 familiar varón con CM • 3 familiares 1º-2º grado con: - CM o CO - 2 con CM o CO + 1 con CM < 35 años • Atipias • Neo lobulillar • Papilomatosis

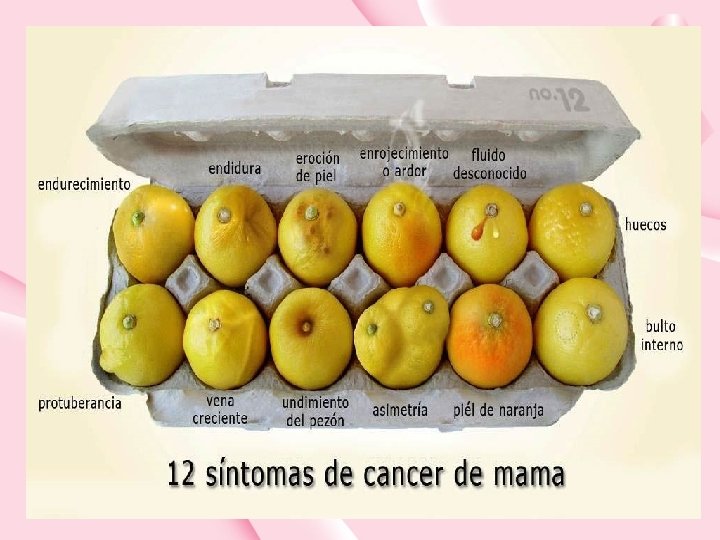
Cuales son los Signos Posibles de cáncer de mama? Nódulo. Es la forma de presentación más frecuente. 65 -75 %. Adenopatías axilares y supraclaviculares. Cambio en el tamaño o la forma de la mama. retracciones en la piel de la mama. Cambios en la vascularización. Cambios en el pezón: retracción, eczema. Secreción por el pezón, especialmente si es sanguinolento. Piel con escamas, eritema, edema (piel de naranja). Mastalgia unilateral y acíclica. Se asocia a CM 2 -5%
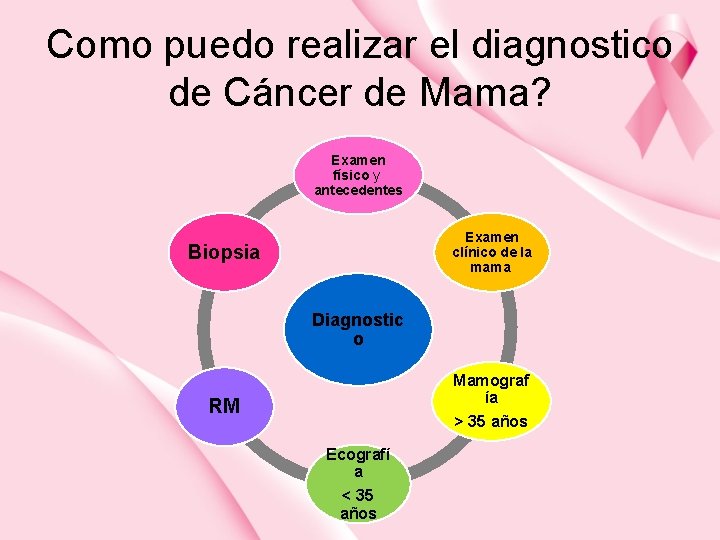
Como puedo realizar el diagnostico de Cáncer de Mama? Examen físico y antecedentes Examen clínico de la mama Biopsia Diagnostic o Mamograf ía RM > 35 años Ecografí a < 35 años

Mamografía • La Mamografía ha demostrado su eficacia como método de detección precoz en mujeres asintomáticas entre 45 y 70 años. Tasas de detección del 5 -7% La reducción de las tasas de mortalidad es variable, pudiendo alcanzar el 30%. • Es la única exploración que ha demostrado validez para el cribado del CM, siendo otras exploraciones un complemento de ésta.

CLASIFICACIÓN BI-RADS 0: Evaluación adicional • Se considera una categoría incompleta, para establecer una categoría precisa evaluación adicional, bien sea mediante técnicas de imagen (proyecciones adicionales, ecografía) o comparación con mamografías anteriores. BI-RADS 1: Negativa • Normal, ningún hallazgo a destacar. • Se recomienda seguimiento a intervalo normal. BI-RADS 2: Claramente Benigna • Normal, pero existen hallazgos benignos. • Se recomienda seguimiento a intervalo normal. BI-RADS 3: Probablemente benigna • Probabilidad de malignidad <2%. • Se recomienda una mamografía unilateral a los 6 meses y bilateral a los 12 y 24 meses de la primera. Si aun hay hallazgos se recomienda una biopsia.

CLASIFICACIÓN BI-RADS 4: Anormalidad sospechosa. • Incluye aquellas lesiones que van a requerir BAG, se divide en tres subcategorías: • 4 a: baja sospecha de malignidad (resultado esperado es de benignidad). VPP 2 -10% • 4 b: sospecha intermedia de malignidad. VPP 1050% • 4 c: sospecha moderada de malignidad. VPP 5095% • Se recomienda biopsia. BI-RADS 5: Altamente sugestiva de malignidad • Hallazgos típicamente malignos. • Probabilidad de malignidad >95% BI-RADS 6: Malignidad conocida. • Lesiones con malignidad demostrada mediante biopsia, previa a terapias definitivas (cirugía, radioterapia o quimioterapia).

CATEGORIAS DGCAS EN BAG Y BAV • B 1: normal o no interpretable (muestra insuficiente, no representativa o no valorable por incidentes técnicos) • B 2: lesiones benignas (fibroadenoma, cambio fibroquístico, proliferaciones intraductales sin atipias, ectasia ductal, adenosis esclerosante, absceso, necrosis grasa) • B 3: lesiones benignas pero de potencial biológico incierto (proliferaciones intraductales atípicas, neoplasia lobulillar, hipercelularidad estromal, lesiones papilares, cicatriz radial, lesión esclerosante compleja, mucocele). Valorar exéresis vs seguimiento • B 4: sospechoso de malignidad (probable carcinoma pero con problemas técnicos por material hemático, fijación defectuosa, material escaso, etc. ) • B 5: maligna

Mamografía - ¿Riesgos? : estudios recientes no han demostrado ningún caso de CM desencadenado por las radiaciones ionizantes de la MRx. Los beneficios superan sobradamente a los posibles riesgos. - La MRx no es una técnica infalible a la hora de detectar un CM. Falsos negativos 10 -35 % - La MRx digital no ha aumentado la tasa detección de CM, objetivo que sí logra la tomosíntesis (MRx por planos) hasta un 27% más de detección - CONTROVERSIAS DEL SCREENING: - desde pv científico: desde 40 a 75 años, anual. Si antecedentes de riesgo desde los 35 años, anual. - cuando se realizan 2 proyecciones se diagnostican un 24% más de CM y el coste solo aumenta un 0. 3 % - si cada 3 años o más, está demostrado que los resultados son los mismos que si no se hiciera cribaje. Por ello las directrices europeas recomiendan cada 2 años.

Mamografía. ¿Por qué entre 50 a 69 años en el PDPCM? - La Unión Europea, en el 2003, recomendó el cribado poblacional para el CM mediante mamografía bienal en las mujeres de 50 a 69 años. - Entre los 40 -49 años no existe ningún estudio randomizado que demuestre reducción de la mortalidad, aunque esta reducción sí se observa en los metanálisis, entre un 15 y un 20 %. El menor riesgo de CM en estas edades, la baja sensibilidad de la MRx y el aumento de falsos positivos ha llevado a la mayoría de sociedades a no recomendar el cribado sistemático en esta franja de edad. - Más allá de los 70 años los estudios no demuestran beneficio en términos de mortalidad. - Los estudios randomizados demuestran, al comparar MRx anual o bianual, que la reducción de la mortalidad es similar. En un análisis del CNI norteamericano, hacer la MRx cada 2 años en lugar de anual no se asociaba a mayor riesgo de diagnosticar la enfermedad en un estadio avanzado en mujeres de más de 50 años pero sí en mujeres de menos de 50 años.

Mamografía. Efectos indeseables del cribado * Falsos positivos (10%), sobre todo entre los 40 -49 años. * Falsos negativos (10 -35%): sobre todo en mujeres con aumento de la densidad mamaria. Hay que explicar a las mujeres que la sensibilidad de la MRx es del 85 -90 % y que por tanto no todas las neoplasias son detectables, especialmente en mamas densas * Sobrediagnóstico (CM histológicamente confirmado que no se habría manifestado clínicamente durante la vida de la mujer) y sobretratamiento * ¿Neoplasias inducidas por la radiación de la MRx? : Yaffe y col. dicen que la MRx induciría 86 CM por cada 100000 mujeres cribadas anualmente, pero que salvaría 5 vidas por mujer fallecida por esta causa. Por tanto el balance sería favorable al cribado. Estudios recientes no han demostrado ningún caso de CM desencadenado por las radiaciones ionizantes de la MRx.

Ecografía La Ecografía no ha demostrado utilidad como método de cribado para cáncer de mama, si bien es una técnica adjunta o complementaria de gran importancia en programas de cribado mamográfico, sobre todo en mujeres jóvenes con mayor densidad mamaria.

RMN MAMAS • Cada vez más utilizada • Elevada sensibilidad para carcinomas infiltrantes • ↑ Falsos Positivos • Basada en la neoangiogénesis tumoral. Por tanto, estudio dinámico tras administración de contraste (gadolinio) • No valida para diagnosticar afectación ganglionar

RMN MAMAS: Indicaciones • Evaluar integridad de prótesis y expansores • Estadificación loco-regional previa a cirugía o neoadyuvancia (estimación exacta del tamaño tumoral). No válida para valorar afectación ganglionar axilar. • Control tras neoadyuvancia • Búsqueda de tumor en casos de carcinoma oculto • Detección de posible recidiva en pacientes con cirugía conservadora (dd con cambios cicatriciales), siempre que los métodos convencionales no resulten concluyentes. Ha de realizarse tras 6 meses post-cirugía o 18 meses post-radioterapia. • Detección sistemática en mujeres de alto riesgo de CM • Otras: telorragias no aclaradas por técnicas clásicas, nódulos múltiples, patrones radiológicos difíciles, etc.
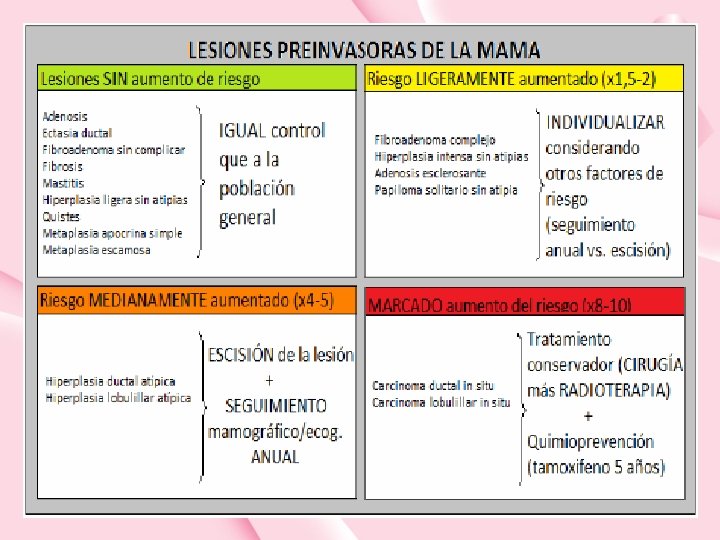

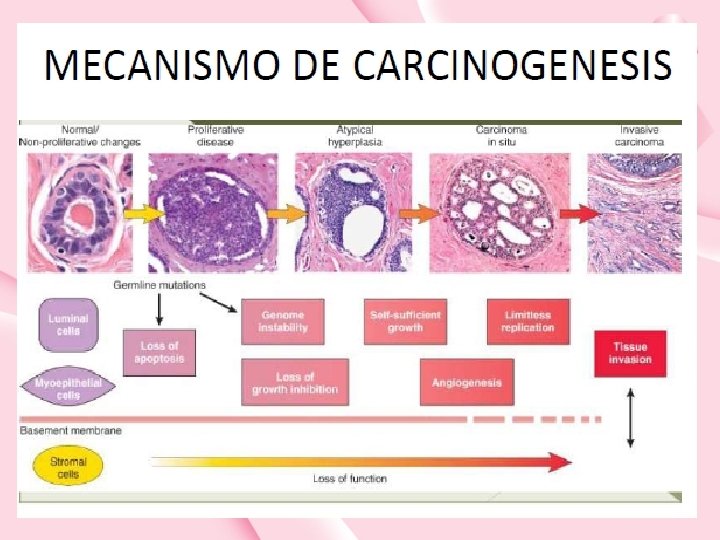
NEOPLASIA INTRAEPITELIAL DUCTAL • Proceso proliferativo del epitelio ductal confinado por la membrana basal y que, por tanto, no invade el estroma subyacente. • Se considera una enfermedad todavía local. Es el Tis de la clasificación TNM. Estadio 0. • El cribado MRx diagnostica un 15% de DIN de todas las neoplasias diagnosticadas • Clínica: asintomáticos en su mayoría • Diagnóstico: microcalcificaciones lineales que siguen el patrón de un conducto. Seguida de distorsión arquitectural y, en menor grado, patrón nodular Nota: el CM microinfiltrante (infiltra < 1 mm). Su comportamiento y pronóstico es similar al CDIS. Requiere BSGC
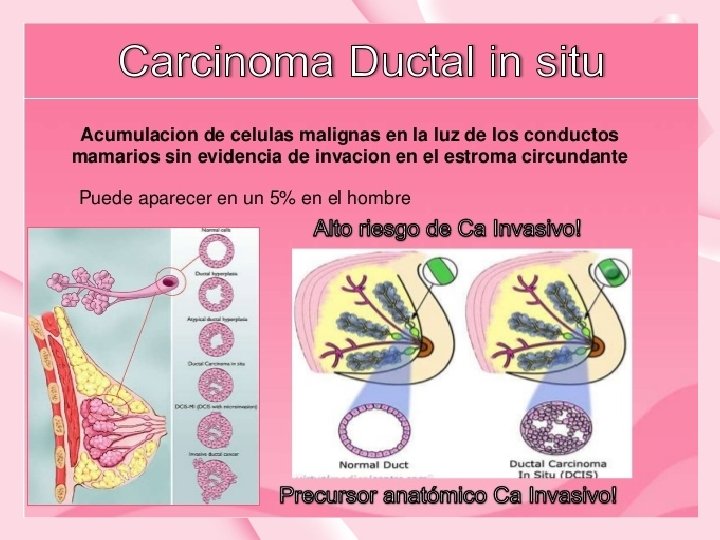
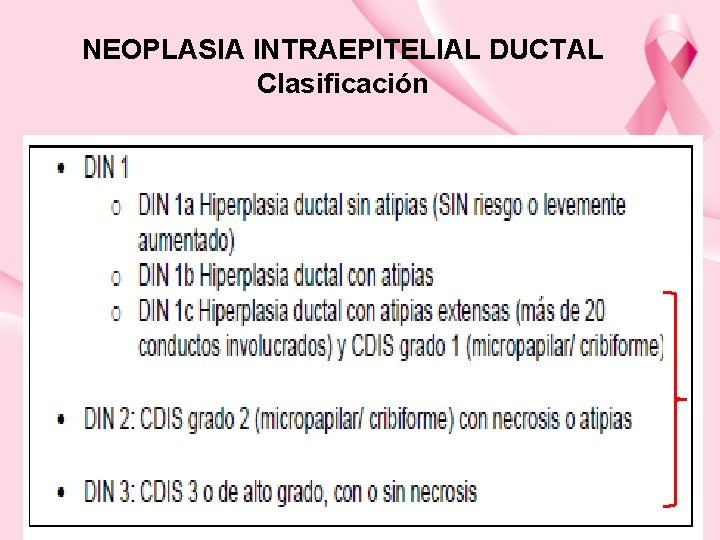
NEOPLASIA INTRAEPITELIAL DUCTAL Clasificación

CARCINOMA DUCTAL IN SITU • Corresponde al DIN 1 c, DIN 2 y DIN 3 • Factores pronósticos ante un CDIS son: * Presencia de necrosis: - Comedocarcinoma: tejido necrótico en la luz ductal con calcificaciones. Generalmente de alto grado y peor pronóstico - No Comedo: subtipos micropapilar, cribiforme y sólido, en orden de mejor a peor pronóstico. * Grado nuclear: grados de Bloom y Richardson (en base a la morfología nuclear, índice mitótico y grado de formación de túbulos) * Tamaño del CDIS * Márgenes de resección: al menos 1 mm de tejido sano

CARCINOMA DUCTAL IN SITU INDICE PRONOSTICO DE VAN NUYS: herramienta para decidir el tratamiento • SI 3 -4: EXCISION • SI 5 -7: EXCISION + RADIOTERAPIA • SI 8 -9: MASTECTOMIA SIMPLE

TT 0 DEL CARCINOMA DUCTAL IN SITU • TUMORECTOMIA SIN RADIOTERAPIA: recurrencias en un 20%, por lo que sólo e debería de indicar en hiperplasias ductales atípicas, CDIS con índice de Van Nuys bajo (3 -4), en pacientes que no toleren la radioterapia, o con expectativas cortas de vida por enfermedades concomitantes. • TUMORECTOMIA + RADIOTERAPIA: DE ELECCION, ya que disminuye de forma significativa las recurrencias (7%) • MASTECTOMIA: sólo si la paciente no acepta el tto conservador, CDIS multicéntrico, e índice pronóstico de Van Nuys alto (8 -9) NO NECESITA CIRUGÍA AXILAR NI RADIOTERAPIA AXILAR: Sólo se acepta en los CDIS extensos (> 3 cm), grado nuclear elevado, comedocarcinoma o microinfiltrante.

NEOPLASIA LOBULILLAR IN SITU • Proliferación de células neoplásicas en la unidad terminal ductolobulillar (TDLU), no invasivo. • Predomina en premenopáusicas (40 -50 años). A diferencia, el CDIS es más frecuente en > 50 años. • Poco frecuente (0. 34 al 2. 9 %) • Asintomático, por lo que su diagnóstico es casual • Es característica la pérdida de expresión de E-cadherina (a diferencia de los ductales). Esto se utiliza como herramienta para diferenciar ductales de lobulillares • El diagnóstico es exclusivamente anatomopatológico, ya que no presenta características clínicas o radiológicas específicas. Se presenta cuando se biopsia la mama por otra lesión, generalmente microcalcificaciones • Predispone a CM ductal y bilateral (aproximadamente 30% de probabilidad e padecer CM invasor en 20 años) • Multicéntrico en el 60 -90 % y bilateral no simultáneo en el 30 -60 %

CLASIFICACION NEOPLASIA LOBULILLAR IN SITU La frecuencia de carcinoma invasor (ductal y lobulillar) aumenta desde el 14 % en LIN 1 al 23 % en LIN 3 •

TTO DEL CARCINOMA LOBULILLAR IN SITU Al no considerarse un verdadero cáncer sino un marcador que identifica a mujeres con > riesgo de CM infiltrante, se propone: • SEGUIMIENTO ANUAL • TUMORECTOMIA: sólo si microcalcificaciones en la mamografía, masas palpables, presencia de necrosis o pleomorfismo, si CDIS asociado o cuando haya discordancia imagen-histología. No precisa márgenes libres • MASTECTOMIA PROFILACTICA: se puede considerar si se asocian otras características de alto riesgo como historia familiar de riesgo o mutaciones BRCA 1 o 2.

CLASIFICACION HISTOLOGICA DEL CM Clasificación histológica del cáncer de mama (OMS) Carcinoma ductal in situ Carcinoma lobulillar in situ Carcinoma ductal invasivo (85% de los casos) Carcinoma lobulillar invasivo (5 -10% de los casos) Carcinoma mucinoso o coloide. 1 -5%. Mujeres mayores. Carcinoma medular. 1 -5%. Mujeres jóvenes. Carcinoma papilar 1% Carcinoma tubular 2%. Mujeres jóvenes. Pronóstico excelente. Carcinoma adenoideo-quístico Carcinoma secretor (juvenil) Carcinoma apocrino Carcinoma metaplásico Carcinoma inflamatorio Enfermedad de Paget del pezón
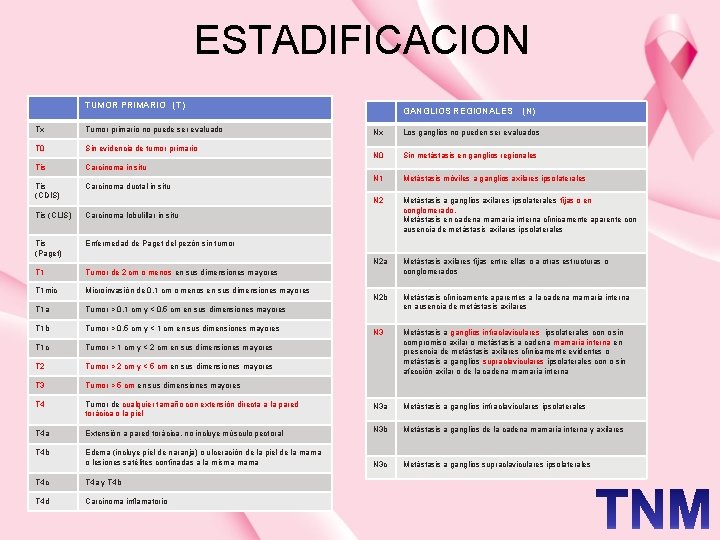
ESTADIFICACION TUMOR PRIMARIO (T) Tx Tumor primario no puede ser evaluado T 0 Sin evidencia de tumor primario Tis Carcinoma in situ Tis (CDIS) Carcinoma ductal in situ Tis (CLIS) Carcinoma lobulillar in situ Tis (Paget) Enfermedad de Paget del pezón sin tumor T 1 Tumor de 2 cm o menos en sus dimensiones mayores T 1 mic Microinvasión de 0. 1 cm o menos en sus dimensiones mayores T 1 a Tumor > 0. 1 cm y < 0. 5 cm en sus dimensiones mayores T 1 b Tumor > 0. 5 cm y < 1 cm en sus dimensiones mayores T 1 c Tumor > 1 cm y < 2 cm en sus dimensiones mayores T 2 Tumor > 2 cm y < 5 cm en sus dimensiones mayores T 3 Tumor > 5 cm en sus dimensiones mayores T 4 Tumor de cualquier tamaño con extensión directa a la pared torácica o la piel T 4 a Extensión a pared torácica, no incluye músculo pectoral T 4 b Edema (incluye piel de naranja) o ulceración de la piel de la mama o lesiones satélites confinadas a la misma mama T 4 c T 4 a y T 4 b T 4 d Carcinoma inflamatorio GANGLIOS REGIONALES (N) Nx Los ganglios no pueden ser evaluados N 0 Sin metástasis en ganglios regionales N 1 Metástasis móviles a ganglios axilares ipsolaterales N 2 Metástasis a ganglios axilares ipsolaterales fijas o en conglomerado. Metástasis en cadena mamaria interna clínicamente aparente con ausencia de metástasis axilares ipsolaterales N 2 a Metástasis axilares fijas entre ellas o a otras estructuras o conglomerados N 2 b Metástasis clínicamente aparentes a la cadena mamaria interna en ausencia de metástasis axilares N 3 Metástasis a ganglios infraclaviculares ipsolaterales con o sin compromiso axilar o metástasis a cadena mamaria interna en presencia de metástasis axilares clínicamente evidentes o metástasis a ganglios supraclaviculares ipsolaterales con o sin afección axilar o de la cadena mamaria interna N 3 a Metástasis a ganglios infraclaviculares ipsolaterales N 3 b Metástasis a ganglios de la cadena mamaria interna y axilares N 3 c Metástasis a ganglios supraclaviculares ipsolaterales

ESTADIFICACION Continuación…. . p. Nx Los ganglios regionales no pueden ser evaluados p. N 0 No hay evidencia histológica de metastasis si se hace búsqueda intencionada de células aisladas p. N 0 (i-) Sin evidencia histológica de metastasis, inmunohistoquimica negativa p. N 0 (i+) Sin evidencia histológica de metástasis, inmunohistoquimica positiva > 0. 2 mm p. N 0 (mol-) Sin evidencia histologica de metástasis, hallazgos moleculares negativos (RT-PCR) p. N 0 (mol+) Sin evidencia histológica de metástasis, hallazgos moleculares positivos (RT-PCR) p. N 1 Metástasis de 1 -3 ganglios axilares o en la cadena mamaria interna detectada por ganglio centinela, pero sin apariencia clínica p. N 1 mi Micrometástasis (> 0. 2 mm pero <2 mm) p. N 1 a Metástasis de 1 -3 ganglios axilares p. N 1 b Metástasis de cadena mamria interna sin evidencia microscópica de enfermedad, detectada por ganglio centinela, clínicamente inaparente p. N 1 c Metástasis de 1 -3 ganglios axilares con enfermedad micróscopica detectada en ganglios de la cadena mamaria interna, clínicamente inaparente p. N 2 Metástasis de 4 -9 ganglios axilares o en ganglios clínicamente aparentes de la cadena mamaria interna en ausencia de metástasis axilares p. N 2 a Metástasis de 4 -9 ganglios axilares (al menos uno >20 mm) p. N 2 b Metástasis en ganglios clínicamente aparentes de la cadena mamaria interna, en ausencia de metástasis axilares p. N 3 Metástasis en 10 o más ganglios axilares o en ganglios infraclaviculares o en ganglios de la cadena mamaria interna clínicamente aparentes en presencia de 1 o más ganglios axilares positivos o en más de 5 ganglios axilares con metástasis microscópicamente negativas de la mamaria interna o metástasis en ganglios supraclaviculares ipsolaterales p. N 3 a Metástasis en 10 o más ganglios axilares o metástasis en ganglios infraclaviculares p. N 3 b Metástasis clínicamente aparentes en la cadena mamria interna en presencia de 1 o más ganglios axilares positivos o más de 3 ganglios axilares y ganglios en la mamaria interna con enfermedad microscópica detectada por ganglio centinela, clínicamente inaparente p. N 3 c Metástasis en ganglios supraclaviculares ipsolaterales METÁSTASIS A DISTANCIA (M) Mx No pueden ser evaluadas M 0 No hay metástasis a distancia M 1 Metástasis a distancia
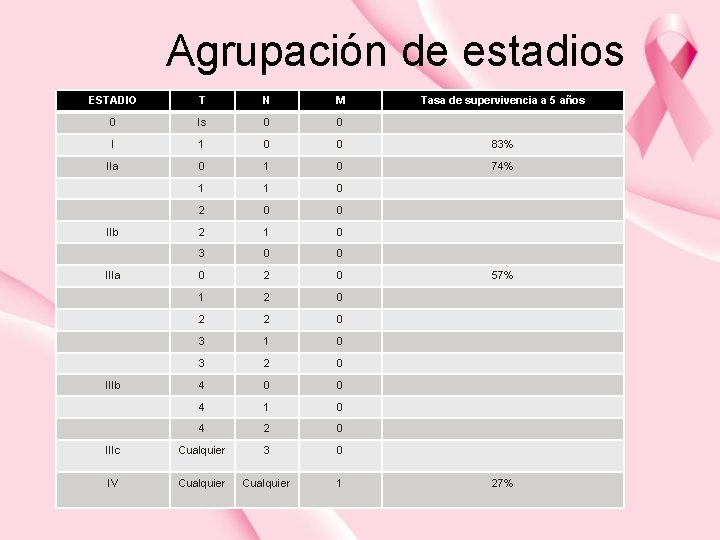
Agrupación de estadios ESTADIO T N M 0 Is 0 0 I 1 0 0 83% IIa 0 1 0 74% 1 1 0 2 0 0 2 1 0 3 0 0 0 2 0 1 2 0 2 2 0 3 1 0 3 2 0 4 0 0 4 1 0 4 2 0 IIIc Cualquier 3 0 IV Cualquier 1 IIb IIIa IIIb Tasa de supervivencia a 5 años 57% 27%
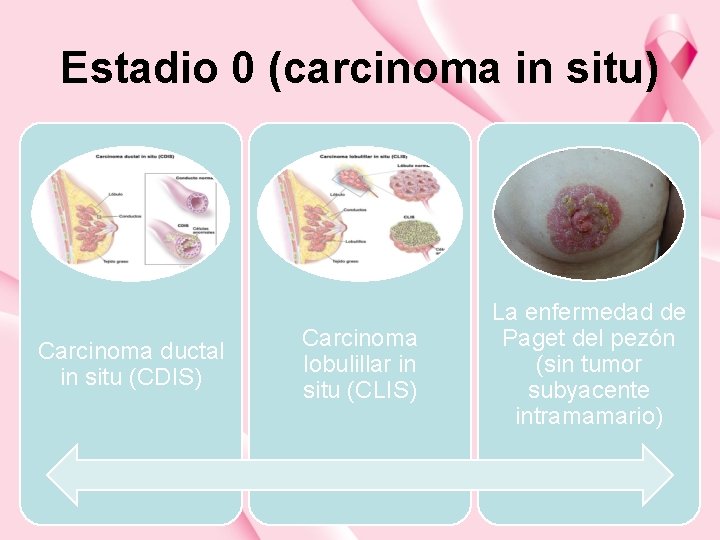
Estadio 0 (carcinoma in situ) Carcinoma ductal in situ (CDIS) Carcinoma lobulillar in situ (CLIS) La enfermedad de Paget del pezón (sin tumor subyacente intramamario)
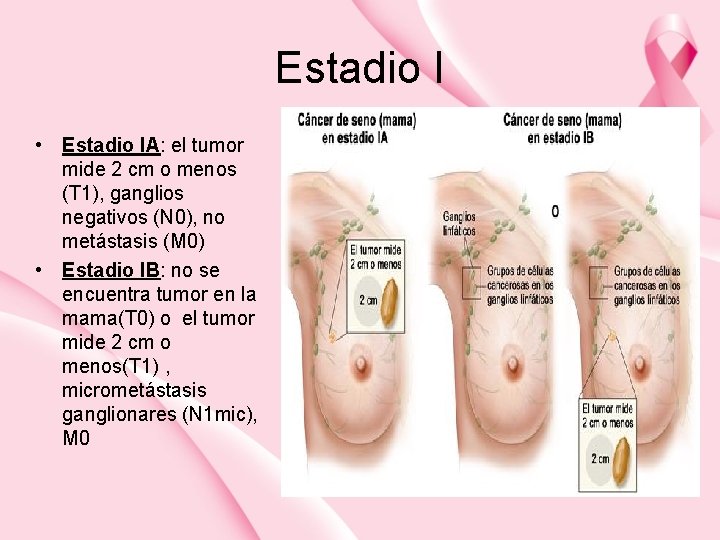
Estadio I • Estadio IA: el tumor mide 2 cm o menos (T 1), ganglios negativos (N 0), no metástasis (M 0) • Estadio IB: no se encuentra tumor en la mama(T 0) o el tumor mide 2 cm o menos(T 1) , micrometástasis ganglionares (N 1 mic), M 0
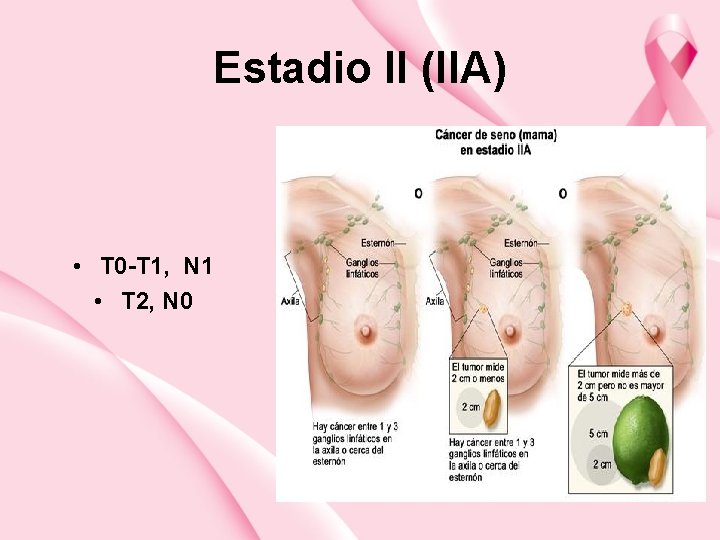
Estadio II (IIA) • T 0 -T 1, N 1 • T 2, N 0
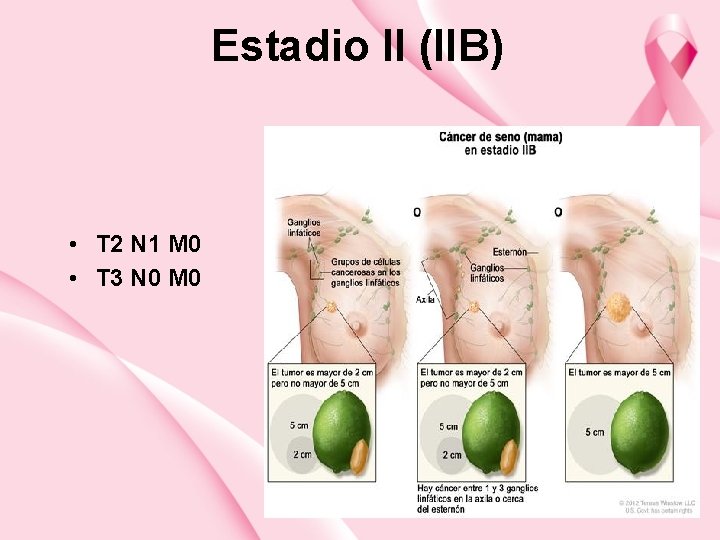
Estadio II (IIB) • T 2 N 1 M 0 • T 3 N 0 M 0
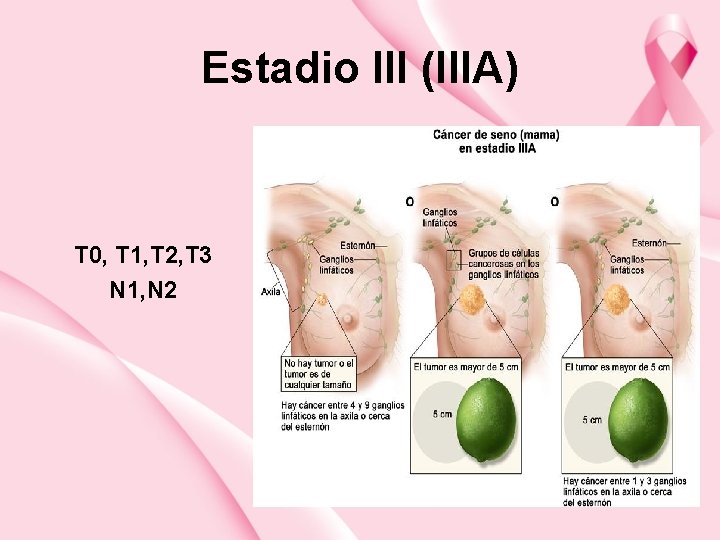
Estadio III (IIIA) T 0, T 1, T 2, T 3 N 1, N 2
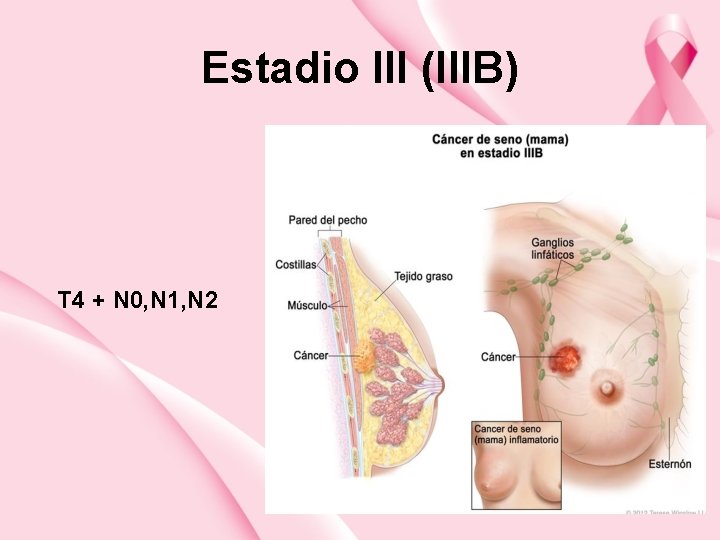
Estadio III (IIIB) T 4 + N 0, N 1, N 2
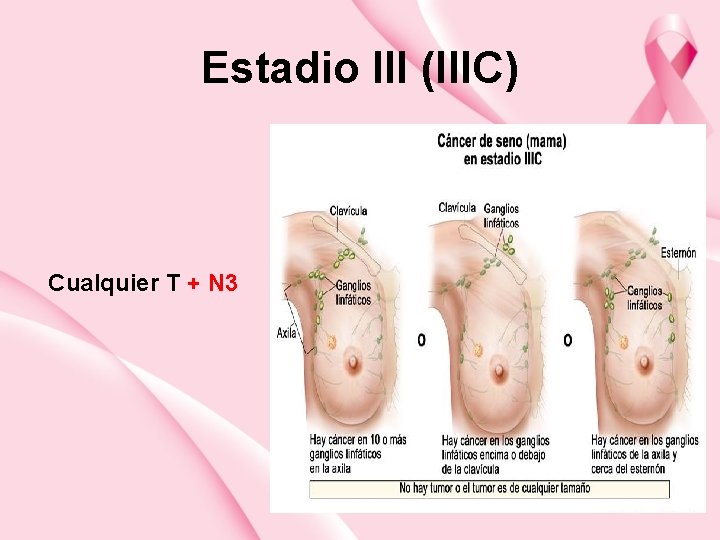
Estadio III (IIIC) Cualquier T + N 3
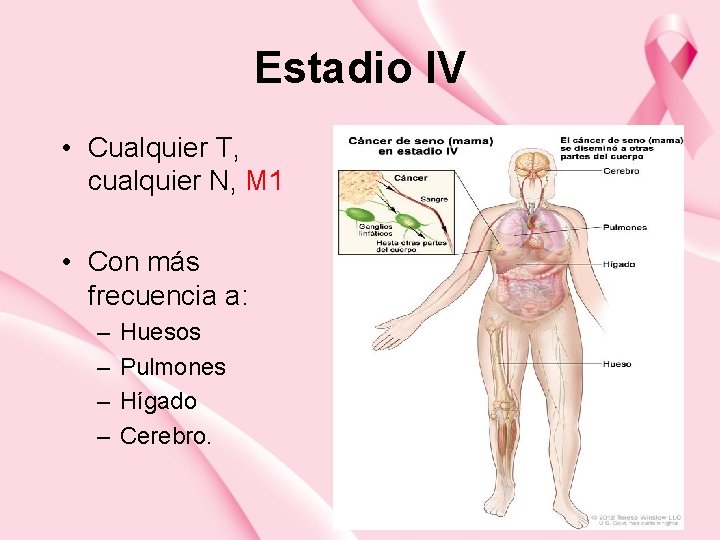
Estadio IV • Cualquier T, cualquier N, M 1 • Con más frecuencia a: – – Huesos Pulmones Hígado Cerebro.
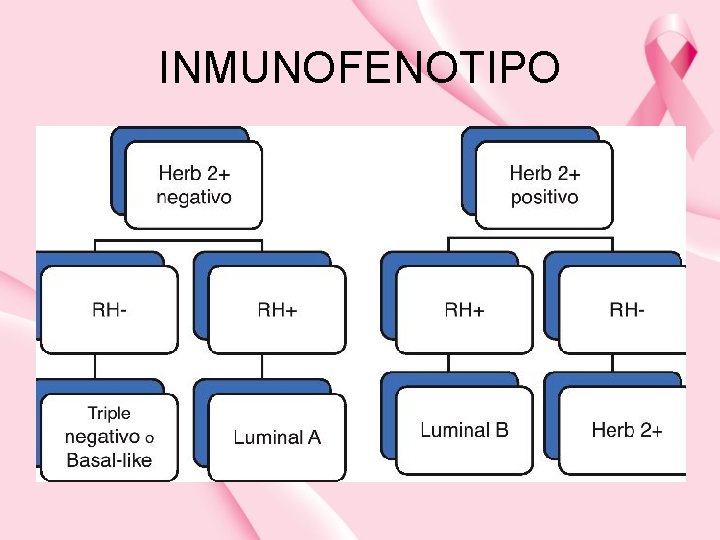
INMUNOFENOTIPO
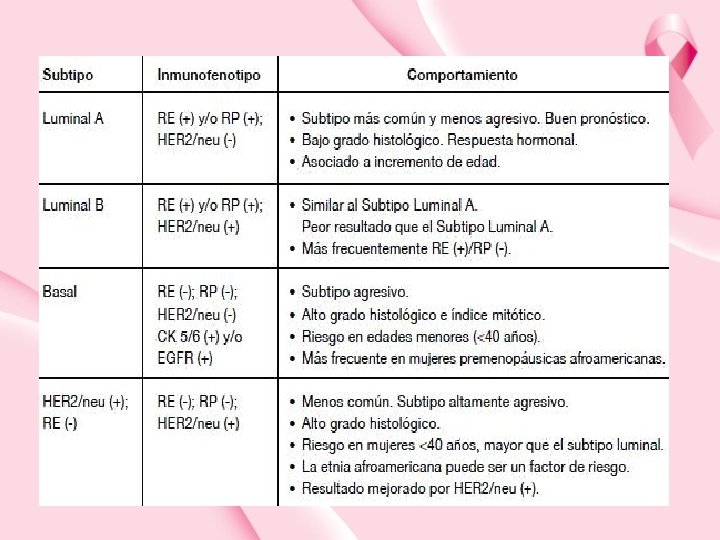
SUBTIPO LUMINAL A LUMINAL B INMUNOFENOTIPO RE+ RP+ HER 2 KI 67 bajo RE+ RP(+/-) HER 2 (+/-) KI 67 alto COMPORTAMIENTO o o o TRIPLE NEGATIVO O BASAL LIKE RERPHER 2 - o o o TIPO HER 2 + REHER 2+ o o o Subtipo más común (50 -60%) Mejor pronóstico Menor incidencia de recaídas. Si lo hace las más frecuentes son óseas y menos viscerales y en SNC > supervivencia en caso de recaídas Alta respuesta a hormonoterapia Escaso beneficio de la quimioterapia 10 -20% de los luminales Peor pronóstico que el luminal A Mayor tasa de recidivas viscerales La supervivencia desde el diagnóstico de la recidiva es inferior Se beneficia de la quimioterapia y hormonoterapia 10 -15 % de los CM Alta tasa de proliferación y mal pronóstico El único tto disponible para estos tumores es la quimioterapia “paradoja del triple negativo”: aunque responden a la quimioterapia, la duración de esta respuesta es corta Un reto para el estudio de nuevos fármacos Peor pronóstico que los luminales Tto específico con Acs monoclonales trastuzumab (herceptin) y pertuzumab, así como pequeñas moléculas como lapitinib y TDM 1 conjugado de anticuerpo y fármaco Alta tasa de respuesta a quimioterapia que incluya antraciclinas y/o taxanos

FACTORES PRONÓSTICOS EN EL CM • Edad: si < 35 años se asocia a alta incidencia de características negativas (grado histológico alto, invasión vascular linfática, componente intraductal extenso, etc. ), tumores más grandes, invasión axilar, RRHH -, índices de proliferación altos y elevada expresión de p 53 • Menopausia: aumenta la frecuencia de receptores hormonales positivos a mayor edad. Cuanto mayor sea el intervalo desde la menopausia mayor probabilidad de respuesta. • ILE en recidivas o metástasis: a mayor intervalo libre mayor sensibilidad a la hormono y quimioterapia • Sexo: peor pronóstico en el varón

FACTORES PRONÓSTICOS EN EL CM • Tamaño tumoral (T): la supervivencia a 5 años es del 91% en tumores < 2 cm y del 63% en > 5 cm. • Ganglios axilares (N): es el factor más importante en CM, pues existe una relación directa entre nº de gglios afectados y la supervivencia, 96 % si gglios negativos y 66 % si afectación de más de 4 gglios • Grado histológico (Bloom-Richardson) y grado nuclear (Fisher)

FACTORES PRONÓSTICOS EN EL CM • Índice de proliferación celular (Ki 67): se asocia a peor pronóstico. Aparte de su valor pronóstico, tiene valor predictivo de respuesta hormonal, ya que la eficacia del tto con letrozol se incrementa en los grupos con ki 67 elevado. • Invasión vascular linfática (IVL): presencia de émbolos tumorales intraendoteliales en el tejido adyacente al tumor. Se considera de mal pronóstico. • Subtipos histológicos: los subtipos papilares, mucinosos, medulares y adenoideos quísticos son de buen pronóstico. El micropapilar y metaplásico son de peor pronóstico.

FACTORES PRONÓSTICOS EN EL CM • Receptores estrogénicos (RE): Ø La tasa anual de recurrencias es > si RE – respecto a las que presentaban RE. Esta probabilidad de recurrencia se iguala a partir de los 5 años. Ø La presencia de RE se asocia con mayor diferenciación histológica, menor índice mitótico y con tumores diploides. Ø En cuanto a la afectación ganglionar, no se ha encontrado relación con la presencia de RE Ø Todos estos datos sugieren que la presencia de RE podría ser mejor marcador de crecimiento tumoral que de capacidad de metástasis.

FACTORES PRONÓSTICOS EN EL CM • Receptores de progesterona (RP): Ø La determinación de RP de forma aislada no se considera un factor predictivo de respuesta a la hormonoterapia y debe valorarse siempre en relación a la presencia o ausencia de RE Ø Sin embargo, se ha demostrado como factor pronóstico independiente de RE y la presencia de afectación ganglionar en pacientes con CM localizado. De hecho, el subtipo luminal B ((RE-/RP+) tienen peor pronóstico que el luminal A (RE y RP positivos)

FACTORES PRONÓSTICOS EN EL CM • Human epidermal growth factor-2 receptor (HER 2): Ø La amplificación y/o sobreexpresión del HER 2 ocurre en el 20% de los CM y se considera factor pronóstico negativo. Ø Se considera positivo si se detecta una alta expresión (> 30 %) Ø El principal atributo del HER 2 es predecir la respuesta biológica con Acs monoclonales (trastuzumab, pertuzumab, TDM 1) y lapatinib, combinados con la quimioterapia, tanto en la enfermedad avanzada como en el tto neoadyuvante y adyuvante. Ø Algunos estudios sugieren que el status HER 2 podría relacionarse con resistencia a citostáticos (antraciclinas o taxanos) y a hormonoterapia

FACTORES PRONÓSTICOS EN EL CM • Proteína p 53: Ø La proteína p 53 actúa como un freno para el crecimiento celular de las células dañadas en el DNA Ø 1/3 de los CM presentan mutaciones del gen p 53 Ø Una expresión elevada de p 53 se asocia a peor pronóstico • Angiogénesis: Ø una mayor neovascularización (regulada por el factor del endotelio vascular VEGF-A) se asocia a peor pronóstico Ø Los ttos antiangiogénicos están en investigación en adyuvancia y no se recomienda usarlos fuera de ensayos clínicos
TRATAMIENTO DEL CM • CIRUGÍA: - tumorectomía - cuadrantectomía - mastectomía - cirugía oncoplástica - BSGC y/o linfadenectomía • QUIMIOTERAPIA • RADIOTERAPIA • HORMONOTERAPIA

TUMORECTOMIA INDICACIONES: - tumor < 4 cm - proporción tamaño tumor-tamaño mama - ausencia multicentricidad(= tumores en distintos cuadrantes) - posibilidad de márgenes libres: en CM infiltrante es suficiente 2 mm (tinta china), y 10 mm en el CDIS (por la tendencia a la multifocalidad). St. Gallen 2015 acepta que el tumor invasivo o in situ no llegue a la tinta independientemente de las características del tumor - ausencia de contraindicación para recibir radioterapia

TUMORECTOMIA CONTRAINDICACIONES ABSOLUTAS: - multicentricidad (¿St. Gallen 2015? ), microcalcificaciones dispersas - irradiación previa de la mama - embarazo, por imposibilidad de radioterapia. Si tercer trimestre se puede realizar tumorectomía y administrar la radioterapia en postparto CONTRAINDICACIONES RELATIVAS: - enfermedades del colágeno por intolerancia a la radioterapia - tumor > 4 cm (mejor neoadyuvancia) - mamas voluminosas por dificultad para conseguir campo de irradiación

MASTECTOMIA TIPOS: • Radical: incluyen linfadenectomía. - Halsted (historia): mama + pectoral > y < + LAH - Patey: mama + pectoral < + LAH - Madden: mama + LAH • Simple o Total: sólo la mama sin LAH • Mastectomía ahorradora de piel • Mastectomía subcutánea: conserva pezón y areola, así como la piel INDICACIONES: las contraindicaciones de la cirugía conservadora

BSGC INDICACIONES • CM invasivo o microinvasivo T 1, T 2 y T 3, con axila clínica, ecográfica y patológicamente (PAAF) negativa • CDIS extenso (>4 cm), de alto grado y/o comedonecrosis • CM en el varón se siguen mismas indicaciones que en mujer • En gestantes o lactantes: no existe evidencia para desaconsejarlo, previa retirada de la lactancia 24 horas. Utilizar dosis mínimas, el mismo día de la cirugía y evitar colorantes vitales • No contraindicado en antecedentes de mamoplastia de aumento o reducción • Si BSGC previa no existe evidencia para desaconsejar una nueva BSGC en caso de recidiva tumoral

BSGC CONTRAINDICACIONES: • CM localmente avanzado con afectación axilar • Afectación axilar confirmado histológicamente (PAAF axilar positivo) • CM inflamatorio • RTx axilar previa ACTITUD ANTE METASTASIS EN GC: • Células tumorales aisladas (p. N 0 i+ o p. N 0 mol+): ≤ 0. 2 mm o < 200 células en un solo corte de tejido. No está indicada LAH ni tto complementario. • Micrometástasis: entre 0. 2 y 2 mm o más de 200 células tumorales en un corte de tejido. No está indicada la LAH. • Macrometástasis: se indica LAH si: - ≥ 3 GC con macrometástasis - si < de 3 GC con macrometástasis se puede evitar la LAH si T 1, T 2 con ganglios clínicamente negativos. Se recomienda RTx que abarque la axila.

NOTAS SOBRE BSGC • EN CASOS DE NEOADYUVANCIA se puede realizar la BSGC aunque aumenta el porcentaje de falsos negativos (13%). Por ello, la otra posibilidad consiste en realizar la BSGC de manera previa a la quimioterapia • Tumores T 4 o carcinoma inflamatorio no son candidatas a GC debido a la posibilidad de obstrucción parcial de linfáticos que pueda incrementar la tasa de falsos negativos • La presencia de ganglios positivos en cadena mamaria interna (son más frecuentes en tumores > 2 cm situados en cuadrantes internos) puede modificar el tto sistémico y la radioterapia, por lo que debe considerarse su exéresis siempre que sea factible con mínima morbilidad

CUANDO HACER LINFADENECTOMIA LAH directamente si: - T 4 y/o Ca. Inflamatorio - Ganglios clínicos y/o ecográficos + con PAAF + LAH tras BSGC si: - T 1, T 2, ¿T 3? (hoy día T 3 se puede considerar como las indicaciones T 1 y T 2) con ganglios clínicos negativos y BSGC con macrometástasis en ≥ 3 GC. (en estos casos se aconseja radioterapia axilar)

QUIMIOTERAPIA INDICACIONES TRADICIONALES Ø CON AFECTACION AXILAR : QTx si ganglios positivos ≥ 4 Ø SIN AFECTACION AXILAR: QTx si factores de riesgo: - Tumor > 2 cm (T 2) - G 2 -G 3 - Invasión vascular o linfática intratumoral - RRHH negativos - Ki 67 alto (>30%) - Edad < 35 años - HER 2 positivo

QUIMIOTERAPIA INDICACIONES ACTUALES • Actualmente (St. Gallen 2015) la administración de quimioterapia se basa en la presencia de: - grado histológico alto (G 2 G 3) - Ki 67 elevado (>30%) - baja expresión de RRHH - positividad para HER 2 - perfil triple negativo No se considera que la afectación axilar justifique “per se” la indicación de quimioterapia

QUIMIOTERAPIA. ST. GALLEN 2015 • LUMINAL A: HT . QTX sólo si factores de riesgo (tamaño tumoral, invasión linfovascular, 4 o más gglios afectos, grado III. No sería indicación tener < 35 años o la invasión de 1 -3 gglios axilares). ACx 4 ó CMFx 6 • LUMINAL B: * HER 2 negativo: HT. QTX sólo si factores de riesgo * HER 2 positivo: HT + QTX + Trastuzumab ACx 4 ± taxanos • TIPO HER 2+: QTX + Trastuzumab ACx 4 + paclitaxel + Trastuzumab • TRIPLE NEGATIVO: sólo QTX. ACx 4 seguido de taxano (paclitaxel semanal preferente). Si mutación BRCA considerar derivado del platino

TERAPIA DIRIGIDA EN HER 2 +. TTO BIOLOGICO • Es un tipo de tratamiento en el que se utilizan medicamentos para identificar y atacar células cancerosas específicas sin dañar las células normales. – Anticuerpos monoclonales (trastuzumab, pertuzumab, bevamizumb y trastuzumab emtansina o TDM 1). La principal toxicidad es la cardíaca. , con disminución de la FE del VI, que suele revertir tras el tto. – Inhibidores de la tirosin-kinasa (lapatinib) actúa inhibiendo HER 2 y EGFR

RADIOTERAPIA • TRAS CIRUGÍA CONSERVADORA: siempre, ya que disminuye la tasa de recidivas. • TRAS MASTECTOMIA: la RTx sobre pared torácica y áreas ganglionares regionales, se administra en pacientes consideradas de alto riesgo, ya que disminuye la recaída locorregional y aumenta la supervivencia global. Se recomienda iniciarla antes de las 12 -16 semanas de cirugía Normalmente 25 sesiones en total (5 por semana) Incidencia de 0. 2 % de sarcomas a 10 años

HORMONOTERAPIA • TAMOXIFENO: es un SERMs (modulador selectivo de los receptores de estrógenos) con acción antiestrogénica en la mama y estrogénica en hueso, hígado y útero. 20 mg/día durante 5 años reduce a 15 años Un 33% la recurrencia y un 9% la mortalidad • INHIBIDORES DE LA SÍNTESIS DE ESTRÓGENOS: - Inhibidores de la aromatasa (anastrozol, letrozol, exemestano): su uso en premenopáusicas está contraindicado pq aumenta la secreción de gonadotropinas debido a la inhibición del feedback de los estrógenos - Análogos de la Gn. RH: supresión reversible de la función ovárica

TAMOXIFENO • 20 mg/día durante 5 años reduce a 15 años un 33% la recurrencia y un 9% la mortalidad • En el caso de precisar quimioterapia, el tamoxifeno se debe administrar siempre al finalizar la quimioterapia (nivel de evidencia IA) • Contraindicado su uso durante el embarazo y la lactancia al ser teratogénico • No causa infertilidad, incluso puede inducir la ovulación, por lo que deben adoptar medidas anticonceptivas durante su toma y hasta dos meses después de suspender el tratamiento • Riesgo de tromboembolismos venosos, pólipos e hiperplasia endometrial, fibromas, cáncer de endometrio y sarcoma uterino (principalmente tumores mullerianos mixtos malignos). En premenopáusicas no parece aumentar el riesgo de cáncer de endometrio. No requieren controles especiales, sólo si sangrados anómalos.

INHIBIDORES DE LA AROMATASA • Indicado solamente en postmenopáusicas. No en pre o perimenopáusicas. • Existen distintos regímenes de administración: - IA durante 5 años - Tamoxifeno 2 -3 años + IA hasta completar 5 años (terapia secuencial) - Tamoxifeno 5 años + IA otros 5 años (terapia prolongada) • Perfil más favorable a nivel de endometrio pero peor a nivel óseo con más fracturas y mayor pérdida de densidad mineral ósea • Menor tasa de recurrencias, mayor tiempo libre de enfermedad y mayor supervivencia global que las pacientes postmenopáusicas en monoterapia con tamoxifeno • Por tanto, el uso de tamoxifeno en monoterapia en pacientes postmenopáusicas debe relegarse sólo a aquellas pacientes contraindicaciones para el uso de IA o que los rechazan

HT EN PREMENOPAUSICAS ST. GALLEN 2015 • Tres posibilidades: - Tamoxifeno - Supresión ovárica + Exemestano • La supresión ovárica se considera indicada en : - < 35 años - niveles altos de estrógenos tras la quimioterapia - más de 4 ganglios axilares afectos - grado III - perfil genético de alto riesgo • Parece más efectiva la supresión ovárica más exemestano (respecto a supresión ovárica más tamoxifeno) en las pacientes consideradas de mayor riesgo, contemplando análogos 5 años y completando tto hormonal hasta 10 años

HT EN POSTMENOPAUSICAS ST. GALLEN 2015 • Sólo Tamoxifeno es una buen opción si bajo riesgo. Tras dos años se puede continuar con tamoxifeno o pasar a IA • Tras 5 años de tamoxifeno se puede continuar el tto hormonal hasta 10 años (opción recomendada en ganglios positivos) o bien parar el tto hormonal (opción recomendada en ganglios negativos) • Inhibidor de la aromatasa si: - más de 4 ganglios afectos - Grado III - Ki 67 alto - edad < 60 años - Her 2 positivo

CANCER DE MAMA Y EMBARAZO • El parto precoz debe evitarse si es posible • La quimioterapia estándar puede administrarse durante el 2º y 3º trimestre, pero no los ttos endocrinos (teratogenos) y anti. Her 2 (produce oligoamnios) • El tto conservador es una opción razonable (la indicación de la técnica quirúrgica es la misma que en no embarazadas) y la BSGC usando radioisótopos es segura (los colorantes vitales están contraindicados) • Puede considerarse una reconstrucción inmediata post mastectomía • En el diagnóstico se incluye ecografía y mamografía (no presenta riesgos para el feto). La RMN no debe realizarse de forma rutinaria • El embarazo tras haber tenido un CM no empeora el pronóstico

CM LOCALMENTE AVANZADO • Concepto que incluye la inoperabilidad como tto inicial, incluyendo por tanto: - tumor > de 5 cm (T 3) - los T 4 (afectación de piel y/o pared costal) - los N 2 (ganglios axilares fijos) - los ganglios supraclaviculares positivos - el carcinoma inflamatorio • La secuencia de tratamiento recomendada es: 1. QTx neoadyuvante: el 80% responden, 20% de remisión completa 2. Cirugía: casi siempre mastectomía más LAH (en casos seleccionados cirugía conservadora) 3. QTX complementaria 4. Rtx Nota: BSGC indicada sólo hasta T 3. no en T 4 o cáncer inflamatorio

ENFERMEDAD DE PAGET • Concepto: lesión neoplásica del epitelio escamoso de la piel de areola y/o pezón caracterizadas por las células de Paget (citoplasma amplio y claro con nucleolos aumentados) • Más del 87% tienen un CM subyacente, invasivo o in situ, en región retroareolar o alejada de ella. Por tanto: - EPP - Carcinoma intraductal intramamario asociado a EPP - carcinoma infiltrante asociado a EPP • El tratamiento puede contemplar: - cirugía conservadora según los criteros del CM subyacente pero siempre incluyendo la exéresis del CAP con margen de seguridad - si EPP sin CM subyacente: exéresis del CAP con margen de seguridad • Las indicaciones de BSGC las marca el CM subyacente

Gracias por su atención
- Slides: 85