Cmo estn distribuidos los electrones de un tomo


¿ Cómo están distribuidos los electrones de un átomo entre sus niveles energéticos ?

• Los niveles energéticos en un átomo se pueden visualizar como un hotel en el cual las mejores habitaciones dobles están en el primer piso.

Distribución de Electrones por Niveles de Energía ATOM’S HOTEL Séptimo Nivel Sexto Nivel Quinto Nivel Cuarto Nivel Tercer Nivel Segundo Nivel Primer Nivel

ATOM’S HOTEL Los electrones como los inquilinos tratarán de ocupar primero las mejores habitaciones del piso 1 y cuando se llene todo el piso, los demás inquilinos comenzarán a ocupar el segundo.

Algunos niveles de energía que rodean a un átomo son: Niveles de Energía Primero Segundo Tercero Cuarto Núcleo

Repasemos algunos conceptos y principios necesarios para representar las configuraciones electrónicas de los átomos.

Cuando trabajamos con la configuaración electrónica de un elemento la partícula principal es el electrón.

Definición de configuración electrónica: es la distribución de electrones a través de los orbitales de un átomo.

Niveles y subniveles • Los niveles de energía tienen ciertos subniveles como: s, p, d y f. EL primer nivel de energía consta de un solo subnivel(1 s), el segundo nivel tiene dos subniveles (2 s y 2 p), el nivel 3 posee tres subniveles(3 s, 3 p y 3 d) y así sucesivamente.

Capacidad de electrones en cada subnivel Subnivel Capacidad de electrones s 2 p 6 d 10 f 14
Diagrama de relación entre los niveles, subniveles y orbitales Veamos la próxima página.
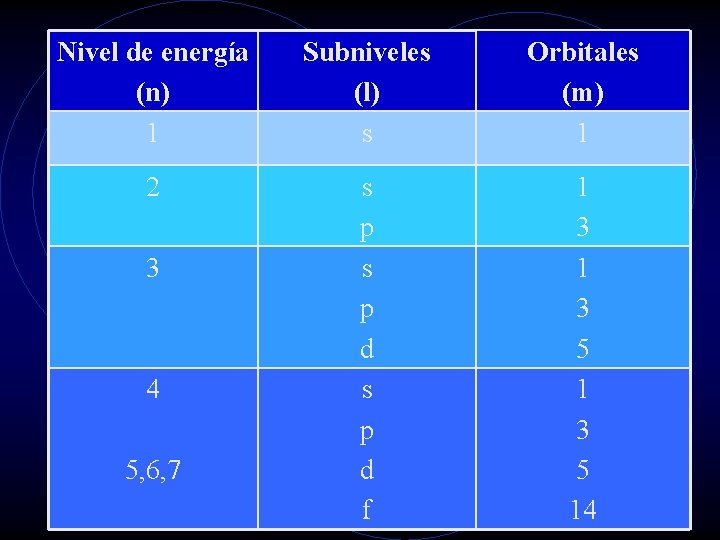
Nivel de energía (n) 1 Subniveles (l) s Orbitales (m) 1 2 s p d f 1 3 5 14 3 4 5, 6, 7

El principio de exclusión de Pauli establece que un máximo de dos electrones pueden ocupar un mismo orbital atómico, pero si los electrones tienen espines opuestos.

El primer electrón se representa con una flecha hacia arriba , describiendo el giro del electrón a favor de las manecillas del reloj y el segundo se representa con una flecha hacia abajo, indicando que el espín del electrón es en contra de las manecillas del reloj.
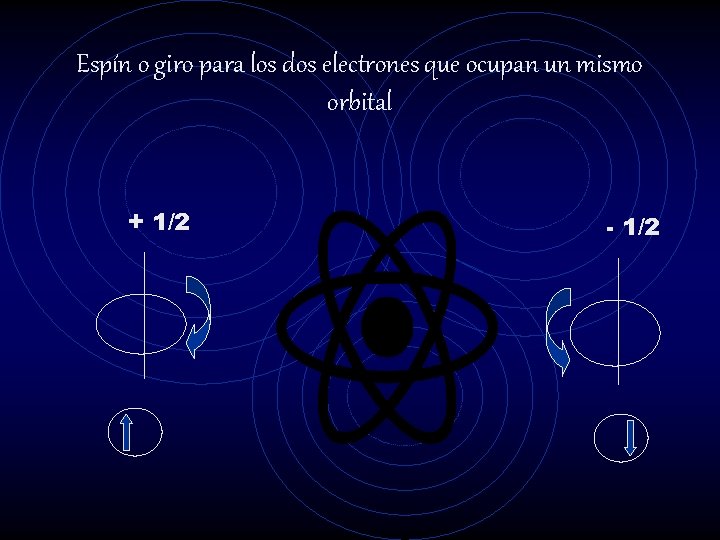
Espín o giro para los dos electrones que ocupan un mismo orbital + 1/2 - 1/2

Regla de Hund establece que electrones cuyo giro es igual deben ocupar todos los orbitales que tienen igual energía, antes de que electrones adicionales que tengan espines opuestos puedan ocupar los mismos orbitales.
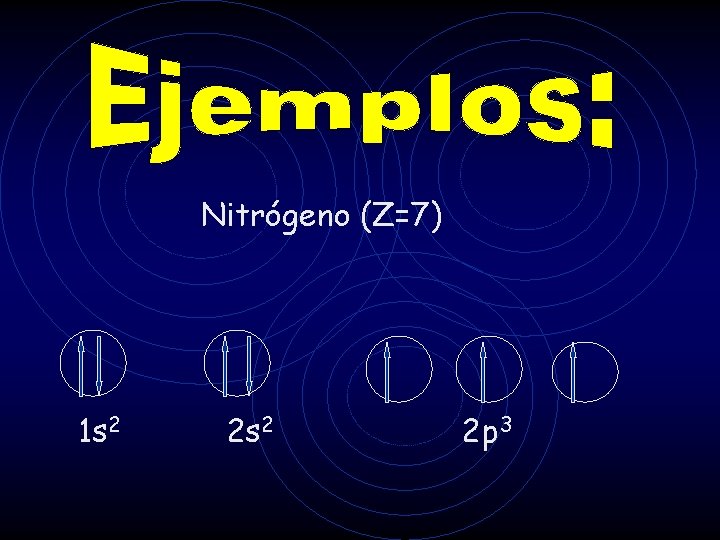
Nitrógeno (Z=7) 1 s 2 2 p 3
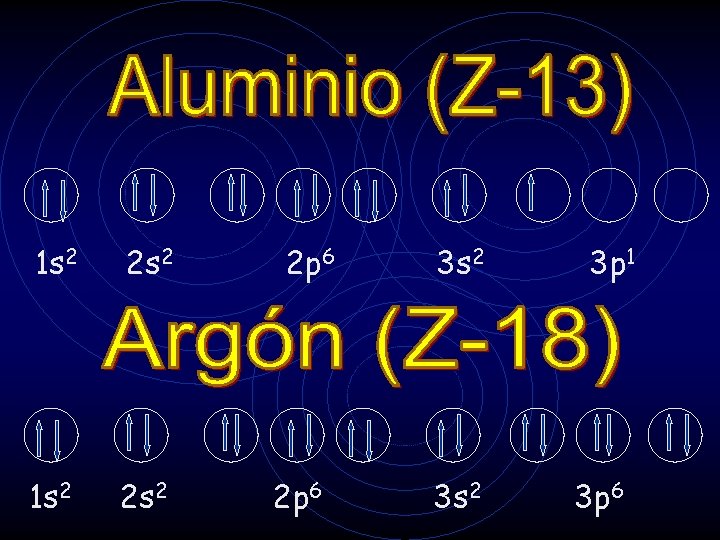
1 s 2 2 s 2 2 p 6 3 s 2 3 p 1 3 p 6

Orden para llenar los orbitales según la Regla Diagonal: 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 6 6 s 2 4 f 14 5 d 10 6 p 6 7 s 2 5 f 14 6 d 10 7 p 6

Configuración electrónica de Ge: 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 2

Si sigues la regla diagonal no hay razón para que te exaltes o te sientas inquieto(a).

A. Identifica a que elemento pertenece cada una de las siguientes configuraciones: 1. 1 s 2 2 p 1= 2. 2. 1 s 2 2 p 4= 3. 3. 1 s 2 2 p 6 3 s 2 3 p 6= 4. 4. 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1=

B. Escribe la configuración electrónica de los siguientes elementos: 1. Galio (Z=31) 2. Niquel (Z=28) 3. Circonio (Z=40) 4. Indio (Z=49)

- Slides: 25