CLCULO DE CONCENTRAES E PREPARAES DE SOLUES TAMPO











- Slides: 12

CÁLCULO DE CONCENTRAÇÕES E PREPARAÇÕES DE SOLUÇÕES TAMPÃO MFB – 1004 BIOCIÊNCIAS Ivanise Correia

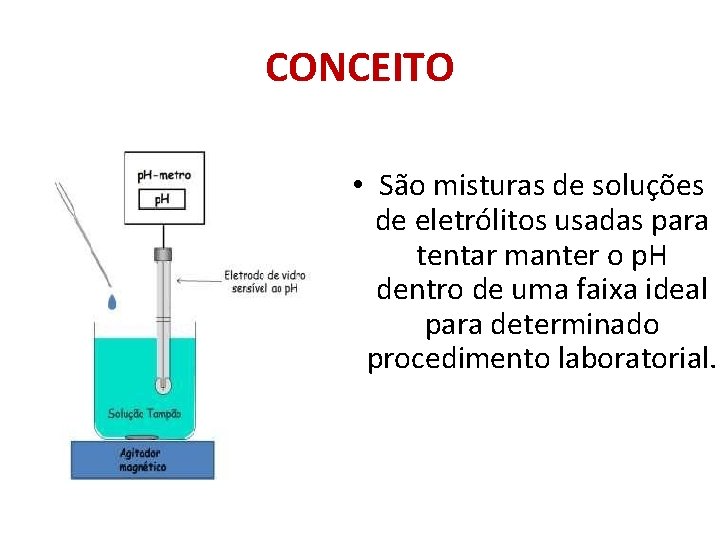
CONCEITO • São misturas de soluções de eletrólitos usadas para tentar manter o p. H dentro de uma faixa ideal para determinado procedimento laboratorial.

CONCEITO • Eletrólitos são substâncias que, quando adicionadas em água, sofrem dissociação (liberam íons) ou ionização (produzem íons). No caso da solução-tampão, além dos sais, são utilizados outro eletrólito: um ácido ou uma base fracos. • Uma solução tampão é composta de um par ácido fraco (ácido conjugado) e seu sal (base conjugada) OU de um composto de uma base fraca (base conjugada) e seu respectivo par (ácido conjugado).

Ácidos fracos • Hidrácidos fracos • São todos os ácidos que não apresentam oxigênio na sua composição e que não têm os ânions cloreto (Cl-), brometo (Br-), iodeto (I-) ou o fluoreto (F-). • Oxiácidos fracos • São todos os ácidos que apresentam oxigênio na sua composição. Nesses compostos, a subtração da quantidade de oxigênios pela quantidade de hidrogênios deverá resultar em zero. Observe o exemplo do ácido bórico (H 3 BO 3): • Obs. : o ácido carbônico (H 2 CO 3), apesar de não seguir a regra proposta, é um oxiácido fraco.

Bases fracas • Uma base é considerada fraca quando não apresenta metal alcalino (elemento pertencente à família IA da tabela periódica Lítio (Li), Sódio (Na), Potássio (K), Rubídio (Rb), Césio (Cs), Frâncio (Fr)) ou metal alcalinoterroso (elemento pertencente à família IIA da tabela periódica - Berílio (Be), Magnésio (Mg), Cálcio (Ca), Estrôncio (Sr), Bário (Ba), Rádio (Ra)).

Comportamento e p. H de uma solução-tampão • As soluções-tampão podem ser ácidas ou básicas, característica associada ao seu p. H (potencial hidrogeniônico ou concentração de íons H+ de um meio). • Na teoria do p. H, meio ácido é aquele que apresenta p. H menor que 7, enquanto meio básico é aquele que apresenta p. H maior que 7. Essas referências são também utilizadas para as soluções-tampão.

Solução-tampão e Bioquímica • A Bioquímica estuda as estruturas (vitaminas, proteínas, carboidratos, etc), a organização e as transformações moleculares que ocorrem na célula (metabolismo) e no meio onde as células estão inseridas. Esses fatores são fundamentais para garantir a sobrevivência, o crescimento e a reprodução dos organismos vivos. • Nas células e fora das células, ocorrem várias reações químicas para a manutenção do organismo vivo. Essas reações, porém, só ocorrem em uma faixa de p. H adequada. • As soluções-tampão têm um papel importante na manutenção do p. H, tanto intracelular quanto do meio extracelular, para o funcionamento de todo o sistema biológico.

Solução-tampão e Bioquímica • Existem várias soluções-tampão em um organismo vivo: • Solução-tampão formado por ácido carbônico e bicarbonato de sódio, substâncias presentes no sangue; • Solução-tampão com a mistura tris-acetato, usada para separar o DNA do RNA; • Solução-tampão de histidina, de glicina e de citrato, soluções-tampão enzimáticas que participam do metabolismo.

Aplicações das soluções-tampão • Biológicas • O sangue é uma solução-tampão formada, principalmente, por substâncias como ácido carbônico (H 2 CO 3) e ânion bicarbonato (HCO 3 -). • Os sistemas enzimáticos relacionados com a proteína histidina também são soluções-tampão. • Químicas • Reações de precipitação, nas quais os produtos formados precipitam na forma de um sólido em virtude da variação no p. H do meio, são soluções-tampão. • Reações eletródicas, que ocorrem em uma pilha ou em uma eletrólise, são também soluções-tampão.

Aplicações das soluções-tampão • Biotecnológicas • Eletroforese: solução-tampão com a presença da substância tris-acetato, que permite a separação do RNA e do DNA da célula. • Quebra do DNA: durante a extração e quebra do DNA, deve haver uma solução-tampão capaz de mantê-lo íntegro. • Lavagem de células: solução-tampão formado por sal e fosfato que tem a função de manter o meio onde as células estão com condições próximas àquelas encontradas no corpo humano.

CONCEITO • 1 - Concentração do tampão: É expressa em molaridade e representa a soma das concentrações dois componentes do tampão (ácido+base). Exemplificando, tampão acetato 0, 1 M significa que a soma do número de mols do ácido mais a do sal é igual a 0, 1. • 2 - p. H do tampão : É dado pela relação do nº. de mols do sal pelo ácido e matematicamente expressa pela fórmula: • p. H = p. Ka + log [sal] / [ácido] (1) • p. Ka = -log Keq • Sendo que pka é uma constante para determinado ácido, valor esse encontrado em manuais de laboratório, e Keq é a constante de equilíbrio de dissociação do ácido fraco.

ATIVIDADE • Tampão fosfato p. H 5, 5 • - Solução A: Dissolver 13, 6 g de fosfato de potássio monobásico em água e completar para 1. 000 m. L com o mesmo solvente. • - Solução B: Dissolver 35, 8 g de fosfato de sódio dibásico dodecahidratado em água e completar para 1000 m. L com o mesmo solvente. • Preparação: Misturar 96, 4 m. L da Solução A e 3, 6 m. L da Solução B. • Segundo a Farmacopeia Brasileira, é ideal que a água usada seja isenta de dióxido de carbono. A solução tampão preparada deverá ser acondicionada em frascos hermeticamente fechados e nas quantidades que serão utilizadas.