Classificazione in base a MECCANISMO monomero Specie attiva
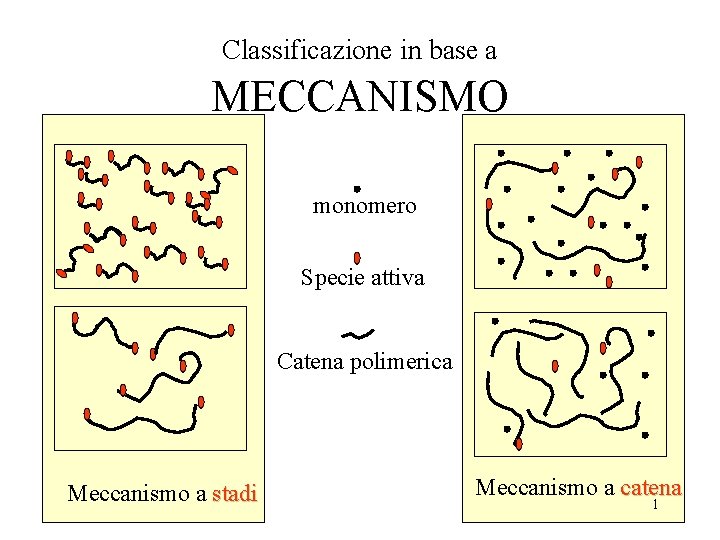
Classificazione in base a MECCANISMO monomero Specie attiva Catena polimerica Meccanismo a stadi Meccanismo a catena 1
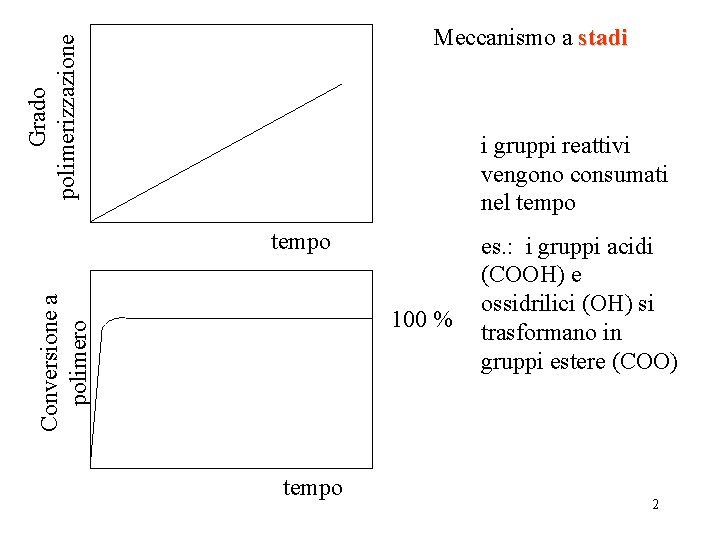
Grado polimerizzazione Meccanismo a stadi i gruppi reattivi vengono consumati nel tempo Conversione a polimero tempo 100 % tempo es. : i gruppi acidi (COOH) e ossidrilici (OH) si trasformano in gruppi estere (COO) 2
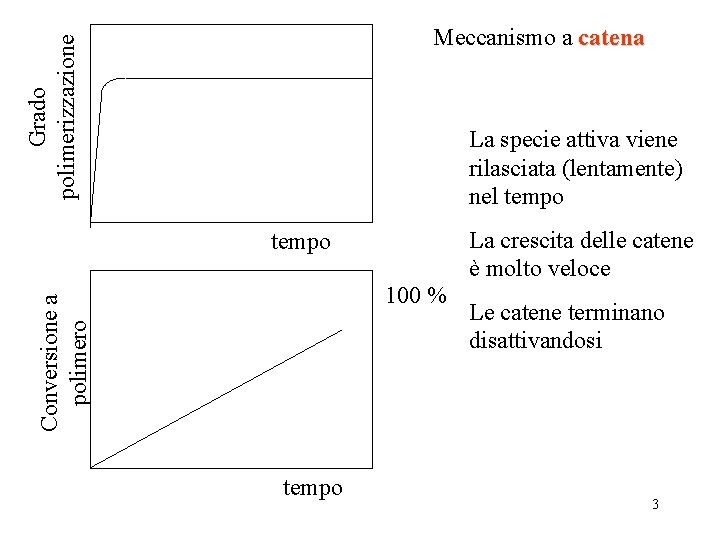
Grado polimerizzazione Meccanismo a catena La specie attiva viene rilasciata (lentamente) nel tempo Conversione a polimero 100 % tempo La crescita delle catene è molto veloce Le catene terminano disattivandosi 3

Altre polimerizzazioni • Interscambio (Es: acetalico, estereo) • Modifica di catene già formate: Idrolisi, esterificazione…. • Polimerizzazioni “viventi ” • Metatesi • Per apertura di anello (ROMP) 4
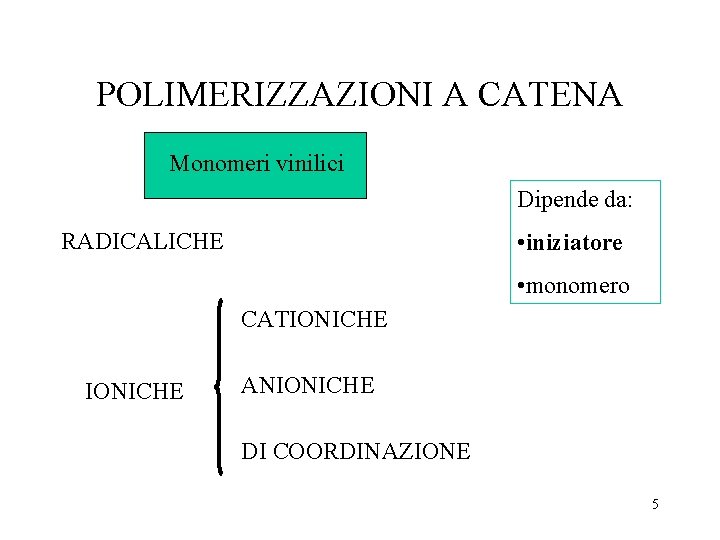
POLIMERIZZAZIONI A CATENA Monomeri vinilici Dipende da: RADICALICHE • iniziatore • monomero CATIONICHE ANIONICHE DI COORDINAZIONE 5
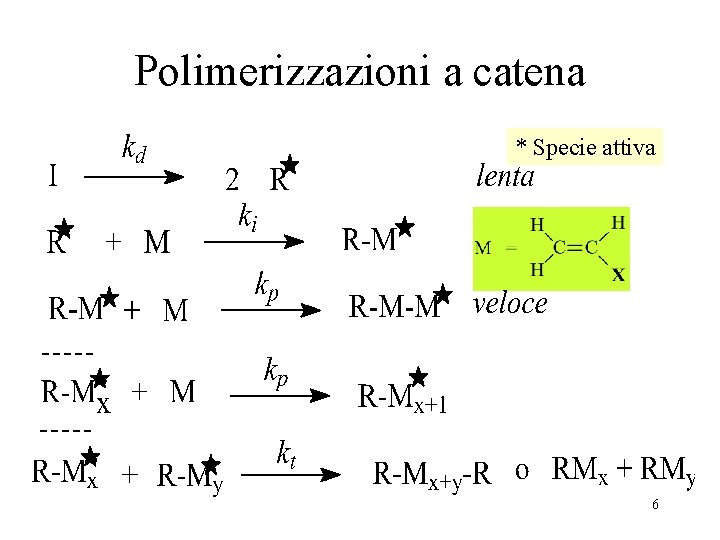
Polimerizzazioni a catena * Specie attiva 6
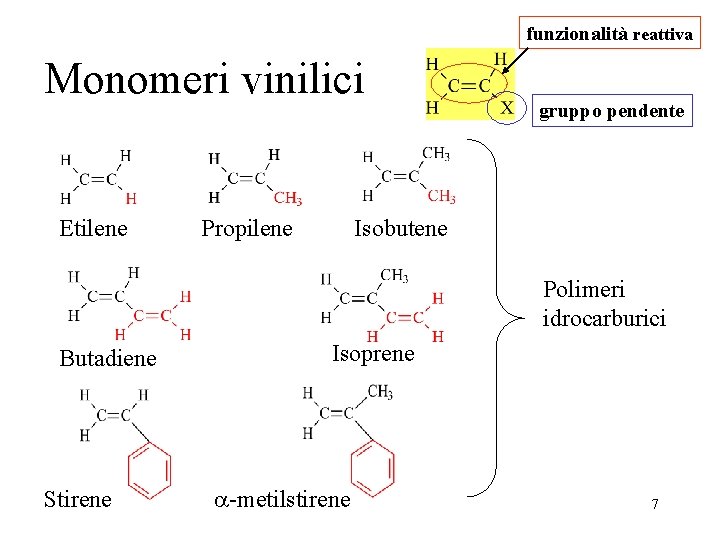
funzionalità reattiva Monomeri vinilici Etilene Propilene gruppo pendente Isobutene Polimeri idrocarburici Butadiene Stirene Isoprene a-metilstirene 7
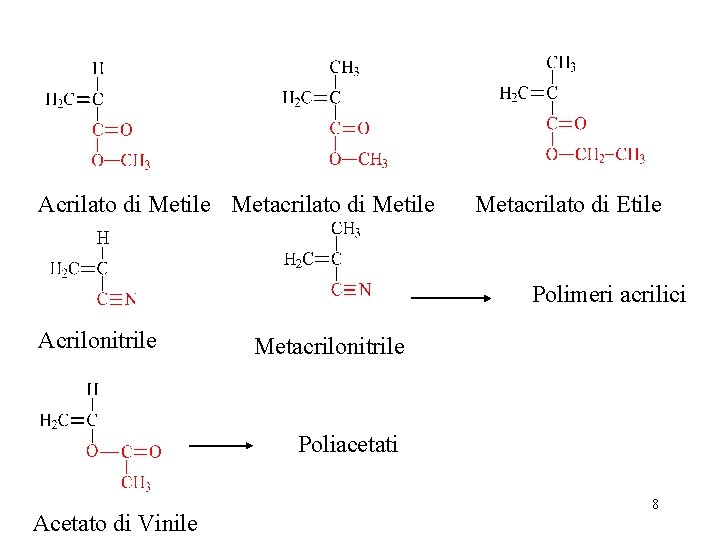
Acrilato di Metile Metacrilato di Etile Polimeri acrilici Acrilonitrile Metacrilonitrile Poliacetati Acetato di Vinile 8
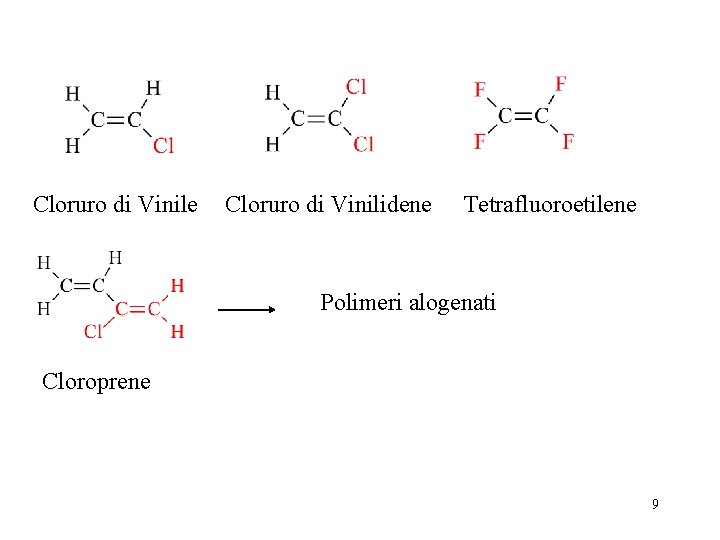
Cloruro di Vinile Cloruro di Vinilidene Tetrafluoroetilene Polimeri alogenati Cloroprene 9
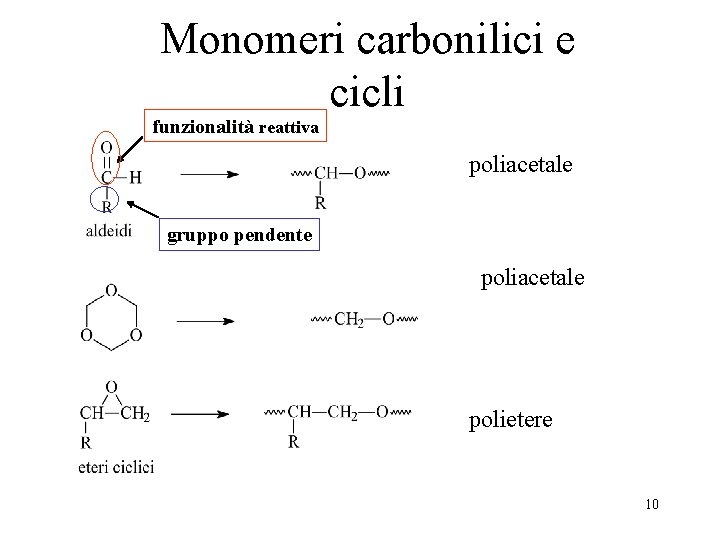
Monomeri carbonilici e cicli funzionalità reattiva poliacetale gruppo pendente poliacetale polietere 10
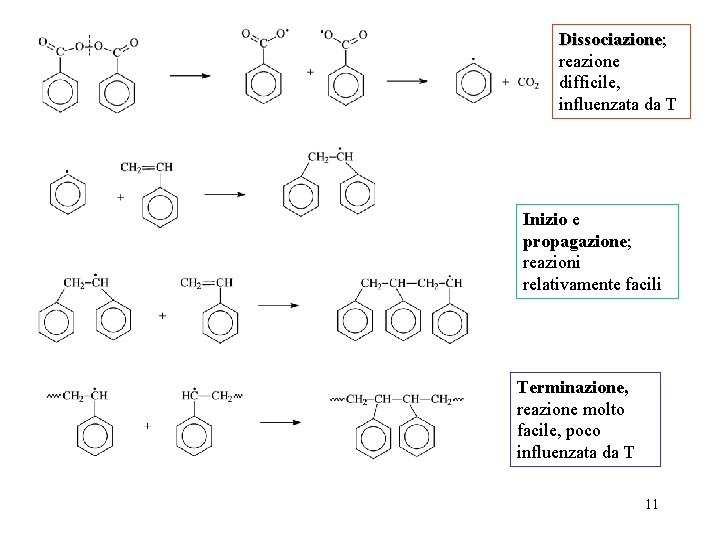
Dissociazione; Dissociazione reazione difficile, influenzata da T Inizio e propagazione; reazioni relativamente facili Terminazione, reazione molto facile, poco influenzata da T 11
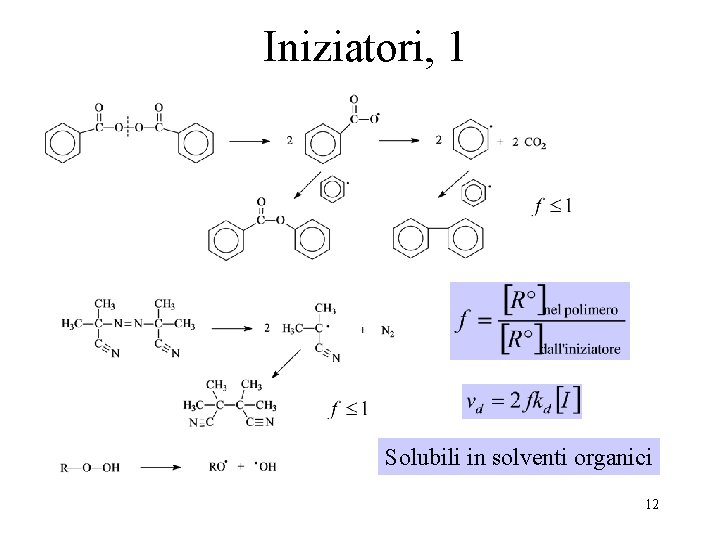
Iniziatori, 1 Solubili in solventi organici 12
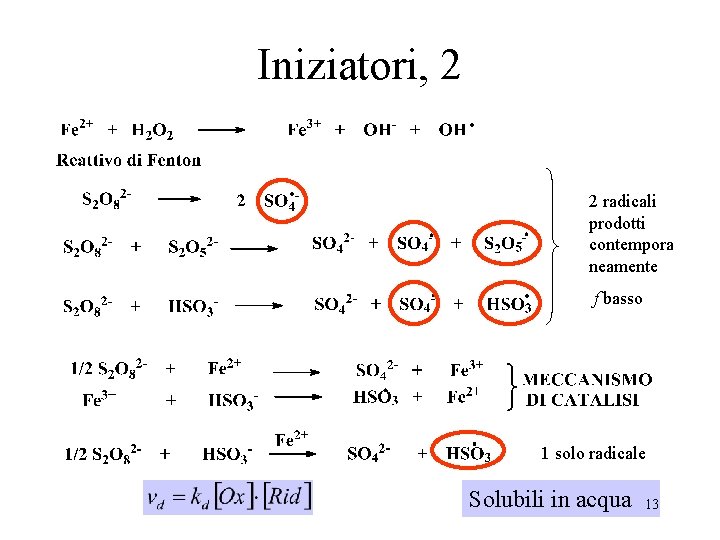
Iniziatori, 2 2 radicali prodotti contempora neamente f basso 1 solo radicale Solubili in acqua 13
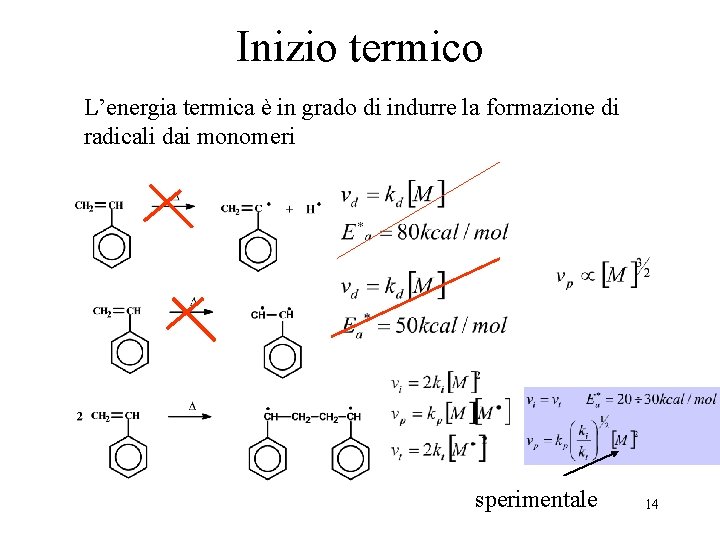
Inizio termico L’energia termica è in grado di indurre la formazione di radicali dai monomeri sperimentale 14
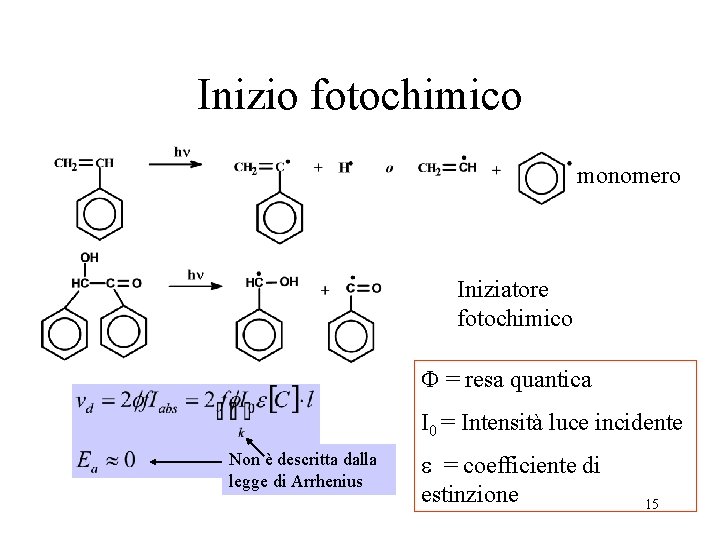
Inizio fotochimico monomero Iniziatore fotochimico F = resa quantica I 0 = Intensità luce incidente Non è descritta dalla legge di Arrhenius e = coefficiente di estinzione 15
![kd kd · I ® 2 R vd = 2 fkd [I ] kd kd kd · I ® 2 R vd = 2 fkd [I ] kd](http://slidetodoc.com/presentation_image/00d20b668ded0f3dc54f2fa68c0781e1/image-16.jpg)
kd kd · I ® 2 R vd = 2 fkd [I ] kd (sec-1) Ed* (k. Jmol-1) T(°C) benzene 3. 17 e-5 123. 4 70 CCl 4 2. 15 e-7 128. 4 40 toluene 1. 60 e-3 121. 3 100 t. But perossido in benzene 8. 80 e-7 146. 9 100 BOPin benzene 1. 48 e-5 123. 8 70 cumene 1. 45 e-6 120. 5 60 AIBN in t. But idroperossido benzene 2. 00 e-5 170. 7 16 169
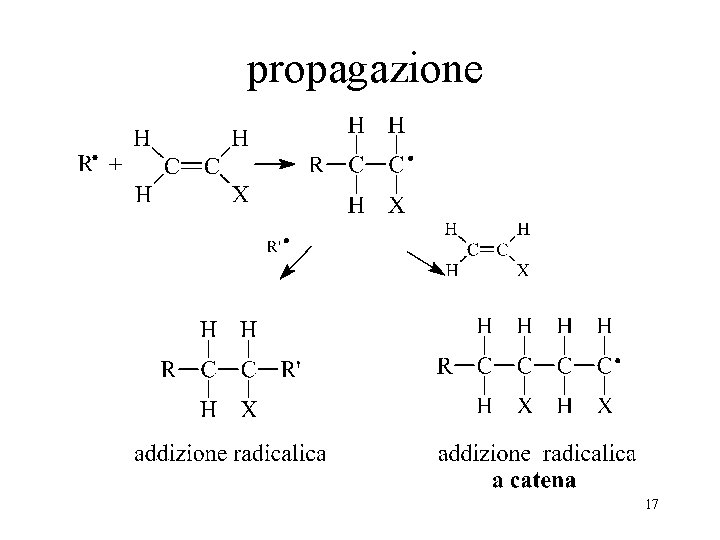
propagazione 17
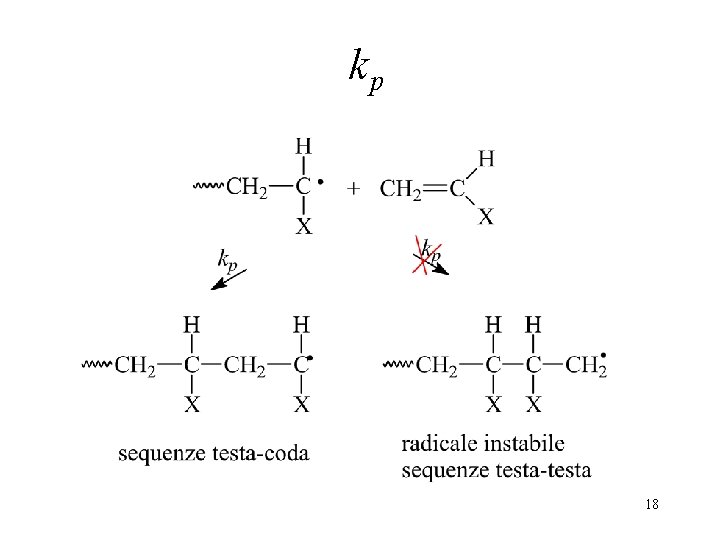
kp 18

kp Valori sperimentali di kp a 60°C kp(l mol-1 sec-1) Ep* (k. Jmol-1) AN 1. 96 e 3 16. 2 MAc 2. 09 e 3 29. 7 MMA 0. 515 e 3 26. 4 STY 0. 165 e 3 26. 0 VAc 2. 30 e 3 18. 0 2 -VPy 0. 186 e 3 33. 0 19
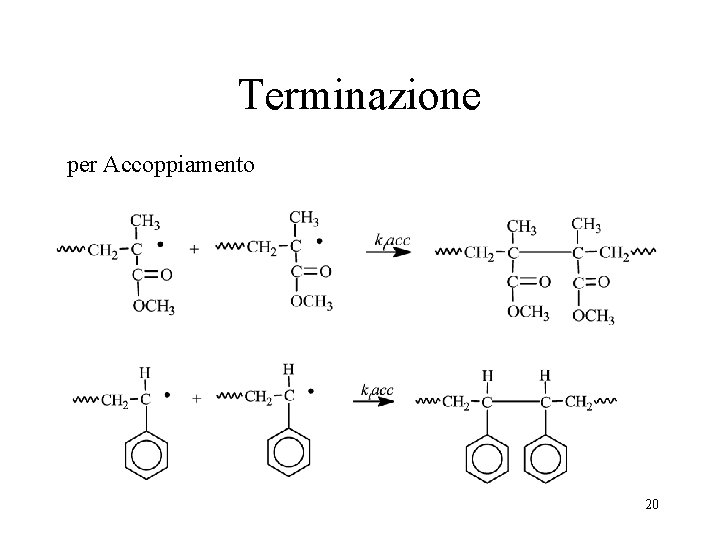
Terminazione per Accoppiamento 20
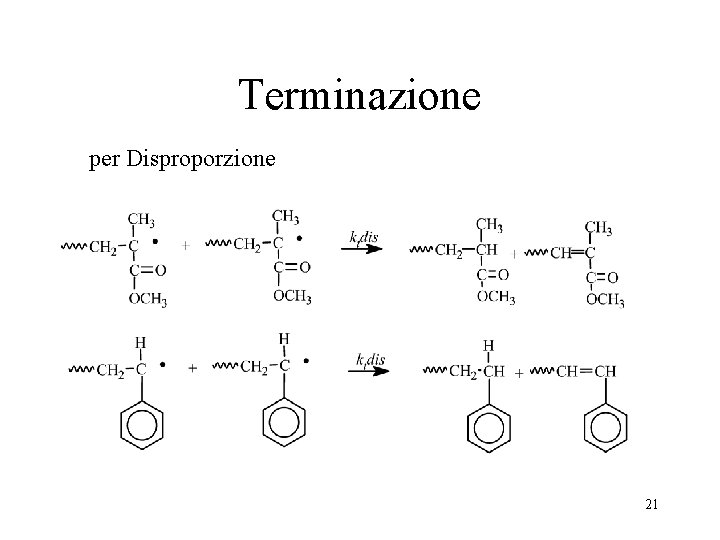
Terminazione per Disproporzione 21

Il meccanismo di terminazione dipende dal monomero e da T kt a T> disproporzione > (Et*>) Valori sperimentali di kt a 60°C (tempi di dimezzamento) kt (l mol-1 sec-1) E*t(k. Jmol-1) AN 78. 2 e 7 15. 5 MAc 0. 95 e 7 22. 2 MMA 2. 55 e 7 11. 9 STY 6. 00 e 7 8. 00 VAc 2. 90 e 7 21. 9 2 -VPy 3. 30 e 7 21. 0 22
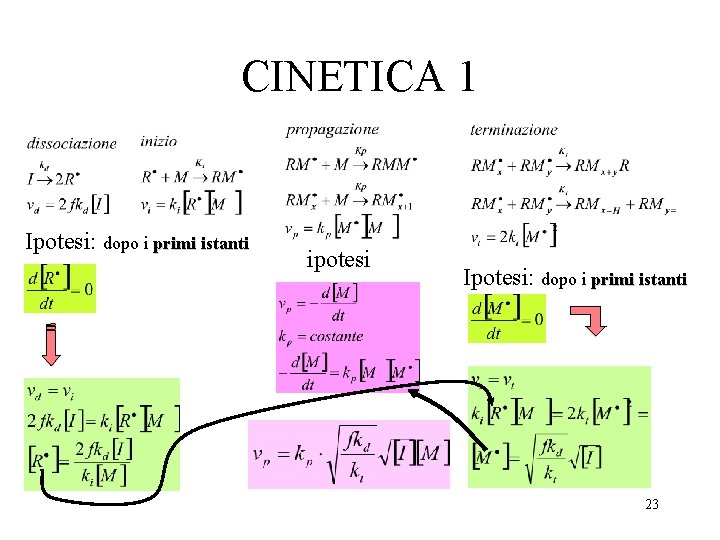
CINETICA 1 Ipotesi: dopo i primi istanti ipotesi Ipotesi: dopo i primi istanti 23
![Verifica sperimentale della legge cinetica [M]= cost pendenza 0. 5 MMA + AIBN [I]= Verifica sperimentale della legge cinetica [M]= cost pendenza 0. 5 MMA + AIBN [I]=](http://slidetodoc.com/presentation_image/00d20b668ded0f3dc54f2fa68c0781e1/image-24.jpg)
Verifica sperimentale della legge cinetica [M]= cost pendenza 0. 5 MMA + AIBN [I]= cost pendenza 1 STY+ BOP MMA + BOP 24
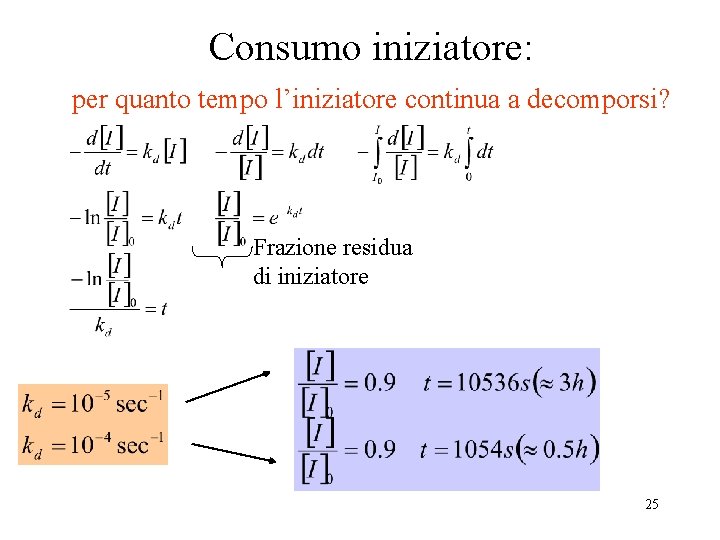
Consumo iniziatore: per quanto tempo l’iniziatore continua a decomporsi? Frazione residua di iniziatore 25

Conversione a polimero: quanto dura una polimerizzazione? Frazione residua di monomero Frazione convertita a polimero 26

Misura sperimentale velocità di reazione nella polimerizzazione in massa Caratteristiche fisiche Densità MMA 0. 944. g. /cm 3 a 20°C 0. 887 g. /cm 3 a 70°C Densità PMMA 1. 190 g. /cm 3 a 20°C 1. 170 g. /cm 3 a 70°C Variazione di volume MMA-PMMA ( a 20°C: -20. 6%; a 70°C: -24. 2%) 27

Misura sperimentale velocità di reazione 28
- Slides: 28