Classificao Peridica dos elementos Disciplina Qumica Professor Rubens

Classificação Periódica dos elementos Disciplina: Química Professor: Rubens Barreto Unidade: II
A descoberta da lei periódica Descoberta de elementos e compostos semelhanças e tendências em suas propriedades Qual seria a relação entre as massas atômicas e as outras propriedades com

Desenvolvimentos preliminares • As tríades de Döbereiner. • O parafuso telúrico de Chancourtois. • As oitavas de Newlands • Lothar Meyer – Desenvolvimento de uma tabela contendo 50 elementos. • Dimitri Mendeleev – Apresentou em 1869 uma outra versão de tabela periódica, melhorando-a nos anos seguintes e em 1871 publicou uma nova versão.
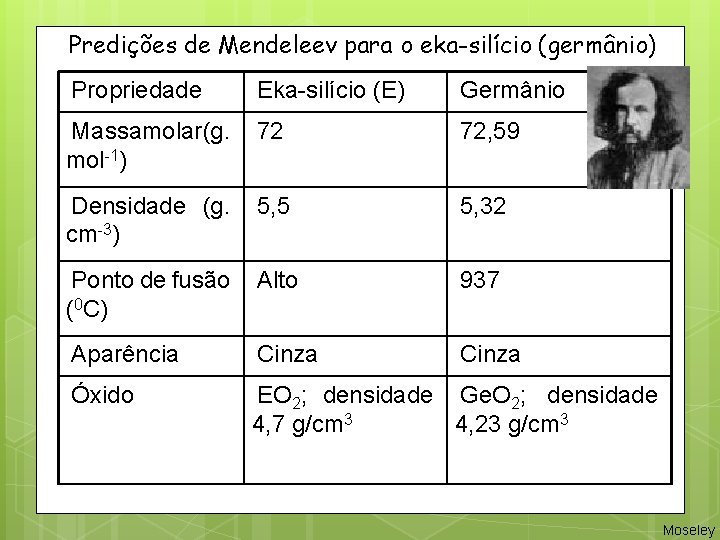
Predições de Mendeleev para o eka-silício (germânio) Propriedade Eka-silício (E) Germânio Massamolar(g. mol-1) 72 72, 59 Densidade (g. cm-3) 5, 5 5, 32 Ponto de fusão (0 C) Alto 937 Aparência Cinza Óxido EO 2; densidade Ge. O 2; densidade 4, 7 g/cm 3 4, 23 g/cm 3 Moseley
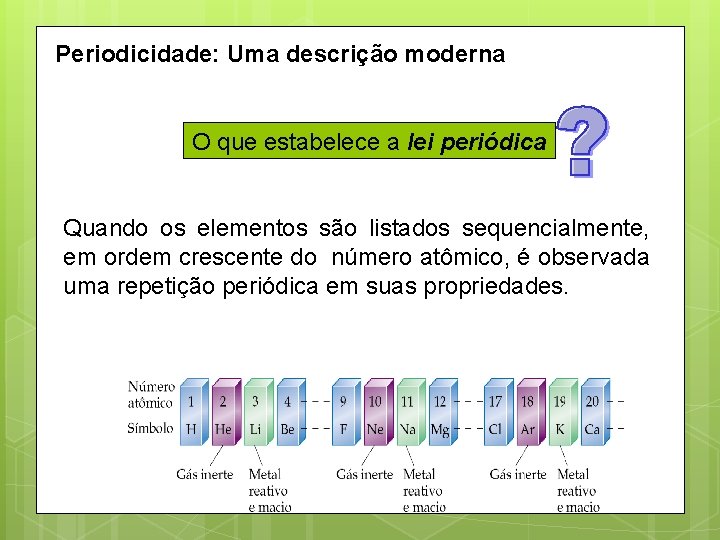
Periodicidade: Uma descrição moderna O que estabelece a lei periódica Quando os elementos são listados sequencialmente, em ordem crescente do número atômico, é observada uma repetição periódica em suas propriedades.

A tabela periódica moderna Períodos: Filas horizontais numeradas de 1 a 7 Grupos: Colunas numeradas de 1 A a 8 A ou de 1 a 18. Grupos representativos Grupos de transição
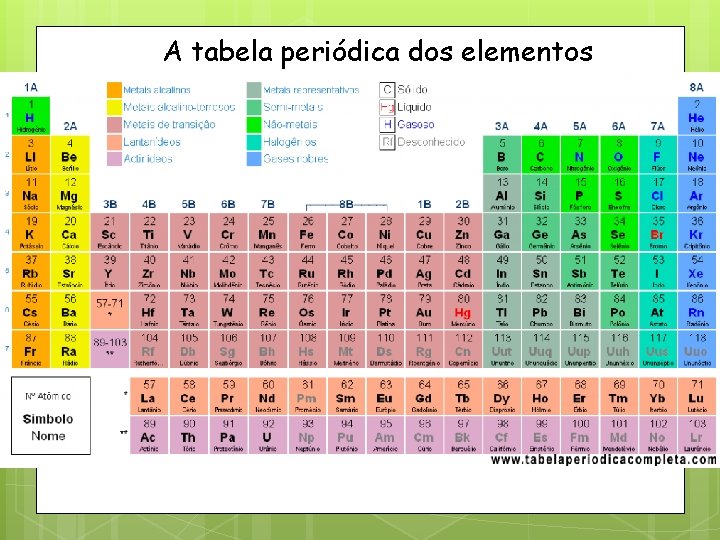
A tabela periódica dos elementos

A periodicidade nas configurações eletrônicas A periodicidade nas propriedades dos elementos é o resultado da periodicidade nas configurações de seus átomos. ¶ Os períodos tem início com um átomo de configuração ns 1. Os seguintes terão configuração ns 2 ¶Cada período é iniciado pela adição de um elétron na nova camada ¶ Número de camadas eletrônicas e período do elemento. ¶ Camada de valência e grupo do elemento Camada de valência – Camada externa do átomo
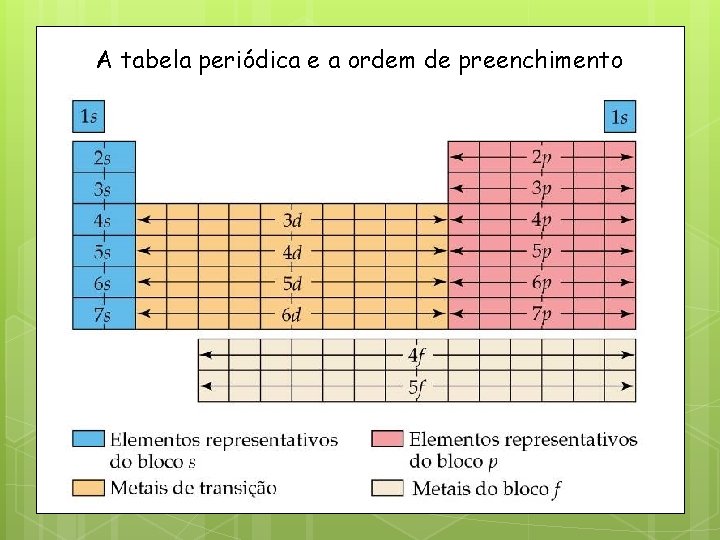
A tabela periódica e a ordem de preenchimento
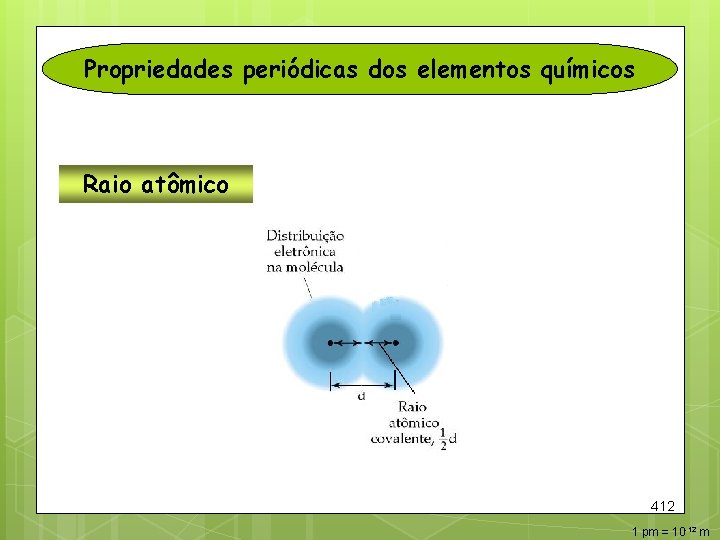
Propriedades periódicas dos elementos químicos Raio atômico 412 1 pm = 10 -12 m
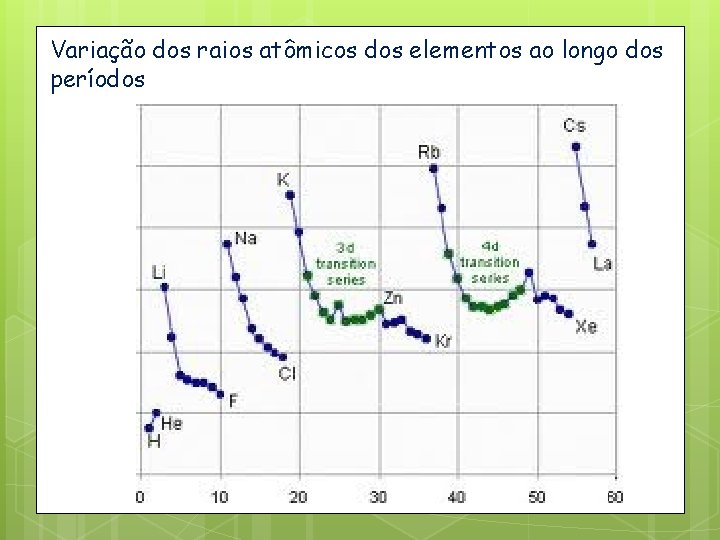
Variação dos raios atômicos dos elementos ao longo dos períodos
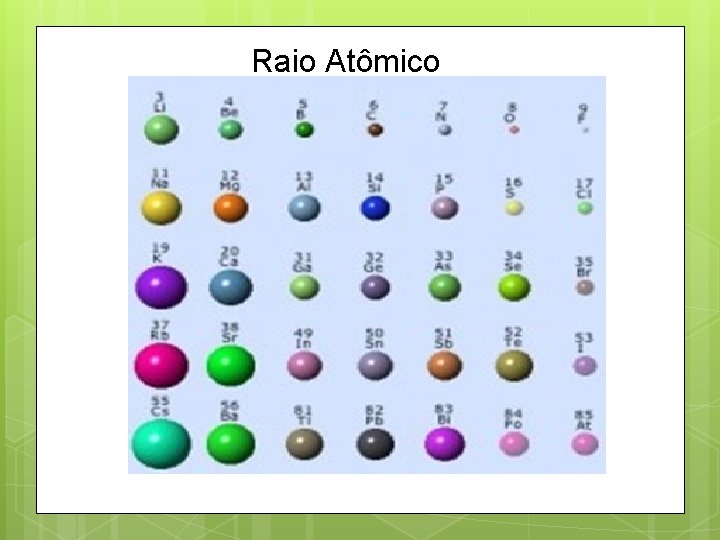
Raio Atômico


Como explicar o decréscimo do raio atômico ao longo do período? E com relação aos grupos da tabela periódica?

Energia de ionização - EI Energia mínima necessária para remover um elétron de um átomo isolado, no seu estado fundamental. Quando um átomo no estado fundamental absorve energia, seus elétrons podem ser transferidos de um nível para outro mais afastado do núcleo. Se a energia for suficientemente alta, será possível arrancar um elétron do átomo em questão, transformando-o num íon positivo. Na(g) (11 p e 11 e-) + EI (5, 1 e. V) Na+ + 1 e-
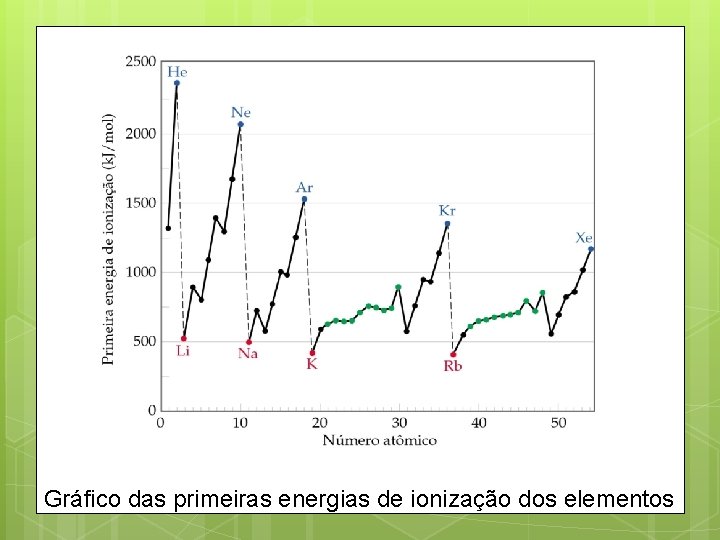
Gráfico das primeiras energias de ionização dos elementos
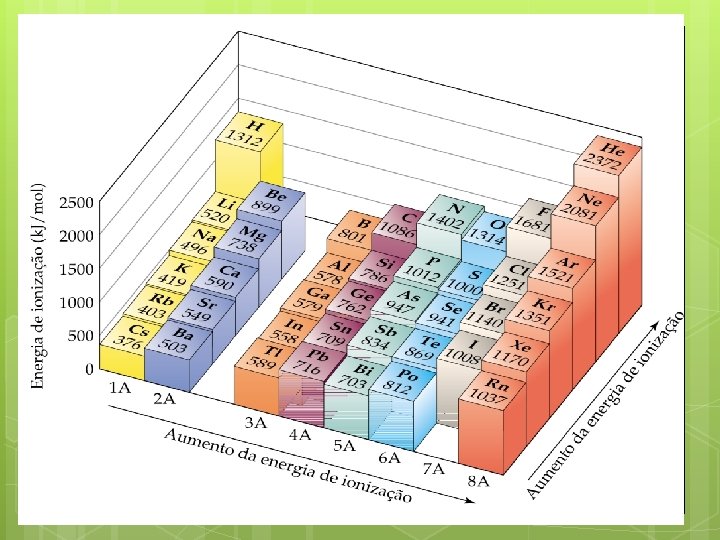

• A energia de ionização diminui à medida que descemos em um grupo. Isso significa que o elétron mais externo é mais facilmente removido ao descermos em um grupo. • Geralmente a energia de ionização aumenta ao longo do período. Por que isto acontece?

Afinidade Eletrônica (AE) Um átomo também pode receber um elétron produzindo um íon negativo: Este processo é normalmente acompanhado por uma liberação de energia, e tal quantidade mede o quão fortemente o elétron se liga ao átomo

A Afinidade Eletrônica é quantidade de energia, envolvida no processo em que um átomo isolado gasoso, no seu estado fundamental, recebe um elétron, formando um íon negativo. A quantidade de energia liberada pelo átomo ao receber elétron será tanto maior quanto mais fortemente o elétron atraído se ligar ao átomo. Cl(g) (17 p+ e 17 e-) + 1 e(recebe e-) Cl-(g) + (17 p+ e 18 e-) E Energia liberada (3, 61 e. V)
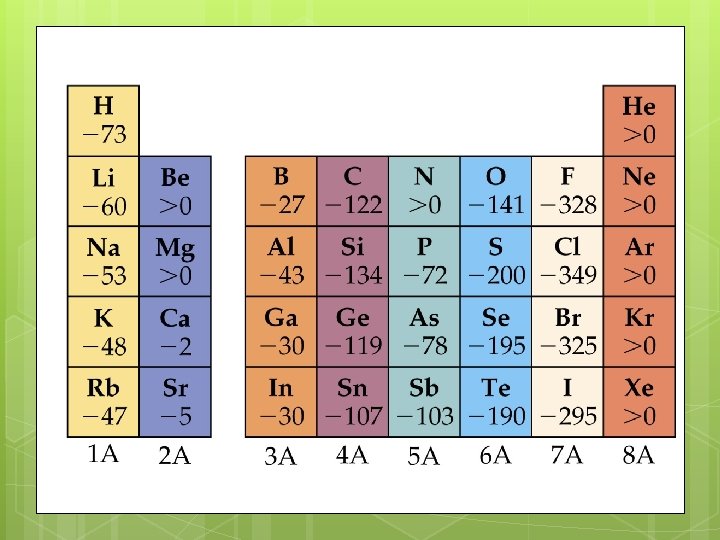
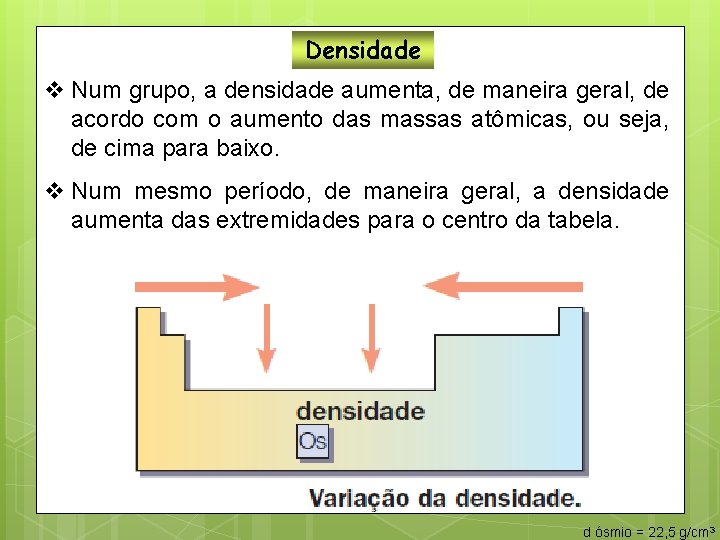
Densidade v Num grupo, a densidade aumenta, de maneira geral, de acordo com o aumento das massas atômicas, ou seja, de cima para baixo. v Num mesmo período, de maneira geral, a densidade aumenta das extremidades para o centro da tabela. d ósmio = 22, 5 g/cm 3

Ponto de fusão (PF) e Ponto de ebulição (PE) v Nas famílias IA e IIA, os elementos de maiores PF e PE estão situados na parte superior da tabela. Na outras famílias, os elementos com maiores TF e TE estão situados geralmente na parte inferior da tabela. v Num mesmo período, de maneira geral o PF e a PE crescem das extremidades para o centro da tabela.
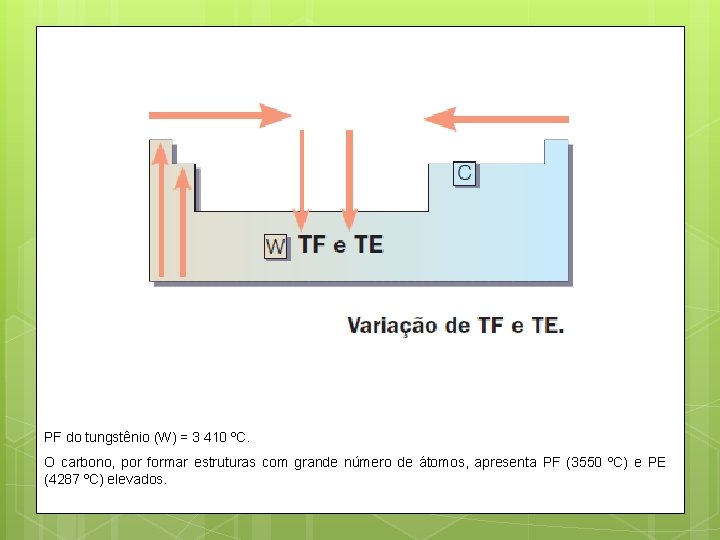
PF do tungstênio (W) = 3 410 ºC. O carbono, por formar estruturas com grande número de átomos, apresenta PF (3550 ºC) e PE (4287 ºC) elevados.

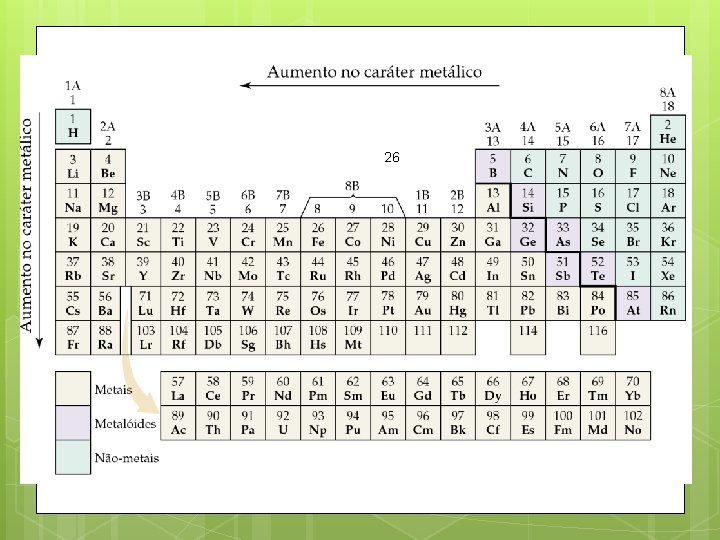
A periodicidade nas propriedades físicas Metais e não-metais: Metais Bons condutores de calor e de eletricidade, são maleáveis e dúcteis, tem alta refletividade e um brilho característico, chamado, Brilho metálico. Não-metais São maus condutores térmicos e elétricos, no estado sólido são quebradiços, e não exibem alta refletividade ou brilho metálico. *Semimetais Apresentam propriedades intermediárias às dos metais e não-metais
26
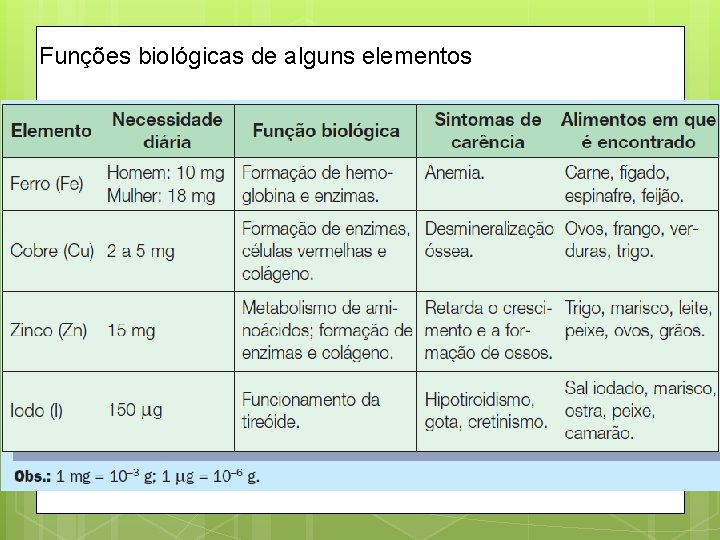
Funções biológicas de alguns elementos
- Slides: 27