CLASIFICACIN DE LA MATERIA CLASIFICACIN DE LA MATERIA








- Slides: 10

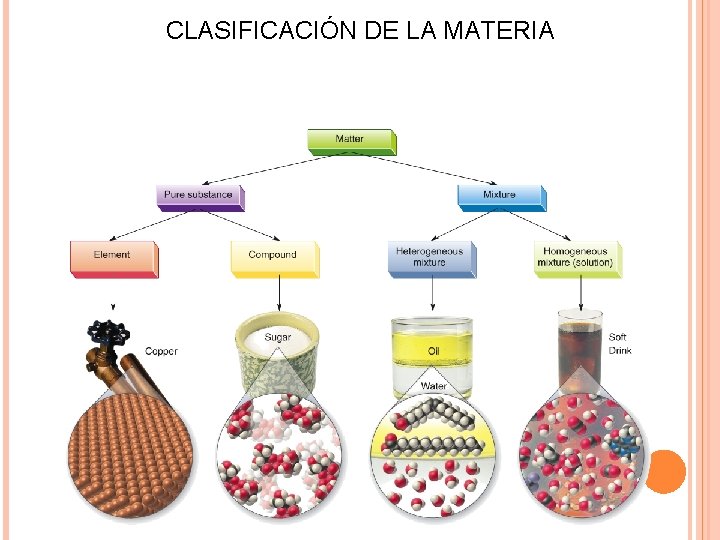
CLASIFICACIÓN DE LA MATERIA

CLASIFICACIÓN DE LA MATERIA Sustancias Puras Tienen una composición constante y propiedades físicas y químicas únicas. Elemento Sustancia pura compuesta por moléculas del mismo átomo Compuesto Sustancia pura compuesta por moléculas de distintos átomos Mezclas Combinación de dos o más sustancias puras Sus propiedades pueden variar de acuerdo a la cantidad de cada sustancia. Homogéneas: composición uniforme Heterogéneas: composición no uniforme

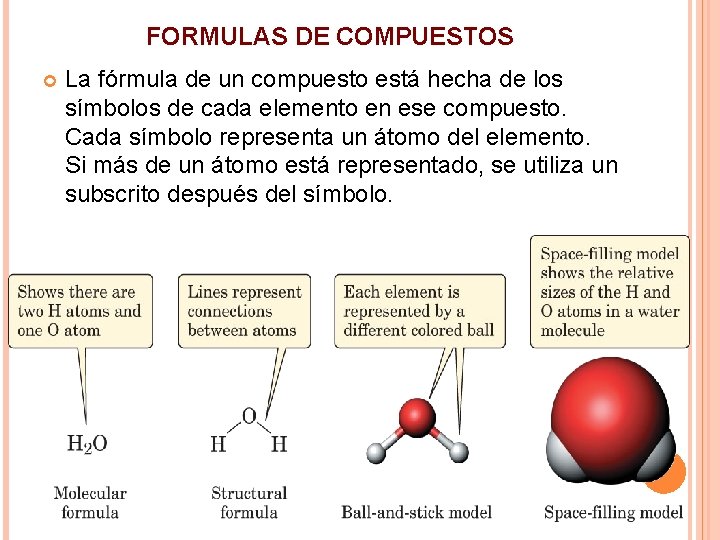
FORMULAS DE COMPUESTOS La fórmula de un compuesto está hecha de los símbolos de cada elemento en ese compuesto. Cada símbolo representa un átomo del elemento. Si más de un átomo está representado, se utiliza un subscrito después del símbolo.

EJEMPLOS DE COMPUESTOS Monóxido de Carbono, CO 1 átomo de C 1 átomo de O Agua, H 2 O 2 átomos de H 1 átomo de O Amonia, NH 3 1 átomo de N 3 átomos de H

CONCEPTOS IMPORTANTES PARA CUANTIFICAR LA MATERIA (ELEMENTOS Y COMPUESTOS) Con instrumentación moderna, se ha podido medir la masa promedio de un átomo. Ejemplo: Para simplificar el cálculo, se establece que el número de masa (no. de protones + no. de neutrones) es igual a la masa atómica en gramos. Ejemplo: 1 átomo de Mg = 4. 037 x 10 -23 g Mg Mg el número de masa = 24. 31 g Mg ¿Cuántos átomos hay de Mg en 24. 31 g Mg? 24. 31 g Mg x 1 átomo Mg = 6. 022 x 1023 átomos Mg 4. 037 x 10 -23 g Mg

CONCEPTO DE MOL Concepto de MOL aplicado a elementos El número de átomos en 1 mol de cualquier elemento se llama el número de Avogadro y es igual a 6. 022 x 1023. 1 mol de cualquier elemento es una muestra del elemento con una masa en gramos igual a la masa atómica de ese elemento. Ejemplos 1 mol Na = 22. 99 g Na = 6. 022 x 1023 átomos Na 1 mol Ca = 40. 08 g Ca = 6. 022 x 1023 átomos Ca 1 mol S = 32. 07 g S = 6. 022 x 1023 átomos S

CONCEPTO DE MOL Concepto de MOL aplicado a compuestos El número de moléculas en 1 mol de cualquier compuesto se llama el número de Avogadro y es igual a 6. 022 x 1023. 1 mol de cualquier compuesto es una muestra del compuesto con una masa en gramos igual a la masa molecular de ese compuesto. Ejemplos 1 mol H 2 O = 18. 02 g H 2 O = 6. 022 x 1023 moléculas H 2 O 1 mol CO 2 = 44. 01 g CO 2 = 6. 022 x 1023 moléculas CO 2 1 mol NH 3 = 17. 03 g NH 3 = 6. 022 x 1023 moléculas NH 3

CONCEPTO DE MOL El MOL y Cálculos Químicos El concepto de mol se puede utilizar para obtener factores de conversión útiles en cálculos químicos que envuelvan elementos y compuestos. One mole quantities of six metals; top row (left to right): Cu beads (63. 5 g), Al foil (27. 0 g), and Pb shot (207. 2 g); bottom row (left to right): S powder (32. 1 g), Cr chunks (52. 0 g), and Mg shavings (24. 4 g). One mole quantities of four compounds: H 2 O (18. 0 g); small beaker Na. Cl (58. 4 g); large beaker aspirin, C 9 H 8 O 4, (180. 2 g); green (Ni. Cl 2 · 6 H 2 O) (237. 7 g).

CALCULOS CON MOL Para elementos: ejemplo calcio Ca 1 mol Ca= 40. 08 g Ca = 6. 022 x 1023 Ca atoms Cualquiera de estas relaciones se pueden utilizar para proveer factores utilizables para resolver problemas numéricos. Ejemplo: and

CALCULOS CON MOL El concepto de mol se puede aplicar a las moléculas para calcular la masa molecular. Ejemplo: compuesto H 2 O 1 mol de uma molécula H 2 O = 2 moles de átomos de H + 1 mol de átomos de O Masa molecular g H 2 O = 2 moles H (1. 008 g H / 1 mol H) + 1 mol O(16. 00 g O / 1 mol O ) = 18. 00 g H 2 O