Clase Prctica Interactiva Diagnstico de parsitos intestinales Objetivos

Clase Práctica Interactiva Diagnóstico de parásitos intestinales Objetivos: q Orientar la toma de muestras. q Mencionar los requisitos que debe cumplir la muestra de heces para el diagnóstico de parásitos intestinales. q Observar trofozoítos y quistes intestinales, y huevos de helmintos. de protozoos q Observar las características macroscópicas de adultos de helmintos.

Regla de oro para el diagnóstico en Parasitología Valorar, identificar y demostrar el parásito para poder determinar la etiología del proceso infeccioso o enfermedad. Aspectos fundamentales a tener en cuenta para solicitar la toma de muestras y los exámenes parasitológicos. q Ciclo de vida de los parásitos. q Habitat usual y ectópico en el hospedero q Manifestaciones clínicas más específicas. q Vías de transmisión.

Ejemplos de muestras a enviar al laboratorio para demostrar la presencia de parásito --Heces --Orina --Esputo --Pus --LCR --Biopsia de tejidos -- Sangre -- Secreciones -- Excreciones -- Otros líquidos -- Aspirados

Requisitos a tener en cuenta para la adecuada obtención de la muestra de heces • Heces frescas recién emitidas y por defecación espontánea, de lo contrario almacenar la muestra a 4 o. C no más de 24 h (promedio 6 horas). • Utilizar frascos limpios de vidrios, plásticos o cartón, de boca ancha, con tapa de rosca. • Rotular correctamente el frasco con datos de identificación del paciente y los datos clínicos.

Requisitos a tener en cuenta para la adecuada obtención de la muestra de heces (cont. ) • No ingerir antiparasitarios al menos durante 72 h antes de obtener la muestra. • No utilizar laxantes, ni colorantes como el bario o el bismuto. • No mezclar con orina. • No usar supositorios.

Métodos de conservación de las muestras • Refrigeración: el frasco se debe colocar en el refrigerador a 4º C por no más de 24 horas. • Preparaciones selladas: pueden hacerse con vaselina, parafina o barniz de uñas, aplicados en los bordes del cubre-objetos. • Formol: se mezcla una cantidad aproximada de 3 g de materias fecales por cada 10 ml de formol diluido al 5 o 10% (se conservan bien los huevos de helmintos y los quistes de protozoos).

Objetivo de los métodos de diagnóstico directo Identificar parásitos reproducción. o sus productos de Ejemplo de método directo Técnica de Baermam: permite extraer larvas de helmintos.

Objetivo de los métodos de diagnóstico indirectos A través de pruebas inmunoserológicas o de otro tipo, obtener resultados que en estrecha unión con la clínica, ofrezcan un diagnostico probable. Ejemplos de métodos Indirectos Inmunológicos: Hemaglutinación indirecta para tripanosomosis americana. Inmunohistoquímico: Microsporidiosis. TAC: permite detectar las lesiones en la neurocisticercosis.

Técnicas para el diagnóstico de las parasitosis intestinales 1 - Examen coprológico directo cualitativo - Macroscópico: hay que observar la consistencia, el color, la cantidad, la presencia de moco, sangre o fragmentos de parásitos. Se usa también el Tamizaje. -Microscópico: Existen varios métodos para la realización de este examen, entre ellos:

Método directo: Simple Se puede utilizar solución salina, eosina o lugol para su realización, permite observar además de los parásitos, eritrocitos, leucocitos, cristales de Charcot-Leyden, restos alimenticios de origen vegetal o animal, levaduras, células de descamación y levaduras.

Método de concentración (Facilita la observación de parásitos) Por Sedimentación • Simple Ej. Copa Cónica • Centrifugación Ej. Técnica de Ritchie Por flotación: • Técnica de Faust con sulfato de zinc, • Técnica de Willis con solución saturada de cloruro de sodio • Técnica de flotación de Sheather (sacarosa)


Métodos de Recuentos de Huevos (examen coprológico directo cuantitativo) Técnica de Kato-Katz: método más recomendable en la actualidad, recomendado por la OMS.
2 - Cultivo (Se utiliza poco en el diagnóstico de parasitosis intestinales) Ej. Papel de filtro- Harada Mori (larvas) Medio de cultivo de Diamond (trofozoítos).

3 - Coloraciones especiales q Hematoxilina férrica (Balantidium coli). q Coloración tricrómica (E. histolytica). q Coloración de Ziehl-Neelsen modificada (Cryptosporidium sp. ) Son útiles para realizar preparaciones permanentes y almacenar o remitir las muestras a laboratorios especializados; con ellas se obtienen detalles morfológicos más exactos, permitiendo diagnosticar mejor las especies.

4 - Procedimientos especiales de diagnóstico q Método de la cinta engomada o de Graham. q Estudio del contenido duodenal, de materiales purulentos y del flujo vaginal.

Situación problémica Considere que usted cuenta con muestras de heces recién emitidas o conservadas en formol, que contienen diferentes estadios evolutivos de protozoos o helmintos de importancia médica. Después de realizar el examen directo correspondiente le concierne realizar el diagnóstico de la enfermedad teniendo en cuenta los resultados del laboratorio de parasitología.
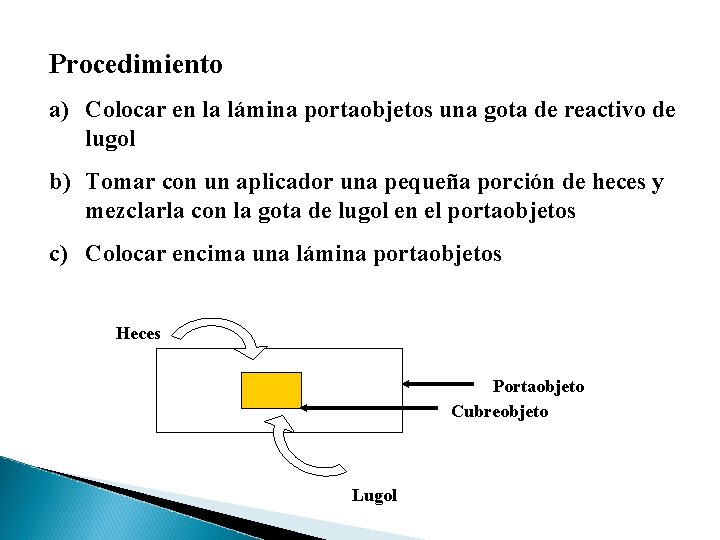
Procedimiento a) Colocar en la lámina portaobjetos una gota de reactivo de lugol b) Tomar con un aplicador una pequeña porción de heces y mezclarla con la gota de lugol en el portaobjetos c) Colocar encima una lámina portaobjetos Heces Portaobjeto Cubreobjeto Lugol
d) Llevar la lámina al microscopio óptico y enfocar con el objetivo de 10 x. Al lograr una imagen nítida, pasar al objetivo de 40 x

-Observe detenidamente las características de los estadios evolutivos según corresponda

Presentación de los resultados a) Realice un informe que contendrá dibujos de los estadios evolutivos observados. b) Identifique el agente biológico que se muestra en las láminas, para ello tenga en cuenta los detalles morfológicos característicos según el estadio evolutivo, la forma infectante y su localización. c) Señale el género del parásito (y si es posible la especie). Recuerde respetar la forma correcta de redactar la nomenclatura binomial.
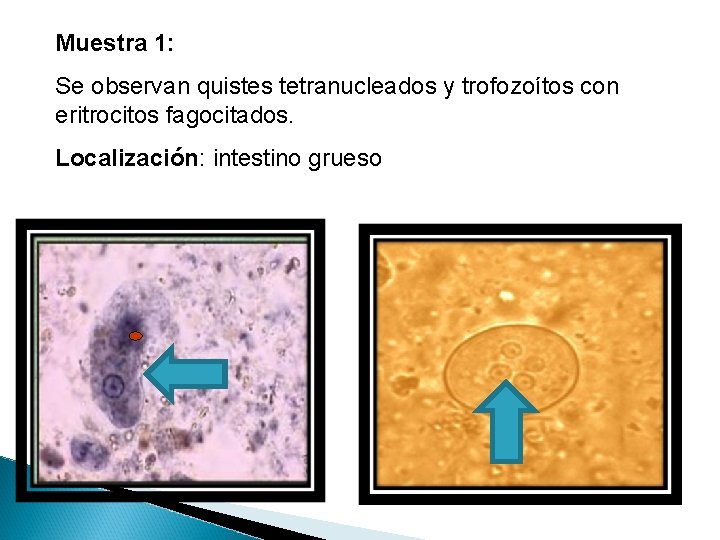
Muestra 1: Se observan quistes tetranucleados y trofozoítos con eritrocitos fagocitados. Localización: intestino grueso
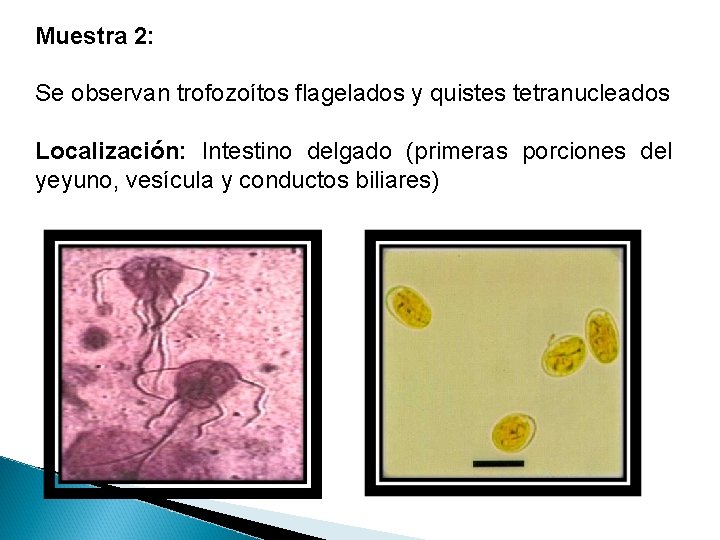
Muestra 2: Se observan trofozoítos flagelados y quistes tetranucleados Localización: Intestino delgado (primeras porciones del yeyuno, vesícula y conductos biliares)
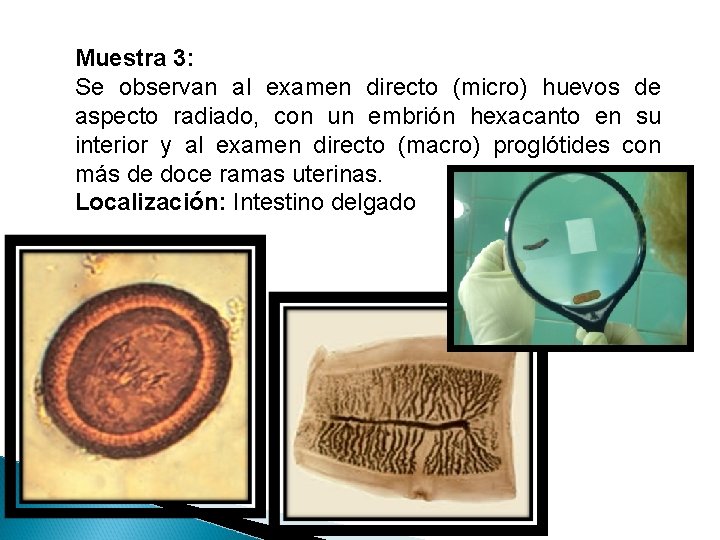
Muestra 3: Se observan al examen directo (micro) huevos de aspecto radiado, con un embrión hexacanto en su interior y al examen directo (macro) proglótides con más de doce ramas uterinas. Localización: Intestino delgado
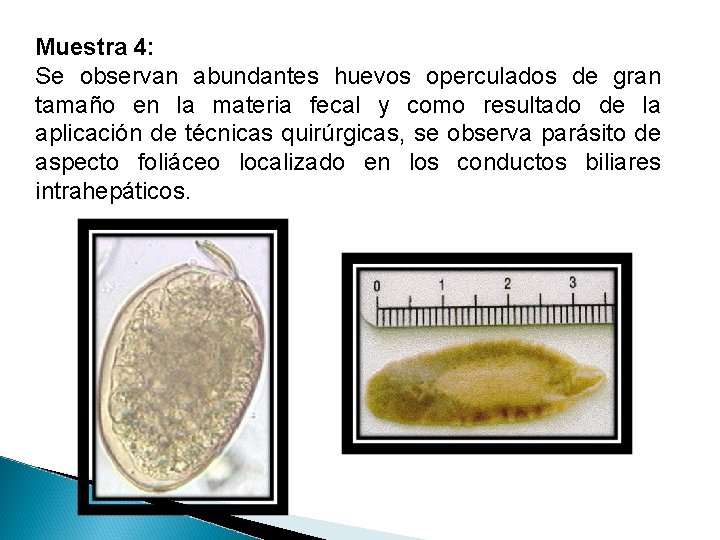
Muestra 4: Se observan abundantes huevos operculados de gran tamaño en la materia fecal y como resultado de la aplicación de técnicas quirúrgicas, se observa parásito de aspecto foliáceo localizado en los conductos biliares intrahepáticos.

Muestra 5 Se observan abundantes huevos embrionados con una cubierta externa mamelonada y se constata lo referido por el paciente, la presencia en la materia fecal de un nematodo intestinal de gran tamaño de color blanquesino.
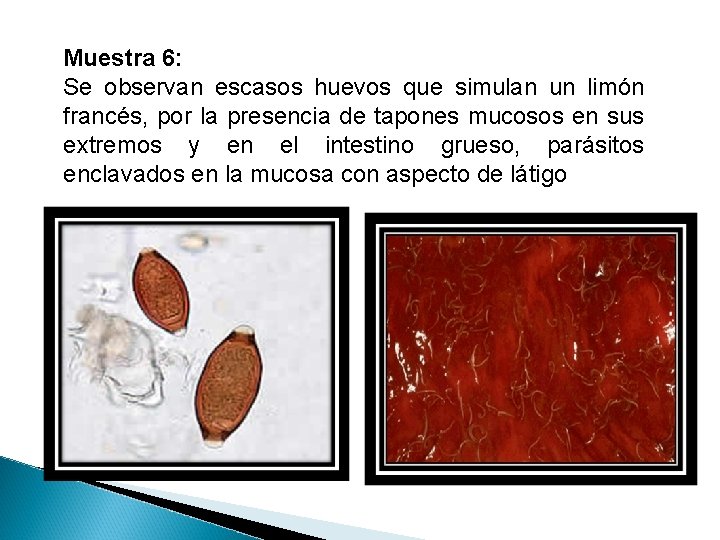
Muestra 6: Se observan escasos huevos que simulan un limón francés, por la presencia de tapones mucosos en sus extremos y en el intestino grueso, parásitos enclavados en la mucosa con aspecto de látigo
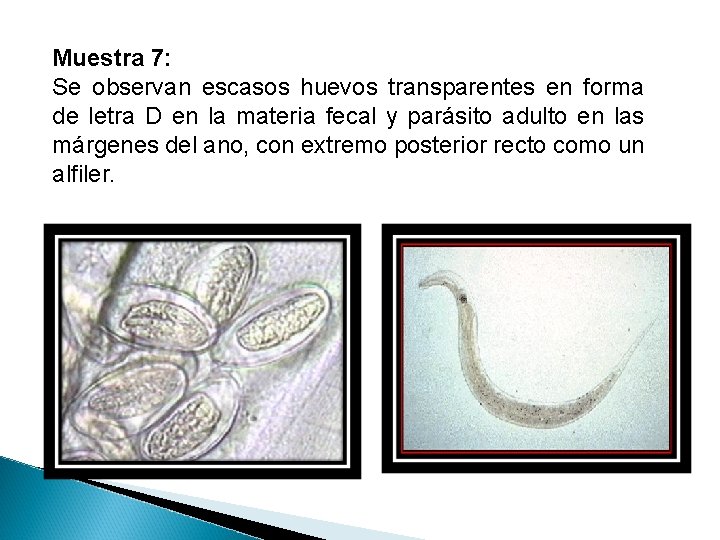
Muestra 7: Se observan escasos huevos transparentes en forma de letra D en la materia fecal y parásito adulto en las márgenes del ano, con extremo posterior recto como un alfiler.
- Slides: 28