Citoszkeleton Sejtmozgs Dr habil Khidail Lszl egyetemi docens
Citoszkeleton – Sejtmozgás Dr. habil. Kőhidail László egyetemi docens Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet 2008.

Citoszkeleton Mikrofilamentumok (aktin) l Mikrotubulusok (tubulin) l Intermedier filamentumok l l. Mikrotubulus asszociált proteinek (MAP-ok) pl. : Motor proteinek
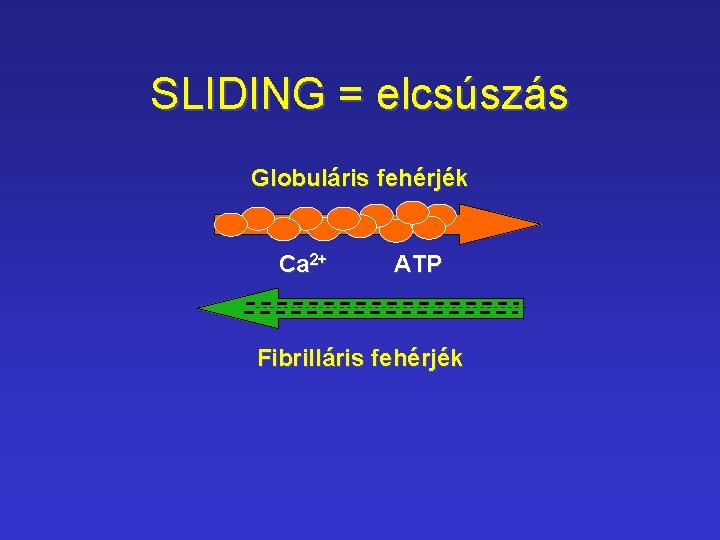
SLIDING = elcsúszás Globuláris fehérjék Ca 2+ ATP Fibrilláris fehérjék

Mikrofilamentumok
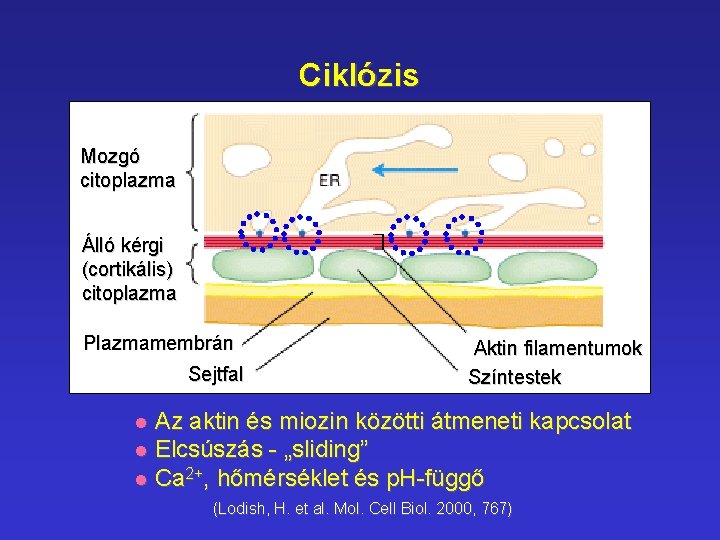
Ciklózis Mozgó citoplazma Álló kérgi (cortikális) citoplazma Plazmamembrán Sejtfal Aktin filamentumok Színtestek Az aktin és miozin közötti átmeneti kapcsolat l Elcsúszás - „sliding” l Ca 2+, hőmérséklet és p. H-függő l (Lodish, H. et al. Mol. Cell Biol. 2000, 767)
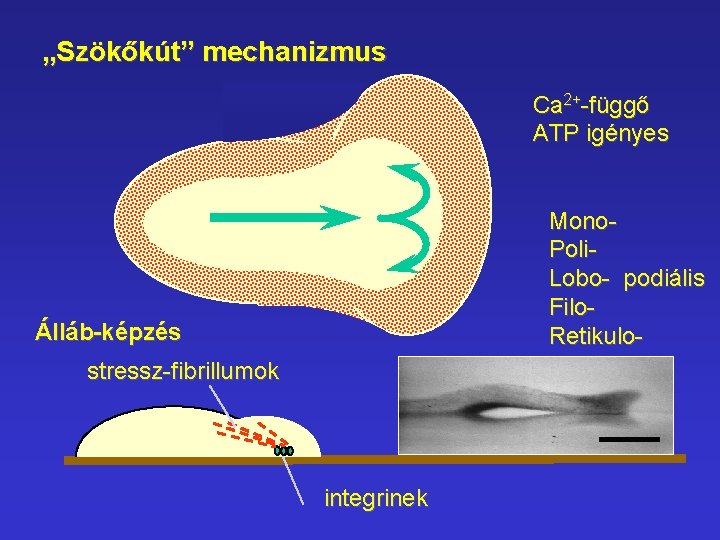
„Szökőkút” mechanizmus Ca 2+-függő ATP igényes Mono. Poli. Lobo- podiális Filo. Retikulo- Álláb-képzés stressz-fibrillumok integrinek
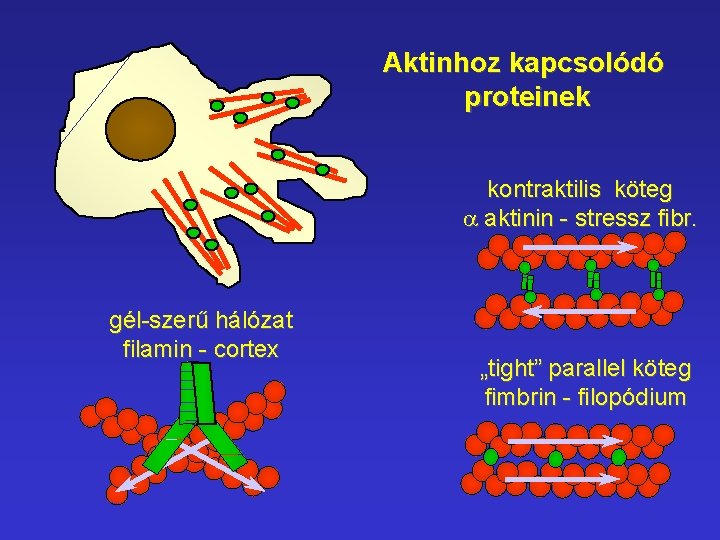
Aktinhoz kapcsolódó proteinek kontraktilis köteg a aktinin - stressz fibr. gél-szerű hálózat filamin - cortex „tight” parallel köteg fimbrin - filopódium
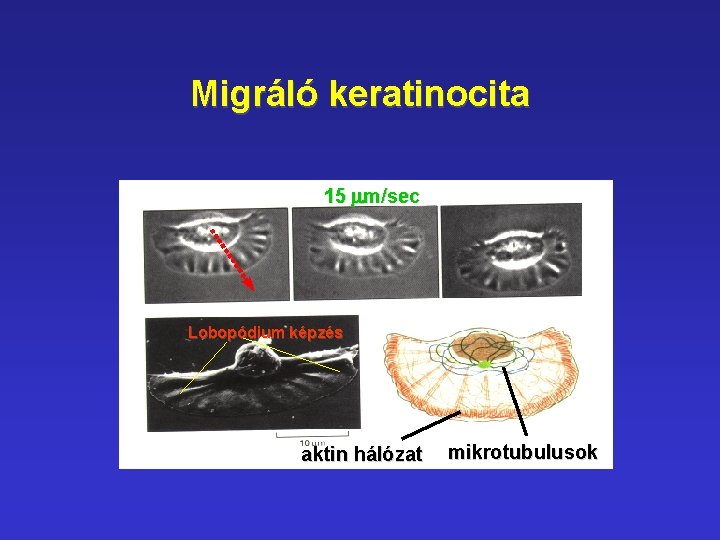
Migráló keratinocita 15 mm/sec Lobopódium képzés aktin hálózat mikrotubulusok
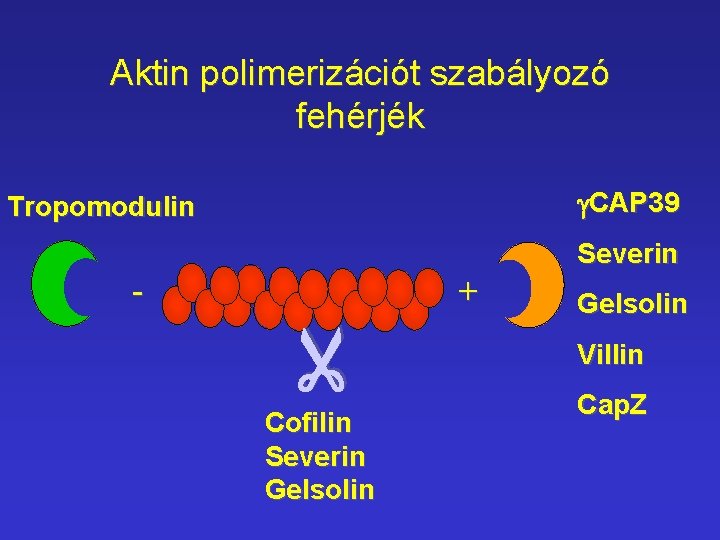
Aktin polimerizációt szabályozó fehérjék g. CAP 39 Tropomodulin + - Cofilin Severin Gelsolin Villin Cap. Z
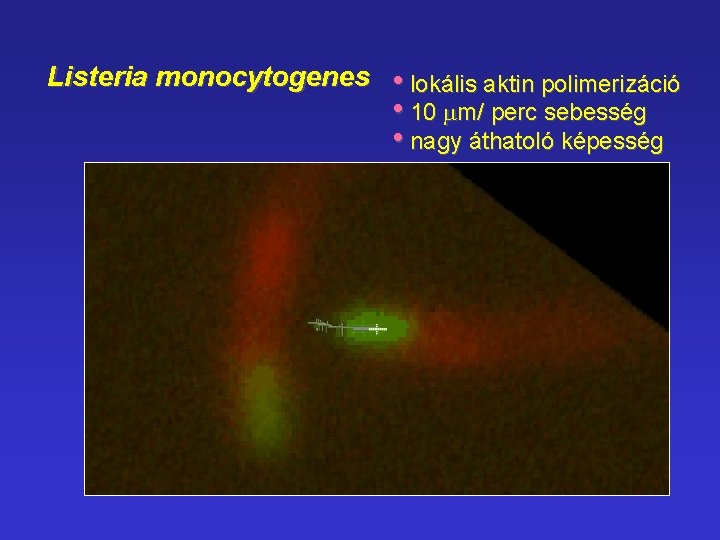
Listeria monocytogenes aktin • lokális aktin polimerizáció • 10 mm/ perc sebesség • nagy áthatoló képesség
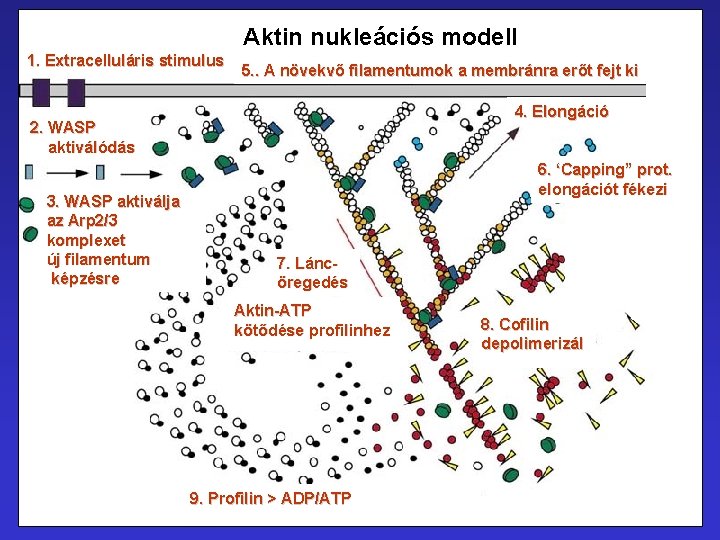
Aktin nukleációs modell 1. Extracelluláris stimulus 5. . A növekvő filamentumok a membránra erőt fejt ki 4. Elongáció 2. WASP aktiválódás 3. WASP aktiválja az Arp 2/3 komplexet új filamentum képzésre 6. ‘Capping” prot. elongációt fékezi 7. Láncöregedés Aktin-ATP kötődése profilinhez 9. Profilin > ADP/ATP 8. Cofilin depolimerizál
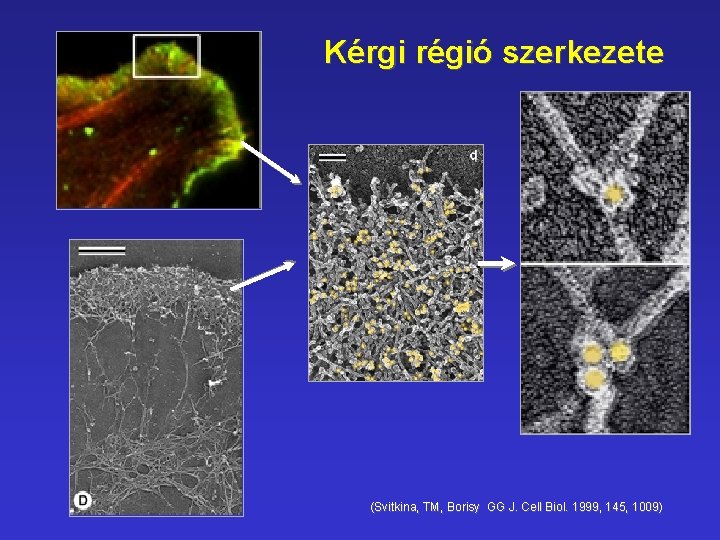
Kérgi régió szerkezete (Svitkina, TM, Borisy GG J. Cell Biol. 1999, 145, 1009)
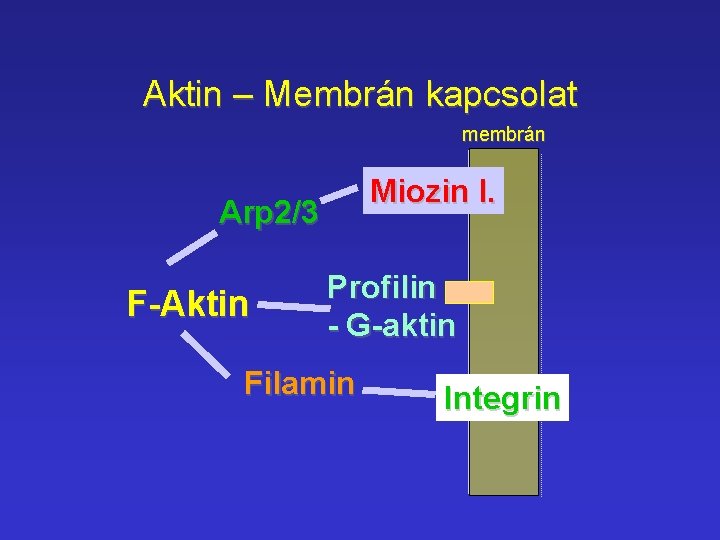
Aktin – Membrán kapcsolat membrán Miozin I. Arp 2/3 F-Aktin Profilin - G-aktin Filamin Integrin
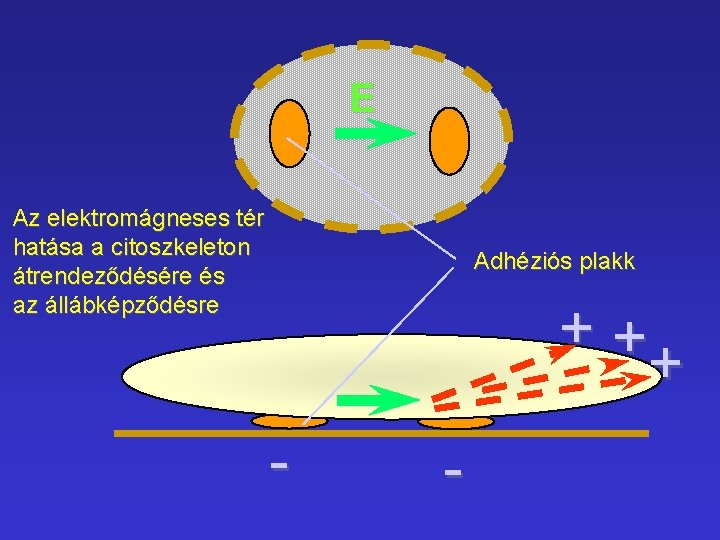
E Az elektromágneses tér hatása a citoszkeleton átrendeződésére és az állábképződésre Adhéziós plakk ++ + - -
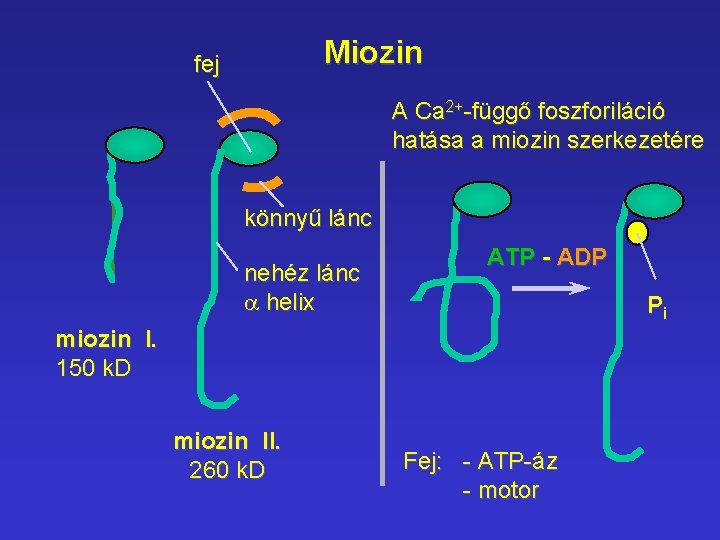
Miozin fej A Ca 2+-függő foszforiláció hatása a miozin szerkezetére könnyű lánc nehéz lánc a helix ATP - ADP Pi miozin I. 150 k. D miozin II. 260 k. D Fej: - ATP-áz - motor
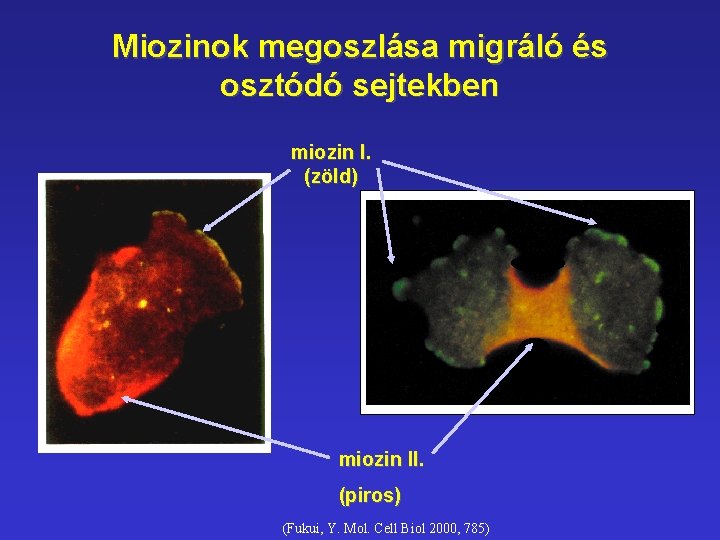
Miozinok megoszlása migráló és osztódó sejtekben miozin I. (zöld) miozin II. (piros) (Fukui, Y. Mol. Cell Biol 2000, 785)
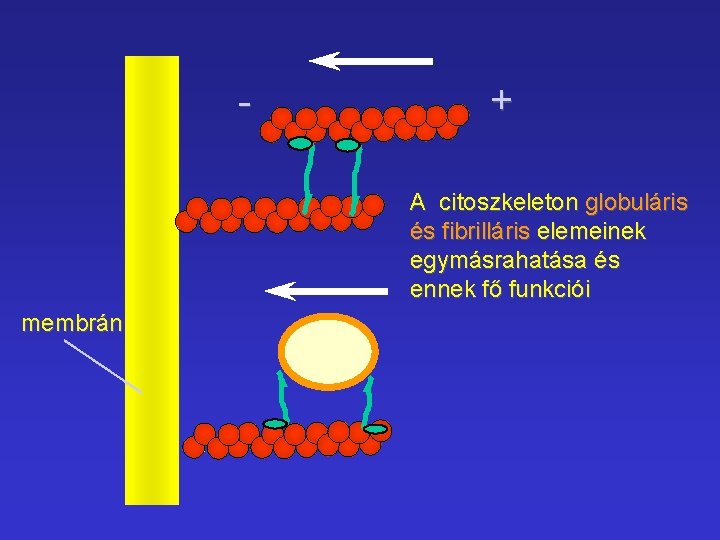
- + A citoszkeleton globuláris és fibrilláris elemeinek egymásrahatása és ennek fő funkciói membrán
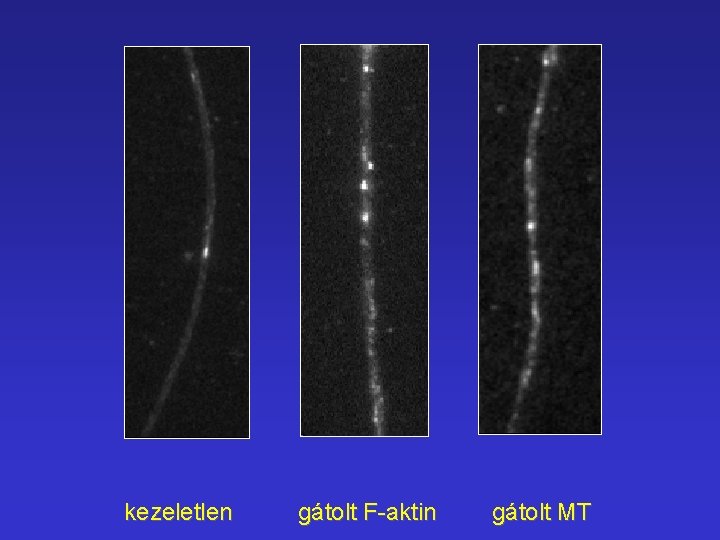
kezeletlen gátolt F-aktin gátolt MT

Mikrotubulusok
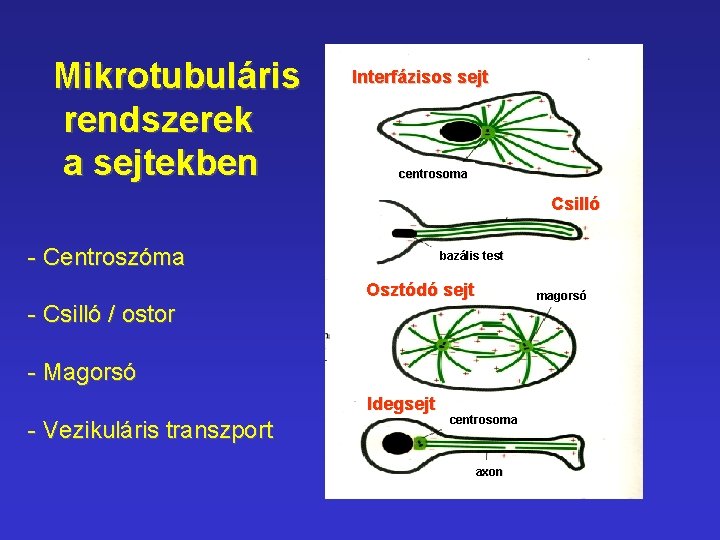
Mikrotubuláris rendszerek a sejtekben Interfázisos sejt centrosoma Csilló - Centroszóma bazális test Osztódó sejt magorsó - Csilló / ostor - Magorsó Idegsejt - Vezikuláris transzport centrosoma axon
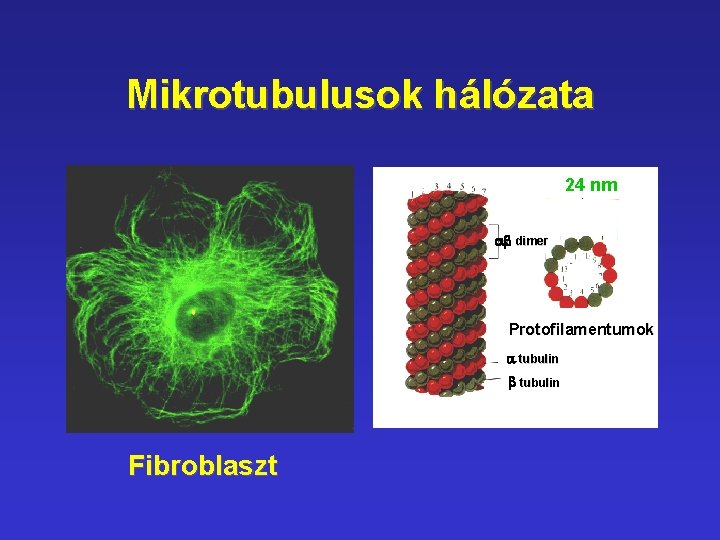
Mikrotubulusok hálózata 24 nm ab dimer Protofilamentumok a tubulin b tubulin Fibroblaszt
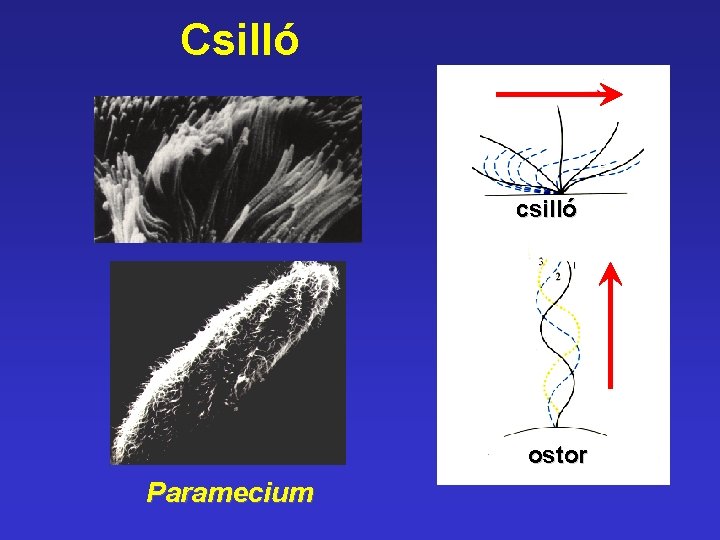
Csilló csilló ostor Paramecium
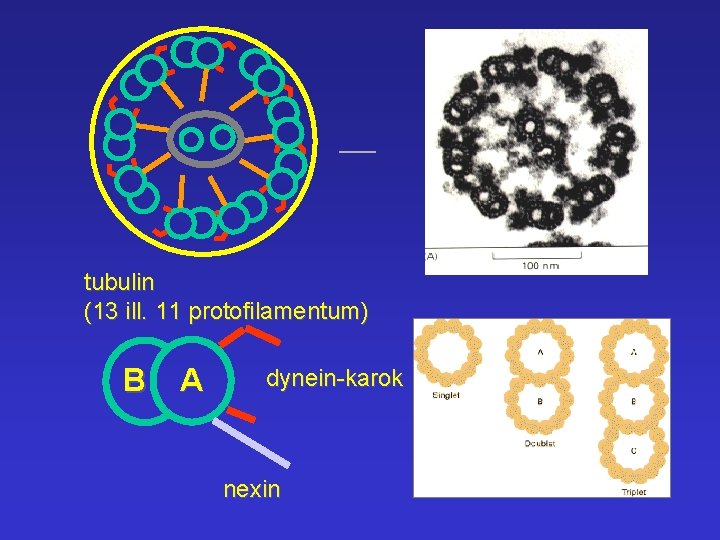
tubulin (13 ill. 11 protofilamentum) B A dynein-karok nexin
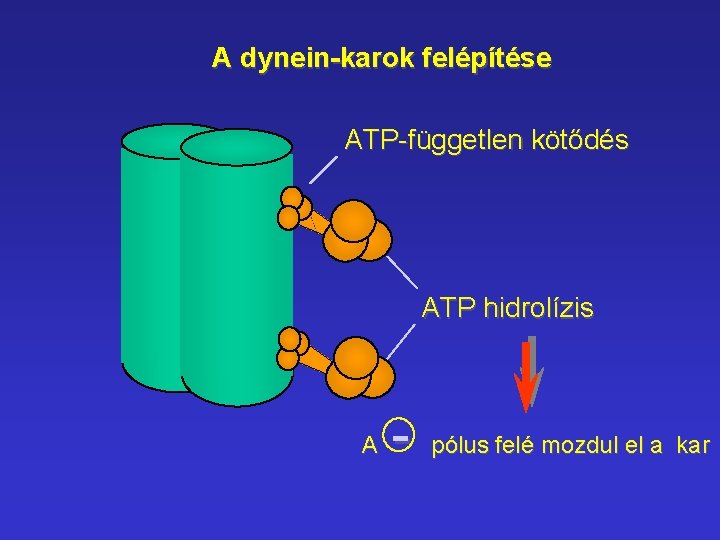
A dynein-karok felépítése ATP-független kötődés ATP hidrolízis A - pólus felé mozdul el a kar
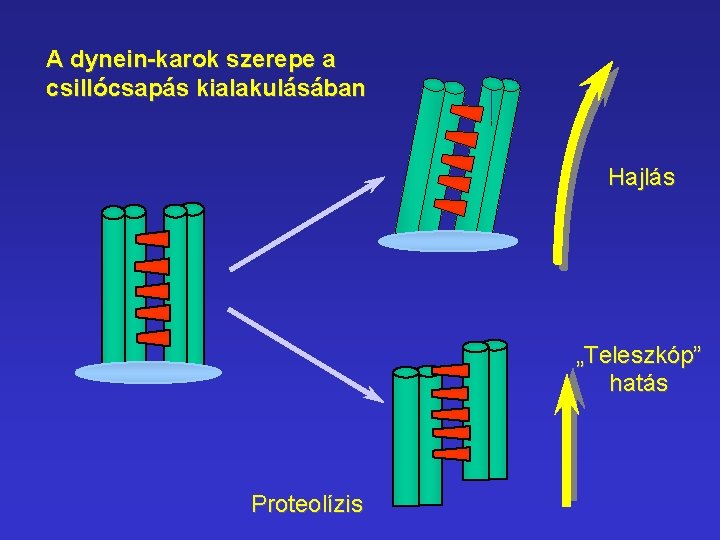
A dynein-karok szerepe a csillócsapás kialakulásában Hajlás „Teleszkóp” hatás Proteolízis

A csillót felépítő molekulák több mint 250 féle molekula 70% a és b tubulin l dynein karok külső - 9 polipeptid - ATP-áz belső - változó összetétel l küllők - 17 polipeptid l

Intermedier filamentumok
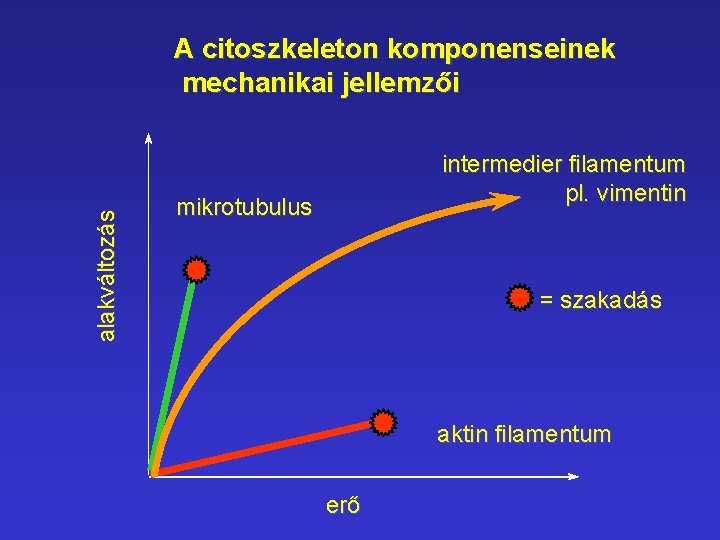
alakváltozás A citoszkeleton komponenseinek mechanikai jellemzői intermedier filamentum pl. vimentin mikrotubulus = szakadás aktin filamentum erő
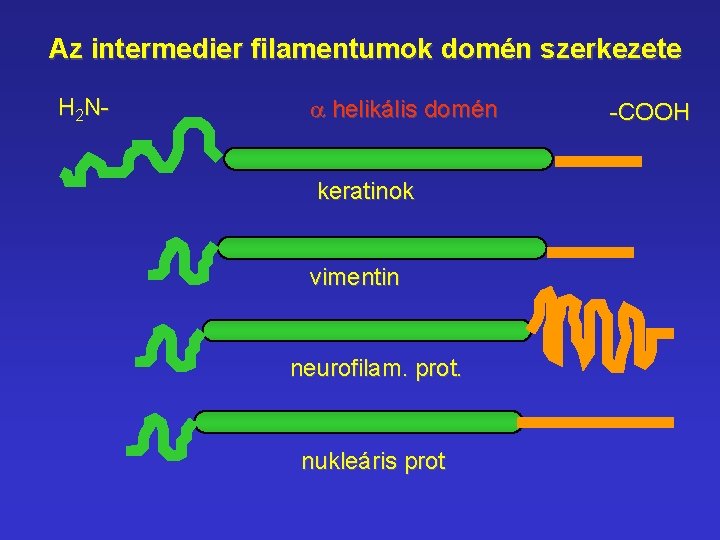
Az intermedier filamentumok domén szerkezete H 2 N- a helikális domén keratinok vimentin neurofilam. prot. nukleáris prot -COOH
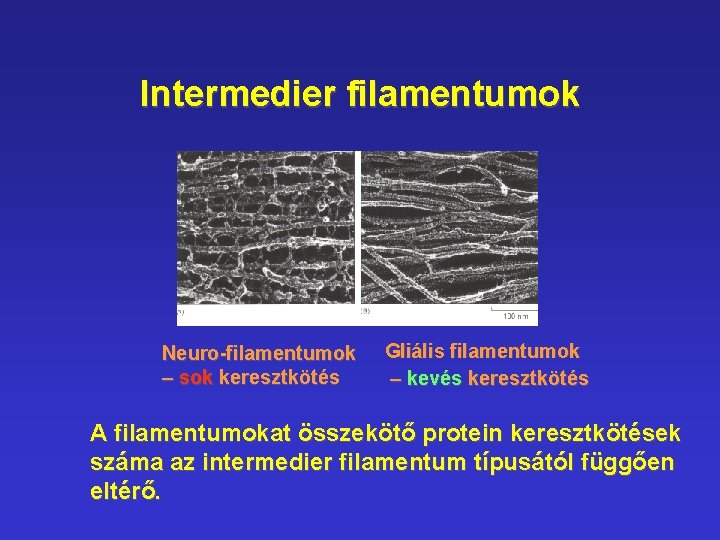
Intermedier filamentumok Neuro-filamentumok – sok keresztkötés Gliális filamentumok – kevés keresztkötés A filamentumokat összekötő protein keresztkötések száma az intermedier filamentum típusától függően eltérő.

Mikrotubulus asszociált proteinek (MAP-ok)

MAP-ok csoportosítása • Strukturális MAP-ok - MT-összeépülése Sejt alak, polaritás - kapcsolódás MF-hoz és IF-hoz • Motor proteinek Membrán transzport - elcsúszás MT-n • Enzimek, szignál molekulák - glikolítikus enzimek - kinázok Molekulák összeépülése egyes helyeken

Motor proteinek
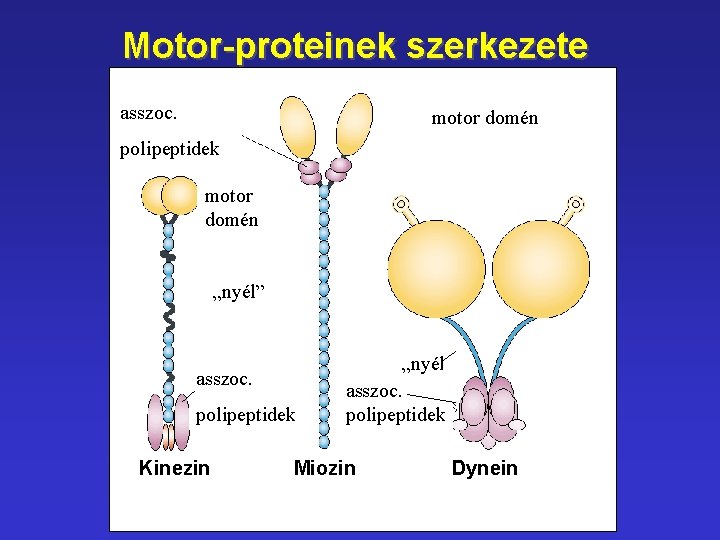
Motor-proteinek szerkezete asszoc. motor domén polipeptidek motor domén „nyél” asszoc. polipeptidek Kinezin „nyél” asszoc. polipeptidek Miozin Dynein
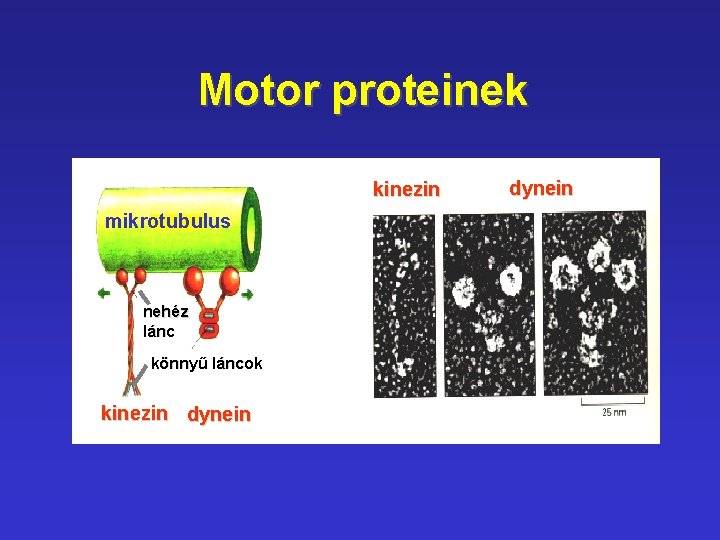
Motor proteinek kinezin mikrotubulus nehéz lánc könnyű láncok kinezin dynein
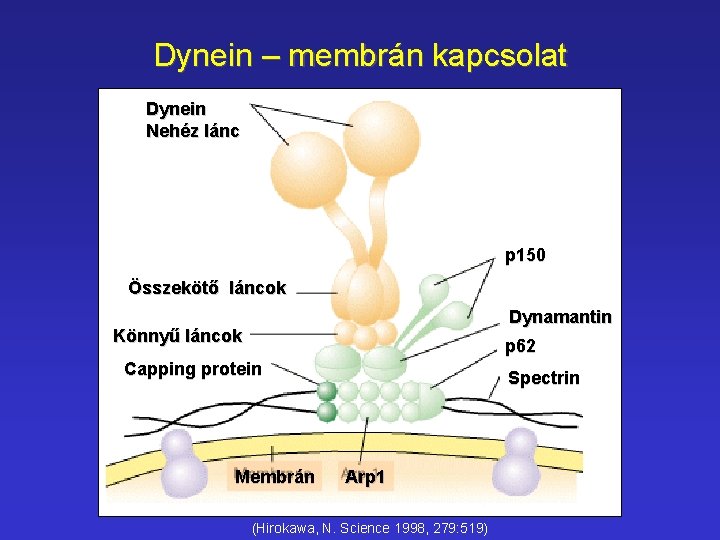
Dynein – membrán kapcsolat Dynein Nehéz lánc p 150 Összekötő láncok Dynamantin Könnyű láncok p 62 Capping protein Membrán Spectrin Arp 1 (Hirokawa, N. Science 1998, 279: 519)
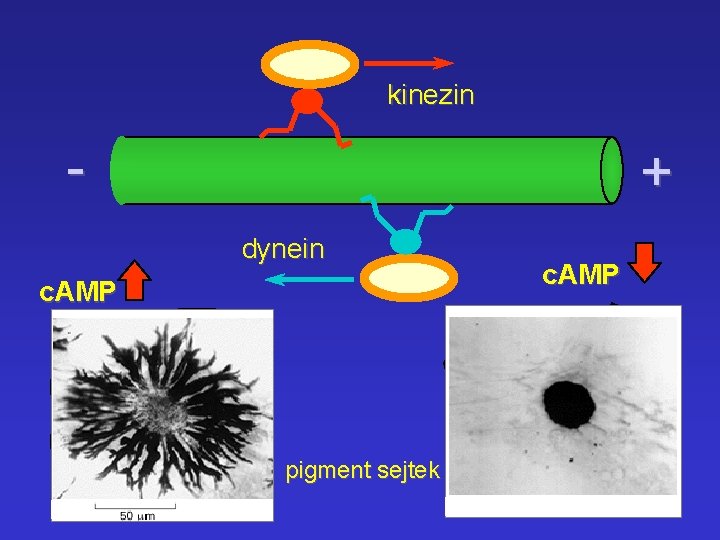
kinezin - + dynein c. AMP pigment sejtek c. AMP
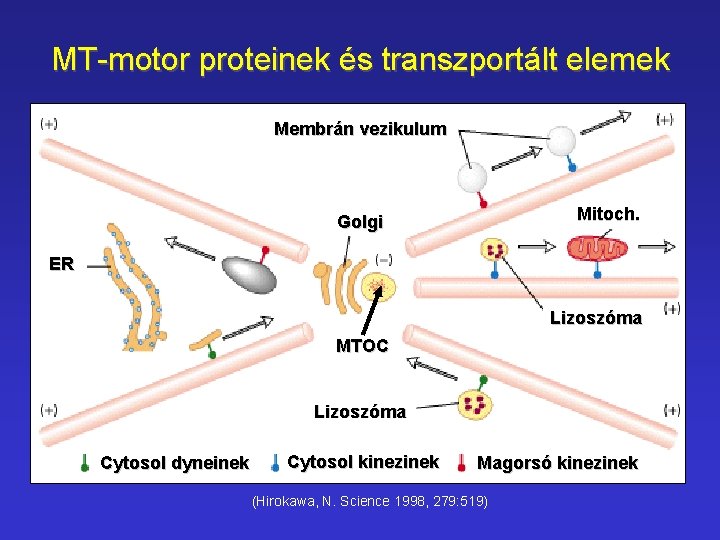
MT-motor proteinek és transzportált elemek Membrán vezikulum Mitoch. Golgi ER Lizoszóma MTOC Lizoszóma Cytosol dyneinek Cytosol kinezinek Magorsó kinezinek (Hirokawa, N. Science 1998, 279: 519)

Van más mechanizmus is …
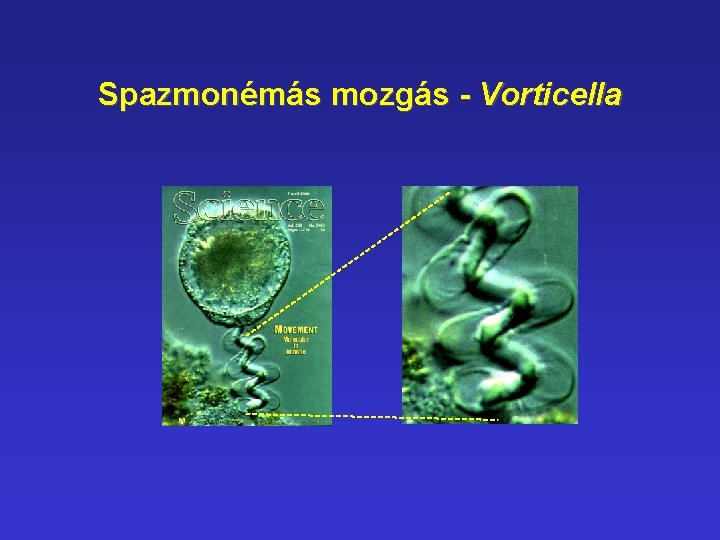
Spazmonémás mozgás - Vorticella
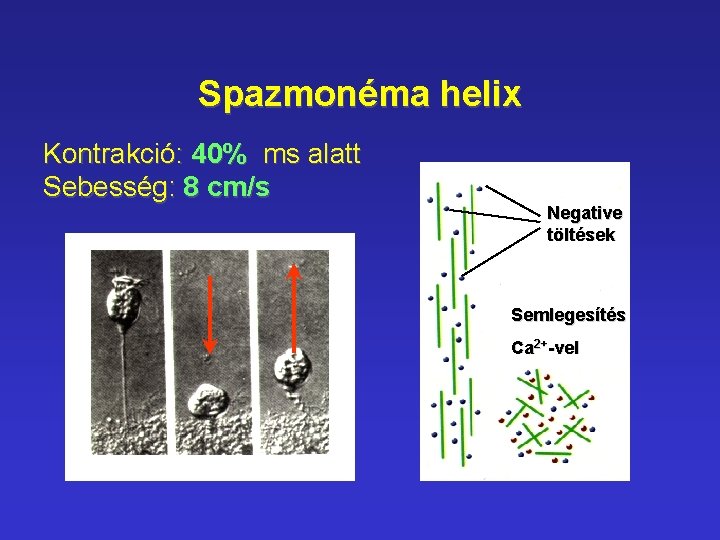
Spazmonéma helix Kontrakció: 40% ms alatt Sebesség: 8 cm/s Negative töltések Semlegesítés Ca 2+-vel
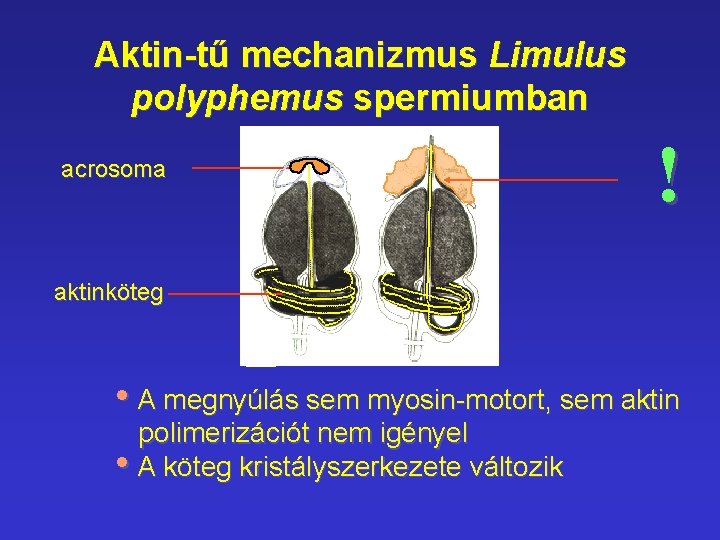
Aktin-tű mechanizmus Limulus polyphemus spermiumban acrosoma ! aktinköteg • A megnyúlás sem myosin-motort, sem aktin polimerizációt nem igényel • A köteg kristályszerkezete változik

Harántcsíkolt izom
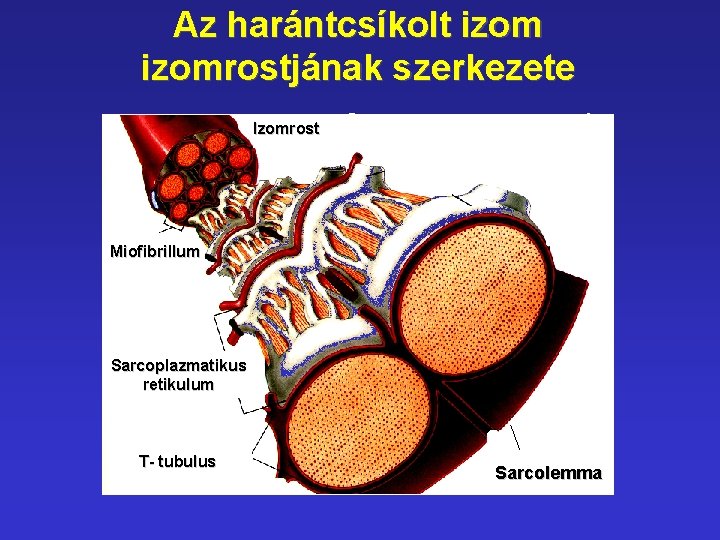
Az harántcsíkolt izomrostjának szerkezete Izomrost Miofibrillum Sarcoplazmatikus retikulum T- tubulus Sarcolemma

A sarcomer FM és TEM szerkezete I csík A csík I csík H csík aktin miozin aktin + aktin

Sarcomer felépítése • Két Z-vonal által határolt működési egység • Z vonal – a-aktinin + dezmin • Vékony filamentum – kb. 600 db a-helikális aktin molekula + tropomiozin + troponinek • Vastag filamentum – kb. 150 -400 db miozin II. molekula
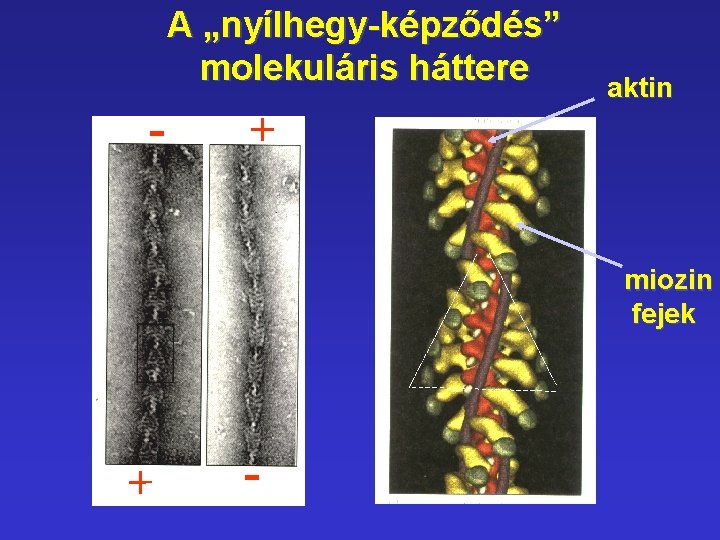
A „nyílhegy-képződés” molekuláris háttere - aktin + miozin fejek + -
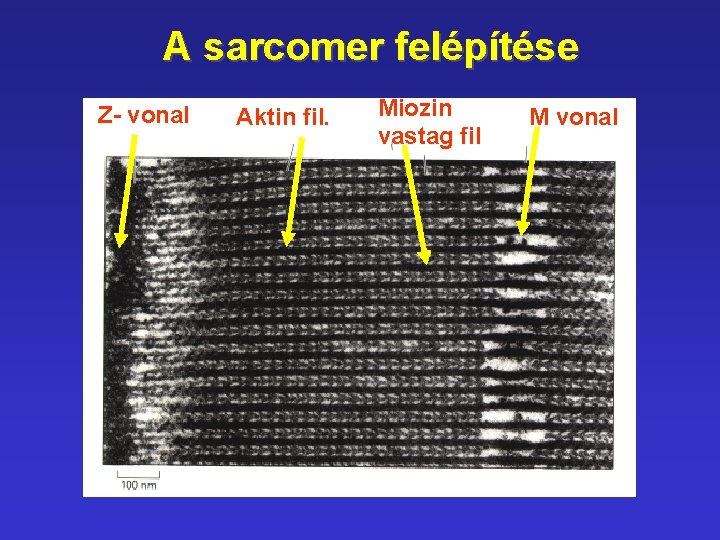
A sarcomer felépítése Z- vonal Aktin fil. Miozin vastag fil M vonal
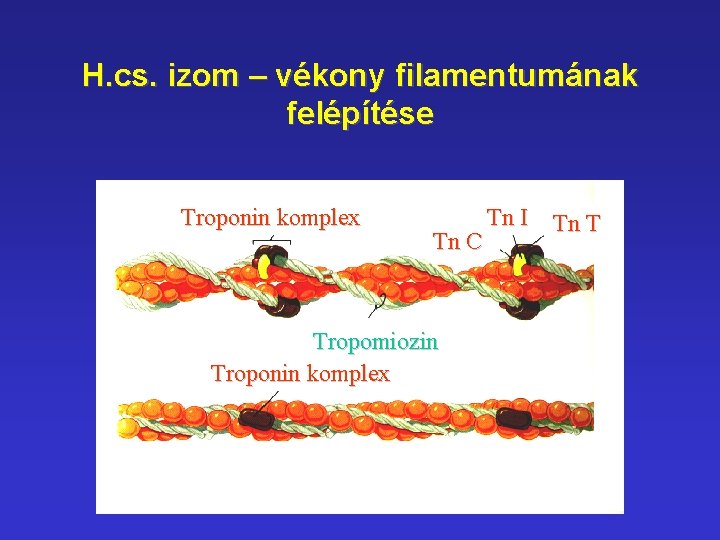
H. cs. izom – vékony filamentumának felépítése Troponin komplex Tn C Tropomiozin Troponin komplex Tn I Tn T

Troponin - Tropomiozin Troponin: • Tn-T tropomiozint köt • Tn-C Ca 2+ kötő (4 Ca 2+/mol = calmodulin) • Tn-I inhibitor Tropomiozin: • kettős a-helix • erősíti a filamentumot (7 kötőhelymol) • gátolja a filamin-aktin kötődést • elősegíti a miozin II kötést
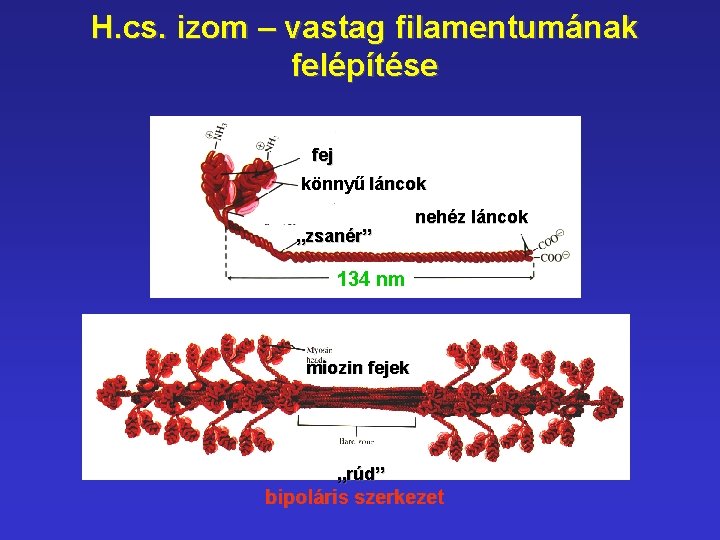
H. cs. izom – vastag filamentumának felépítése fej könnyű láncok „zsanér” nehéz láncok 134 nm miozin fejek „rúd” bipoláris szerkezet
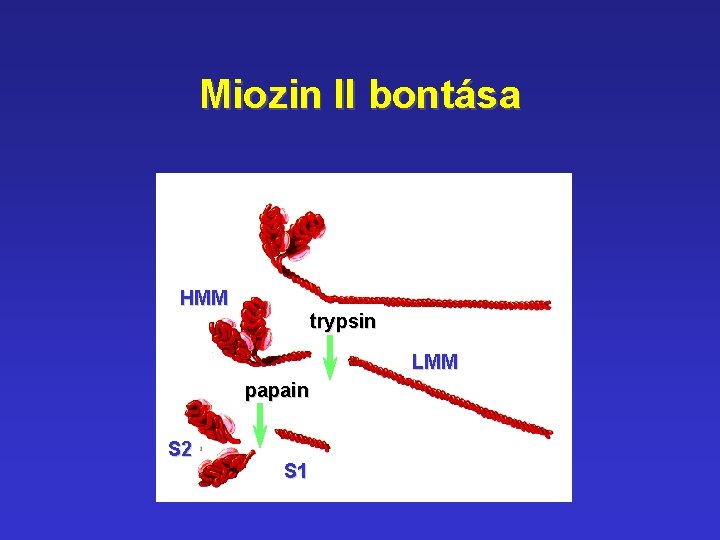
Miozin II bontása HMM trypsin LMM papain S 2 S 1
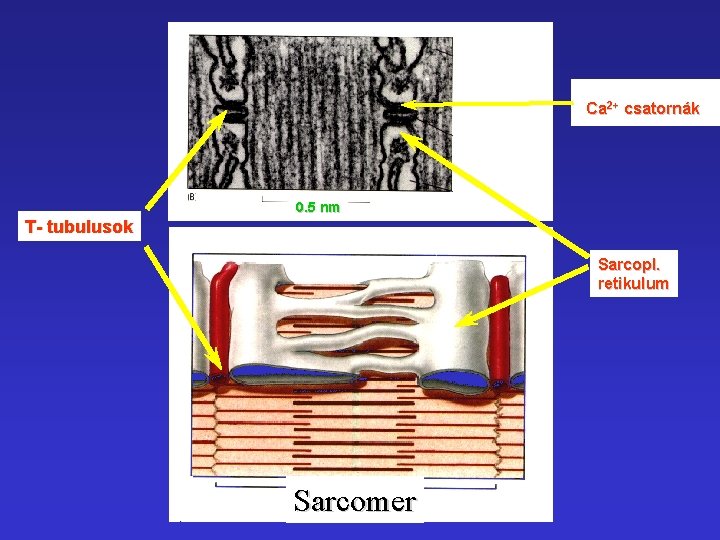
Ca 2+ csatornák 0. 5 nm T- tubulusok Sarcopl. retikulum Sarcomer
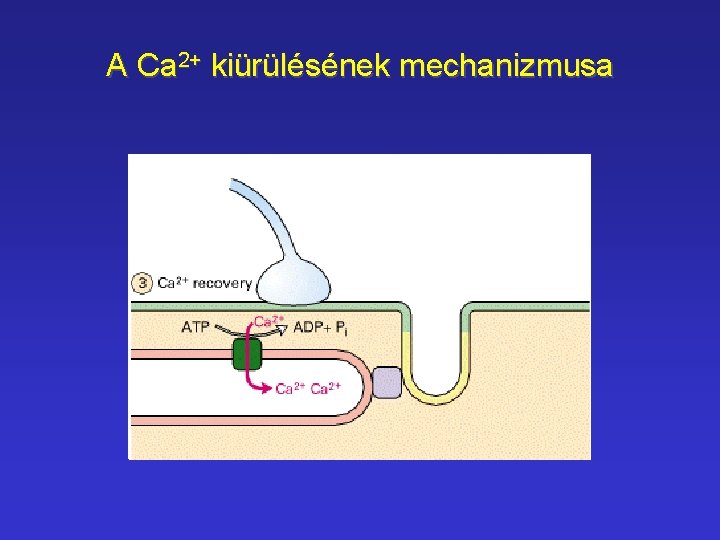
A Ca 2+ kiürülésének mechanizmusa

Tropomiozin hatása Az aktinhoz kötődő tropomiozin gátolja a miozin bekötődését Ca 2+ hatására a miozin-kötőhely szabaddá válik
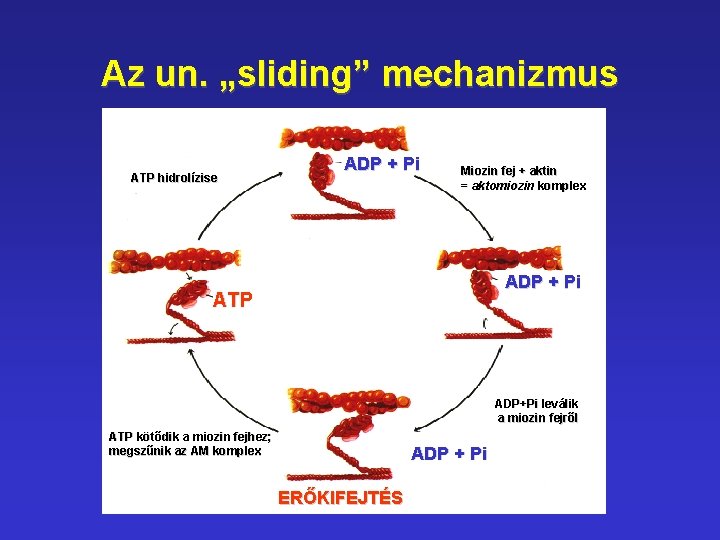
Az un. „sliding” mechanizmus ATP hidrolízise ADP + Pi Miozin fej + aktin = aktomiozin komplex ADP + Pi ATP ADP+Pi leválik a miozin fejről ATP kötődik a miozin fejhez; megszűnik az AM komplex ADP + Pi ERŐKIFEJTÉS
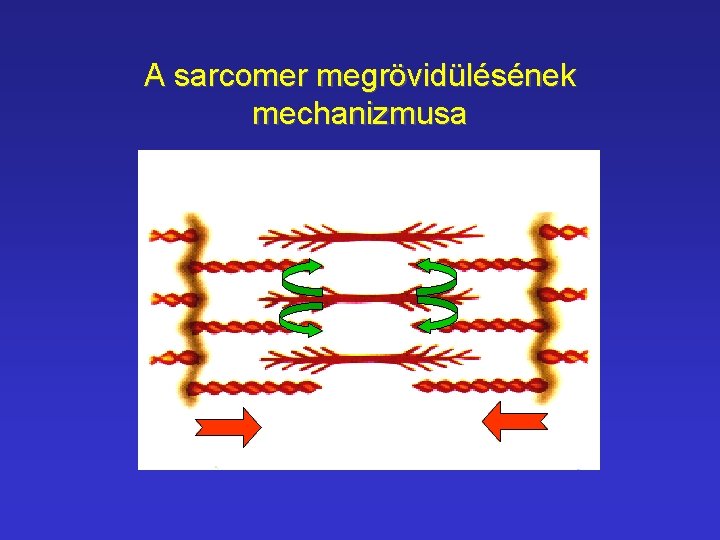
A sarcomer megrövidülésének mechanizmusa Sarcomer A csík
![Az aktin és proteinjeinek kapcsolata a slidinget megelőzően Aktin + TM [Aktin-TM] + Tn-T Az aktin és proteinjeinek kapcsolata a slidinget megelőzően Aktin + TM [Aktin-TM] + Tn-T](http://slidetodoc.com/presentation_image_h2/1a43d84fc788cb4f869dac00793fc9ab/image-58.jpg)
Az aktin és proteinjeinek kapcsolata a slidinget megelőzően Aktin + TM [Aktin-TM] + Tn-T [Aktin-TM-Tn-T] + Tn-I Miozin nem tud kötődni [Aktin-TM-Tn-T-Tn-I] + Tn-C [Aktin-TM-Tn-T-Tn-I-Tn-C] Ca 2+ kötődik és Tn-I gátlása TM-en megszűnik
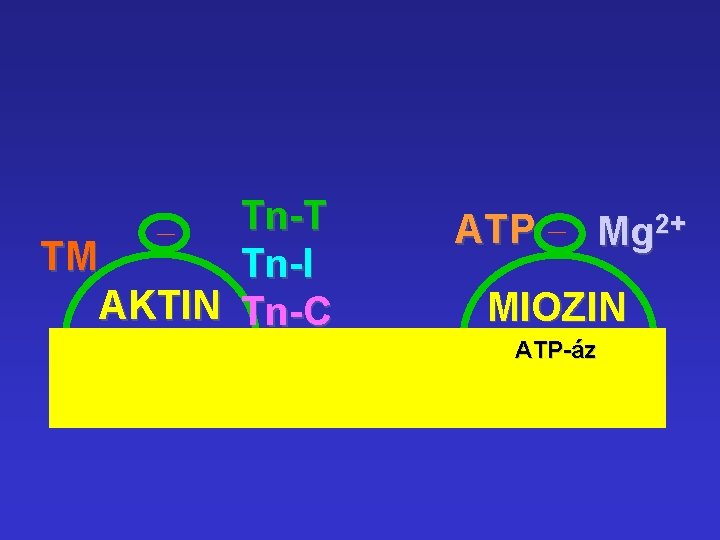
Tn-T TM Tn-I AKTIN Tn-C ATP Mg 2+ MIOZIN ATP-áz
![Ca 2+ [10 -8 10 -6 M] Tn-T TM Tn-I AKTIN Tn-C ATP Mg Ca 2+ [10 -8 10 -6 M] Tn-T TM Tn-I AKTIN Tn-C ATP Mg](http://slidetodoc.com/presentation_image_h2/1a43d84fc788cb4f869dac00793fc9ab/image-60.jpg)
Ca 2+ [10 -8 10 -6 M] Tn-T TM Tn-I AKTIN Tn-C ATP Mg 2+ MIOZIN ATP-áz
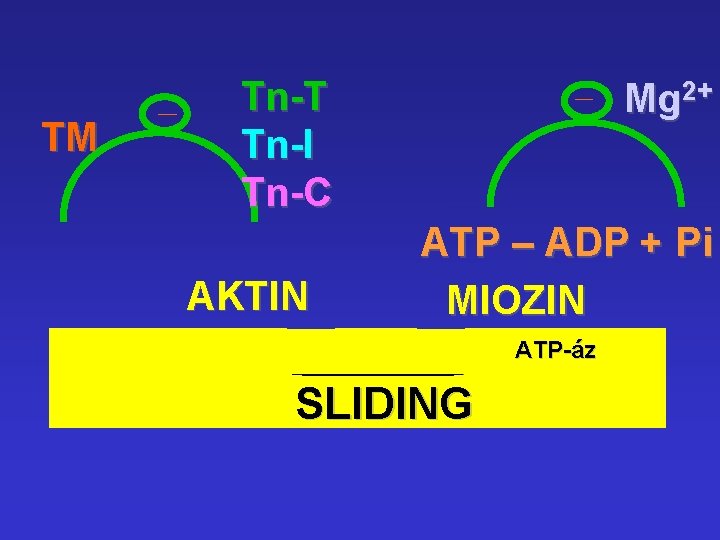
TM Tn-T Tn-I Tn-C AKTIN Mg 2+ ATP – ADP + Pi MIOZIN ATP-áz SLIDING

Az izommozgás energiaforrása kreatin kináz kreatin foszfát + ADP kreatin + ATP (arginin foszfát) (arginin) DG = - 3 kcal/mol
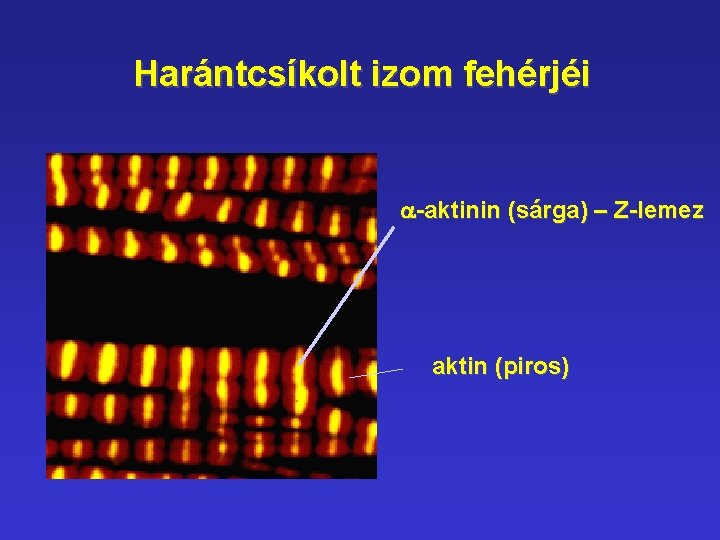
Harántcsíkolt izom fehérjéi a-aktinin (sárga) – Z-lemez aktin (piros)
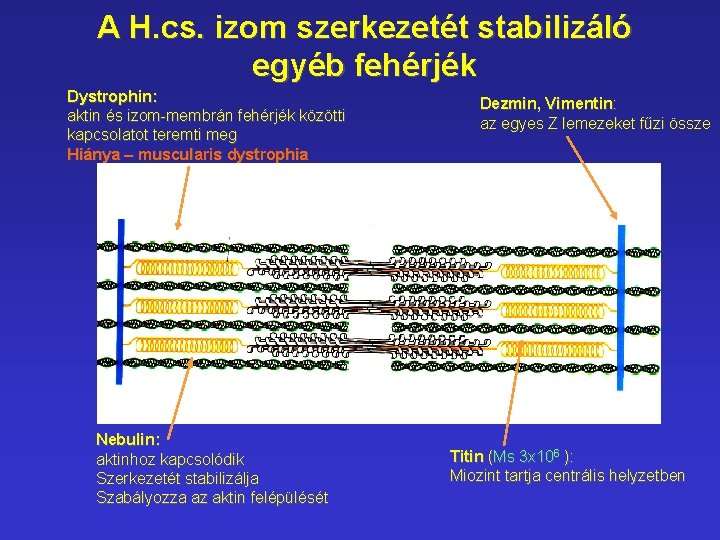
A H. cs. izom szerkezetét stabilizáló egyéb fehérjék Dystrophin: aktin és izom-membrán fehérjék közötti kapcsolatot teremti meg Hiánya – muscularis dystrophia Nebulin: aktinhoz kapcsolódik Szerkezetét stabilizálja Szabályozza az aktin felépülését Dezmin, Vimentin: az egyes Z lemezeket fűzi össze Titin (Ms 3 x 106 ): Miozint tartja centrális helyzetben
- Slides: 64