Citokrm oxidz A citokrm c oxidz defincija A









- Slides: 15

Citokróm oxidáz

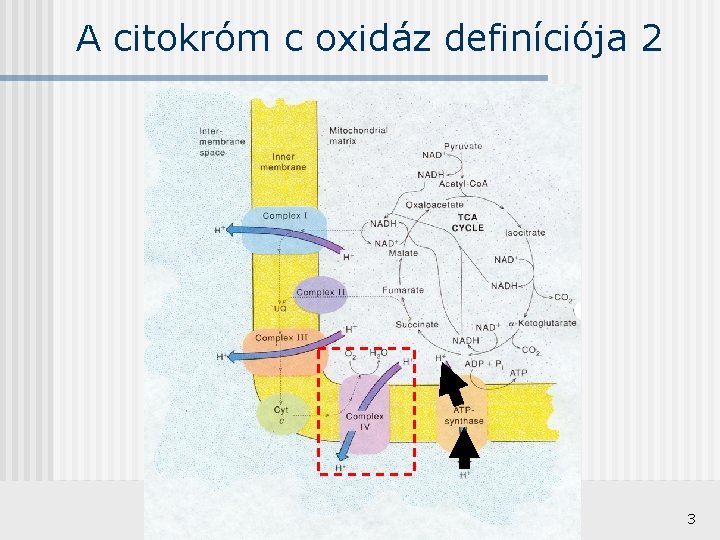
A citokróm c oxidáz definíciója A citokróm c oxidáz (COX) a légzési elektrontranszferlánc IV. komplexét alkotja. A mitokondrium belső membránjának illetve a baktériumok sejtmembránjában egy integráns fehérjéje. A elektrontranszferlánc tagjai: - NADH-UQ oxidoreduktáz szukcinát-UQ reduktáz UQ-cit-c oxidoreduktáz avagy citokróm bc 1 komplex citokróm-c oxidáz A citokróm c oxidáz szerepe, hogy elektront vesz át a III. komplexről, a két komplex között a szállítást a citokróm c biztosítja, ezért is hívják cyt-c oxidáznak. A folyamat során egy hidrogén iont jutat át a mitokondriális mátrixból a membránok közti térbe, miközben egy O 2 molekulát vízzé redukál. 2

A citokróm c oxidáz definíciója 2 3

A citokróm c oxidáz feladata A COX feladata kettős: 1. A légzési elektrontranszport lánc végén az oxigén vízzé történő redukciója egy elektrondonortól (pl. citokróm c) kapott elektronok és a vizes fázisban lévő protonok segítségével (kémiai vagy sztöchiomet-rikus protonok). Ezért terminális oxidázként is említik. O 2 + 4 e-p + 4 H+n = 2 H 2 O A 4 elektron 4 citokróm c-től származik időben egymás után. A 4 elektron a lánc elején 2 NADH molekula redukciójából ered. 2. A redox reakció szabadentalpiájának felhasználásával 4 további proton transzportja a membránon keresztül (proton pumpa). 4 H+n 4 H+p 4

A citokróm c oxidáz sztöhiometriája A teljes működést leíró egyenlet: O 2 + 4 e-p + 8 H+n 2 H 2 O + 4 H+p , ahol p és n a membrán külső (pozitív) és belső (negatív) oldalát jelentik. Az egyenlet szerint a protontranszport sztöchiometriája megfelel 4 proton transzportjának a membránon keresztül. Azaz az elektromos töltéstranszport sztöchiometriája: 8 pozitív töltés transzportja minden egyes O 2 molekulára vagy minden 2 NADH molekulára. 5

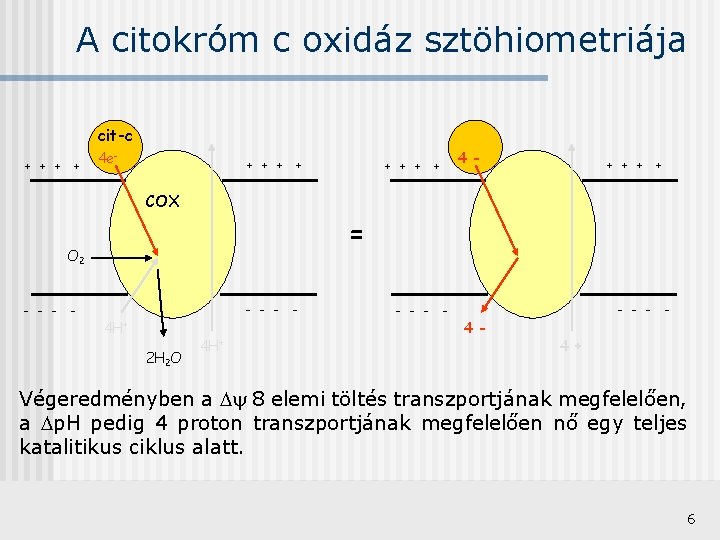
A citokróm c oxidáz sztöhiometriája cit-c + + 4 e- + + COX - - 4 H+ 2 H 2 O 4 - + + = O 2 - - + + 4 H+ - - - - 4 + Végeredményben a 8 elemi töltés transzportjának megfelelően, a p. H pedig 4 proton transzportjának megfelelően nő egy teljes katalitikus ciklus alatt. 6

A citokróm c oxidáz energetikája A homeosztázisban dinamikus egyensúly van, tehát adott membránpotenciál és p. H különbség mellett folyik a töltések és protonok transzportja. Például: Egyensúlyban = 180 m. V, p = 200 m. V (a különbség a p. H-ból adódik). A cit-c redoxpotenciálja Eh = 290 m. V, az ½ O 2/H 2 O páré pedig 800 m. V. Négy elektron átjutásakor a szabadentalpia-különbség, m. V-ban kifejezve: E = 4 x ( 800 -290 -180) > 1200 m. V. Ez elegendő lenne 6 proton átjuttatására a 200 m. V-os proton elektrokémiai potenciálkülönbségen. A valóságban a COX csak 4 protont pumpál. A működése tehát szabadentalpia-disszipációval jár, ezért nem reverzibilis! 7

Különböző forrásokból származó citokróm c oxidázok Mindegyikben közös a katalitikus centrumok elhelyezkedése, környezete, oxidációs állapotai: Cu. A: 2 rézion, 1 -szeresen redukálható: 2 Cu. AII + Cu. AI (kupri kupro) hem a: 1 -szeresen redukálható: Fe. III Fe. II (ferri ferro) binukleáris centrum: hem a 3 + Cu. B: 2 -szeresen redukálható: Fe. III + Cu. BII Fe. II + Cu. BI , de a katalitikus ciklus közben a ferril forma (Fe. IV) is fellép átmenetileg. 8

Különböző forrásokból származó citokróm c oxidázok 2 eukarióta mitokondriális COX: Alegységek száma > 10. Ebből a 4 legnagyobbat a mitokondriális DNS kódolja. A két hem és a Cu. B az I. alegységhez, a Cu. A a II. alegységhez kötött. prokarióta COX (pl. Rhodobacter sphaeroides, Paracoccus denitrificans): Alegységek száma 3 -4. A két hem és a Cu. B az I. alegységhez, a Cu. A a II. alegységhez kötött. 9

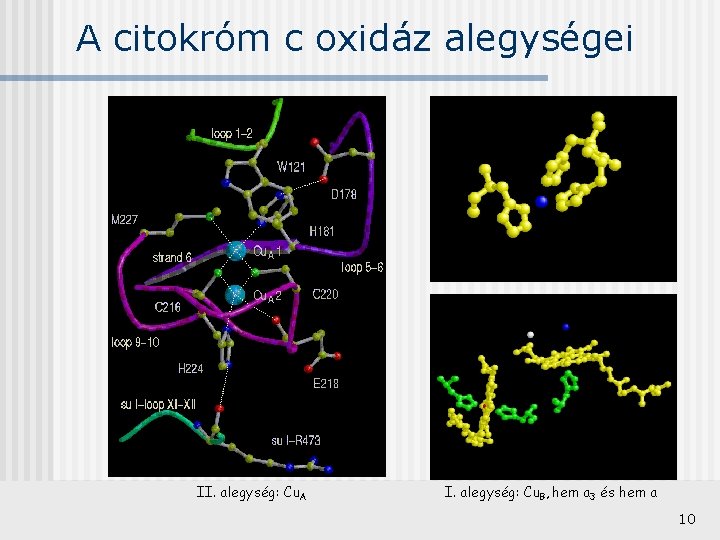
A citokróm c oxidáz alegységei II. alegység: Cu. A I. alegység: Cu. B, hem a 3 és hem a 10

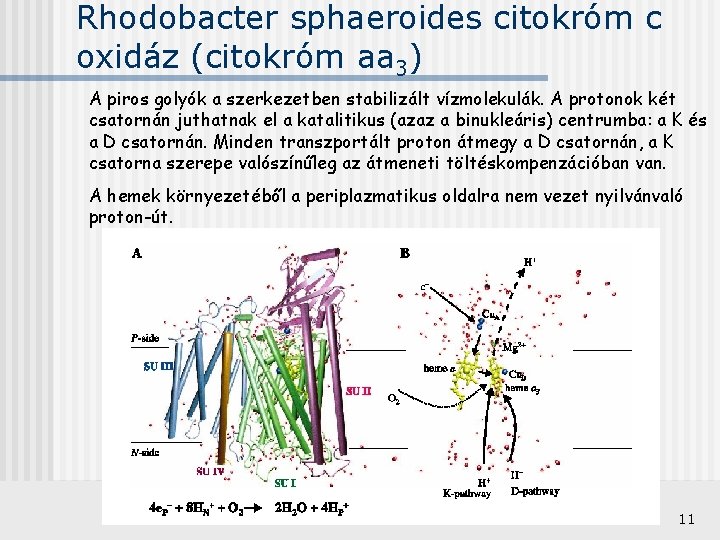
Rhodobacter sphaeroides citokróm c oxidáz (citokróm aa 3) A piros golyók a szerkezetben stabilizált vízmolekulák. A protonok két csatornán juthatnak el a katalitikus (azaz a binukleáris) centrumba: a K és a D csatornán. Minden transzportált proton átmegy a D csatornán, a K csatorna szerepe valószínűleg az átmeneti töltéskompenzációban van. A hemek környezetéből a periplazmatikus oldalra nem vezet nyilvánvaló proton-út. 11

Rhodobacter sphaeroides citokróm c oxidáz (citokróm aa 3) A D csatorna jól ki van bélelve vízmolekulákkal és poláros aminosav oldalláncokkal. Ennek fontos szerepe van a proton vezetőképességben. 12

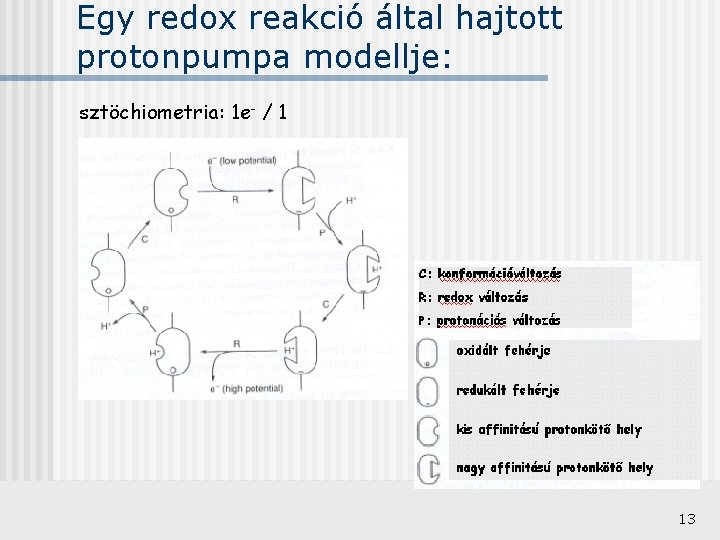
Egy redox reakció által hajtott protonpumpa modellje: sztöchiometria: 1 e- / 1 13

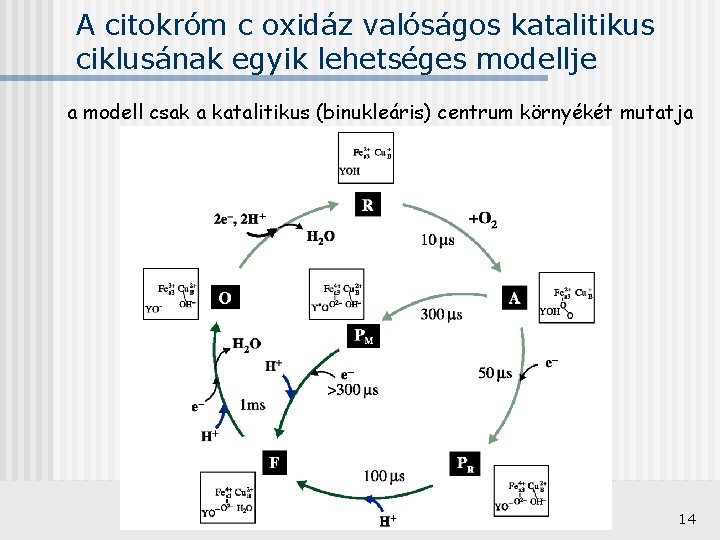
A citokróm c oxidáz valóságos katalitikus ciklusának egyik lehetséges modellje a modell csak a katalitikus (binukleáris) centrum környékét mutatja 14

A citokróm c oxidáz alkalmazásai n. A szabad gyökök közül réz szintjét enzimatikus úton alacsonyan tartja. n Növényélettanban oxidáz tesztet használnak a Pseudomonas és Vibrio fajoktól történő elkülönítésében. Az oxidáz teszt: Egy csepp oxidáz reagenst cseppentsünk a szűrőpapír szeletre, majd a tesztmikrobák ferde agar tenyészetéből steril üvegbot segítségével (közönséges oltókacs alkalmazásánál a Fe 2+- ionok jelenléte téves pozitivitást eredményezhet) kis mennyiségű baktériumtömeget kenünk az előzőleg impregnált szűrőpapírra. A pozitív reakciót a 30 -60 másodperc alatt bekövetkező lilás elszíneződés jelzi. Az egy percen túl bekövetkező elszíneződést negatívnak kell tekinteni. n. A élelmiszeriparban a maradékanyagoknak állati eredetű élelmiszerekben való előfordulását mutatják ki a segítségével. n A citokróm c oxidáz enzim működésének megváltozását az Archeimer-kórban szenvedőknél is megfigyelték 15