CINTICA QUMICA Prof Tatiane Barcellos 1 Objetivo Estuda

CINÉTICA QUÍMICA Profª. : Tatiane Barcellos

1 - Objetivo Estuda a velocidade das reações químicas e os fatores que influem nessa velocidade.

2 -VELOCIDADE MÉDIA DAS REAÇÕES • É o quociente da variação da molaridade (mol ou massa) do reagente (ou produto) em um dado intervalo de tempo. Obs. : [X] molaridade
![N 2 + 3 H 2 2 NH 3 • Ex: TEMPO [NH 3] N 2 + 3 H 2 2 NH 3 • Ex: TEMPO [NH 3]](http://slidetodoc.com/presentation_image_h2/5bd4a0fea0fd040c87dad1228495fe69/image-4.jpg)
N 2 + 3 H 2 2 NH 3 • Ex: TEMPO [NH 3] [N 2] [H 2] 0 0 100 300 10 32, 5 84, 75 251, 25 15 40 80 240
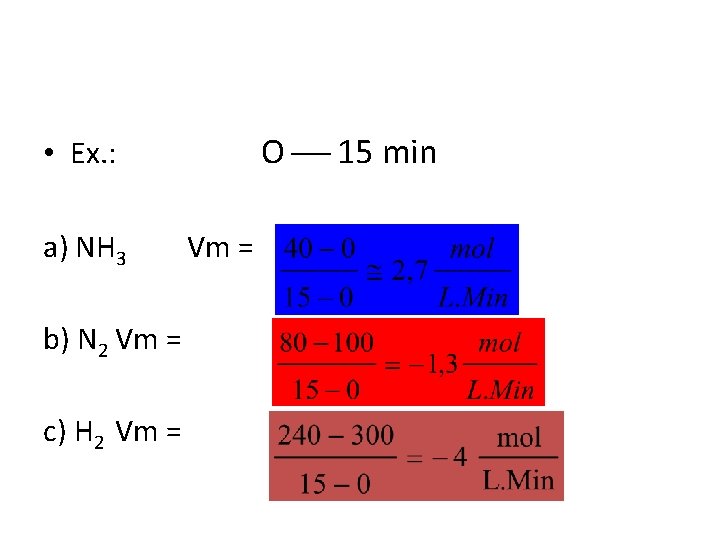
O 15 min • Ex. : a) NH 3 b) N 2 Vm = c) H 2 Vm =

EXEMPLO (FEI-SP) A combustão do butano (C 4 H 10) correspondente à equação: C 4 H 10 + 13/2 O 2 → 4 CO 2 + 5 H 2 O + Energia Se a velocidade da reação for 0, 05 mol butano/minuto, qual a massa de CO 2 produzida em 1 hora? RESOLUÇÃO: C 4 H 10 1 mol 0. 05 mol CO 2 4 x 44 g=176 g X Logo: X=8, 8 g/min Mas: 8, 8. 60 =528 g / h
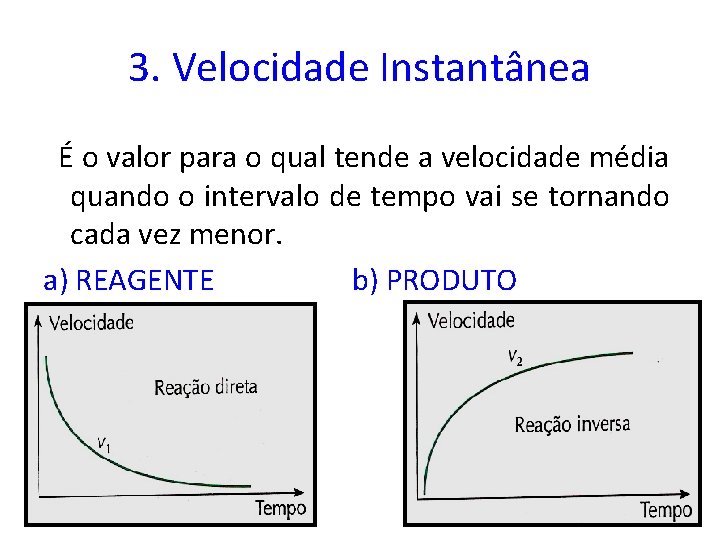
3. Velocidade Instantânea É o valor para o qual tende a velocidade média quando o intervalo de tempo vai se tornando cada vez menor. a) REAGENTE b) PRODUTO

EXEMPLO (Cesgranrio-RJ) O gráfico a seguir representa a variação das concentrações das substâncias X, Y e Z durante a reação em que elas tomam parte. A equação que representa a reação é: a)X + Z Y b)X + Y Z c)X Y + Z d)Y X + Z e)Z X + Y

4. Fatores que Afetam a Velocidade das Reações a) Superfície de Contato;

b) Afinidade Química; Ex. : Fe + H 2 O Na + H 2 O explosiva c) Estado Físico: sólido < líquido < gasoso d) Estrutura Cristalino; Cgraf + O 2 CO 2 Cdiam + O 2 CO 2 (reação lenta) Obs. : Quanto mais compacta a estrutura cristalina, menor a velocidade da reação. e) Reagentes Dissolvidos; Ag. NO 3(s) + Na. C (s) X Ag. NO 3(aq) + Na. C (aq) Ag. C (aq) + Na. NO 3(aq)

f) Concentração das substâncias: Quanto mais concentrada, mais rápida será a reação. g) Pressão: Maior a pressão, mais rápida a reação em reações entre gases. h) Temperatura; Regra de Van’t Hoff: Um aumento de 10ºC faz com que a velocidade da reação dobre. I) Catalisadores. Substância capaz de acelerar uma reação sem ser consumido durante a reação.
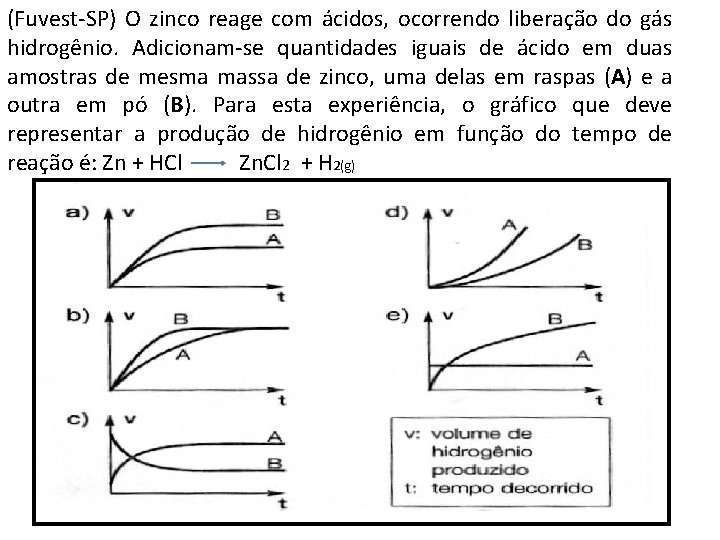
(Fuvest-SP) O zinco reage com ácidos, ocorrendo liberação do gás hidrogênio. Adicionam-se quantidades iguais de ácido em duas amostras de mesma massa de zinco, uma delas em raspas (A) e a outra em pó (B). Para esta experiência, o gráfico que deve representar a produção de hidrogênio em função do tempo de reação é: Zn + HCl Zn. Cl 2 + H 2(g)
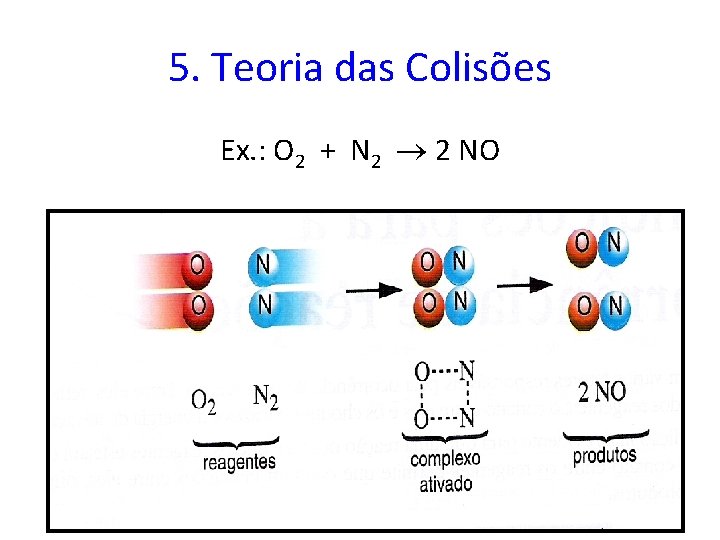
5. Teoria das Colisões Ex. : O 2 + N 2 2 NO

Segundo a teoria das colisões, a velocidade depende de: a) freqüência dos choques; b) orientação dos choques; c)energia dos choques. Energia de ativação (Eat): é a quantidade de energia fornecida ao reagente necessária para a formação do complexo ativado.
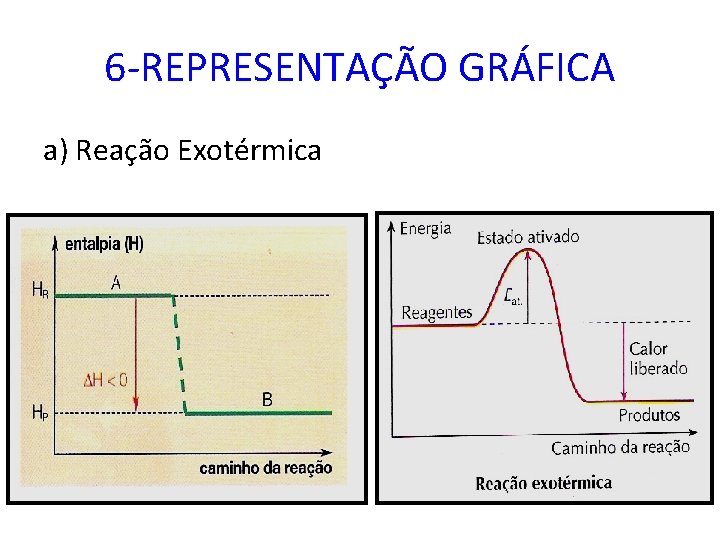
6 -REPRESENTAÇÃO GRÁFICA a) Reação Exotérmica
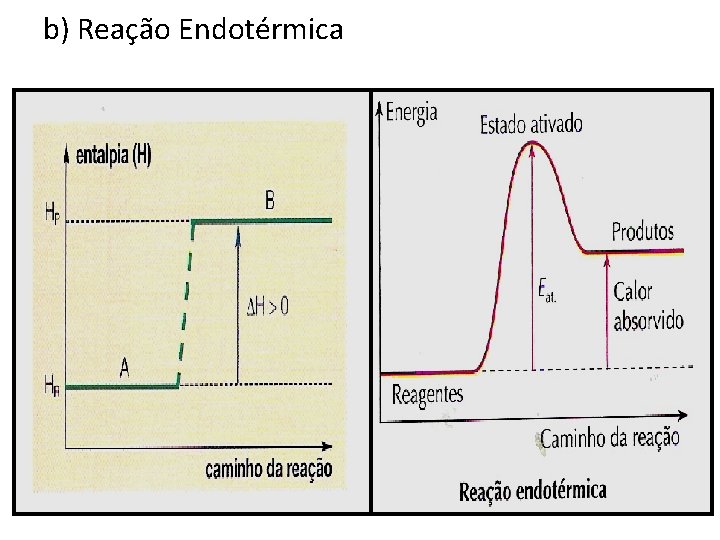
b) Reação Endotérmica
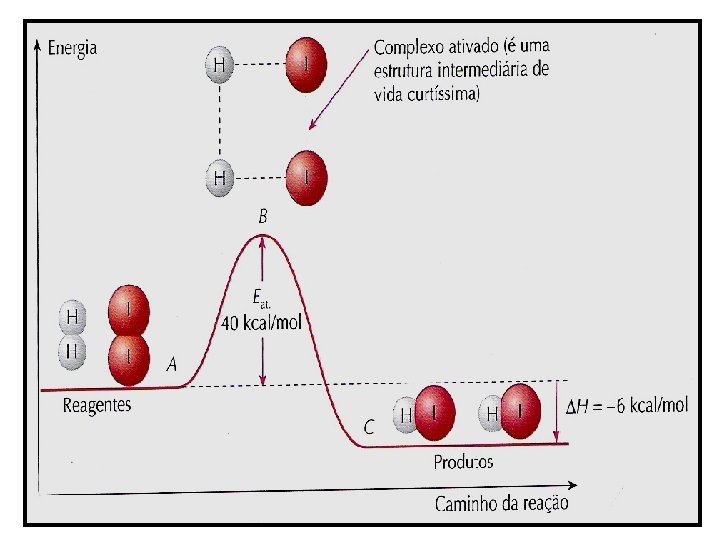

(UFBA) Considere o diagrama abaixo para a seguinte reação: A entalpia da reação e a energia de ativação representadas são, respectivamente: A energia de ativação é 28 Kcal/mol. E a entalpia é 25 kcal/mol.

7. Lei da Velocidade (Lei da ação das massas/guldberg-waage) Seja a reação genérica: a. A + b. B c. C+d. D V = K. [A]a. [B]b Onde: K Constante Cinética da Velocidade (depende dos fatores que influem na velocidade da reação principalmente a temperatura).

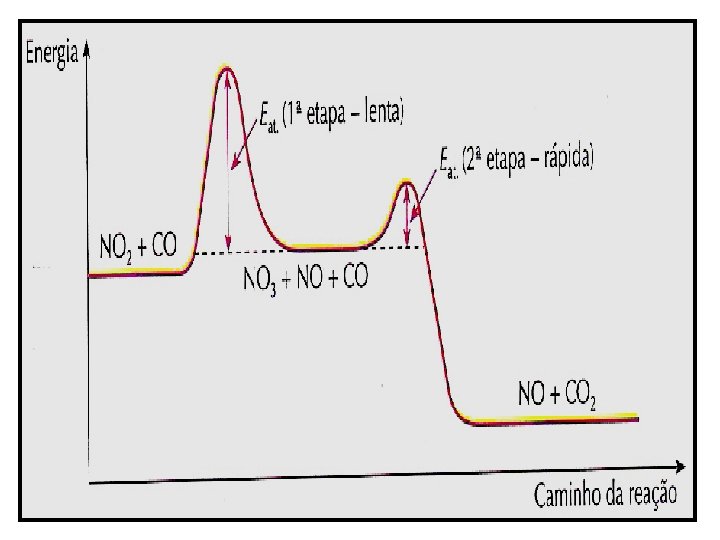
Mecanismo da Reação: Conjunto de reações elementares ou parciais segundo as quais ela se processa. Reação Global: NO 2 + CO NO + CO 2 Reações Elementares: 2 NO 2→NO 3 + NO (LENTA) NO 3 +CO → NO 2 + CO 2 (RÁPIDA) Logo: V = k. [NO 2]2 Obs. : A velocidade da reação dependerá da etapa lenta. Ordem Expoente Ordem Global Soma dos expoentes Molecularidade n. º de moléculas que se chocam em cada etapa da reação. Ex. : H 2 + I 2 2 HI V = K. [H 2]. [I 2]
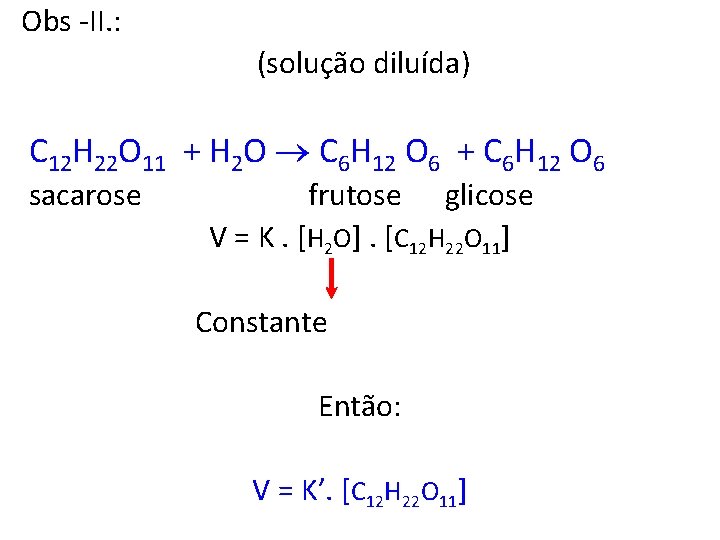
Obs -II. : (solução diluída) C 12 H 22 O 11 + H 2 O C 6 H 12 O 6 + C 6 H 12 O 6 sacarose frutose glicose V = K. [H 2 O]. [C 12 H 22 O 11] Constante Então: V = K’. [C 12 H 22 O 11]
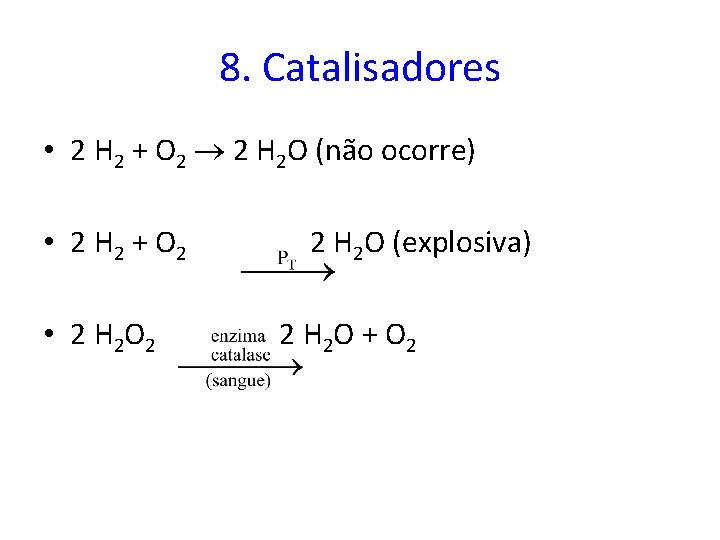
8. Catalisadores • 2 H 2 + O 2 2 H 2 O (não ocorre) • 2 H 2 + O 2 • 2 H 2 O 2 2 H 2 O (explosiva) 2 H 2 O + O 2

8. 1. Conceitos a) Catálise: é o aumento da velocidade da reação provocado pelo catalisador. b) Promotor ou ativador: substância que acentua o efeito do catalisador, embora sozinha não tenha efeito catalítico. Ex. : N 2 + 3 H 2 → 2 NH 3 (Fe + K 2 O + A 2 O 3) c) Veneno ou anticatalisador: diminui ou anula o efeito do catalisador: Ex. : N 2 + 3 H 2 → 2 NH 3 (Fe + As) d) Autocatálise: é o processo que ocorre quando um dos produtos da reação age como catalisador da própria reação. CH 3 COOC 2 H 5 + H 2 O CH 3 COOH + C 2 H 5 OH Obs. : A reação é lenta até a formação do ácido.

8. 2. Tipos de Catálise a) Homogênea 2 SO 2(g) + O 2(g) 2 SO 3(g) b) Heterogênea 2 SO 2(g) + O 2(g) 2 SO 3(g)

8. 3. Mecanismo da catálise a) Formação do composto intermediário Reação Global: 2 SO 2 + O 2 2 SO 3 Mecanismo: 2 NO + O 2 2 NO 2 (rápida) 2 NO 2 + 2 SO 2 2 SO 3 + 2 NO (rápida)
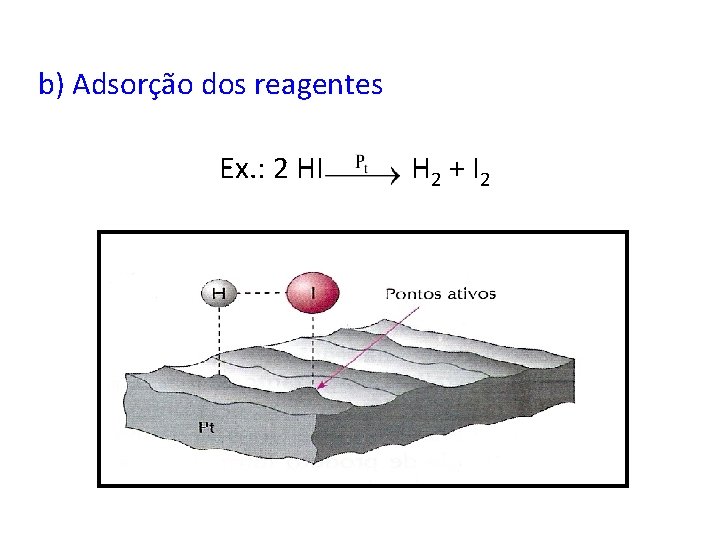
b) Adsorção dos reagentes Ex. : 2 HI H 2 + I 2
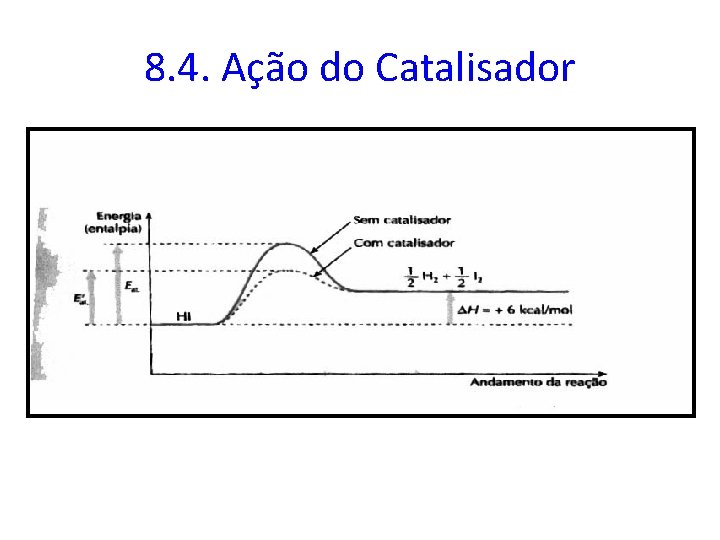
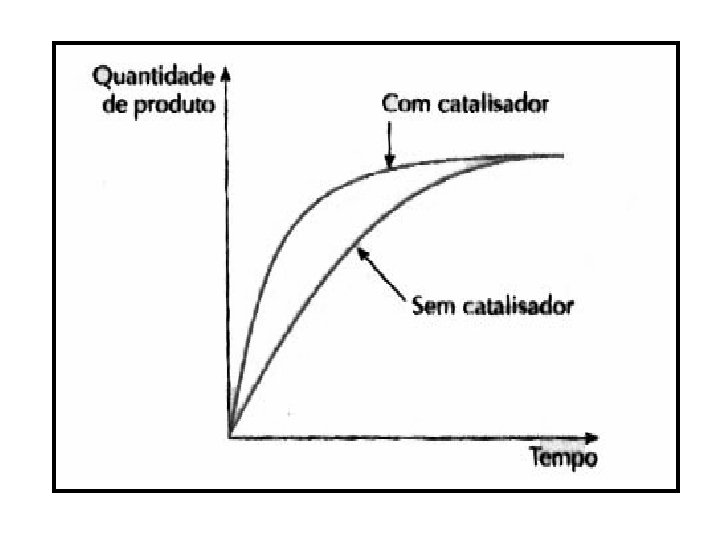
8. 4. Ação do Catalisador

• o catalisador nunca muda o H da reação (isto é, a quantidade total de calor ou energia liberada ou absorvida pela reação); • o catalisador tanto age na reação direta como na reação inversa; • o catalisador não altera o rendimento da reação (quantidade de produto formado), apenas permite obter os produtos mais rapidamente.
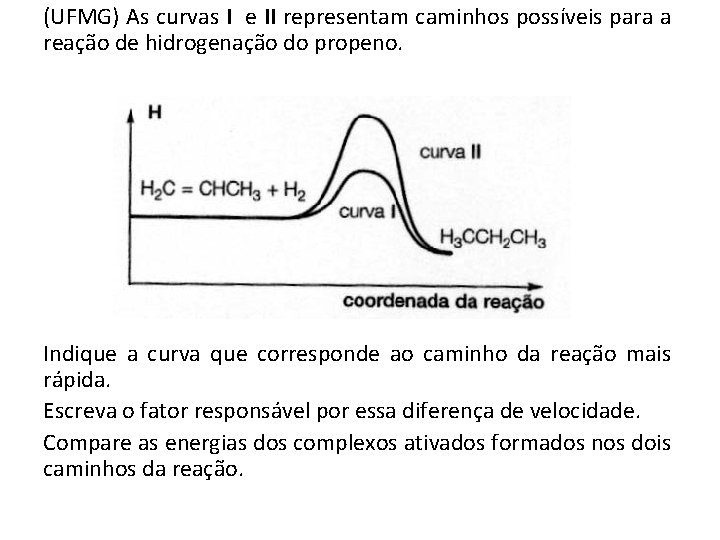
(UFMG) As curvas I e II representam caminhos possíveis para a reação de hidrogenação do propeno. Indique a curva que corresponde ao caminho da reação mais rápida. Escreva o fator responsável por essa diferença de velocidade. Compare as energias dos complexos ativados formados nos dois caminhos da reação.
- Slides: 31