CINTICA QUMICA Prof Agamenon Roberto Parte da qumica

CINÉTICA QUÍMICA Prof. Agamenon Roberto

Parte da química que estuda a rapidez das reações Oxidação do ferro Explosão da pólvora (ocorre de forma lenta) (ocorre de forma rápida). Prof. Agamenon Roberto

Rapidez (velocidade) média de formação e de consumo É uma grandeza que indica como as quantidades de reagente(s) e produto(s) dessa reação variam com o passar do tempo VM = Prof. Agamenon Roberto ∆ quantidade ∆ tempo
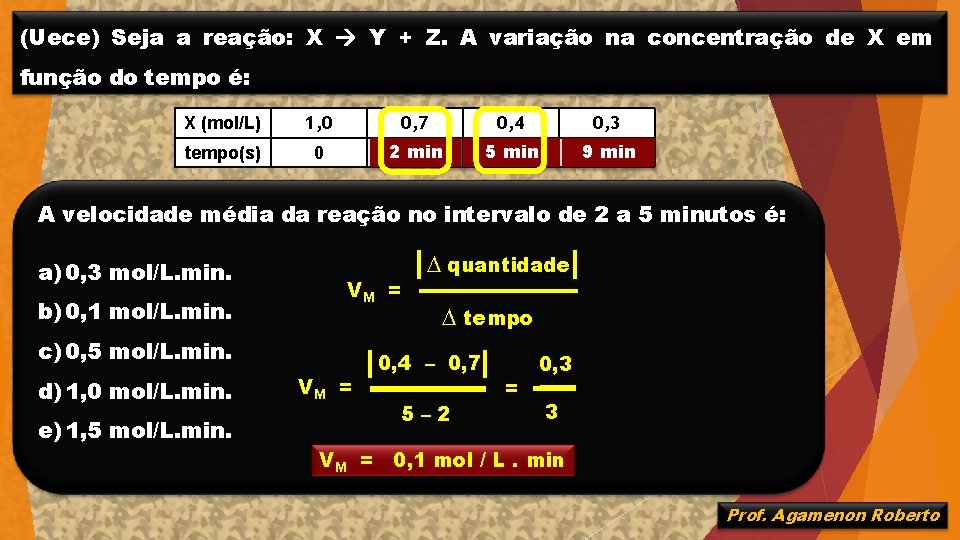
(Uece) Seja a reação: X Y + Z. A variação na concentração de X em função do tempo é: X (mol/L) 1, 0 0, 7 0, 4 0, 3 tempo(s) 0 2120 min 5300 min 9540 min A velocidade média da reação no intervalo de 2 a 5 minutos é: a) 0, 3 mol/L. min. b) 0, 1 mol/L. min. VM = c) 0, 5 mol/L. min. d) 1, 0 mol/L. min. e) 1, 5 mol/L. min. VM = ∆ quantidade ∆ tempo 0, 4 – 0, 7 5– 2 = 0, 3 3 VM = 0, 1 mol / L. min Prof. Agamenon Roberto

TEORIA DAS COLISÕES De acordo com a teoria das colisões pode-se afirmar que a velocidade de uma reação depende da: Ø frequência das colisões Ø energia das colisões Ø orientação das moléculas nas colisões Prof. Agamenon Roberto
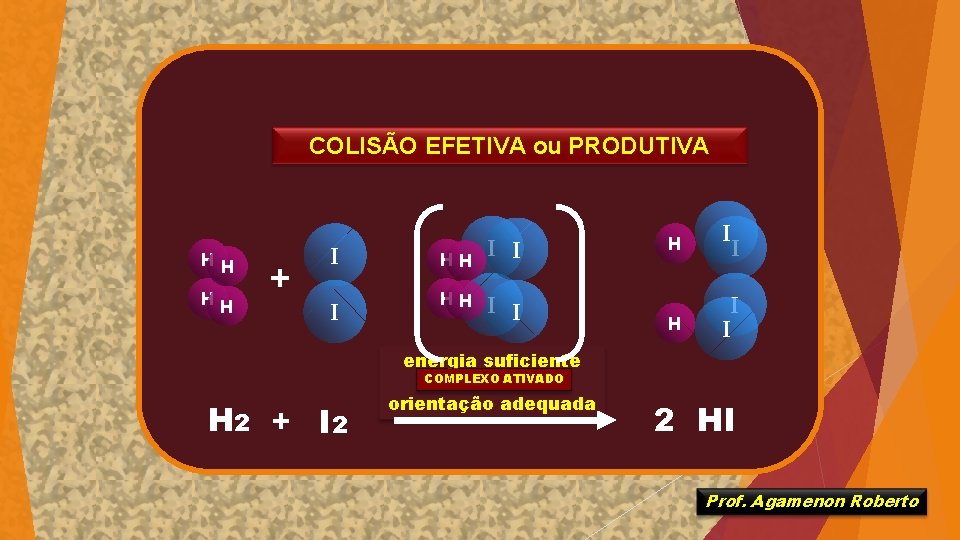
COLISÃO EFETIVA ou PRODUTIVA HH HH + I I H 2 + I 2 HH HH I I energia suficiente COMPLEXO e ATIVADO orientação adequada H I I 2 HI Prof. Agamenon Roberto

COLISÃO NÃO EFETIVA ou NÃO PRODUTIVA H I Sem energia suficiente e orientação adequada Prof. Agamenon Roberto

COLISÃO NÃO EFETIVA ou NÃO PRODUTIVA H I energia suficiente e orientação inadequada Prof. Agamenon Roberto

FATORES QUE AFETAM A RAPIDEZ DAS REAÇÕES CONCENTRAÇÃO DOS REAGENTES Maior concentração dos reagentes Menor concentração dos reagentes Prof. Agamenon Roberto maior rapidez da reação menor rapidez da reação

FATORES QUE AFETAM A RAPIDEZ DAS REAÇÕES PRESSÃO EM REAÇÕES COM GASES Maior pressão Menor pressão maior rapidez da reação menor rapidez da reação Prof. Agamenon Roberto

FATORES QUE AFETAM A RAPIDEZ DAS REAÇÕES EFEITO DA TEMPERATURA Maior temperatura Menor temperatura Prof. Agamenon Roberto maior rapidez da reação menor rapidez da reação

FATORES QUE AFETAM A RAPIDEZ DAS REAÇÕES EFEITO DA SUPERFÍCIE DE CONTATO Maior superfície de contato Menor superfície de contato maior rapidez da reação menor rapidez da reação Prof. Agamenon Roberto

FATORES QUE AFETAM A RAPIDEZ DAS REAÇÕES EFEITO DO CATALISADOR Com catalisador maior rapidez da reação Sem catalisador menor rapidez da reação Prof. Agamenon Roberto
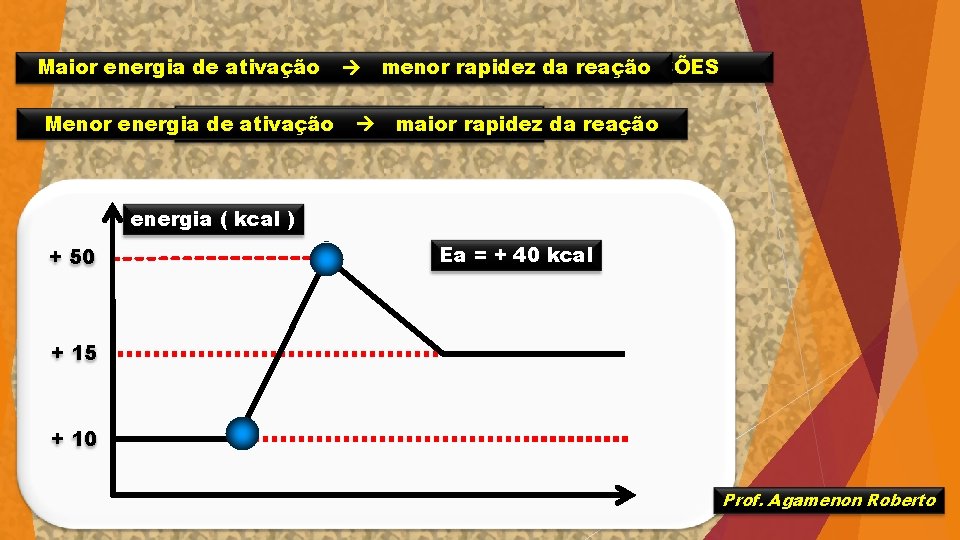
Maior energia FATORES de ativação QUE AFETAM menor A RAPIDEZ rapidez da. DAS reação REAÇÕES Menor energia ENERGIA de ativação. DE ATIVAÇÃO maior rapidez da reação energia ( kcal ) + 50 Ea = + 40 kcal + 15 + 10 Prof. Agamenon Roberto


(Unifor-CE) Considerando os fatores que alteram a rapidez das transformações químicas, pode-se afirmar apodrecerá mais rapidamente se estiver: a) Sem casca, em geladeira. b) Em pedaços, congelada. c) Inteira, exposta ao sol. d) Em pedaços, exposta ao sol. e) Com casca, exposta ao sol. Prof. Agamenon Roberto que uma fruta
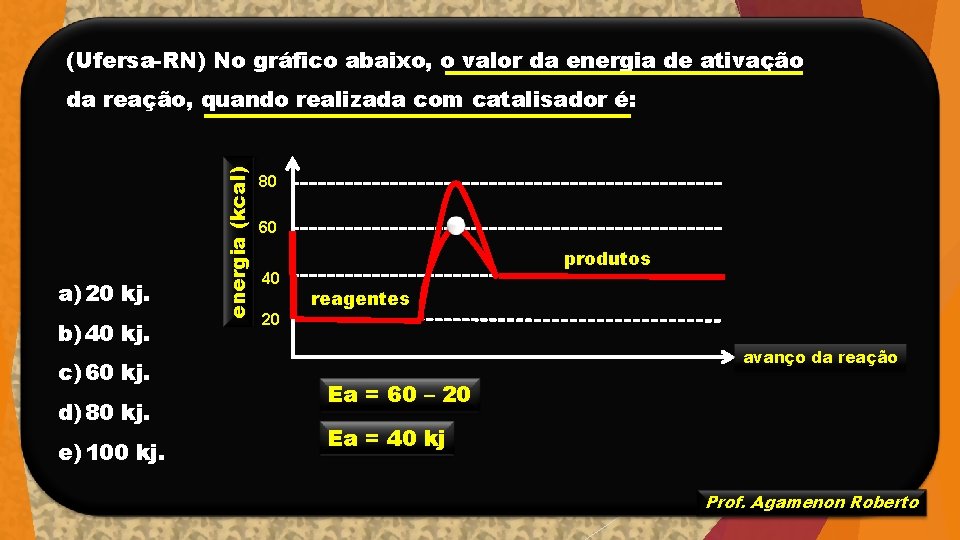
(Ufersa-RN) No gráfico abaixo, o valor da energia de ativação a) 20 kj. b) 40 kj. c) 60 kj. d) 80 kj. e) 100 kj. energia (kcal) da reação, quando realizada com catalisador é: 80 60 40 produtos reagentes 20 avanço da reação Ea = 60 – 20 Ea = 40 kj Prof. Agamenon Roberto

O carvão é combustível constituído de uma mistura de compostos ricos em carbono. A situação do combustível, do comburente e a temperatura utilizada favorecerão a combustão do carbono com maior velocidade, é, na ordem: a) carvão em pedaços, ar atmosférico, 0°C. b) carvão pulverizado, ar atmosférico, 30°C. c) carvão em pedaços, oxigênio puro, 20°C. d) carvão pulverizado, oxigênio puro, 100°C. e) carvão em pedaços, oxigênio líquido, 50°C. temperatura em que superfície concentração de contato ocorre a reação

Fatores que influem na rapidez da reação Maior superfície de contato maior rapidez da reação Maior concentração maior rapidez da reação Maior temperatura maior rapidez da reação voltar

LEI DE VELOCIDADE OU LEI CINÉTICA Para uma reação genérica: a A + b B Produtos Denomina-se LEI CINÉTICA a seguinte expressão: v = k [ A ] x. [ B ]y Prof. Agamenon Roberto
![LEI DE VELOCIDADE OU LEI CINÉTICA v = k [ A ] x. [ LEI DE VELOCIDADE OU LEI CINÉTICA v = k [ A ] x. [](http://slidetodoc.com/presentation_image_h2/b5446c21dc68eb8b0fa8bc93a40bc753/image-21.jpg)
LEI DE VELOCIDADE OU LEI CINÉTICA v = k [ A ] x. [ B ]y Onde os valores de “ x ” e “ y ” são determinados experimentalmente Os expoentes “ x ” e “ y ” são chamados de ORDEM DA REAÇÃO x: ordem da reação em relação a A y: ordem da reação em relação a B x + y: ordem global da reação Prof. Agamenon Roberto

Para as reações ELEMENTARES os valores dos expoentes são iguais aos coeficientes das substâncias na equação química Para a reação: 2 NO (g) + H 2 (g) N 2 O (g) + H 2 O (g) A lei da velocidade é: v = k [ NO ] Prof. Agamenon Roberto 2 [ H 2 ]

A reação A + 2 B P se processa em uma única etapa. Qual a velocidade desta reação quando K = 0, 3 L/mol. min, [A] = 2, 0 mol/L e [B] = 3, 0 mol/L? a) 5, 4. k = 0, 3 L / mol. min b) 4, 5. [ A ] = 2, 0 mol/L c) 1, 8. d) 18, 0. e) 54. [ B ] = 3, 0 mol/L v = 0, 3 x v = 0, 3 2 x x 2 32 x 9 v = 5, 4 Prof. Agamenon Roberto

A equação X + 2 Y XY 2 representa uma reação, cuja equação da velocidade é: v = k. [X]. [Y] Indique o valor da constante de velocidade, para a reação dada, sabendo que, quando a concentração de X é 1 mol/L e a de Y é 2 mol/L, a velocidade da reação é de 3 mol/L. min. : a) 3, 0. b) 1, 5. c) 1, 0. d) 0, 75. e) 0, 5. k=? [ X ] = 1, 0 mol/L [ B ] = 2, 0 mol/L v = 3 mol/L. min Prof. Agamenon Roberto 3=k k = x 3 2 1 x 2

(Unip-SP) A poluição é uma das causas da destruição da camada de ozônio. Uma das reações que podem ocorrer no ar poluído é a reação do dióxido de nitrogênio com o ozônio: 2 NO 2 (g) + O 3 (g) N 2 O 5 (g) + O 2 (g) Essa reação ocorre em duas etapas: I. NO 2 (g) + O 3 (g) NO 3 (g) + O 2 (g) II. NO 3 (g) + NO (g) N 2 O 5 (g) (lenta) (rápida) Assinale a lei de velocidade para essa reação: a) v = k [NO 2]2 [O 3] b) v = k [NO 2] [O 3] c) v = k [NO 3] [NO 2] d) v = k [NO 2]2 [O 3] + k’ [NO 3] [NO 2] e) v = k [NO 2] Prof. Agamenon Roberto

Na decomposição térmica da amônia expressa pela equação: 2 NH 3 (g) N 2 (g) + 3 H 2 (g) Duplicando-se a concentração molar de NH 3, a velocidade da reação ficará: a) inalterada. b) duas vezes maior. c) três vezes maior. d) quatro vezes maior. e) seis vezes maior. v = k [ NH 3 ] 2 [ NH 3 ] = x mol /L v = k x 2 [ NH 3 ] = 2 x mol /L v’ = k ( 2 x )2 v’ = 4 k x 2 v’ = 4 v Prof. Agamenon Roberto

Para uma reação elementar do tipo: 1 A + 2 B 1 C Pode-se afirmar que: a) A velocidade de consumo de A é igual à velocidade de formação de C. b) A velocidade de consumo de B é a metade da velocidade de formação de C. c) A soma das velocidades de consumo de A e B é igual à velocidade de formação de C. d) A velocidade da reação é dada pela relação v = k. [A]. [B]. e) A reação de segunda ordem. v = k. [A]. [B]2 (1 + 2 = 3) = 3º ordem Prof. Agamenon Roberto

(UFMA) Ao se estudar uma reação representada pela equação: 2 A (g) + B 2 (g) Foram coletados os seguintes dados: 2 AB (g) [A] inicial [B] inicial Velocidade (mol. L – 1. S – 1) 0, 05 1, 25. 10 – 5 0, 05 0, 10 2, 50. 10 – 5 0, 10 0, 05 5, 00. 10 – 5 Qual das opções abaixo contém a equação correta da velocidade para essa reação? a) v = k. [B]2. b) v = k. [A]. [B]2. c) v = k. [A]. [B]. d) v = k. [A]2. e) v = k. [A]2. [B].
![2 A (g) + B 2 (g) [A] inicial [B] inicial 0, 05 0, 2 A (g) + B 2 (g) [A] inicial [B] inicial 0, 05 0,](http://slidetodoc.com/presentation_image_h2/b5446c21dc68eb8b0fa8bc93a40bc753/image-29.jpg)
2 A (g) + B 2 (g) [A] inicial [B] inicial 0, 05 0, 10 0, 05 1 2 3 2 AB (g) Velocidade (mol. L – 1. S – 1) 1, 25. 10 2, 50. 10 5, 00. 10 – 5 – 5 v = k [A]x. [B]y 2 1 2, 50. 10 – 5 1, 25. 10 – 5 2=2 y=1 y = k. (0, 05) x . (0, 10) y 3 5, 00. 10 – 5 k. (0, 05) x . (0, 05) y 1 1, 25. 10 – 5 4=2 x . (0, 05) y k. (0, 05) x . (0, 05) y x 22 = 2 x=2 = k. (0, 10) x v = k [A]2. [B]

(UFMA) Ao se estudar uma reação representada pela equação: 2 A (g) + B 2 (g) Foram coletados os seguintes dados: 2 AB (g) [A] inicial [B] inicial Velocidade (mol. L – 1. S – 1) 0, 05 1, 25. 10 – 5 0, 05 0, 10 2, 50. 10 – 5 0, 10 0, 05 5, 00. 10 – 5 Qual das opções abaixo contém a equação correta da velocidade para essa reação? a) v = k. [B]2. b) v = k. [A]. [B]2. c) v = k. [A]. [B]. d) v = k. [A]2. e) v = k. [A]2. [B]. v = k [A]2. [B]
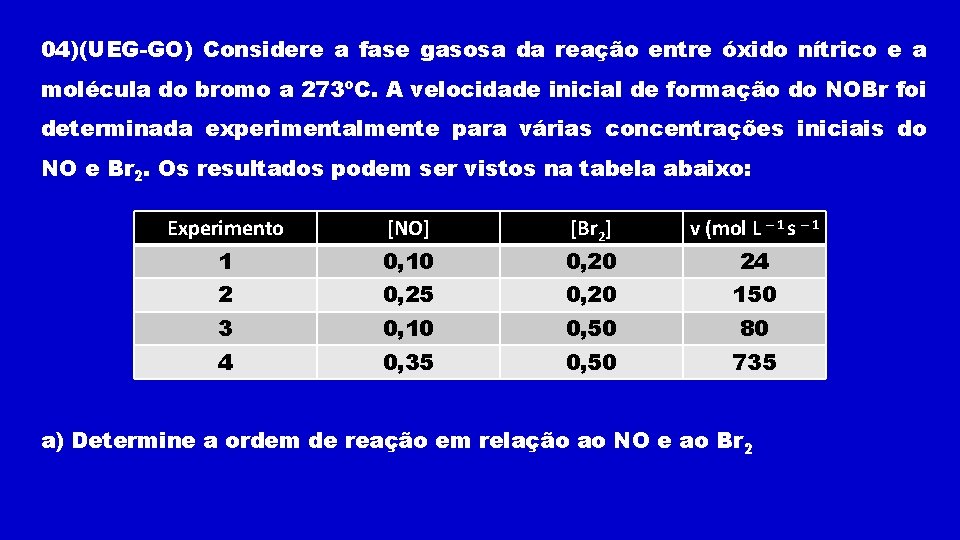
04)(UEG-GO) Considere a fase gasosa da reação entre óxido nítrico e a molécula do bromo a 273ºC. A velocidade inicial de formação do NOBr foi determinada experimentalmente para várias concentrações iniciais do NO e Br 2. Os resultados podem ser vistos na tabela abaixo: Experimento [NO] [Br 2] v (mol L – 1 s – 1 1 0, 10 0, 20 24 2 0, 25 0, 20 150 3 0, 10 0, 50 80 4 0, 35 0, 50 735 a) Determine a ordem de reação em relação ao NO e ao Br 2
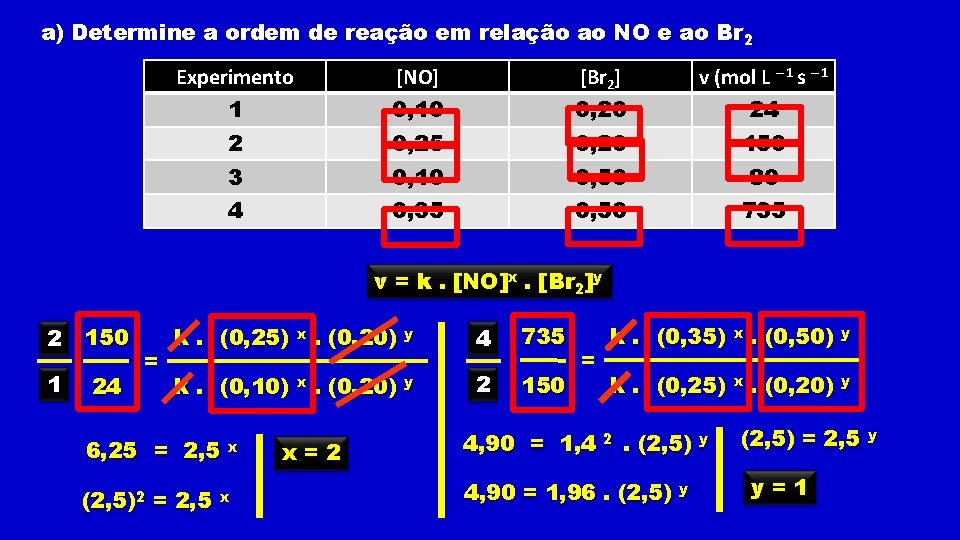
a) Determine a ordem de reação em relação ao NO e ao Br 2 Experimento [NO] [Br 2] v (mol L – 1 s – 1 1 0, 10 0, 20 24 2 0, 25 0, 20 150 3 0, 10 0, 50 80 4 0, 35 0, 50 735 v = k. [NO]x. [Br 2]y 2 150 1 24 = k. (0, 25) x k. (0, 10) x 6, 25 = 2, 5 (2, 5)2 = 2, 5 x x . (0, 20) y x=2 4 735 2 150 = 4, 90 = 1, 4 k. (0, 35) x . (0, 50) y k. (0, 25) x . (0, 20) y 2 . (2, 5) 4, 90 = 1, 96. (2, 5) y y (2, 5) = 2, 5 y=1 y
![x=2 y=1 v = k. [NO]x. [Br 2]y 2ª ordem em relação ao NO x=2 y=1 v = k. [NO]x. [Br 2]y 2ª ordem em relação ao NO](http://slidetodoc.com/presentation_image_h2/b5446c21dc68eb8b0fa8bc93a40bc753/image-33.jpg)
x=2 y=1 v = k. [NO]x. [Br 2]y 2ª ordem em relação ao NO v = k. [NO]2. [Br 2]1 1ª ordem em relação ao Br 2 b) Determine a constante de velocidade na temperatura considerada. Experimento [NO] [Br 2] v (mol L – 1 s – 1 1 0, 10 0, 20 24 2 0, 25 0, 20 150 3 0, 10 0, 50 80 4 0, 35 0, 50 735 24 = k. [0, 10]2. [0, 20] 24 = k. 0, 01. 0, 2 24 = k. 0, 002 k= 24 0, 002 k = 12. 000 mol – 2 . L 2 . s – 1

(PUC-MG) considere o diagrama energética de uma reação: energia (kj) Ea = 500 – 200 Ea = 300 kj 500 400 300 200 100 ∆H = 400 – 200 ∆H = + 200 kj caminho da reação É correto afirmar que essa reação possui respectivamente uma energia de ativação e uma variação de entalpia de: a) 500 kj e + 400 kj. b) 100 kj e + 200 kj. c) 300 kj e + 200 kj. d) 100 kj e + 400 kj. e) 300 kj e – 200 kj.
- Slides: 34