CINTICA QUMICA IV FsicoQumica Frente 3 Bruno D

CINÉTICA QUÍMICA IV Físico-Química – Frente 3 – Bruno : D

ENCONTRO NACIONAL DO ENSINO DE QUÍMICA 2016
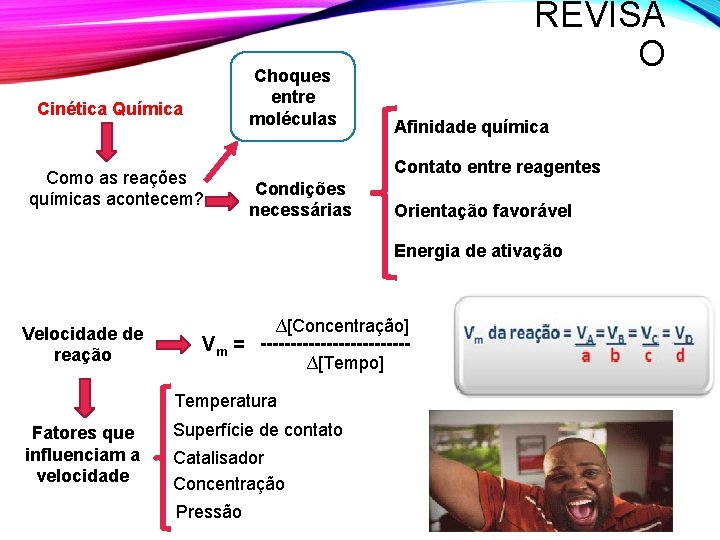
Choques entre moléculas Cinética Química Como as reações químicas acontecem? REVISÃ O Afinidade química Contato entre reagentes Condições necessárias Orientação favorável Energia de ativação Velocidade de reação ∆[Concentração] Vm = ------------∆[Tempo] Temperatura Fatores que influenciam a velocidade Superfície de contato Catalisador Concentração Pressão
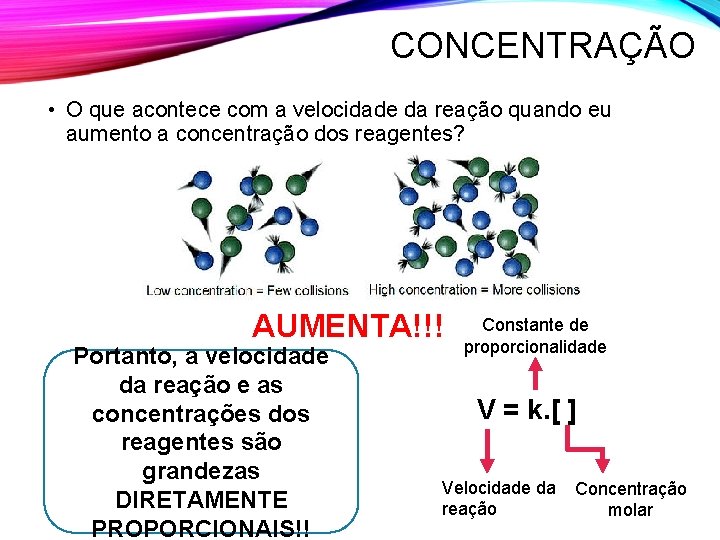
CONCENTRAÇÃO • O que acontece com a velocidade da reação quando eu aumento a concentração dos reagentes? AUMENTA!!! Portanto, a velocidade da reação e as concentrações dos reagentes são grandezas DIRETAMENTE PROPORCIONAIS!! Constante de proporcionalidade V = k. [ ] Velocidade da reação Concentração molar

LEI DAS VELOCIDADES “A velocidade de uma reação química é diretamente proporcional ao produto das concentrações molares dos reagentes, para cada temperatura, elevadas a expoentes experimentalmente determinados. ” a. A + b. B c. C + d. D V = k. [A]x. [B]y • • • V = velocidade da reação k = constante de velocidade [A] = concentração molar de A [B] = concentração molar de B X e Y = expoentes experimentalmente determinados

PARA REAÇÕES ELEMENTARES • O que são reações elementares? Aquelas que acontecem em apenas UMA etapa! Quando uma reação é elementar, os expoentes da lei das velocidades são os próprios coeficientes estequiométricos 2 CO + 1 O 2 2 CO 2 V = k. [CO]2. [O 2]1

REAÇÕES NÃO ELEMENTARES • Reações não elementares são aquelas que acontecem em mais de uma etapa A etapa lenta é a determinante da velocidade da reação!! V = k. [H 2]1. [NO]2
![CO(g) + NO 2(g) CO 2(g) + NO(g) V = k. [NO 2]2 Por CO(g) + NO 2(g) CO 2(g) + NO(g) V = k. [NO 2]2 Por](http://slidetodoc.com/presentation_image_h2/2f56cf2f0e502e3c0fd04253ed2c8087/image-8.jpg)
CO(g) + NO 2(g) CO 2(g) + NO(g) V = k. [NO 2]2 Por que o CO não está na fórmula da velocidade de reação? ?

Etapa 1 (lenta): NO 2 (g) + NO 2 (g) NO 3 (g) + NO(g) Etapa 2 (rápida): NO 3 (g) + CO (g) CO 2 (g) + NO 2 (g) Reação global: CO(g) + NO 2 (g) CO 2 (g) + NO(g) O CO está na etapa rápida da reação, por isso ele não está na fórmula de velocidade de reação!!
- Slides: 9